盐酸吗啡片溶出度测定方法的改进
王天学,张敏娟,魏文芝,陈学艳,袁 璐,张耀元,段广佩
(1.青海省食品检验检测院,西宁 810016;2.青海省药品检验检测院/青海省中藏药现代化研究重点实验室,西宁 810016)
盐酸吗啡片为国家特殊管理的麻醉药品,属选择性阿片受体激动剂,是强效镇痛药,适用于其他镇痛药无效的急性剧痛,如严重创伤、战伤、烧伤和癌症晚期等疼痛,临床应用广泛[1-5],国内现有2家生产企业。盐酸吗啡片现行标准收载于《中国药典》2015年版二部[6],其溶出度方法为溶出度与释放度测定法(《中国药典》2015年版四部通则0931 第三法,即小杯法)[7],该方法用紫外-可见分光光度法,将第二法(桨法)的溶出介质体积由900 mL(或1 000 mL)缩减为100~250 mL,同时相应缩小搅拌桨(桨叶直径由74 mm缩小为45 mm)从而实现溶出度测定。两者的转换本身缺乏严谨的科学依据[8],且为我国特有的溶出度检查方法,通用性不足;采用紫外-可见分光光度法进行测定,灵敏度不高,专属性不强。溶出度实验是评价口服固体制剂质量的一种重要手段,能更加全面评价药品生产工艺,完善质量标准[9],以保障用药安全有效,因此对盐酸吗啡片溶出度方法进行优化十分必要。参考国外药典及相关文献[10-19],参照《中国药典》2015年版四部中溶出度与释放度测定方法的要求,建立通用性较好的桨法为盐酸吗啡片溶出度实验方法,并采用专属性较强、灵敏度较高的HPLC-DAD方法测定吗啡溶出度。
1 仪器与材料
1.1仪器 RCZ-8MD型智能溶出实验仪(天津天大天发科技有限公司);真空脱气机(上海富科思分析仪器有限公司);e2695-2998高效液相色谱仪,包括Empower3软件工作站,二极管阵列检测器(美国Waters公司);CP 225D电子天平(德国Sartorius公司)。
1.2试药 盐酸吗啡片(生产厂家A,规格:5 mg,批号:20141031,20140811,20140521,20140217和20150324;生产厂家B,规格:10 mg,批号:1150403,1150101,1140903,1140905和1150606)。吗啡对照品(批号171201-201324,质量分数为99.1%),由中国食品药品检定研究院提供;甲醇为色谱纯(德国Merck公司);磷酸氢二钾为分析纯(天津百世化工有限公司);水为纯化水。
2 方法与结果
2.1色谱条件 色谱柱:Waters XBrige C18色谱柱(250 mm×0.46 mm,5 μm);流动相:甲醇-0.05 mol·L-1磷酸氢二钾溶液(10∶90);流速:1.0 mL·min-1;检测波长:235 nm;柱温:35 ℃;进样量:20 μL。理论塔板数按照吗啡峰计算为7 800。
2.2溶液的制备
2.2.1对照品溶液 精密称取吗啡对照品11.25 mg,置于100 mL量瓶中,加流动相振摇使溶解,并稀释至刻度,摇匀,作为吗啡对照品溶液。
2.2.2供试品溶液 取样品适量,采用《中国药典》2015年版四部溶出度与释放度测定第二法(桨法),以900 mL水为溶出介质,转速为50 r·min-1,依法操作,30 min时,取溶出液5 mL,用0.45 μm滤膜滤过,取续滤液,即得。
2.3系统适用性实验 取2.2项下制备的对照品溶液、供试品溶液和溶出介质(水)各20 μL,按照2.1项下色谱条件进行测定,记录色谱图,见图1。由图1可知,在该色谱条件下,理论塔板数以吗啡峰计≥7 000,保留时间为4.050 min。结果表明,其他成分对测定无干扰。
2.4线性关系考察 精密量取2.2.1项下制备的对照品溶液0.1,1.0,5.0,10.0和20.0 mL,置于100 mL量瓶中,加流动相溶解并稀释至刻度,摇匀,即得系列对照品溶液。精密量取上述对照品溶液20 μL,按照2.1项下色谱条件进样测定,记录峰面积。以吗啡质量浓度为横坐标(x)、峰面积为纵坐标(y)进行线性回归,得吗啡回归方程为y=1 117.1x+18 839.5(r=1.000 0)。结果表明,吗啡质量浓度线性范围为0.111 5~111.487 5 μg·mL-1。
2.5精密度实验 取2.2.1项下制备的对照品溶液适量,按照2.1项下色谱条件进样测定,记录峰面积。结果吗啡峰面积的RSD值为0.1%(n=6),结果表明,仪器精密度良好。
2.6稳定性实验 取2.2.2项下制备的供试品溶液适量,在室温下放置0,4,8,12和24 h,按照2.1项下色谱条件进样测定,记录峰面积。结果吗啡峰面积的RSD值为0.4%(n=5),结果表明,供试品溶液在室温放置24 h内稳定性良好。
2.7重复性实验 取样品(批号1150403)适量,按照2.2.2项下方法制备供试品溶液,按照2.1项下色谱条件进样测定,记录峰面积。结果表明,吗啡峰面积的RSD值为1.8%(n=6),重复性良好。
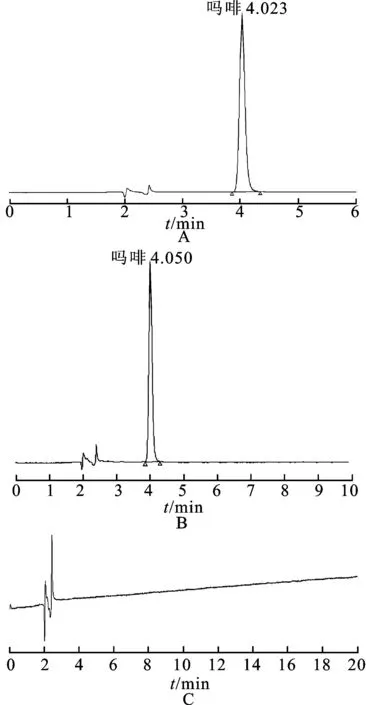
图1HPLC图
A.吗啡对照品;B.供试品;C.溶出介质(水)。
Fig.1 HPLC chromatograms
A.reference substance of morphine;B.test sample;C.water.
2.8加样回收率实验 取样品(批号1150403)共9份,分别置于100 mL量瓶中,加流动相使溶解并稀释至刻度,摇匀,精密量取续滤液2.5 mL,置于50 mL量瓶中,加入低、中、高质量浓度的吗啡对照品溶液,加流动相稀释至刻度,摇匀,按照2.1项下的色谱条件进样测定,记录峰面积,并计算加样回收率,结果见表1。
2.9溶出介质的选择 取2个厂家的样品适量,按照《中国药典》2015年版四部通则0931第二法(桨法),分别以水、0.1 mol·L-1盐酸溶液、pH值为4.0醋酸盐缓冲溶液和pH值为6.8磷酸盐缓冲溶液作为溶出介质,体积为900 mL,转速为50 r·min-1,于5,10,20,30,45和60 min取样,按照2.1项下色谱条件进样测定,考察不同厂家样品在4种溶出介质中的累积溶出曲线,见图2和图3。
由图2和图3可知,样品在4种介质中的溶出行为均相似。查阅国外药典(日本药局方JP16)中“盐酸吗啡片”溶出度测定项下,其溶出介质为水[20],现行《中国药典》2015年版二部中,溶出介质亦为水,因此选择水为溶出介质。
表1加样回收率实验结果
Tab.1 Results of recovery tests

取样量/g样品含量/mg加入量/mg测得量/mg加样回收率/%平均加样回收率/%RSD/%0.080 040.247 70.243 80.493 8100.96100.10.90.080 270.248 40.243 80.489 899.010.080 710.249 80.243 80.492 499.530.079 960.247 40.325 00.574 4100.590.079 540.246 10.325 00.576 1101.500.080 270.248 40.325 00.572 299.610.079 970.247 50.406 30.656 0100.540.080 200.247 50.406 30.648 798.750.079 250.245 20.406 30.652 6100.25
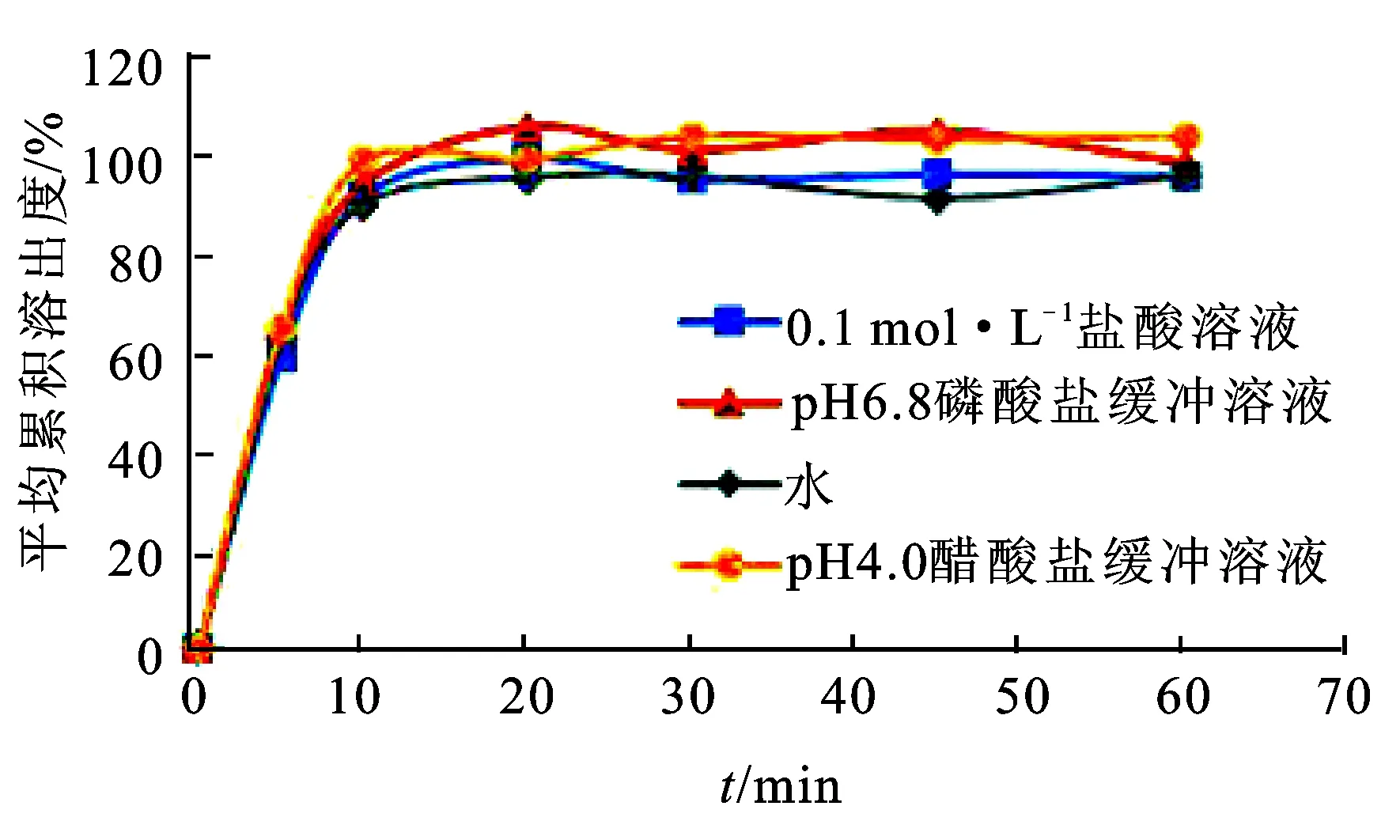
图2样品(5mg)在4种介质中的溶出曲线
Fig.2 Dissolution curves of sample (5 mg) in 4 kinds of dissolution media

图3样品(10mg)在4种介质中的溶出曲线
Fig.3 Dissolution curves of sample (10 mg) in 4 kinds of dissolution media
2.10转速的确定 取样品(批号1150403和20150324),以水为溶出介质,溶出介质体积为900 mL,转速分别为50和75 r·min-1,于5,10,20,30,45和60 min取样,按照2.1项下色谱条件进样测定,考察样品在不同转速和时间点的平均累积溶出度,结果见表2。由表2可知,样品在转速为50 r·min-1时即可达到较理想的平均累积溶出度,因此选择50 r·min-1为本实验的转速。
2.11取样时间的确定 取样品(批号1150403和20150324)适量,各6份,以水为溶出介质,溶出介质体积为900 mL,转速为50 r·min-1,于5,10,20,30,45和60 min取样,按照2.1项下色谱条件进样测定,考察样品在不同时间点的平均累积溶出度,结果见图4。由图4可知,样品在30 min时溶出曲线达到平台期。
表2A、B厂家样品在不同转速及不同取样时间点的平均累积溶出度
Tab.2 Average accumulative dissolution of samples from manufactures A and B at different rotation speeds and different times

批号时间/min平均累积溶出度/%转速/50 r·min-1转速/75 r·min-111504035605910929320969430999745959860969720150324595941098992099100309910045100101609999
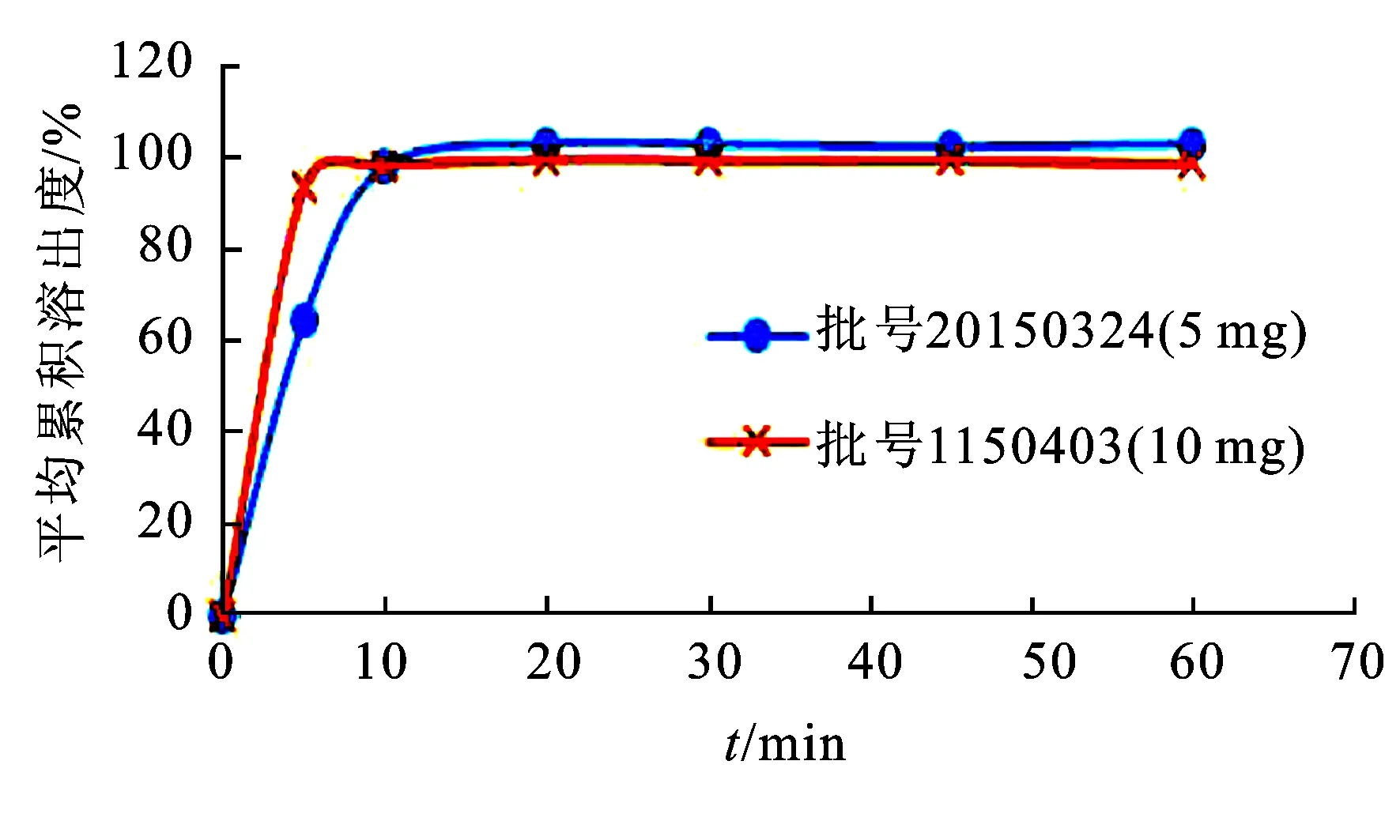
图4样品(5mg)在不同时间点的溶出曲线(n=6)
Fig.4 Dissolution curves of sample (5 mg) at different time points (n=6)
2.12滤膜吸附实验 取2.2.1项下滤过前和滤过后的对照品溶液适量,经0.45 μm的微孔滤膜滤过,取续滤液1,2,3,5和6 mL,按照2.1项下的色谱条件进样测定。结果0.45 μm微孔滤膜对吗啡的吸附量小于2.0%(n=5),符合规定[21]。
2.13样品溶出度测定 取10批样品各适量,按照2.2.2项下方法制备供试品溶液,再按照2.1项下色谱条件进样测定,记录峰面积并计算吗啡的溶出度,结果见表3。
表3样品溶出度实验结果
Tab 3 Results of dissolution determination of samples

(n=6)
3 讨论
将10批次样品应用原标准检测方法与本实验方法测得溶出度及RSD值结果进行比较,结果见表4。由表4可知,原方法测得溶出度平均值、溶出度RSD值较本实验方法偏高,本实验方法通用性更佳、检测灵敏度更高、专属性更强;按照生产企业分析,A厂家溶出度结果RSD值较B厂家略高,说明A厂家样品批间差异、溶出度离散性较B厂家略大,提示A厂家应进一步优化生产工艺,以提高批间一致性,降低产品质量风险。
表42种方法测得溶出度平均值与RSD结果比较
Tab 4 The comparison of the average dissolution and RSD results determined by the 2 methods

(n=6)
综上所述,改进后的盐酸吗啡片溶出度测定方法提高了方法灵敏度、专属性、准确性和通用性,适用于盐酸吗啡片的溶出度测定。

