具有聚集荧光增强性质的双(4-二乙氨基水杨醛)缩偶氮二甲酰肼二丁基锡的合成和晶体结构
冯泳兰 邝代治 张复兴 庾江喜 蒋伍玖 朱小明
(衡阳师范学院化学与材料科学学院,功能金属有机材料湖南省高校重点实验室,功能金属有机化合物湖南省重点实验室,衡阳 421008)
0 引 言
含偶氮基(-N=N-)的偶氮化合物由于具有顺、反几何异构的结构特征及稳定性的差异,表现出特殊的光学性质,在染色、光学元件和灵敏显色剂等领域具有广泛的应用[1-5],引起了光学材料和分析化学工作者的兴趣。偶氮基的氮存在孤电子对,可与金属配位,产生结构多样的配合物[6-7],对调控结构和开发新性质材料起着重要作用;许多偶氮化合物还具有较好的生物活性[8-9],引起了合成化学、结构化学和药物化学工作者的关注。偶氮化合物主要通过重氮盐的偶联反应、氧化偶氮化合物和硝基化合物的还原反应,芳香胺的氧化反应或氢化偶氮化合物的氧化反应制备,还可通过氧化具有替在偶氮键的联二脲(NH2CONH-NHCONH2)制得含4个可配位氮、氧原子的偶氮二甲酰胺(NH2CON=NCONH2)等。偶氮二甲酰胺可用于组装偶氮二甲酰胺/金属-有机骨架复合材料[10],但由于偶氮二甲酰胺中酰胺基的配位作用较弱,与金属较难配位,人们由酰胺联想到酰肼,利用酰肼的氨基与醛、酮缩合,衍生出具有强配位作用的亚胺Schiff碱为配体[11-12],进而合成其金属配合物[13]。
我们在甲醇溶液中,将卡巴肼、(4-二乙氨基)水杨醛和二乙酸二丁基锡混合加热,“一锅法”合成了新型双(4-二乙氨基水杨醛)缩偶氮二甲酰肼丁基锡配合物[Sn(L)(n-butyl)2]n(T),初步研究了该配合物在DMF、THF、EtOH、MeOH 和甲苯及其有机溶剂-水混合溶剂体系中的荧光性质,结果表明,T在上述溶剂中具有良好的聚集荧光增强性质。
1 实验部分
1.1 仪器和试剂
Bruker Avance 500核磁共振仪(瑞士Bruker公司,1H、13C和119Sn NMR核磁共振谱测定用TMS作内标,119Sn NMR谱还用Me4Sn外标,CDCl3为溶剂);IR Prestige-21傅立叶红外光谱仪 (日本岛津公司,4 000~400 cm-1,KBr压片);F-7000 荧光光谱仪(日本岛津公司),PE-2400(Ⅱ)元素分析仪 (美国 PE公司);Bruker SMART APEXⅡCCD X射线单晶衍射(德国Bruker公司);X-4双目体视显微熔点测定仪(北京泰克仪器有限公司)。
二乙酸二丁基锡(95%)、卡巴肼和4-(二乙氨基)水杨醛(化学纯)购于萨恩化学技术(上海)有限公司。其它试剂、溶剂均为化学纯。
1.2 配合物的合成
向反应瓶中加入2 mmol(0.180 2 g)卡巴肼、2 mmol(0.386 4 g)(4-二乙氨基)水杨醛、2 mmol(0.702 1 g)二乙酸二丁基锡和15 mL甲醇。搅拌反应物混合均匀后加热回流反应24 h,冷却至室温,得黄色甲醇溶液,静置4 d析出棕黄色晶体。减压旋转蒸发甲醇溶液除去大部分溶剂,过滤,用少量甲醇重结晶,又得部分棕黄色晶体,合并得产品0.62 g,产率64.7%。m.p.124 ℃;1H NMR(CDCl3,500 MHz):δ8.34(s,2H,Ar-H),6.92~6.94(m,2H,Ar-H),6.13~6.15(m,2H,Ar-H),5.95(s,2H,N=C-H),3.38~3.40(m,8H,NCH2-),1.19~2.03(m,48H,甲基和丁基的亚甲基氢);13C NMR(CDCl3,500 MHz):δ170.61(C=O),168.67(-C=N),159.27,153.60,136.16,106.69,103.29,100.58(Ar-C),77.28~76.77(CDCl3),44.53(-N-CH2-),26.92,26.49,21.63(-CH2-),13.61(-CH3),12.84(-CH3);119Sn(CDCl3,500 MHz):δ-191.78。IR(KBr,cm-1):2 959,2 922,2 870,855(m,νC-H),1 597(s,νC=O),1 524(s,νC=N),592(s,νSn-O),530(s,νSn-N),482(s,νSn-C);元素分析按 C40H64N8O4Sn2计算值(%):C,50.13;H,6.73;N,11.69。 实测值(%):C,50.27;H,6.75;N,11.53。
1.3 配合物晶体结构的测定
选取尺寸0.23 mm×0.21 mm×0.20 mm的晶体,在Bruker SMART APEXⅡCCD衍射仪上,采用经石墨单色化的 Mo Kα 射线(λ=0.071 073 nm),于296(2)K,以φ~ω扫描方式收集衍射数据。全部数据经Lp因子和多重扫描吸收校正后,由直接法解出晶体结构,全部非氢原子坐标在差值Fourier合成中陆续确定,由理论加氢法给出氢原子在晶胞中的位置坐标。对氢原子和非氢原子坐标及其各向同性和各向异性热参数采用全矩阵最小二乘法修正;全部结构分析计算工作采用SHELXTL-97程序完成[14]。
CCDC:1868342。
2 结果与讨论
2.1 配合物的晶体结构
卡巴肼具有2个能与醛缩合的氨基,可形成单取代的醛缩卡巴肼,也可形成1,5-双取代的醛缩卡巴肼Schiff碱。在我们的实验条件下,用卡巴肼与4-二乙氨基水杨醛按物质的量之比1∶1反应,得到一个由2个卡巴肼之间脱去1个肼分子产生偶氮键相连,并与2个4-二乙氨基水杨醛缩合,含有10个可配位N、O原子的新配体。这种偶氮二甲酰肼缩双水杨醛,往往发生酮式(Ⅰ)与烯醇式(Ⅱ)相互转化(Scheme 1)[15-16],烯醇氧与二乙酸二丁基锡的乙酸根交换配位,形成“一锅法”合成,获得未见文献报道的标题配合物。
晶体分子结构分析表明,配体的偶氮键(-N=N-)以反式构型分别连接甲酰肼缩 (4-二乙胺基水杨醛),配合物由配体的烯醇式(Ⅱ)与2个二丁基锡配位组成一个以-N=N-为中心对称的独立结构单元。由于偶氮原子分别与2个Sn原子配位而削弱了N=N键,键长(0.141 8(7)nm)明显比未配位的键(0.127 8(3)nm)增长[17]。 每个锡原子分别与烯醇式 O(1)、酚羟基O(2)、Schiff碱的亚氨 N(1)和偶氮 N(3),以及邻近分子的烯醇式氧原子配位。5个氮、氧原子与Sn(1)原子配位稠合成曲面的结构。以偶氮链为中心的2组二面角∠Sn(1)-N(3)-N(3ii)-Sn(1ii)和∠C(9)-N(3)-N(3ii)-C(9ii)(Symmetry codes:ii-x+1,y,-z+1/2) 分 别 为176.92°和 170.20°,其中 μ2-O(1)桥联 2 个 Sn 原子,由一个共价O-Sn键(0.249 3(3)nm)和一个配键O→Sn(0.255 3(3)nm)组成Sn2O2棱形四元环,O(1)-O(1i)和 Sn(1)-Sn(1i)(Symmetry codes:i-x+1,-y+1,-z+1)之间的空间距离分别为0.268 4和0.427 3 nm。亚氨N(1)和酚羟基O(2)与Sn组成六元环,中间的=N-N=C(O-)-N=N-C(O-)=与Sn形成2个五元环,2个二乙氨基苯处于曲面的两边,从独立单元的c轴方向看去,类似一“竹筏”形,Sn(1)上的2个丁基竖立于船的上、下方,如同“船夫及倒影”。独立单元的O-Sn键、N-Sn和C-Sn键长及配基原子与锡原子之间的键角各不相等(表2),因此,配合物中心锡与配基原子形成畸变程度较大的五角双锥构型[18]。
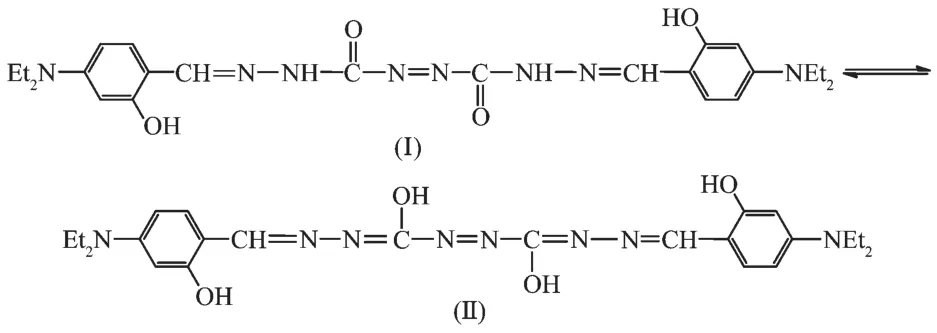
Scheme 1 Keto-enol interconversion of 1,8-disubstituted azodicarbonhydrazide
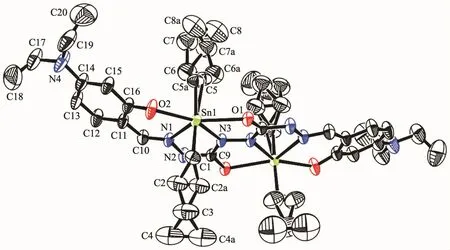
图1 配合物T的分子结构图Fig.1 Molecular structure of the complex T

表1 配合物T的晶体学数据Table 1 Crystallographic data of complex T

表2 配合物T的部分键长和键角Table 2 Selected bond lengths(nm)and angles(°)for complex T
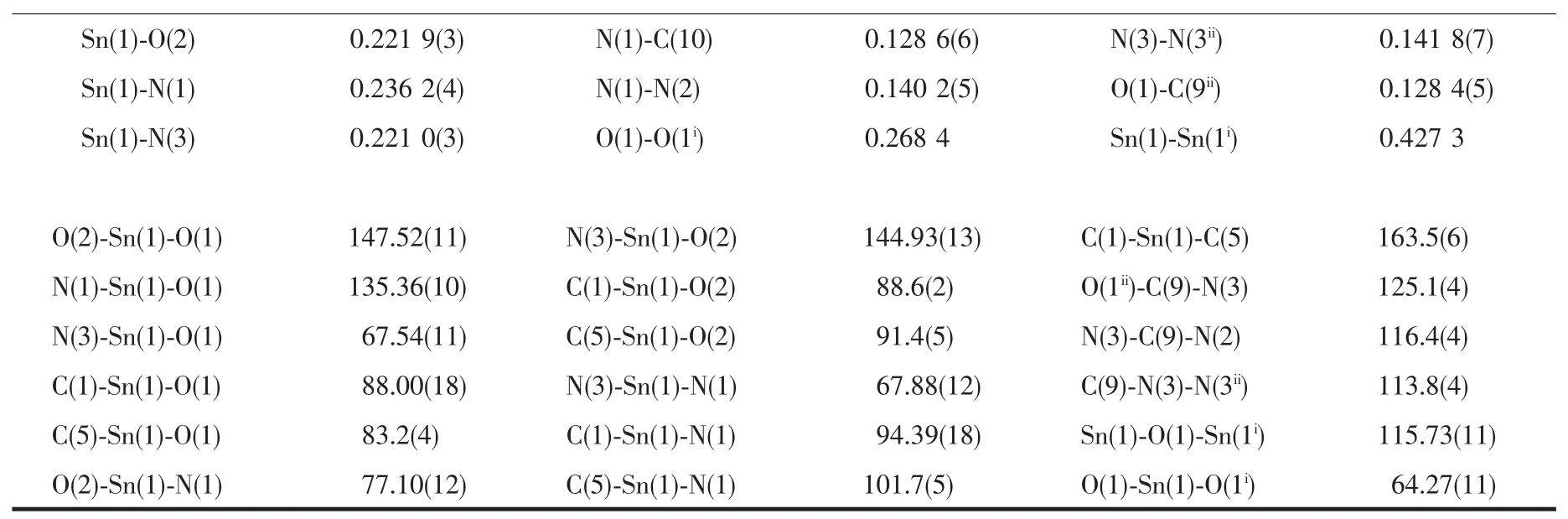
续表2
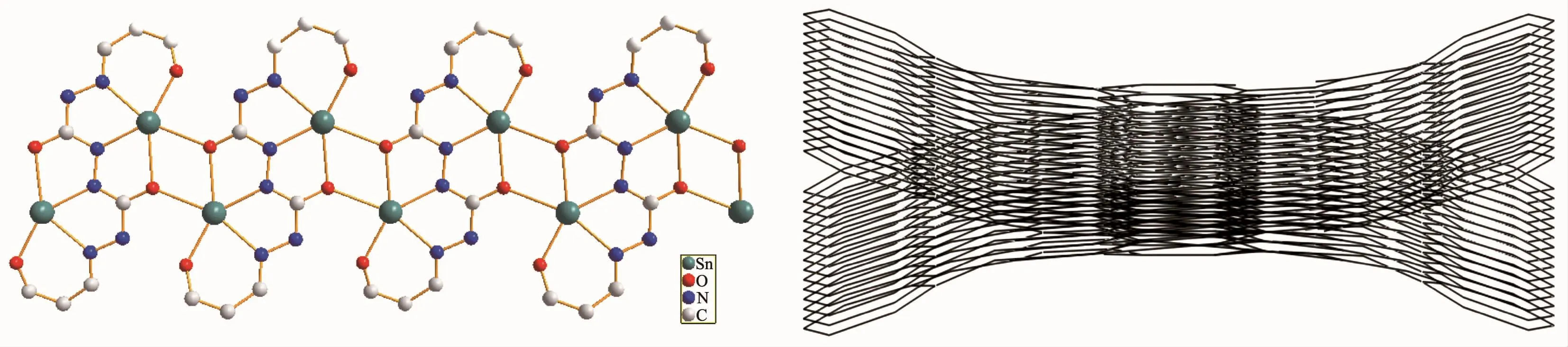
图2 配合物T的带状 (左)和竹筏状 (右)结构Fig.2 One dimensional band-like(left)and bamboo raft-like(right)structure of the complex T
值得指出的是,通过烯醇式氧原子的桥联配位作用(图2(左)),独立单元向一维带状无限扩展,产生“竹筏状”超分子结构,形成竹筏船及其倒影形状,如图 2(右)所示。
2.2 谱学特征
配合物T具有多种红外光谱特征峰。在2 959、2 922、2 870和2 855 cm-1出现较强的氮连乙基的甲基、亚甲基和丁基的νC-H伸缩振动峰,并在1 466和1 389 cm-1分别出现甲基νs,C-H和甲基、亚甲基的νas,C-H特征峰。苯环上的νC-H较弱,被甲基、亚甲基的νC-H所掩盖。羰基 νC=O、希夫碱 νC=N和偶氮 νN=N键特征峰由于与锡原子配位作用分别移于1 597、1 524和 1 424 cm-1。 在 482 cm-1(νSn-C)[19]、592 cm-1(νSn-O)和530 cm-1(νSn-N)[20-21]的 弱 特 征 峰 均 表 征 和 进 一 步 证 实了配合物的结构。
受苯环上3个不同取代基的影响,3个苯环H在1H NMR谱出现化学位移在 8.34、6.92~6.94和6.13~6.15的3组峰;与锡配位的希夫碱(N=CH-)的H质子的化学位移在5.95,与锡原子相连的亚甲基质子受锡原子的影响化学位移出现在3.38和3.40,其它甲基、亚甲基的质子化学位移在1.19~2.03,为多重峰。13CNMR更具有特征,羰基(C=O)和希夫碱(N=C)的碳谱线受到氧、氮的作用分别出现在170.61和168.67;苯环碳也由于受基团的影响在100.58~159.27之间分裂出6条谱线及甲基、亚甲基的多个谱线。
2.3 配合物-有机溶剂-水体系的荧光性质
从结构和键参数可看出,双 (4-二乙氨基水杨醛)缩偶氮二甲酰肼配体含有多个生色基的共轭链,当它与二丁基锡配位形成配合物后产生刚性平面的大共轭体系,可能成为发光分子,因此,我们对配合物在有机溶剂(OS)和OS-H2O混合溶液进行荧光性能研究。
配制配合物T分别在有机溶剂N,N-二甲基甲酰 胺 (DMF)、 四 氢 呋 喃 (THF)、 乙 醇 (EtOH)、甲 醇(MeOH)和甲苯及OS-H2O中浓度为1.04μmol·L-1的溶液。室温下,先测试DMF、THF、EtOH与水的体积比为8∶2时和MeOH、甲苯中T-OS-H2O溶液体系中的紫外-可见吸收光谱,发现它们的最大吸收峰分别位于 366 nm(DMF-H2O)、270 nm(THF-H2O)、400 nm(EtOH-H2O)、270 nm(MeOH)和 400 nm(甲苯)处。再分别以此波长为激发波长(λex)在荧光光谱仪上对不同含水体积分数的T-OS-H2O体系扫描,测得TOS-H2O的荧光光谱,探索T-OS-H2O体系中水的含量对荧光强度的影响,结果见图3和表3。实验发现:
(1)配合物T在这5种有机溶剂中均有良好的荧光性质。随着体系中水含量变化,体系的发射峰波长(λem)和激发波长不同,5种T-OS-H2O体系均在400 nm以上出现发射峰,其发射波长与相应的激发波长比较,波长位移Δλ均在40 nm以上:78 nm(DMF-H2O),172 nm(THF-H2O),44 nm(EtOH-H2O),170 nm(MeOH),40 nm(甲苯)。
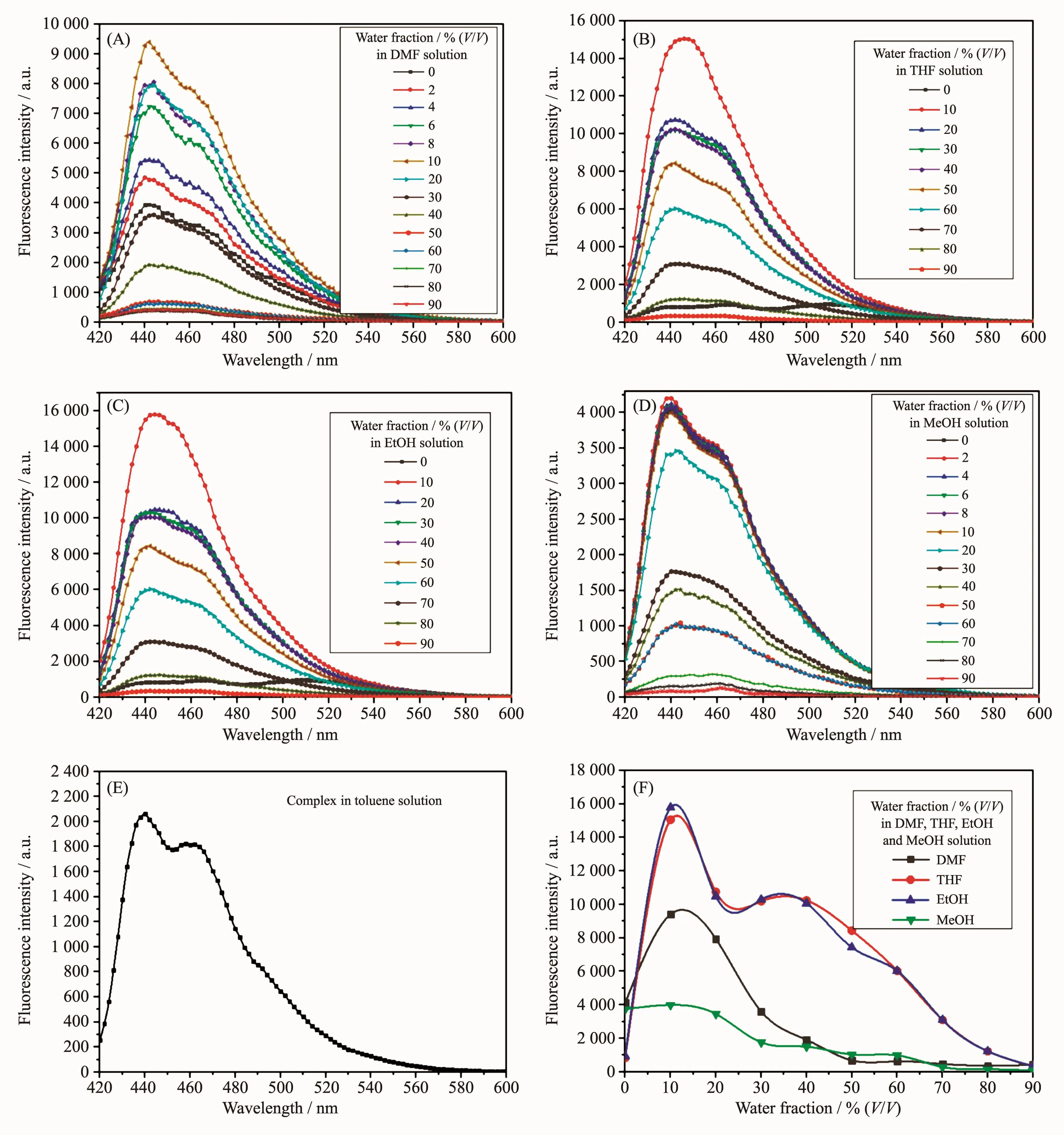
图 3 配合物 T 在不同含水量的 DMF-水 (A)、THF-水 (B)、EtOH-水 (C)、MeOH-水 (D)和甲苯(E)溶剂中的荧光光谱及各体系的最大荧光强度随含水体积分数的变化图(F)Fig.3 Fluorescence spectra of complex T in DMF-water(A),THF-water(B),EtOH-water(C),MeOH-water(D)and toluene(E)solvents with different water volume fraction,and variation in the maximum fluorescence intensity of each system with water volume fraction(F)

表3 配合物T在DMF-水和MeOH-水的体系中最大荧光强度随含水体积分数0~20%的变化Table 3 Maximum fluorescence intensity of T in DMF-H 2O and MeOH-H 2O system varies with the volume fraction of water content from 0 to 20%
(2)当含水的体积分数在0~10%范围内,除配合物T在甲苯中与水形成不稳定体系外,其它的TDMF-H2O(A)、T-THF-H2O(B)、T-EtOH-H2O(C)和 TMeOH-H2O(D)四个体系,均随着水含量的增加,体系的最大荧光强度呈不同程度的增加(图3F,表3)。当体系中含水量达10%(V/V)时荧光强度最大I10%,I10%与水含量为零时的荧光强度I0比,即I10%/I0值,分别为 2.28(DMF),16.64(THF),18.04(EtOH) 和 1.07(MeOH),表明体系在含水量0~10%浓度范围具有聚集荧光增强(AIEE)的性质[22],其中 T-EtOH-H2O 和 TTHF-H2O的AIEE性质更明显。配合物T在EtOH、THF、DMF和MeOH溶液虽具有发光性能,且这些有机溶剂与水有着较好的溶解性,但EtOH、THF、DMF和MeOH的极性与水不同,当在EtOH、THF、DMF和MeOH溶液中增加水的体积分数时,根据相似相溶原理,T分子可能开始聚集,在溶液中形成小的簇,荧光发光强度明显增加[23]。当水的体积分数大于10%后,随着水含量增加荧光强度缓慢下降,最终发生荧光淬灭,这可能是由于T在一定含水量的溶液中不稳定导致失去聚集荧光增强效应。
2.4 理论计算
为了理解发光现象,我们根据晶体结构的各原子坐标,考虑到配合物的对称性,取其中一个独立单元,用Gaussian 03W程序的DFT/b3lyp/lanl2dz基组[24],计算分析配合物的分子轨道[25]。用参与组合分子轨道的各类原子轨道系数的平方和并经归一化处理,表示该部分原子上的电子云分布。把配合物原子分为 Sn(1)、O(1)、O(2)、N(1-3)、N(4)、C(9)、C(10)、C(11-16)、C(1-8,17-20)和 H 等 10 组,理论计算配合物分子基态和激发态的电子云分布。结果显示,在最低未占分子轨道(LUMO),轨道成分主要集中于N(1)~N(3)原子上(41.77%),其中 N(2)和 N(3)上分别分布25.33%和11.27%,另外N(4)上分布了5.35%;其次是希夫碱的 C(10)(6.44%)和苯环 C(11)~C(16)碳(16.64%);锡原子、羰基碳C(9)和H原子分布较少并且它们在HOMO、LUMO分布变化不大。而在最高占据分子轨道(HOMO),轨道成份主要集中于O(1)(47.09%)及 N(1)~N(3)原子上(30.36%),其中 N(2)分布 6.78%、N(3)分布 18.08%,N(1)在 HOMO(5.50%)、LUMO(5.17%)分布变化不大;其次是苯环C(11)~C(16)碳(8.28%);O(2)(0.69%)和 C(10)(2.18%)变少,其它原子分布更少。这些轨道成分,预示着电子云主要集中分布于偶氮二甲酰肼缩苯甲醛配位链Ar-CH=N-N=C(OH)-N=N-C(OH)=N-N=CH-Ar上,通过二乙胺基的N原子与苯环共轭参与形成大共轭离域π体系[17]。这个含有多个发色基的配体,与锡配位组成平面刚性结构,形成强荧光物质分子。当激发态的LUMO电子向HOMO转移时,主要由N(2)和苯环 C(11)~C(16)碳及其相连的 N(4)、C(10)原子的电子云向 O(1)转移而发光[26]。
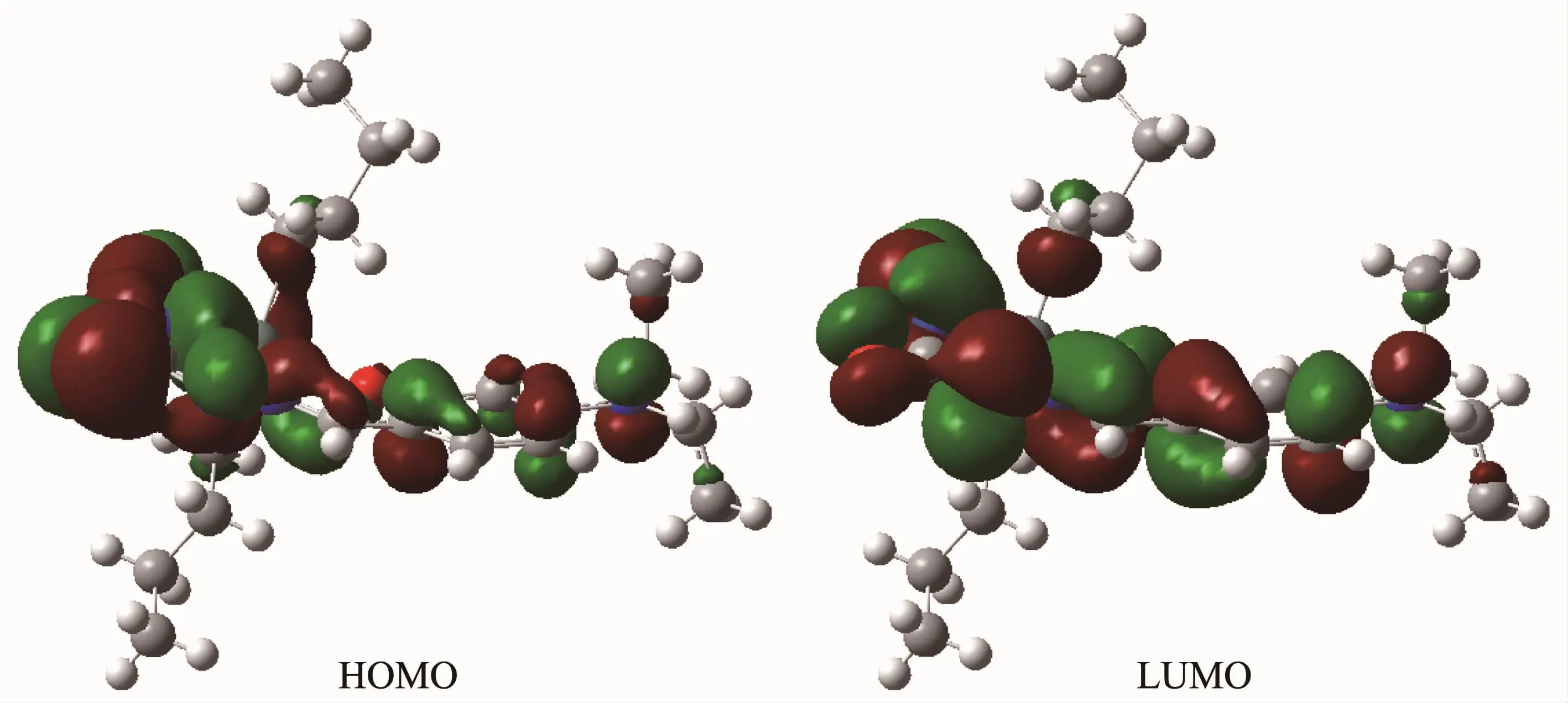
图4 DFT/b3lyp/lanl2dz计算配合物的前沿(HOMO,LUMO)分子轨道Fig.4 Frontier molecular orbitals(HOMO,LUMO)of the complex calculated by the DFT/b3lyp/lanl2dz method
3 结 论
在甲醇溶液中,以卡巴肼、(4-二乙氨基)水杨醛和二乙酸二丁基锡为反应物,“一锅法”合成了五角双锥构型的新型双(4-二乙氨基水杨醛)缩偶氮二甲酰肼二丁基锡配合物,配合物在二甲基甲酰胺、四氢呋喃、乙醇、甲醇和甲苯等溶剂及其0~10%含水量的溶液(甲苯除外)中具有强荧光发射峰和良好的聚集荧光增强性质,含水量大于10%发生荧光淬灭。可作为有机发光材料进一步研究。

