建立杏仁核电刺激慢点燃和匹罗卡品化学点燃耐药性颞叶癫痫模型并对比癫痫发作和海马超微结构的变化
王丽琨,周 鑫,伍国锋,洪 震
癫痫是多种原因导致的慢性脑部疾病,全球约有5000万癫痫患者[1],美国约有300万[2],我国约有900~1000万[3],且每年以新增45万的速度递增[4]。约有30%的癫痫患者经过系统正规的药物治疗,仍不能得到有效的控制,成为耐药性癫痫。耐药性癫痫模型则是研究耐药机制及发现新的治疗靶点的重要工具。杏仁核电刺激慢点燃癫痫模型是公认的颞叶癫痫的模型。但制作耗时耗力,难以点燃,植入的电极头容易脱落和感染。而匹罗卡品癫痫模型也是理想的颞叶癫痫模型,急性期表现为癫痫持续状态,随后有大约2 w的潜伏期是异常兴奋性环路形成的关键时期,慢性期主要表现为自发性反复发作,但死亡率较高[5],且对大鼠的脑组织损伤较重。本实验主要是对比两种模型之间癫痫发作持续时间、发作频率、发作级别、脑电图和超微结构的差异,评估是否可用匹罗卡品模型来取代杏仁核电刺激慢点燃模型,以期能够选择出更适合研究耐药机制的癫痫模型。
1 材料及方法
1.1 器材及试剂 DW-2000脑立体定向仪,BL-420F生物机能实验系统,BL-420F刺激器,HF30型可拆式屏蔽室(成都泰盟科技有限公司制造),镍铬漆包线(重庆仪表厂),自制连接器,自制牙科钻,自制深部电极,直径0.1 mm,刺激电极。苯巴比妥注射液(上海新亚药业有限公司),卡马西平(山东大学齐鲁医院)匹罗卡品、阿托品(美国Sigma公司),苯妥英钠纯品(武汉远城科技发展有限公司)。
1.2 实验分组 健康成年雄性SPF级SD大鼠130只,体重180~220 g,平均(200.5±4.3)g,由贵州医科大学动物实验中心提供。随机选择10只作为正常组,余下120只分别进行两种模型制作。模型制作成功后分别选择杏仁核模型和匹罗卡品模型,每组共10只进行对比癫痫发作的级别、频率和发作的时间。
1.3 杏仁核耐药颞叶癫痫模型的制作 实验方法同本课题组先前发表的文章[6,7]雄性SD大鼠60只,模型制作成功后以苯妥英钠(Phentoin,PHT)及苯巴比妥(Pentobarbital,PB)筛选耐药模型,依据杏仁核后放电阈值(after discharges threshold,ADT)变化,应用抗癫痫药物后与对照ADT比较,给药后ADT不增加或增加小于20%为耐药模型;ADT增高20%以上纳入药物敏感;ADT值变化不定不纳入实验分组。
1.4 匹罗卡品耐药性颞叶癫痫模型的制作 选取雄性SD大鼠60只腹腔注射匹罗卡品30 mg/kg[8~10],直至出现4级及以上持续发作;癫痫持续状态 (status epilepticus,SE)出现持续90 min后,用地西泮10 mg/kg终止发作。发生SE的大鼠约经过10 d~14 d潜伏期,即进入自发性发作阶段。将14 d后有自发性发作的大鼠即为造模成功。在其右侧杏仁核植入电极监测脑电图,植入方法同前[6,7],使用24 h视频脑电监护系统记录大鼠发作频率,持续时间及发作级别。用脑电图监测杏仁核放电的情况,记录脑电图的频率、波幅、发作持续时间,共记录2 w。2 w后开始筛选耐药模型,腹腔注射PB[11],总量30 mg/kg,每天两次,给药过程共持续2 w,记录发作次数和脑电图变化;用PB后癫痫发作持续时间和发作频率减少大于50%的为药物敏感的大鼠;用PB后癫痫发作持续的时间和发作的频率减少小于50%的为耐PB的癫痫大鼠[8,12]。对耐PB的癫痫大鼠,继续选用卡马西平(Carbamazepine,CBZ)进行耐药性筛选,CBZ灌胃,40 mg/kg/次,1 d 3次,连续给药14 d。判断方法如前。
1.5 电镜标本制备及观察判定 将动物麻醉后固定,开胸暴露心脏后以4%多聚甲醛灌注,灌注固定后取含有海马结构的2~3 mm厚冠状切面脑块,然后用2.5%戊二醛进行固定。取皮质及海马CA1区1 mm3组织各3块,1%锇酸固定2 h,丙酮脱水,环氧树脂包埋0.1%醋酸铀和3%柠檬酸铅双重电子染色5 min,H-600透射式电子显徽镜下进行超微结构观察,每个组织块观察3个铜网,选择病灶部位照像并病理分析,记录海马神经元超微结构变化。
2 结 果
2.1 杏仁核耐药性癫痫模型制作 用SD大鼠60只制作模型,成功点燃31只,点燃成功率为51.6%。在点燃后仅有1只大鼠出现自发性发作,自发性发作率为3.33%。平均每只大鼠点燃约需6~10 w,31只完全点燃耗时约15 w。将31只癫痫大鼠进行耐药筛选,2只死亡,29只中有10只对PHT耐药,再进行PB的筛选,其中有2只是对PB敏感的,对两种药物耐药的有8只,ADT值不定不能分组5只,药物敏感大鼠16只,耐药率为27.58%。每只癫痫大鼠要经过6 w的耐药性筛选,筛选出这8只耐药性癫痫大鼠耗时约20 w,近5 m。
2.2 匹罗卡品耐药性癫痫模型制作 用SD大鼠60只制作模型,有自发性发作29只,成功率为48.33%,植入杏仁核电极后死亡3只,癫痫自发性发作率为100%。模型制作分为4批,每次15只,每周制作一批。约耗时6 w,共有26只大鼠进行耐药筛选过程,其中对PB耐药有15只,再行CBZ药物筛选,其中3只对CBZ敏感,剩下的12只既对PB耐药也对CBZ耐药,共筛选出耐药模型大鼠12只,不能分组3只,药物敏感癫痫大鼠11只,耐药率为46.15%,而杏仁核模型为27.58%。 可见匹罗卡品模型更易导致耐药性癫痫模型。药物筛选耗时4 w,制作匹罗卡品耐药性癫痫模型约耗时10 w。
2.3 两种模型的行为学对比 在癫痫发作的级别上,杏仁核模型发作Racine分级平均秩次为7.00;而匹罗卡平模型发作Racine 分级平均秩次为14.00(P=0.07),两种方法无显著性差异,但匹罗卡品模型较杏仁核电刺激点燃模型癫痫发作持续的时间长,发作的频率高(见表1)。
2.4 癫痫大鼠脑电图变化 正常大鼠脑电图波形频率以5~10 Hz为主,波幅小于20 μV。杏仁核模型的癫痫发作时脑电图频率增加达到20~30 Hz,波幅增高达到80~90 μV;而匹罗卡品模型发作时的脑电图则表现为频率30 Hz以上,波幅100~1000 μV,以连续高波幅棘波、棘尖波或棘慢波、尖慢波发放为主(见图1)。
2.5 耐药性癫痫海马组织超微结构变化 正常大鼠电镜下神经元结构总体能观察到丰富的细胞器,核膜完整的,线粒体和内质网正常。匹罗卡品敏感及耐药模型的超微结构的损伤均较杏仁核严重(见图2)。
2.6 耐药性癫痫患者海马组织超微结构变化 本课题组在临床工作中收集了8例耐药性癫痫患者的脑组织,这些患者是根据临床表现、视频脑电图监测及神经影像学检查确诊为耐药性颞叶癫痫的,通过多种的抗癫痫药物长期不能控制癫痫的发作,行手术切除致痫灶,全部患者术中留取海马、颞叶病灶脑组织作病理检查,观察颞叶癫痫患者病灶脑组织病理结构变化。电镜结果提示:部分髓鞘增厚、水肿,髓鞘板层结构松解紊乱,神经元轴突水肿,神经胶质细胞水肿、细胞器减少。与上述匹罗卡品耐药性癫痫大鼠表现基本一致,提示匹罗卡品模型方法可靠易行(见图3)。
表1 杏仁核慢点燃模型与匹罗卡品模型发作持续时间及频率
与杏仁核点燃模型组比较*P<0.05,有显著性差异。由上表可见,匹罗卡品癫痫模型发作持续的时间及发作的频率均较杏仁核电刺激模型增加
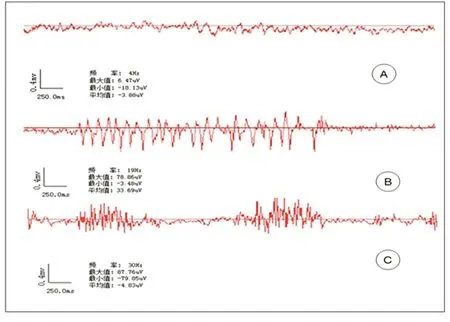
图1 杏仁核模型及匹罗卡品模型大鼠脑电图变化(A.正常脑电图,以正常的α波和β波为主;B.杏仁核模型大鼠脑电图,频率19 Hz,波幅在100 μV以下,以连续发放的尖波为主;C.匹罗卡品模型脑电图,频率30 Hz,波幅在100 μV以上)
3 讨 论
杏仁核模型成功率51.6%,匹罗卡品模型为48.33%。但是杏仁核模型有自发性癫痫发作的大鼠仅有1只,为3.33%,而匹罗卡品模型都有自发性发作,自发率为100%。所不同的是杏仁核模型从刺激开始到大鼠出现行为上的癫痫发作需要6~8 w,有时长达2个多月也没有发作,只有弃用,耗时较长,31只完全点燃耗时约15 w。且需每天刺激,在刺激时大鼠烦躁异常,容易抓脱电极或者颅内感染导致实验失败;而匹罗卡品模型,从注射药物开始30 min内即出现SE的表现,抽搐停止后2 w,若出现自发性癫痫发作,即为模型成功,模型制作相对简便,29只制作成功的周期为6 w。模型成功后癫痫发作频繁,癫痫发作持续时间和发作频率都较杏仁核模型明显增多,自发性发作率高。但匹罗卡品模型的死亡率较高为26.7%,实验中死亡16只。
只有在普通癫痫模型的基础上经过作用机制不同的两种抗癫痫药物治疗足够时间,仍然无效的才能认为是耐药性癫痫模型。本实验中对杏仁核和匹罗卡品模型,我们均用两种作用机制不同的一线抗癫痫药(PB、PHT或CBZ)进行耐药性癫痫的筛选,杏仁核模型选用的是PHT和PB,耗时6 w,而匹罗卡品模型选用的是PB和CBZ,耗时4 w,原因是PHT和CBZ作用机制是基本一致的钠通道阻滞剂,而PHT由于在临床中应用副作用很大,已经逐渐退出临床使用,所以在试验过程中价格昂贵,购买困难。而CBZ目前广泛的应用于临床,是国际抗癫痫协会推荐的一线抗癫痫药物,目前广泛用作耐药性模型的筛选[13,14]。
我们实验结果表明杏仁核耐药性癫痫耐药率27.58%,匹罗卡品耐药率为38.48%,筛选过程与Wang等使用马桑内酯点燃制作的耐药性癫痫模型类似[14],筛选结果与Bethmann K等的研究结果相似[13]。本研究结果表明,无论是电点燃模型还是化学模型筛选出来的耐药性癫痫动物均是客观可靠的,但匹罗卡品模型耐药率较杏仁核电刺激点燃模型耐药率明显升高,使用该模型制作耐药颞叶癫痫模型成功率更高。耐药性癫痫模型海马细胞超微结构表现为核膜不完整、轴索变性水肿、线粒体变性,这些变化类似于Gao等近期发表的研究[15],他们认为线粒体超微结构损伤与实验性颞叶癫痫的长期发作密切相关,而且线粒体易于受到癫痫发作的损害。我们的耐药性颞叶癫痫患者海马组织标本提示髓鞘水肿、增厚、膜结构松解紊乱,实验研究结果与此类似。上述研究结果从形态学上进一步证明了杏仁核点燃耐药模型及匹罗卡品点燃耐药模型的可靠性。
总之,两种模型都是可靠的耐药性颞叶癫痫的模型,杏仁核模型主要是对大鼠脑组织损伤小,能够模拟人类癫痫发作过程,但制作过程复杂困难,耗时长,耐药率低。而匹罗卡品模型制作简便,自发率高,癫痫发作持续的时间及频率高,超微结构破坏严重,更利于耐药性机制的研究。
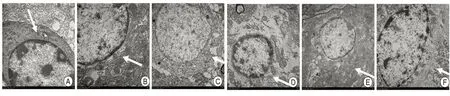
图2 杏仁核及匹罗卡品模型海马超微结构(电镜×1500倍)。图A~D为正常电镜下神经元结构;B为杏仁核敏感组的海马神经元:神经元形态有所改变,但核膜基本完整,可见线粒体肿胀,细胞器减少;E为匹罗卡品敏感组海马神经元,E的损伤较B更为严重,胞体浓缩变性,核皱缩变形,核膜有轻度内陷,线粒体肿胀,粗面内质网肿胀变性,胞浆淡染,核膜不规则;C为杏仁核耐药组海马神经元,在B的基础上可见部分髓鞘增厚、水肿,髓鞘板层结构松解紊乱,神经元轴突水肿,神经胶质细胞水肿;F为匹罗卡品耐药组,在E的基础上可见,粗面内质网减少,内质网的核糖体脱落,游离核糖体解聚,胞质中微丝增多, F的损伤较C更加严重。提示匹罗卡品耐药模型的超微结构的损伤较杏仁核严重
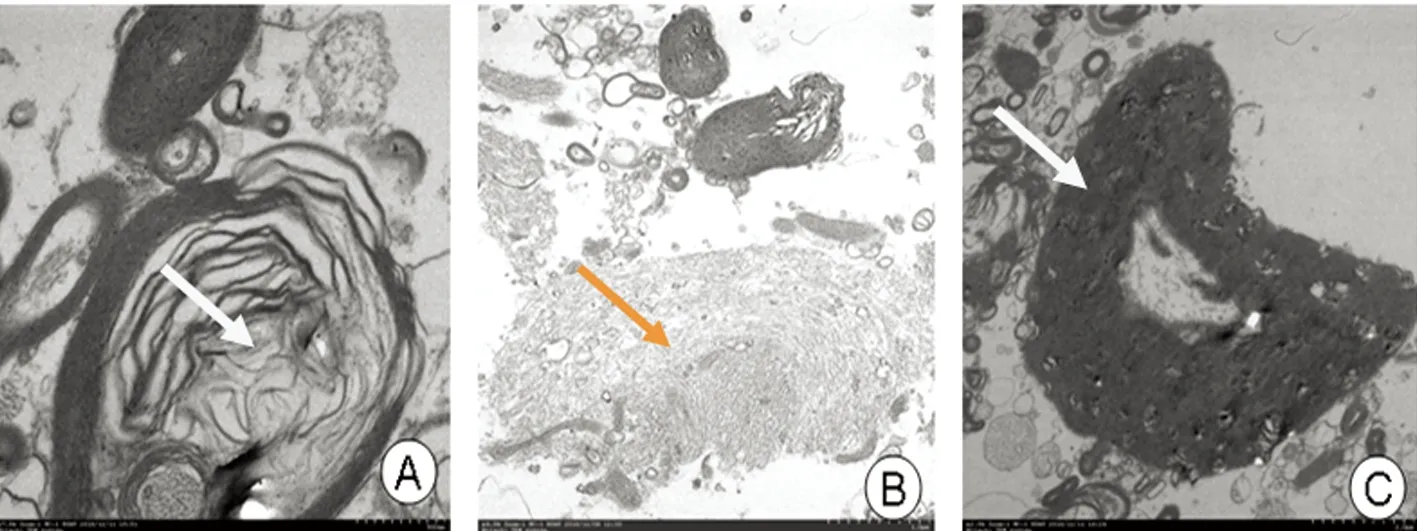
A和C提示髓鞘增厚、水肿,部分髓鞘板层结构松解紊乱;B示神经元轴突水肿,神经胶质细胞水肿、细胞器减少
图3 耐药性癫痫患者电镜下脑组织超微结构变化

