12 例低磷性骨软化症误诊误治临床分析
许志阳 李文波 黄子达 方心俞 张文明
作者单位:350005 福州,福建医科大学附属第一医院关节外科
低磷性骨软化症 ( hypophosphatemic osteomalacia,HO ) 是由低血清磷酸盐水平致骨基质磷酸盐矿化缺陷引起的罕见代谢性骨病[1]。该病根据病因可分为遗传性、散发性、药物性、肿瘤性四类[2]。HO 临床表现为渐进加重骨痛,肌痛,疲乏无力,行走困难,反复或多发应力性骨折。实验室检查常示低血磷、高血碱性磷酸酶,血钙、血钾正常或降低,甲状旁腺素、降钙素一般正常;24 h 尿磷大都升高,但当血磷过低时 24 h 尿磷可不升高。骨 X 线片可见骨密度普遍减低,骨小梁影模糊,常见假骨折线,骨密度显示骨质疏松[3-4]。
临床工作中 HO 被延误诊治的病例屡见不鲜[5-8]。究其原因,HO 疼痛症状分布广泛,定位模糊,缺乏明显特异性,容易与其它病症混淆,如:脊柱关节病,骨质疏松症,多发性骨髓瘤,转移性骨病,风湿性多肌痛,多发性肌炎,纤维肌痛,弥漫性特发性骨质增生症和甲状旁腺疾病等[9]。此外,本病为罕见代谢性疾病,临床医师对本病认识不足,生化血磷酸盐水平降低在临床工作中往往不受重视也可能是临床延误诊治的重要原因。
HO 早期诊断及时治疗可预防不良后果如骨折等的发生,改善本病的预后及提高患者的生活质量。相关文献报道,药物性 HO,确定诊断后停止相关药物,补充中性磷,钙剂和维生素 D 可治愈[10]。肿瘤性 HO 确定诊断并成功定位致病肿瘤后,予完整手术切除可治愈[11]。本研究通过回顾性分析 2008年 7 月至 2016 年 10 月福建医科大学附属第一医院骨肿瘤与关节外科收治的 12 例 HO [ 7 例阿德福韦酯相关 ( ADVO ),2 例肿瘤性,3 例散发性 ] 的临床表现和诊治经过,结合文献分析,旨在比较不同病因HO 的临床特征并解释相关机制,分析临床延误诊治原因,总结诊断方法和治疗规范。
资料与方法
一、纳入与排除标准
1. 纳入标准:选自 2008 年 7 月至 2016 年 10 月于我科确诊为 HO 且治愈或治疗后长期缓解者。
2. 排除标准:( 1 ) 严重骨质疏松伴低血磷者 ( 抗骨质疏松治疗有效 );( 2 ) 晚期淋巴伴低血磷瘤者;( 3 ) 原发或转移性恶性骨肿瘤伴低血磷者。
本研究共纳入 12 例,男 7 例,女 5 例,年龄20~72 岁,平均年龄 49.9 岁。其中 7 例患乙型病毒性肝炎 5~40 年,平均 16.3 年。均服用抗乙肝病毒药物阿德福韦酯 ( ADV ) 10 mg / 天治疗,用药时间2~6 年,平均 4.6 年。2 例经相关影像检查发现肿瘤 ( 分别位于左胸壁和右踝部 ),经手术切除,术后病理证实为磷酸盐尿性间叶肿瘤。余 3 例无明显家族史及相关抗逆转录病毒药服药史,相关影像检查无阳性发现,考虑散发性 HO,予口服中性磷、补充钙和维生素 D 后疼痛症状可缓解,生化指标恢复正常。
二、临床表现
症状体征:11 例表现为全身多部位骨关节疼痛( 包括腰背部、胸部肋骨、髋部和股骨、膝关节和踝关节 ),6 例因膝关节疼痛伴行走困难就诊,4 例因髋部疼痛就诊,1 例因渐进加重腰背部、胸部季肋区疼痛就诊。1 例因双下肢膝内翻畸形 10 余年,伴双膝关节疼痛 1 年就诊。体格检查:8 例胸廓挤压痛阳性,6 例脊柱叩击痛阳性,活动受限,6 例膝关节压痛阳性,4 例髋部“4 字试验”阳性。1 例略呈“0”形腿,肌力及肌张力均正常。
实验室检查:血、粪常规、肝功能、血钾、血钙、血氯均正常。血尿酸 72.7~352.7 μmol / L,除病例 8,9,10,12 外,余病例尿酸均降低,血肌酐均正常。12 例均行尿常规检查,6 例表现非糖尿病性糖尿和蛋白尿。肾小球滤过率和血清胱抑素 C 均正常。7 例行 24 h 尿磷检查,2 例正常,5 例降低。血磷 0.32~0.65 mmol / L,均降低。骨代谢指标:血碱性磷酸酶 85~528 U / L,除病例 9 数据丢失,病例 10 正常,其余患者血碱性磷酸酶升高。8 例行骨代谢检查,6 例表现为 25 ( OH ) D3降低,总 I 型胶原氨基端延长肽 ( PINP ) 升高和 β 胶原特殊序列( β-CTx ) 升高,骨钙素 ( N-MID ) 均正常。
影像检查:12 例均行骨 X 线片检查,提示所示部位诸骨骨密度减低,骨小梁稀疏,4 例伴股骨颈骨折,有假性骨折线。5 例行全身骨显像,均示全身多发骨代谢异常活跃,见于多处肋骨,脊柱,骨盆,踝、膝及髋关节等。3 例行18F-PET / CT 检查,2 例发现高代谢病灶,后证实为肿瘤相关 ( TIO ) 的致病肿瘤。
三、诊断与治疗
12 例中有 10 例曾被错误诊断并延误治疗或予不恰当手术或药物治疗。其中被误诊为骨质疏松4 例 ( 2 例予“密盖息”治疗后血磷进一步下降 ),股骨颈病理性骨折 2 例 ( 1 例于外院行人工髋关节置换术 ),颈椎病 1 例 ( 于我院脊柱外科行颈椎前路椎管减压术+颈椎植骨术+前入路颈椎融合术 ),胸椎病变 1 例 ( 于我院神经外科行 T5~9椎管内病变探查+固定术 ),双膝骨性关节炎 1 例 ( 于外院行关节腔内注射玻璃酸钠 ),腰椎间盘突出症 1 例 ( 对症抗炎止痛处理 )。患者经上述治疗后全身疼痛症状均无明显缓解。余 2 例外院均予抗炎止痛对症治疗,效果均不理想。
12 例经我科明确诊断后,给予治疗,患者全身疼痛症状均明显缓解,复查血生化指标恢复正常。2 例 TIO 发现致病肿瘤后均予手术切除,术后病理回报典型磷酸盐尿性间叶肿瘤,术后 2 周血磷升至正常,症状缓解,随访 2 个月症状消失。1 例 8 年后肿瘤原位复发,症状复现,予再次手术后治愈。7 例确诊为 ADVO 的 HO,均予停用 ADV,改恩替卡韦抗病毒治疗,同时予补充中性磷 ( 磷酸氢二钾6.4 g+磷酸氢二钠 73.1 g+1000 g 蒸馏水,每次 20~40 ml,3~4 次 / 天 ),钙剂和维生素 D 治疗。血磷2 周至 2 个月恢复正常,症状 2 周至 3 个月缓解或消失,患者症状消失后予停服中性磷、钙剂和维生素 D。3 例散发性 HO 予补充中性磷、钙剂、维生素D 后疼痛症状均缓解或消失,此后定期复查血磷,间断补充中性磷,患者未再发疼痛症状。
结 果
HO 常以膝、踝关节疼痛为首发表现,随着病情的进展,疼痛呈向心性、进行性加重,继而波及双髋关节,腰骶部及季肋部,影响翻身及行走,负重活动时加重,呈全身弥漫性疼痛及触痛[12]。结合12 例症状特点分析,肿瘤性、ADVO、散发性 HO 表现并无明显区别。分析 12 例尿检查,ADVO HO 常伴尿糖升高 ( 2.8~11.0,平均 5.22 mmol / L ),尿蛋白亦升高 ( 0.3~0.7,平均 0.47 g / L ),肿瘤性 HO 患者及散发性 HO 患者则大多正常 ( 表 1 )。分析 12 例生化指标,均表现血磷降低。ADVO HO 患者常伴血尿酸降低 ( 72.7~196.4,平均 135.9 μmol / L ),TIO 患者及散发性 HO 患者则大多正常,12 例肾小球滤过率 ( GFR )、胱抑素 C 和血肌酐 ( Cr ) 均正常 ( 表 2 )。骨代谢表现为骨矿化原料 25 ( OH ) D3和血磷不足,代表成骨细胞活性的碱性磷酸酶 ( AKP ) 升高 ( 136~528,平均 250.2 U / L )、总 I 型胶原氨基端延长肽( PINP ) 亦升高 ( 39.6~156.7,平均 100.2 ng / ml ),代表破骨细胞活性的指标 β-CTx 亦升高 ( 0.38~3.34,平均 1.38 ng / ml ) ( 表 3 )。
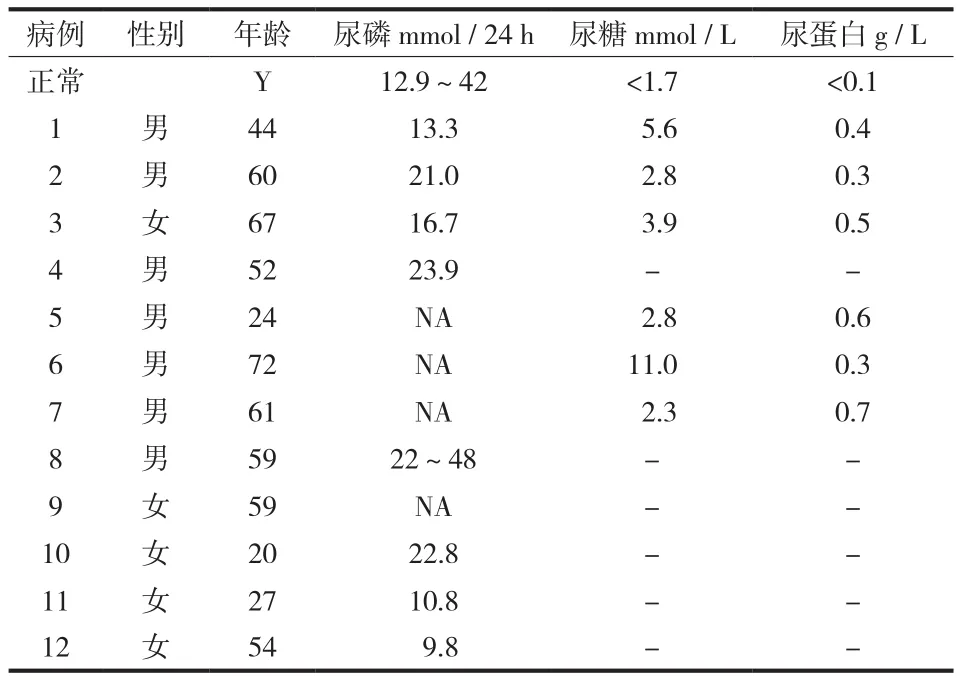
表1 12 例尿检查Tab.1 Urine examination of the 12 patients

表2 12 例血生化检查Tab.2 Blood biochemical tests of the 12 patients
本组 10 例曾被误诊,误诊率 83.3%,误诊时间 1~16 个月,平均 8.9 个月,其中被误诊为骨质疏松 4 例 ( 33.3% ),脊柱关节病 5 例 ( 41.7% ),膝关节退行性变 1 例 ( 8.3% )。3 例被误用了骨软化症禁用的密盖息 ( 鲑降钙素 ) 治疗,1 例股骨颈骨折行人工髋关节置换手术,2 例脊髓疾病并行手术治疗( 表 4 )。ADVO 患者均停用 ADV,改用其它抗病毒药,同时补充碳酸钙、骨化三醇及磷酸盐治疗 ( 2 周至 3 个月,平均 1 个月 );TIO 患者予手术切除肿瘤,1 例同时予补充磷酸盐 2 周;散发性 HO 长期间断补充磷酸盐。患者疼痛及肌无力症状均逐渐缓解并最终消失。12 例确诊前均经多模式对症止痛治疗,症状缓解均不明显。

表3 12 例骨代谢指标Tab.3 Bone metabolism of the 12 patients

表4 12 例误诊误治情况Tab.4 Misdiagnosis and mistreatment of the 12 patients
讨 论
HO 临床表现主要为进展性骨关节疼痛,常开始于负重部位,如膝踝关节,疼痛呈向心性、进行性加重,逐渐扩散到髋部、腰背和肋骨,常伴肌肉疲劳无力和行走困难[3]。HO 实验室检查几乎均表现低血磷、高血碱性磷酸酶,药物性 HO 常伴低尿酸血症、非糖尿病性糖尿和蛋白尿,肿瘤性 HO 及散发性 HO 患者则几乎见不到。其原因是 ADV 相关HO 主要发病机制是药物损伤肾小管引起的范可尼综合征[12];肿瘤性 HO 主要是神经内分泌肿瘤分泌调节因子 FGF23 调节肾脏磷代谢[13];散发性 HO 具体机制尚不明确,以肾脏磷代谢异常为主,一般不伴肾损害[14]。
研究表明,人体代谢经肾小球滤过的磷 80%~90% 被肾小管重吸收,其中 65% 在近端肾小管[15],体内的尿酸约 2 / 3 经肾小球滤过,其中近 90% 在近端肾小管主动重吸收[16]。ADVO HO 因肾脏近曲小管阴离子转运蛋白 1 ( HOAT1 ) 对某些药物 ( 如 ADV )有较强的浓聚作用,引起 ADV 在近曲小管上皮细胞内蓄积,抑制线粒体 DNA ( mtDNA ) 聚合酶,使线粒体耗竭,阻断上皮细胞的氧化呼吸,最终导致近曲小管上皮细胞功能障碍及凋亡,表现为近曲小管功能障碍为特征的范可尼综合征[17]。范可尼综合征是近端肾小管复合性功能缺陷疾病,由于近端肾小管对多种物质的重吸收障碍,临床表现为肾性糖尿、蛋白尿、磷酸盐尿、尿酸盐尿等,并相应出现低血磷、低尿酸及近端肾小管性酸中毒,进而导致骨病 ( 骨软化、骨质疏松,表现为骨痛、骨畸形 ) 的发生[18]。
文献报道,甲状旁腺素 ( PTH )、内分泌成纤维细胞生长因子 ( FGF23 )、降钙素、心钠素、糖皮质激素,高钙血症和磷酸盐负荷抑制肾磷酸盐重吸收[19]。相反,IGF-1,生长激素,胰岛素,甲状腺激素,EGF,碱中毒,低钙血症和磷酸盐剥夺 ( 消耗 ) 刺激肾脏磷酸盐重吸收。目前比较公认的肾小管磷酸盐重吸收的主要调节剂是 PTH 和 FGF23[15]。本组 12 例除 3 例未检测 PTH 外,余病例 PTH 均正常,除 1 例血钙稍低,余病例均正常。肿瘤性 HO与肿瘤分泌成纤维细胞生长因子 ( FGF23 ) 有关,FGF-23 通过与肾小管上皮细胞成纤维细胞因子 1c受体 ( FGFR1c ) 及其共受体结合,形成活化的受体复合物进一步减少近端小管钠磷转运子 ( NaPi-11a和 NaPi-11c ) 的表达,从而抑制了肾脏对磷的重吸收引起低磷血症[20]。故这类患者无肾小管损害,不表现非糖尿病性糖尿、蛋白尿,且血尿酸正常。同理,散发性 HO 患者尿常规正常,血尿酸正常,仅表现为低血磷和高血碱性磷酸酶,可以推测患者并无肾小管功能障碍,可能系这类患者体内高表达与肾脏磷代谢调节相关因子的调控基因,有待进一步研究证实。
HO 临床诊断困难,误诊误治常见,本组 12 例有 10 例曾被误诊为骨质疏松、脊柱关节病等,并予不当治疗。主要原因为 HO 疼痛症状分布广泛,定位模糊,缺乏明显特异性[6],此外,本病属罕见疾病,临床医师对本病认识不足,常过分依赖影像学发现,未能全面分析这些患者存在的其它实验室生化异常表现[8]。结合本组病例实验室生化特点,临床疑诊 HO 病例,尚需鉴别其病因。若同时合并低尿酸,非糖尿病性糖尿、蛋白尿等肾小管功能障碍表现,考虑 ADVO HO 可能性大,详细追问有无相关服药史。对于肾小管功能正常患者,需进一步完善相关检查排除肿瘤性 HO 可能,文献报道肿瘤性 HO 致病肿瘤的定位方法有全身 CT 或磁共振成像[21],奥曲肽显像[22],全身静脉分段取血测FGF-23 水平[23-25],PET / CT 检查[26-33]。现有研究认为,基于生长抑素受体的扫描包括99Tc-HYNIC-TOC SPECT / CT 和68Ga-DOTA-TATE PET / CT 对致病肿瘤的定位敏感性和特异性均最佳[34]。散发性 HO 必须排除肾脏疾病继发原因,而且无家族史,无基因突变和肿瘤性骨软化症方可诊断[8]。
HO 经明确诊断后,针对不同病因给予合理治疗,均能取得较好疗效。对于 ADVO HO,立即停用 ADV,改用恩替卡韦抗乙肝病毒治疗,同时予碳酸钙 ( 1.5 g / 天 ) 和骨化三醇 ( 0.5 μg / 天 ),若合并严重代谢性酸中毒的患者,予加用碳酸氢钠 ( 1.5 g /天 )[3]。值得注意的是,Wei 等[3]研究认为此类患者不需要常规补充磷酸盐,相反,Xu 等[10]则建议常规口服中性磷溶液补充元素磷 ( Na2HPO4 · 12H2O 73.1 g,NaH2PO4 6.4g,H2O 1000 ml,pH=7.0,20~40 ml / 天 )。结合笔者的病例分析,建议对于血磷酸盐较低、病程较长的患者给予补充元素磷 ( 口服中性磷或甘油磷酸钠 )。有学者认为 ADV 所致肾小管损害是可逆的[35],笔者认为可通过复查其血磷、血尿酸、尿常规来评价患者肾小管功能恢复情况。对于肿瘤性 HO,致病肿瘤一经定位,手术完全切除肿瘤是最有效的治疗方案,当肿瘤位于骨头,边界不清,难以完全切除时,可以考虑扩大范围的肿瘤边缘刮除,相比之下,行肿瘤刮除术复发的风险高于肿瘤完整切除术[36],术后定期复查血磷可帮助早期发现复发肿瘤,及时干预,减少骨折等不良后果发生[11]。对于散发性 HO,予长期补充磷酸盐、碳酸钙、骨化三醇可缓解甚至消除全身骨痛等症状。
结论:临床表现为进展性多发骨关节疼痛,伴肌肉疲劳无力和行走困难的患者,应全面分析其实验室生化异常表现。生化表现低血磷、高血碱性磷酸酶者应考虑到 HO 诊断,伴低尿酸血症、非糖尿病性糖尿和蛋白尿者应追问有无 ADV 服药史以明确是否为 ADVO HO;不伴低尿酸血,尿常规正常患者应进一步追问家族史及完善相关检查鉴别肿瘤性 HO 和散发性 HO。确诊 ADVO HO 患者,立即停用 ADV,改用恩替卡韦抗乙肝病毒治疗,同时予碳酸钙和骨化三醇治疗,病程较长、症状较重者同时补充磷酸盐,治疗过程定期复查血磷、血尿酸和尿常规检查。肿瘤性 HO 定位致病肿瘤后均应手术切除,肿瘤完整切除术优于肿瘤刮除术,术后定期复查血磷可早期发现肿瘤复发。散发性 HO 长期补充磷酸盐、碳酸钙和骨化三醇可缓解全身骨痛等症状。

