HPLC-MS/MS法同时测定枫蓼肠胃康合剂、胶囊中10种成分
梁 颖,许文佳,符策奕,陈国彪
(海南省药品检验所,海南 海口 570216)
枫蓼肠胃康是以辣蓼和牛耳枫为原料制成的纯中药制剂,具有理气健胃、除湿化滞等功效[1],临床上对急慢性肠胃炎、肠易激综合征、溃疡性结肠炎等胃肠道疾病具有显著疗效[2-5],并且无明显不良反应。国家食品药品监督管理总局颁布的枫蓼肠胃康标准中,以芦丁为含有量指标对其进行质量控制,但中药复方制剂具有多组分、多靶点、协同作用的特点,单一成分难以全面反映其质量和疗效[6]。近年来报道枫蓼肠胃康中的有效成分主要为黄酮[7-10],并用液相色谱法对其进行定量分析[11-13];另有学者确定其中含有酚酸类成分,并测定其含有量[14-15],但迄今尚无同时对黄酮、酚酸等多种成分进行准确定量分析的报道。
高效液相色谱-质谱联用法(HPLC-MS/MS)具有较高的专属性和灵敏度,可在较短时间内同时对酚酸、黄酮类成分进行有效分离,并完成准确定性定量分析[16],大大提高了检测效率。因此,本实验建立该方法同时测定枫蓼肠胃康合剂、胶囊中10种成分(没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素)的含有量,以期全面评价该复方质量。
1 材料
1.1 仪器 U3000 液相色谱仪(美国Thermo公司);API4000+质谱仪,配置AB SCIEX质谱工作站(美国AB公司);Mili-Q 超纯水器(美国Millipore公司);XS205DU 电子分析天平(德国Sartorius公司);SK8210HC 超声波提取仪(上海科颉贸易有限公司)。
1.2 试药 枫蓼肠胃康合剂(海南万州制药有限公司,批号 151001、151102、151103、151201、160101、160102);枫蓼肠胃康胶囊(海口奇力制药股份有限公司,批号 S141201、S141202、S141203)。没食子酸(批号 110831-201605,含有量 90.8%)、原儿茶酸(批号 110809-200503)、芦丁(批号 100080-201610,含有量 91.9%)、金丝桃苷(批号 111521-201708,含有量 95.1%)、山柰酚-3-O-芸香糖苷(批号111207-201602,含有量90.8%)、槲皮苷(批号 111538-200302)、槲皮素(批号 100081-201509,含有量 98.1%)、山柰酚(批号 110860-201310,含有量 93.2%)、芹菜素(批号111901-201102,含有量 99.6%)、异鼠李素(批号 110860-201410,含有量 99.9%)对照品均购自中国食品药品检定研究院。甲醇、乙腈、乙酸为色谱纯;水为超纯水(电阻率18.2 MΩ·cm)。有机滤膜(尼龙,0.22 μm)。
2 方法与结果
2.1 对照品溶液制备 精密称取没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素对照品适量,甲醇分别制成 1.107、1.087、1.130、0.976、1.265、1.072、1.146、0.456、0.813、0.092 7 mg/mL 贮备液,分别精密吸取 2、10、10、1、10、5、1、2、1、10 mL,置于同一 100 mL 量瓶中,甲醇分别稀释成 0.022 1、0.108 7、0.113 0、0.009 76、0.126 5、0.053 6、0.011 5、0.009 12、0.008 13、0.009 27 mg/mL,即 得,于 4 ℃ 下保存。
2.2 供试品溶液制备 精密量取2 mL 合剂于50 mL量瓶中,甲醇定容至刻度,摇匀,精密量取1 mL 于 10 mL 量瓶中,甲醇定容至刻度,摇匀,即得(用于测定芦丁、没食子酸)。再取胶囊内容物适量,混匀,精密称取 0.4 g,置于 50 mL 量瓶中,加 40 mL 甲醇超声 20 min,放冷,甲醇定容至刻度,摇匀,精密量取 2 mL,置于10 mL 量瓶中,甲醇稀释至刻度,摇匀,即得(用于测定芦丁、没食子酸)。上机测定前,溶液均用 0.22 μm 微孔滤膜过滤。
2.3 色谱条件 Luna C8色谱柱(2 mm×100 mm,3 μm);流动相乙腈(A)-水(B)(含 0.1% 乙酸),梯度洗脱(0~2 min,5%A;2~4 min,5%~20%A;4~6 min,20%A;6~12 min,20%~30%A;12~17 min,30%A;17~23 min,30%~5%A;23~30 min,5% A);柱温 35 ℃;体积流量0.3 mL/min;进样量 1 μL。
2.4 质谱条件 电喷雾负离子模式,多反应监测(MRM);离子喷雾负电压 4.5 kV;离子源温度450 ℃;帘气 15 kPa;碰撞气氮气;雾化气45 kPa;辅助气 45 kPa,质谱参数见表1,总离子流色谱图见图1。

表1 各成分质谱参数Tab.1 MS parameters for various constituents
2.5 方法学考察

图1 各成分总离子流色谱图Fig.1 Total ion current chromatograms of various constituents
2.5.1 线性关系考察 取 “2.1”项下贮备液适量,50%甲醇制成系列质量浓度对照品溶液,在“2.3”~“2.4”项条件下进样测定。以色谱峰峰面积为纵坐标(Y),溶液质量浓度为横坐标(X)进行回归,以 S/N=10 为定量限,S/N=3 为检测限,结果见表2,可知各成分在各自范围内线性关系良好。
2.5.2 精密度试验 取 “2.5.1”项下中间质量浓度的对照品溶液,在 “2.3”~“2.4”项条件下进样测定 6 次,测得没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素峰面积 RSD分别为6.55%、6.30%、6.29%、5.59%、6.89%、5.67% 、6.24% 、6.75% 、6.75% 、4.23% ,表 明仪器精密度良好。
2.5.3 重复性试验 取合剂(批号151201)、胶囊(批号 S141201)适量,按 “2.2”项下方法制备供试品溶液各 6 份,在 “2.3”~“2.4”项条件下进样测定,测得合剂供试品溶液中没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素含有 量 RSD 分 别 为 4.90%、2.95%、6.47%、5.23% 、7.55% 、7.47% 、5.19% 、3.31% 、5.60% 、5.28%,胶囊供试品溶液中分别为4.93%、7.87%、6.40% 、7.10% 、8.91% 、3.44% 、6.54% 、6.88% 、7.91%、7.55%,表明该方法重复性良好。
2.5.4 稳定性试验 取合剂(批号151201)、胶囊(批号 S141201)适量,按 “2.2”项下方法制备供试品溶液,室温下于 0、2、4、8、12、24 h在 “2.3”~“2.4”项条件下进样测定,测得合剂供试品溶液中没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素含有量 RSD 分别为5.15% 、5.62% 、6.37% 、5.50% 、6.68% 、4.88% 、2.21% 、5.34% 、7.27% 、6.88% ,胶 囊供试品溶液中分别为 3.98%、6.30%、5.37%、6.28% 、7.73% 、4.27% 、8.54% 、6.46% 、7.47%、7.22%,表明溶液在24 h 内稳定性良好。
2.5.5 加样回收率试验 精密移取合剂(批号151201)1 mL,置于 50 mL 量瓶中,精密加入“2.1”项下对照品溶液适量(使对照品加入后成分含有量与测定成分原含有量的比例约为80%、100% 、120% ),平行 3 份,按 “2.2”项下方法制备供试品溶液 A,在 “2.3”~“2.4”项条件下进样测定,计算 8种成分(芦丁、没食子酸除外)回收率;同法制备供试品溶液B,计算芦丁、没食子酸回收率。结果,没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素平均加样回收率分别为101.7%、104.0%、101.3%、100.4%、95.4%、99.5% 、102.0%、100.4% 、102.0% 、101.4%,RSD分别为3.5%、6.4%、8.7%、8.0%、8.0%、4.3%、5.2%、7.5% 、6.2% 、5.7%。
精密称取胶囊(批号S141201)内容物0.2 g,置于50 mL 量瓶中,精密加入 “2.1”项下对照品溶液适量(使对照品加入后成分含有量与测定成分原含有量比例约为 80%、100%、120%),平行3 份,按 “2.2”项下方法制备供试品溶液 A,在“2.3”~“2.4”项条件下进样测定,计算 8种成分(芦丁、没食子酸除外)回收率;同法制备供试品溶液B,计算芦丁、没食子酸回收率。结果,没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素平均加样回收率分别为 101.6%、103.6% 、99.3% 、96.8% 、99.9% 、101.7% 、100.7%、102.6%、98.2%、98.7%,RSD 分别为3.6% 、7.0% 、7.6% 、8.9% 、4.4% 、5.5% 、6.1% 、4.6% 、6.2% 、7.1% 。

表2 各成分线性关系Tab.2 Linear relationships of various constituents
2.5.6 样品含有量测定 取合剂6 批(批号151001、151102、151103、151201、160101、160102)、胶囊 3批(S141201、S141202、S141203),按 “2.2”项下方法制备供试品溶液,在 “2.3”~“2.4”项条件下进样测定,计算含有量,结果见表3。
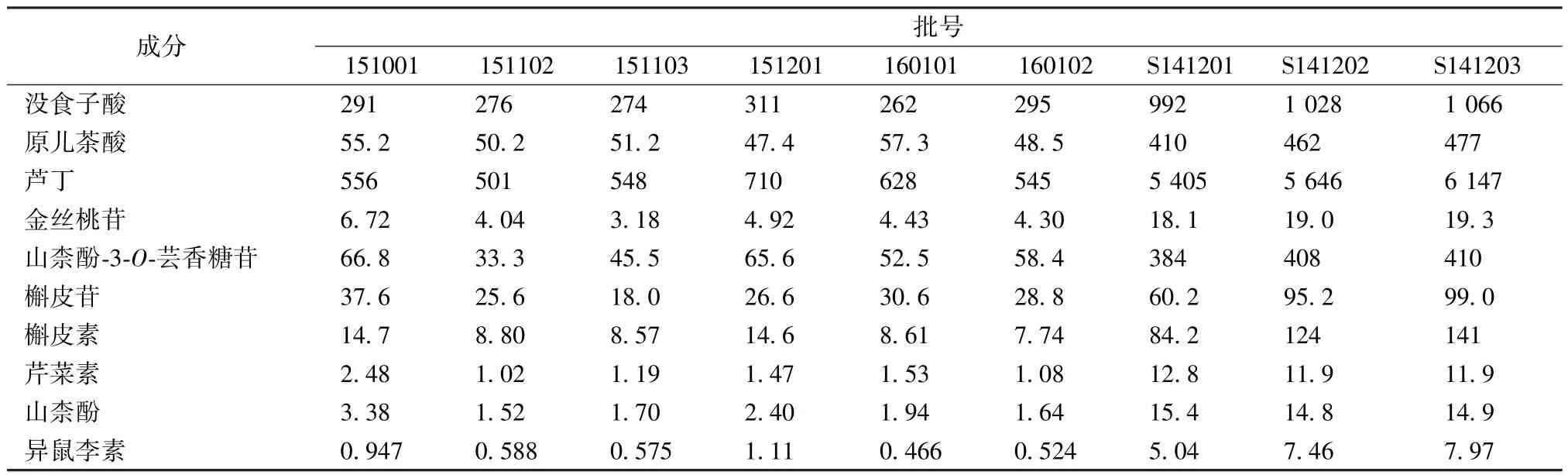
表3 各成分含有量测定结果(n=3)Tab.3 Results of content determination of various constituents(n=3)
3 讨论
3.1 色谱柱选择 文献中通常采用C18色谱柱分离成分,但预实验发现该色谱柱下槲皮素、山柰酚色谱峰拖尾严重,山柰酚、芹菜素、异鼠李素色谱峰分离度不理想,而采用C8色谱柱时各色谱峰分离度比较理想,峰形尖锐对称,故选择其作为分离柱。
3.2 色谱、质谱条件优化 由于10种成分中有一些性质接近,故选择梯度洗脱方式,可使所有成分得到完全分离。本实验分别考察甲醇-水、乙腈-水、甲酸-水、乙酸-水、乙酸铵-水的分离效果,发现流动相为甲醇-水时色谱峰噪音较大,响应值偏低,故选择乙腈-水,为了改善待测成分色谱峰峰形,又在流动相中加入一定量酸,最终确定流动相为乙腈-水(含 0.1% 乙酸),此时峰形良好,在17 min内可洗脱出所有成分,从而提高了分离效率。在研究离子扫描模式时发现,黄酮、酚酸类成分在负离子模式下的响应值较高,基于山柰酚灵敏度相对偏低,故提高其驻留时间为100 ms。
3.3 含有量分析 在6 批枫蓼肠胃康合剂、3 批枫蓼肠胃康胶囊中,芦丁含有量最高,并且不同批次样品中各成分含有量存在一定差异,这可能与工艺生产过程中投料药材来源、产地、采收期等,以及不同厂家煎煮、浓缩等环节中温度、湿度控制存在差异有关[17-18]。
4 结论
本实验建立HPLC-MS/MS 法同时测定枫蓼肠胃康合剂、胶囊中没食子酸、原儿茶酸、芦丁、金丝桃苷、山柰酚-3-O-芸香糖苷、槲皮苷、槲皮素、芹菜素、山柰酚、异鼠李素的含有量,该方法高效快速,准确可靠,可为该制剂质量控制提供新的参考方法。