磷酸氢钙生产过程中重金属物质脱除方法改进研究
何 晗
(贵州工业职业技术学院,化学与材料工程学院,贵州 清镇 551400)
磷酸氢钙在生产过程中,由于重金属的含量较高,往往导致产品的重金属含量超标或大量损失磷元素的情况,努力脱除重金属和降低磷的损失是磷酸氢钙生产过程所面对的重要问题[1]。盐酸萃取法在脱除重金属物质中已有多年历史,随着磷元素的紧缺,磷酸氢钙在生产过程中要尽量避免磷元素的损失,还要保证重金属物质的有效脱除,因此,本文采用盐酸萃取法对磷酸氢钙中重金属物质进行脱除[2]。
1 磷酸氢钙生产过程中重金属物质脱除方法优化
(1)设定重金属物质脱除参数。PbS在化学反应中以沉淀的形式存在,且体积非常小,但是PbS沉淀的形成过程需要给予一定的反应条件,因此采用Pb2+和S2-在一定条件下形成沉淀的方式来对磷酸氢钙生产过程中的重金属进行脱除。在酸性环境中Pb2+和S2-很容易就会形成沉淀,降低磷酸氢钙中Pb2+的含量。但是在实际脱除过程中并不是一个简单的生成沉淀的化学反应,脱除过程是一个固、液、气共存的体系,很多因素都会控制PbS沉淀的生成过程,例如温度、PH值、加入盐酸的量、沉淀生成的时间、搅拌强度等。通过进行多次实验进行对比,排除各种因素对沉淀生成的影响,得出影响沉淀生成的因素主要是PH值、反应的时间和加入S2-的量。为了加速重金属PbS沉淀的快速生成,需要让重金属沉淀尽快变大并沉底。因此,实验过程中主要控制Na2S的加入量、溶液的PH值、反应的温度和时间、搅拌强度等因素,使PbS沉淀尽快沉底。
(2)计算沉淀的质量分数。实验过程中,通过计算PbS沉淀的质量分数,来验证磷酸氢钙生产过程中重金属物质是否被完全脱除,从而提高磷酸氢钙的生产效率,首先根据化学方程式计算沉淀的质量,再计算PbS沉淀的质量分数,化学方程式如下:
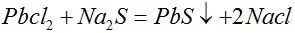

根据硫化铅的质量得出硫化铅的质量分数,再结合硫化钠的加入量和PH值的选择,来脱除磷酸氢钙中的重金属物质。
(3)控制硫化钠的加入量。硫化钠的加入量直接影响PbS沉淀生成的多少,如果加入少量的硫化钠就会导致溶液中还有未反应的重金属存在,如果加入过量的硫化钠会导致溶液中的重金属完全反应,而溶液中还会存在硫化钠溶液,造成得到的磷酸氢钙不纯,是磷酸氢钙和硫化钠的混合物,脱除过程中,溶液的PH值设置在1.5~2.5之间,在溶液中分别加入5ml、10ml和15ml的硫化钠溶液,结果表明,当PH=2.5时,加入15ml质量分数为5%的硫化钠溶液能够完全使PbS沉淀并沉底,最终得到的磷酸氢钙为合格品。
(4)确定萃取液PH值。磷酸氢钙生产过程中重金属物质脱除过程的萃取液采用盐酸,盐酸为酸性体系,与Na2S会发生化学反应,产生硫化氢气体并逸出,而且盐酸的酸性越大,逸出的硫化氢气体就越多。硫化氢气体不仅会污染环境,还会危害职业卫生,导致溶液中的二价硫离子浓度降低,硫化钠的消耗量增加。同时,重金属的硫化物在PH值不同的情况下会发生沉淀或溶解,为了使重金属铅能够有效的被沉淀,加Na2S的时候,要降低溶液的酸度使PH值升高,但是溶液的PH值升高就会导致溶液中磷的损失增大,因此,适当的PH值能保证脱铅效果达到最佳。实验选取的溶液PH值为1.7、1.9、2.4进行,结果显示:PH值等于2.4时,可以将溶液中的Pb2+完全沉淀,达到有效脱除重金属的目的。
(5)实现重金属物质脱除。为了检验重金属物质脱除方法的有效性,通过不同的外界因素对PbS沉淀质量分数的影响进行检测。首先,盐酸加入量的多少影响PbS沉淀质量,盐酸加入过少会使溶液的PH值升高,溶液的PH值升高会使磷元素大量损失,同时,PH升高还可以达到脱氟的目的,使脱铅效果最佳。
其次,萃取液中铅的含量也会影响PbS沉淀质量,铅的含量过多,PbS沉淀生成的质量就多,会造成脱氟不彻底,在萃取过程中,不但要保证重金属铅被完全脱除,还要确保氟也被脱除,从而达到重金属物质的完全脱除。
脱除磷酸氢钙中重金属物质的过程中,要随时观察一切外界因素对脱除结果的影响,并及时化解不利因素的影响,提高磷酸氢钙的纯度。
2 脱除重金属物质实验
本文重点介绍了盐酸萃取法在磷酸氢钙生产过程中脱除重金属物质,为了证明盐酸萃取法比传统脱除法得到的磷酸氢钙纯度高,制定脱除重金属物质实验。
(1)实验材料选择。实验采用质量分数为32.15%的五氧化二磷粉末,重金属中铅的质量分数为428*10-6,盐酸的质量分数为11.5%,质量分数为5%的Na2S溶液。
(2)实验过程。实验采用盐酸萃取法,取磷酸氢钙粉末100g,烧杯中装入70ml的水将磷酸氢钙粉末调匀并升温,向烧杯中加入450ml的盐酸溶液,萃取时的温度保持在40-50摄氏度之间,40分钟后,用石灰乳调节萃取液的PH值,不同的PH值条件下,分别加入不同量的硫化钠溶液反应,通过使用盐酸萃取发与原始脱除法,检测磷酸氢钙中铅的含量。
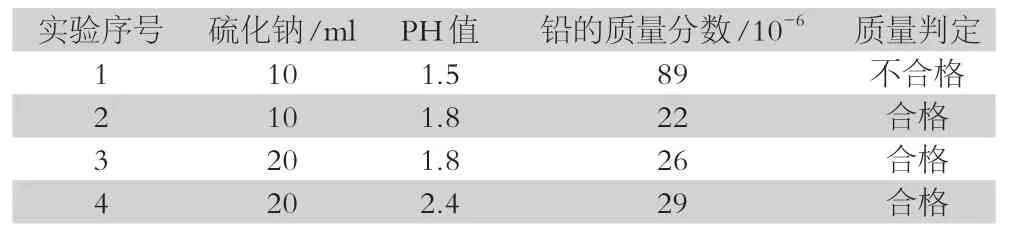
表1 盐酸萃取法实验数据

5 30 1.8 28 合格6 30 2.4 24 合格
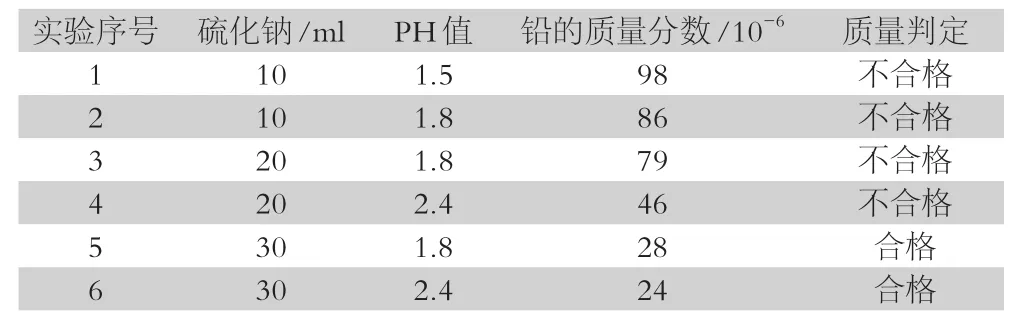
表2 原始脱除法实验数据
实验结果表明如表1、2,盐酸萃取法比原始脱除法得到的硫酸氢钙纯度高、产品合格率高,硫化钠的加入量和溶液的PH值也会影响实验结果,当硫化钠的加入量为30ml、溶液的PH值在2.4和1.8的时候,铅的质量分数小,磷酸氢钙中含铅率低,生产的产品为合格产品,因此,采用盐酸萃取法,且硫化钠的加入量多且溶液的PH值越高,重金属物质脱除的越彻底,磷酸氢钙的纯度越高,产品的合格率越高。
3 结语
重金属物质脱除方法的研究在磷酸氢钙生产过程中具有重要意义。随着科技的进步,重金属物质脱除方法也在不断更新和完善,为磷酸氢钙的生产做出巨大贡献,磷酸氢钙的纯度也越来越高。我国的工业生产中,在重金属物质脱除方法上已经取得了一定的成绩,但还有突破的机会,希望本文的研究能提高磷酸氢钙的生产效率,提升磷酸氢钙的纯度,降低重金属含量指标,为工业生产节约成本、提高利润。

