浅析有机化学重排反应的产生原理
苗培果

【摘 要】有机化学中的反应有非常多的分类,本文就重排反应这一类,进行了一些浅显的讨论和分析,同时介绍了一些重排反应在材料合成和医药领域的具体应用。
【关键词】有机化学;重排反应;产生原理
【中图分类号】R122.1【文献标识码】B【文章编号】1005-0019(2019)13--01
一、有机化学存在的意义
化学在我们日常的生活中无处不在,比如在工业领域,各种粘合剂、清洗剂、油漆等,跟我们健康相关的医药领域,各种感冒药、消炎药,各种制作食品时使用的添加剂等等,都是用到了有机化学的一些反应原理。可以说有机化学改变了我们的生活。
二、有机化学重排反应的概念
2.1 分子重排。
首先我们先了解分子重排,所谓分子重排是指在一些有机化学的反应中,由于试剂的催化或者某些介质的影响,重键的位置发生移动、官能团发生转移或者发生扩环、缩环作用等,这些反应的过程被称为分子重排。
2.2 重排反应。
重排反应是指在某一分子内,某一原子或者基团从一个原子迁到另一个原子而形成新分子的化学反应。通常依据迁移的原子或者基团的起始位置和终止位置的不同,可以将重拍反应分为不同的类别。我们在实际进行合成的运用当中,主要运用其生成双碳键的是σ-迁移重排和正碳离子重排,有的时候也会使卡宾或者自由基参与其中。
三、有机化学重排反应的产生原理
有机化学的重排反应有很多种类,本文选取几个比较典型的重排反应来简单分析一下其中的产生原理。
3.1 Fries重排
酚酯与氯化铝或氯化锌等Lewis酸共热,发生酰基重排以后,能够生成邻羟基和对羟基芳酮的混合物,该反应过程被称为Fries重排。
在制备酚酯的时候,如果所处的温度较低,那么得到的会是对位异构体,如果实验时所运用的温度较高,那么将会得到邻位异构体。同时,相对于芳香酸酚酯,脂肪酸酚酯更容易发生重排反应,这主要与脂肪酸酚酯中的酰基体积有关,其中的酰基体积越大,越容易发生重排反应,但是当苯环上连有强性的吸电基时,会导致其重排的反应度降低。各种酰基重排的活性次序如下:
RCO>PhCH2CO>PhCH2CH2CO>PhCH=CHCO>PhCO
通過上式我们可以看出,邻位重排反应发生的几率与酰基的体积有很大的关系,体积大,发生重排的可能性就大。而当酰基上连有硝基或者卤原子等强性吸电基的时候,发生重排的可能性降低。
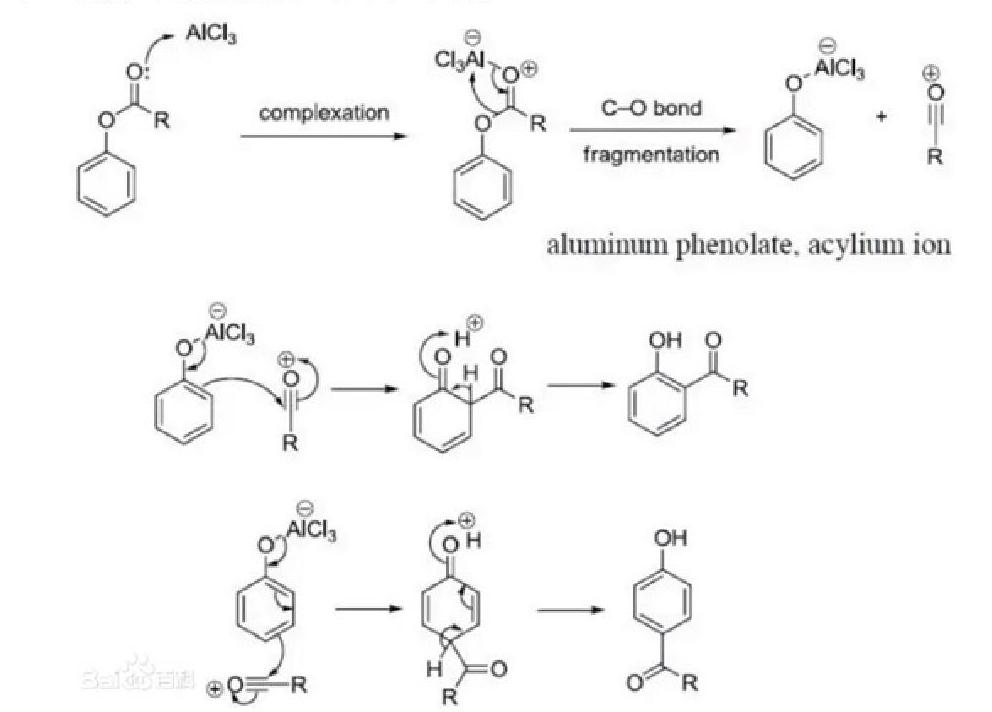
反应机理:Fries 重排的机理并不是十分明确,大部分时候我们认为其使分子内反应,但是从交叉实验的结果看来,Fries重排也可能发生在分子之间。至目前一个比较被广泛接受的反正原理如下图。
该反应原理中,首先是酚酯的羰基氧与路易斯酸性的铝原子进行配位。然后铝基重排到酚氧上,C-O 键断裂,产生酚基铝化物和酰基正离子。酰基正离子接下来在苯环上酚基的邻位或对位对其发生亲电芳香取代,再经水解得到产物羟基芳酮。
3.2 Claisen重排反应
通常,在低温环境下,烯丙基醚是很稳定的,但是一旦在高温200摄氏度的环境中烯丙基醚就会发生重排反应,重排成为邻烯丙基酚,那么这种反应就被称为Claisen重排反应。当发生重排反应时,要看烯丙基芳基醚相邻的两个位置以及对位有没有被取代基占据,如果没有被取代基所占据,此时重排主要得到两个邻位产物,但是当两个相邻位置都让取代基占据的时候,此时重排就会得到对位产物,而当对位和邻位均被占据的时候,就不会发生克莱森重排反应。克莱森重排反应发生时,C-0键断裂开,同时,碳-碳键中的π键也断裂,其中的α-β碳原子之间形成л键,双键从β-γ位转移到α-β位置,在整个反应中,烯丙基不仅发生了重排,同时也进行了异构化。反应机理:克莱森重排反应发生时中间会经过一个环状的过渡态,可以说是个协同反应,所以芳环上取代基的电子效应对重排无影响。
经过一次[3,3]s 迁移和一次由酮式到烯醇式的互变异构,使得烯丙基芳基醚重排为邻烯丙基酚;烯丙基芳基酚的两个相邻位置都被取代基占领的情况下,发生重排时先经过一次[3,3]s 迁移到邻位,此时由于取代基占据着邻位,无法发生互变异构,接着只能又发生一次[3,3]s 迁移移动到对位,然后经互变异构得到对位烯丙基酚。
取代的烯丙基芳基醚重排时,无论原来的烯丙基双键是Z-构型还是E-构型,重排后的新双键的构型都是E-型,这是因为重排反应所经过的六元环状过渡态具有稳定椅式构象的缘故。
3.3 Beckmann重排 贝克曼重排反应是由名字为恩斯特·奥托·贝克曼的德国化学家发现的,因此得名为贝克曼重排反应,其反应过程是由酸来催化的,如果反应物是肟,那么其经过酸的催化,重排反应为酰胺,如果反应物是环肟,那么此时的重排反应物是内酰胺。有如下反应式,该反应式是一个已经广泛的应用于生产生活中的一个反应:
该反应式的反应物就是环己酮,经过贝克曼重排以后生成己内酰胺。己内酰胺就是尼龙6的十分重要的原材料,所以贝克曼重排反应也是对工业生产十分重要的一个反应。在硫酸等酸中以及在五氯化磷、三氯化磷、苯磺酰氯和亚硫酰氯等可以产生强酸的物质中,肟发生重排反应,反应发生相应的取代酰胺。 就比如,环己酮肟在硫酸的作用下发生重排反应,生成己内酰胺。
反应原理:其反应原理为肟在酸作用下,反应发生质子化脱去一分子水,与此同时与羟基处于反位的基团迁移到缺电子的氮原子上,所形成的碳正离子与水反应得到酰胺。
而通过实验二苯甲酮肟的重排反应我们可以发现,在50摄氏度的时候是最适合其发生贝克曼重排反应的温度。在低于50摄氏度的温度时,二苯甲酮肟的转化率较低,这是因为转化反应物需要温度的催化,温度过低也导致活化能不足以支撑发生反应。当温度超过50摄氏度以后,随着温度的不断升高,其转化率也不断降低,这是由于温度过高影响了质子氢与肟羟基氧之间的结合,从而破坏了氢键的形成,使得肟羟基不容易从二苯甲酮肟中脱离出来,最终降低了二苯甲酮肟的转化率。
贝克曼溶剂的主要成分是乙酸、盐酸等,该溶剂主要在日常生产中常用来当做催化剂,有时候也可以使用硫酸和多磷酸等别的酸来做催化剂,在工业生产中制造酰胺的时候,用的最多的是硫酸,这是因为用硫酸和氨进行中和反应以后会得到一种使用广泛的化肥原料硫酸铵,硫酸铵富含氮和硫,能有效改良土壤。
3.4 Curtius 重排
Curtius 重排反应是1890年由Theodor Curtius首先发现的,因此得名。该重排反应是指在加热的条件下,酰基叠氮发生重排反应生成异腈酸酯,这个时候如果加入水,由于水的介入,异腈酸酯会立刻分解,进一步形成脱掉一个碳的胺。但是如果加入的不是水,而是进入合适的醇作为反应剂,此时就会很快形成以各种氨基酸酯类基团作为胺基的保护基。
反应机理: 酰基叠氮在加热下失去氮气生成酰基乃春(氮烯),然后烃基迅速迁移,生成异氰酸酯。有上面分析我们可知该重排反应的特点是,可应用于生成少一个碳的胺类化合物。
Curtius 重排反应还有一些其他方面的应用,比如以苯基环戊基甲酸为原料,經过酰氯化,再接受叠氮化钠进攻,得到酰基叠氮化合物,在加热条件下,酰基叠氮脱氮气重排生成异腈酸脂,经过酸性水解,从而得到胺类化合物。
四、有机化学重排反应的应用
有机化学的重排反应在各个方面都有广泛的应用。比如贝克曼重排反正生成的己内酰胺,在服装工业生产上有着重要的作用;硫酸铵也是贝克曼重排反正生成的,在农业生产领域有着重要的作用;药物合成方面,通过重排反应也为我们解决了很大的问题。
结论
有机化学渗透到了我们生活中衣食住行的方方面面,与我们的生活密不可分,正确认识有机化学的各种重排反应,对于探索未知的世界,起着十分重要的作用,也为我们不断发现新事物奠定坚实的基础。
参考文献
张霜梅. 浅谈有机化学中分子的重排反应[J]. 天中学刊,1997,12(2):101 -104.
邢其毅,裴伟伟,徐瑞秋,等. 基础有机化学[M]. 北京:高等教育出版社,2005:515 -517.
邢其毅,裴伟伟,徐瑞秋,等. 基础有机化学[M]. 北京:高等教育出版社,2005:778 -779.
丁金城. 浅谈重排反应[J]. 淄博师专学报,1994(4):31 -37.
Zhang, W. Q.; Zheng, Y.; Ma, L. Textbook of Orangnic Chemistry (Fifth Edition), Beijing, 2014, pp. 385.
Lin, C. R.; Yu, L. J.; Li S. H.; Karton, A. Chem. Phys. Lett. 2016, 659,100.

