中药免煎颗粒及中药饮片所含有效成分的对比研究
何洪俊 李进 黄新强

摘要 目的:研究对比中药免煎颗粒及中药饮片所含有效成分。方法:选取深圳三九现代中药有限公司生产的大黄中药免煎颗粒与大黄中药饮片,以高效液相色谱法检测大黄中药免煎颗粒与大黄中药饮片中大黄酚、大黄酸、大黄素的含量。同时,采用高效液相色谱法检测大黄中药免煎颗粒与大黄中药饮片中黄芪甲苷的含量。结果:大黄免煎颗粒中大黄酚、大黄酸、大黄素含量分别为3.50 mg/g、9.44 mg/g、3.13 mg/g,大黄饮片中大黄酚、大黄酸、大黄素含量分别为3.34 mg/g、9.57 mg/g、3.05 mg/g。黄芪饮片中的黄芪甲苷含量分别为0.80 mg/g、0.83 mg/g。结论:大黄中药免煎颗粒与大黄中药饮片中大黄酚、大黄酸、大黄素以及黄芪甲苷的含量差异不明显,在临床实际工作中可根据患者的具体情况灵活选用。
关键词 中药免煎颗粒;中药饮片;有效成分;黄芪甲苷;高效液相色谱法;大黄酚;大黄酸;大黄素
A Comparative Study on the Effective Components of Chinese Herbal Medicine in Decocting-Free Granules and Decocting Pieces
He Hongjun,Li Jin,Huang Xinqiang
Abstract Objective:To study and compare the active ingredients contained in decocting-free granules and decocting pieces of Chinese herbal medicine.Methods:The content of chrysophanol,chrysophanic acid and emodin in Radix et Rhizoma Rhei decocting-free granules and Radix et Rhizoma Rhei decocting pieces produced by Shenzhen Sanjiu Modern Chinese medicine Co.,Ltd.was detected by high performance liquid chromatography(HPLC).Meanwhile,HPLC method was also used to determine the content of astragaloside in Radix et Rhizoma Rhei decocting-free granules and Radix et Rhizoma Rhei decocting pieces.Results:The contents of chrysophanol,chrysophanic acid and emodin in Radix et Rhizoma Rhei decocting-free granules were 3.50 mg/g,9.44 mg/g,3.13 mg/g,respectively.The contents of chrysophanol,chrysophanic acid and emodin in Radix et Rhizoma Rhei decocting pieces were 3.34 mg/g,9.57 mg/g and 3.05 mg/g,respectively.The contents of astragaloside in Radix Astragali seu Hedysari decocting pieces were 0.80 mg/g and 0.83 mg/g respectively.Conclusion:There is no significant difference in the content of chrysophanol,chrysophanic acid,emodin and astragaloside in Radix et Rhizoma Rhei decocting-free granules and Radix et Rhizoma Rhei decocting pieces.It can be selected flexibly according to the specific conditions of patients in clinical practice.
Key Words Decocting-free granules of Chinese herbal medicine; Decocting pieces of Chinese herbal medicine; Active ingredients; Astragaloside; High performance liquid chromatography; Chrysophanol; Chrysophanic acid; Emodin
中圖分类号:R282文献标识码:Adoi:10.3969/j.issn.1673-7202.2019.11.012
中药免煎颗粒是近年来于中药饮片的基础上发展形成的一种新剂型,由于其具有剂量准确以及使用简便等优势,在全球范围内中药市场上颇受欢迎[1]。然而,免煎颗粒在临床治疗中是否能完全替代中药饮片,临床治疗效果优劣与否尚未完全明确,亦是目前临床医务人员重点关注的热点问题之一[2-4]。迄今为止,临床上关于中药免煎颗粒及中药饮片中有效成分含量比较的相关研究并不多见。因此,应从质量标准、临床疗效以及药效学等方面对中药免煎颗粒及中药饮片予以全面评价,并以此作为根据评估中药免煎颗粒及中药饮片的质量差异情况[5-7]。鉴于此,本文通过选用大黄作为研究对象,对其中药免煎颗粒及中药饮片中主要有效成分含量进行测定对比,旨在为临床中药免煎颗粒及中药饮片的选用提供指导作用,现将结果报道如下。
1 仪器与试药
1.1 仪器 1)LC-10AT高效液相色谱仪(日本岛津公司生产);2)LC-10AT泵;3)SPD-10A可变波长紫外检测器;4)C-R8A数据处理系统。
1.2 试剂 1)甲醇;2)乙腈;3)蒸馏水;4)正丁醇;5)氢氧化钠。以甲醇和乙腈作为色谱纯,其他试剂均为分析纯。
1.3 分析样品 主要包括大黄免煎颗粒与大黄中药饮片(深圳三九现代中药有限公司,生产批号1069001W)、大黄酚对照品、大黄酸对照品、大黄素对照品,黄芪甲苷对照品,上述对照品均由中国药品生物制品鉴定所生产,生产批号分别为0796-200313、0756-200210、0756-200210、0781-200309。
2 方法与结果
2.1 色谱条件 4.6 mm×250 mm的C18色谱柱(天津深杭公司生产);流动相为甲醇与浓度为0.1%磷酸的混合溶液,将2者按照85∶15的比例进行混匀;流速控制为1.0 mL/min;检测波长设置为254 mm;以室温作为柱温。
2.2 对照品溶液的制备 分别精密称取大黄酚对照品、大黄酸对照品、大黄素对照品适量,并加入甲醇溶液进行定容,制备成1.2 mg/mL、2.5 mg/mL以及0.56 mg/mL的对照品溶液。精密称取适量的黄芪甲苷对照品,加入甲醇进行溶解处理,制备成0.27 mg/mL的对照品溶液。
2.3 供试品溶液制备 精密称取10 g的大黄免煎颗粒以及100 g的大黄饮片。将大黄免煎颗粒采用蒸馏水予以溶解,并定容至100 mL。大黄饮片则予以粉碎处理,并过14目筛,置入8倍量的蒸馏水反复煎煮3次,每次煎煮完成后均40 min过滤,合并滤液,水浴浓缩,待其冷却后采用个蒸馏水定容至100 mL。精密吸取大黄免煎颗粒与大黄饮片所制备好的样品溶液10 mL,严格根据2000版《中华人民共和国药典》[8-9]中所制定的相关方式予以制备,最后定容至100 mL的供试品溶液。精密称取10 g的大黄免煎颗粒以及100 g的大黄饮片。将大黄免煎颗粒采用蒸馏水予以溶解,并定容至100 mL。大黄饮片则予以粉碎处理,并过14目筛,置入8倍量的蒸馏水反复煎煮3次,每次煎煮完成后均40 min过滤,合并滤液,水浴浓缩,待其冷却后采用个蒸馏水定容至100 mL。精密吸取大黄免煎颗粒与大黄饮片所制备好的样品溶液10 mL,严格根据2000版《中华人民共和国药典》中所制定的相关方式予以制备,最后定容为100 mL的供试品溶液。分别精密吸取供试品溶液20 mL采用水饱和正丁醇重复4次萃取,合并正丁醇液,并加入浓度为0.5%的氢氧化钠溶液重复洗涤3次,除去碱液层,将正丁醇彻底挥发干净,采用甲醇溶液对残渣进行溶解,定容至50 mL。
2.4 专属性试验 分别取10 μL的各对照品溶液及供试品溶液,按2.1描述的色谱条件实施专属性试验,发现有关对照品溶液和供试品溶液均在色谱图相同的时间区域未出现相同的色谱峰,表明此次试验的专属性良好。
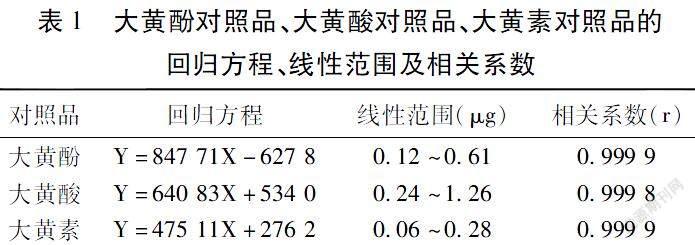
2.5 线性关系考察 分别精密称取大黄酚对照品、大黄酸对照品以及大黄素对照品溶液1.0、2.0、3.0、4.0、5.0 mL,并分别将其放置于100 mL的容量瓶中,加入甲醇予以定容处理,采用0.45 μm的微孔滤膜予以过量处理。随后精密吸取10 μL的溶液注入液相色谱仪中,将进样量设为横坐标(X),峰面积设为纵坐标(Y),完成标准曲线的绘制,并计算出回归方程以及相关系数情况。大黄酚对照品、大黄酸对照品、大黄素对照品的回归方程、线性范围及相关系数如表1所示。表明了上述对照品于颔联该范围内和峰面积具有良好的线性关系。
分别精密吸取1.0、2.0、3.0、4.0、5.0 mL对照品溶液放置于100 mL的容量瓶中,采用甲醇进行稀释、定容。并予以0.45 μm微孔滤膜进行过滤处理,随后精密吸取10 μL的溶液,注入液相色谱仪中,将黄芪甲苷进样量设为横坐标(X),峰面积设为纵坐标(Y),完成标准曲線的绘制,并计算出回归方程以及相关系数情况:Y=178 734 4.5X-301.03,r=0.999 8。结果显示黄芪甲苷在0.028~0.137 μg范围内,与峰面积具有良好的线性关系。
2.6 中间精密度试验 精密吸取大黄酚对照品、大黄酸对照品、大黄素对照品溶液10 μL,重复进样5次,对其含量的相对标准偏差值进行测定,结果显示大黄酚、大黄酸、大黄素的相对标准偏差值分别为1.21%、1.67%、1.17%,表明了该方法的精密性良好。精密吸取个对照品溶液10 μL,重复进样5次,对其含量的相对标准偏差值进行测定,结果显示其含量的相对标准偏差值为1.30%,提示该方法的精密度较佳。
2.7 供试品溶液稳定性试验 于室温条件下,分别于大黄免煎颗粒的样品溶液配制完成后的0、2、6、8、12 h内对其含量进行测定,结果显示相对标准偏差值为1.88%,表明黄芪甲苷的含量至少与12 h内处于稳定状态。于室温条件下,分别于大黄免煎颗粒的样品溶液配制完成后的0、2、6、8、12 h内对其含量进行测定,结果显示大黄酚、大黄酸以及大黄素的相对标准偏差值分别为0.66%、1.89%、0.92%,结果显示大黄酚、大黄酸以及大黄素的含量至少于12 h内处于稳定状态。
2.8 重复性试验 为保证本次实验的客观性,实施短时间内HPLC重复试验,精密量取相同批号的供试品溶液,设置进样量为10 μL,给予连续性进样,此次研究表明色谱峰的RSD均值是1.79%,且各色谱峰RSD均<3%,这提示本次研究涉及的供试品溶液的重复性良好。
2.9 回收率实验 精密称取5分已知含量的大黄免煎颗粒,分别角度定量的对照品,根据供试品的制备方式完成制备,随后精密吸取10 μL完成进样测定,计算器加样回收率以及相对标准偏差值。结果显示大黄酚、大黄酸以及大黄素的加样回收率以及相对标准偏差值分别为96.0%(5.2%)、94.6%(3.3%)、95.0%(2.6%)。精密称取适量已知含量的黄芪免煎颗粒,加入一定量的对照品,严格根据供试品的制备方式制备,精密吸取10 μL进样测定,结果显示加样回收率以及相对标准偏差值分别为95.97%、5.5%。
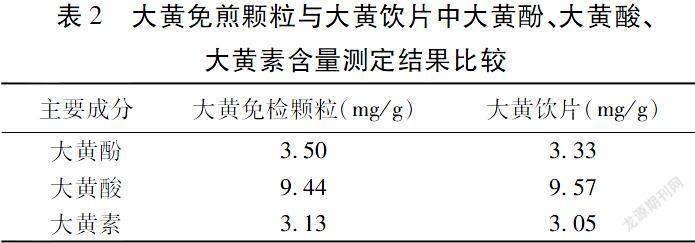
2.10 样品测定结果 将上述供试品溶液予以0.45 μm的微孔滤膜予以过滤处理,分别进样10 μL测定含量,并将大黄免煎颗粒中的大黄酚、大黄酸以及大黄素含量转变为相当的生药中的含量后予以对比分析。结果显示大黄免煎颗粒中大黄酚、大黄酸、大黄素含量分别为3.50 mg/g、9.44 mg/g、3.13 mg/g,大黄饮片中大黄酚、大黄酸、大黄素含量分别为3.34 mg/g、9.57 mg/g、3.05 mg/g。见表2。
将上述供试品溶液予以0.45 μm的微孔滤膜予以过滤处理,分别进样10 μL测定含量,并将大黄免煎颗粒中的黄芪甲苷含量转变为相当的生药中的含量后予以对比分析。结果显示黄芪免煎颗粒、黄芪饮片中的黄芪甲苷含量分别为0.80 mg/g、0.83 mg/g。见表3。
3 讨论
由于中药具有疗效显著、不良反应较少以及预后较佳等优势,近年来开始被广泛用于临床多种疾病的治疗中,且已获得显著的效果[10-12]。中药饮片主要是指中药材通过中医药理论以及传统中药炮制方式,经由加工炮制后可直接用于临床治疗的一类中药,主要包括部分经产地加工的中药切片,原形药材饮片,切割或炮制的饮片[13]。中药免煎颗粒主要是指单味中药配方颗粒,其主要是采用现代制药技术提取、浓度、分离、干燥、制备以及包装而成,乃是在传统中药饮片汤剂的基础上开展而来,两者相比,中药免煎颗粒具有有效避免中药煎煮过程以及煎煮过程的繁琐和煎煮过程中难以精准掌握的技巧等,且有效避免了中药煎煮所散发出来的令人不悦的气味。且有研究报道显示[14-16],中药免煎颗粒相比中药饮片具有有效成分含量较高,服用量较少,应用简便等优点。然而,另有研究报道显示[17-18],中药免煎颗粒相比中药饮片可能存在有效成分降低的可能,从而对患者的临床治疗造成不利影响。
本文结果显示,大黄免煎颗粒中大黄酚、大黄酸、大黄素含量分别为3.50 mg/g、9.44 mg/g、3.13 mg/g,大黄饮片中大黄酚、大黄酸、大黄素含量分别为3.34 mg/g、9.57 mg/g、3.05 mg/g。与此同时,黄芪饮片中的黄芪甲苷含量分别为0.80 mg/g、0.83 mg/g。这说明了大黄中药免煎颗粒与中药饮片中的大黄酚、大黄酸、大黄素以及黄芪甲苷等主要有效成分含量无明显差异。这提示了在临床予以患者中药治疗时,可综合患者的综合情况选用更为适合的中药。本研究主要是从大黄的主要功效成分含量方面对比中药免煎颗粒和中药饮片之间的质量差别,但中药饮片及其制剂质量的优劣与否并非仅单凭某一种或一类化学成分含量的高低便可进行准确判断[19-21]。我们认为,借鉴临床上中药化学研究的成果,正确选用专属性强、能效为全面评价中药材质量的化学标准成分,同时充分利用指纹图谱等一系列现代中药分析技术,可在一定程度上完善中药免煎颗粒质量标准评价体系。这为今后的研究提供了方向,可针对上述方面予以深入研究,从而获取更为准确、可靠的数据,为临床中药免煎颗粒与中药饮片的选用提供指导作用[22-23]。另有研究报道显示[24-26],中药免煎颗粒不仅可有效保留中药的所有属性,通识课提升中药的利用率;而中药饮品的炮制过程遵循着严密的中医理论,其独特的煎煮以及其他炮制方式会形成糊化的淀粉,从而有利于促进酶性药物的溶解,进一步达到促进药效发挥的作用。
综上所述,中药免煎颗粒与中药饮片的主要有效成分含量无明显差异,在临床实际工作中可按照患者的具体情况灵活选用,在保证治疗效果的基础上,尽量实现良好的药学价值。
参考文献
[1]李睿,翟华强,田伟兰,等.中药煮散的历史源流及其与现代配方颗粒的对比性分析[J].中国中药杂志,2016,41(5):965-969.
[2]王宪英,刘国强,刘洋,等.免煎颗粒剂与中药饮片治疗风热感冒临床疗效的系统评价与Meta分析[J].中国药物经济学,2018,13(8):120-125.
[3]赵鑫,韩燕霞,吉軍霞,等.中药免煎颗粒和中药饮片的对比研究概述[J].山西职工医学院学报,2017,27(5):62-63.
[4]郝磊,李军山,高晗,等.不同企业中药配方颗粒规格的差异及分析[J].中国现代中药,2016,18(9):1097-1099.
[5]穆瑶,彭其胜,陈欢,等.葛根、槐花饮片及其免煎颗粒中黄酮类有效成分的含量比较[J].贵阳中医学院学报,2017,39(2):19-22.
[6]李睿,翟华强,田伟兰,等.中药煮散的历史源流及其与现代配方颗粒的对比性分析[J].中国中药杂志,2016,41(5):965-969.
[7]林朝龙,廖琳燕.中药饮片与免煎单味中药配方颗粒临床使用情况比较[J].按摩与康复医学,2015,33(14):78-79.
[8]Gao J,Zhang J,Qu Z,et al.Study on the mechanisms of the bronchodilator effects of Folium Eriobotryae and the selected active ingredient on isolated guinea pig tracheal strips[J].Pharm Biol,2016,54(11):2742-2752.
[9]常姗,宋芳,马琳琳,等.中药免煎颗粒剂散装与小剂量包装应用的对比分析[J].中医临床研究,2017,9(1):135-136.
[10]Guan HW,Xu LJ,Dong H,et al.Application of reverse molecular docking technology in target prediction,active ingredient screening and action mechanism exploration of traditional Chinese medicine[J].China Journal of Chinese Materia Medica,2017,42(23):4537-4541.
[11]任雷生,赵军磊,付旭晖,等.红光照射联合中药塌渍和他克莫司软膏治疗面部糖皮质激素依赖性皮炎疗效观察[J].新乡医学院学报,2017,34(3):238-240.
[12]Yu L,Jin W,Li X,et al.Optimization of Bioactive Ingredient Extraction from Chinese Herbal Medicine Glycyrrhiza glabra:A Comparative Study of Three Optimization Models[J].Evid Based Complement Alternat Med,2018,15(2018):6391414-6391415.
[13]邱承权.中药免煎颗粒与中药饮片中有效成分含量比较分析[J].中国处方药,2018,16(3):32-33.
[14]李燕,吴皓东.黄芩、金银花免煎颗粒与中药饮片不同剂型的对比研究[J].新疆中医药,2018,36(3):37-40.
[15]Zhang J,Zhang J,Wang S,et al.Development of an Oral Compound Pickering Emulsion Composed of Nanocrystals of Poorly Soluble Ingredient and Volatile Oils from Traditional Chinese Medicine[J].Pharmaceutics,2018,10(4):170-171.
[16]Tang T,Yang S,Zhao H,et al.Analysis of traditional Chinese medicine components by high performance liquid chromatography with diode array detection based on double qualitative principles[J].Se Pu,2018,36(8):766-771.
[17]Xin T,Su C,Lin Y,et al.Precise species detection of traditional Chinese patent medicine by shotgun metagenomic sequencing[J].Phytomedicine,2018,1(47):40-47.
[18]张永红.中药免煎颗粒和中药饮片的主要特点及药效比较[J].世界临床医学,2016,10(14):149-149.
[19]Li Q,Sun Y,Guo H,et al.Quality control of the traditional Chinese medicine Ruyi jinhuang powder based on high-throughput sequencing and real-time PCR[J].Sci Rep,2018,8(1):8261-8262.
[20]張斐姝,蔡舒婷,舒忻,等.中药配方颗粒的临床运用概况与未来趋势[J].中国医药导报,2016,13(16):70-73.
[21]Wang N,Tan HY,Chan YT,et al.Identification of WT1 as determinant of heptatocellular carcinoma and its inhibition by Chinese herbal medicine Salvia chinensis Benth and its active ingredient protocatechualdehyde[J].Oncotarget,2017,8(62):105848-105859.
[22]Huang L,Li H,Xie D,et al.Personalizing Chinese medicine by integrating molecular features of diseases and herb ingredient information:application to acute myeloid leukemia[J].Oncotarget,2017,8(26):43579-43591.
[23]Hou F,Wen L,Peng C,et al.Identification of marine traditional Chinese medicine dried seahorses in the traditional Chinese medicine market using DNA barcoding[J].Mitochondrial DNA A DNA Mapp Seq Anal,2018,29(1):107-112.
[24]任树林,贺佩瑾.薄芝糖肽注射液、注射用血塞通联合水蛭免煎颗粒治疗椎-基底动脉供血不足性眩晕的临床观察[J].河北中医,2018,40(2):196-200.
[25]Li Y,Wang J,Lin F,et al.A Methodology for Cancer Therapeutics by Systems Pharmacology-Based Analysis:A Case Study on Breast Cancer-Related Traditional Chinese Medicines[J].PLoS One,2017,12(1):169363-169364.
[26]Hitomi S,Ono K,Terawaki K,et al.[6]-gingerol and[6]-shogaol,active ingredients of the traditional Japanese medicine hangeshashinto,relief oral ulcerative mucositis-induced pain via action on Na+ channels[J].Pharmacol Res,2017,3(117):288-302.
(2018-10-25收稿 责任编辑:杨阳)
基金项目:滁州市科技指导性计划项目(201501)作者简介:何洪俊(1974.07—),女,本科,主管中药师,研究方向:中草药的调剂、储存保管,中成药的调理、不良反应,E-mail:2624112278@qq.com

