3D-STE预测ST段抬高型心肌梗死PCI术后左室重构的价值
ST段抬高型心肌梗死属于临床常见危重心血管疾病,临床采用经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)法对病人进行再灌注治疗[1]。PCI治疗后病人病情虽得到明显好转,但有一部分病人仍面临出现左心室重构的风险,病情严重者逐渐发展为慢性心力衰竭,严重威胁病人的生命健康[2]。超声心动图为临床检测心血管疾病常用的方法,能够检测左心室室壁各节段运动情况,主要采用目测法进行评价,具有主观性,与操作者经验有关,灵敏度较低[3]。三维斑点追踪超声心动图(3D-STE)是近期发展的新技术,可准确测定心肌各节段在三维空间内应变参数的变化,进而更精确地评价心肌运动,对于心肌缺血更敏感[4]。目前对于3D-STE在ST段抬高型心肌梗死PCI术后左室重构中的预测研究不多,本研究通过对我院ST段抬高型心肌梗死PCI术后病人行3D-STE检测,以探究其应变参数在病人术后左室重构中的预测价值。
1 资料与方法
1.1 临床资料 选择2015年8月—2016年11月我院收治的98例心肌梗死病人,均经冠状动脉造影证实,病人心电图均表现为ST段抬高,符合急性ST段抬高型心肌梗死诊断标准[5],病人入院后接受PCI治疗,其中男58例,女40例;年龄33~79(55.19±8.13)岁;单支冠状动脉病变61例,双支或以上冠状动脉病变37例。
1.2 纳入与排除标准 纳入标准:①经冠状动脉造影、心电图、心肌酶学检测等确诊为ST段抬高型心肌梗死;②住院后均接受PCI治疗;③病人家属知情同意。排除标准:①合并风湿性心脏病、心肌病、肺源性心脏病、心内膜炎、主动脉夹层;②活动性出血;③接受过创伤性心肺复苏手术;④图像质量欠佳影响观察;⑤置入起搏器。
1.3 检测方法
1.3.1 多普勒超声心动图检测 病人手术治疗后3 d、6个月进行常规超声心动图检查,所用设备为GE公司Vivid7 彩色超声诊断仪,采取左侧卧位,同时连接心电图,叮嘱病人呼气后屏气,心动图帧频为50~70帧/s,常规选取胸骨左室长轴面,主要测定左室舒张末内径(left ventricular end-diastolic,LVEDD),心尖双拼面法(simpson)测定左心室收缩末期容积(left ventricular end systolic volume,LVESV)、左心室舒张末期容积(left ventricular end diastolic volume,LVEDV)、左室射血分数(left ventricular ejection fraction,LVEF)。于心尖四腔平面用脉冲多普勒记录二尖瓣舒张早、晚期血流峰值(E、A),计算两者比值(E/A)。以上参数均测定3个心动周期,取平均值。
1.3.2 二维斑点追踪超声心动图检测 采集心尖两腔、三腔以及四腔切面二维动态图,保存连续6个心动周期动态图,并将图像传送至Echo PAC工作站,采用机器自带3DT软件进行分析,根据屏幕顶端标记对心尖四腔、中二尖瓣左侧、右侧、心尖6处进行描记,系统自动在图像中勾画出心内膜、心外膜,沿心内膜边界选取感兴趣区(region of interest,ROI),使其覆盖心肌全层,厚度与心肌厚度维持一致。系统将ROI分为心基底段、中间段、心尖段18个心肌节段,追踪成功后进行分析,根据心电图R波为收缩期开始,主动脉关闭时间作为收缩期末,R-R期作为1个心动周期,软件自动得出此期间峰值应变参数值,包括整体纵向峰值应变(global longitudinal strain,GLS)、整体环向峰值应变(global circumferential strain,GCS)、整体径向收缩期峰值应变(global radial strain,GRS)以及整体面积应变(global area strain,GAS)参数指标。
1.3.3 随访 病人出院后随访1年,术后6个月进行超声心动图复查,根据病人LVESV比初次增加15%定义为左室重构,分为重构组、非重构组。

2 结 果
2.1 两组临床资料比较 术后6个月复查显示,34例病人发生左室重构,64例病人未发生左室重构。两组在性别、体质指数(BMI)、并发症等方面比较,差异无统计学意义(P>0.05)。重构组年龄高于非重构组,肌钙蛋白(cTnI)低于非重构组,差异均有统计学意义(P<0.05)。详见表1。
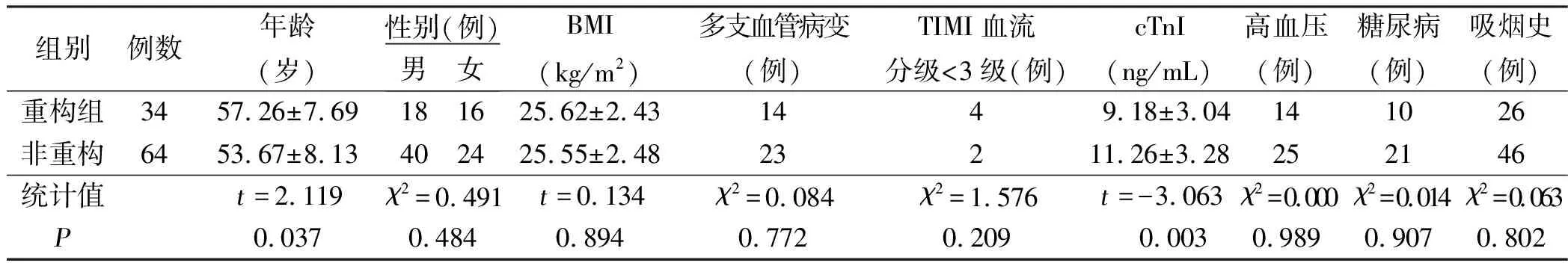
表1 两组临床资料比较
2.2 两组常规超声心动图指标比较 术后3 d两组LVEDV、LVESV、LVEDD、LVEF、E/A比较,差异无统计学意义(P>0.05)。术后6个月重构组LVEDV、LVESV、LVEDD高于非重构组,LVEF、E/A低于非重构组,差异均有统计学意义(P<0.05)。详见表2。

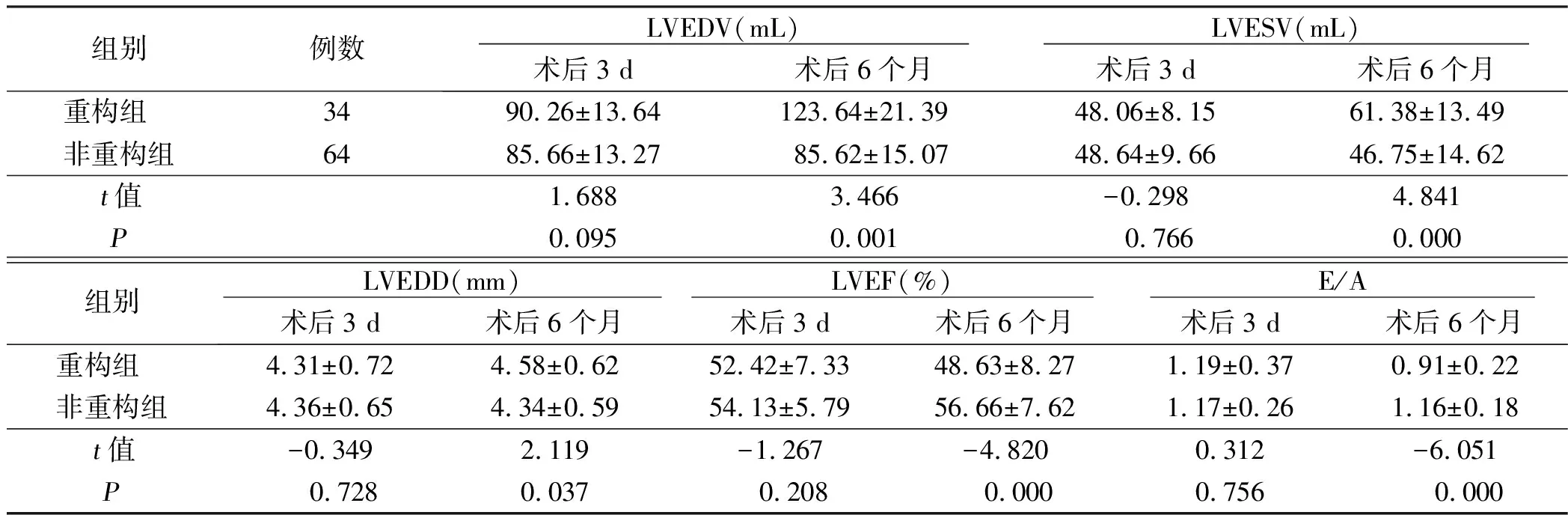
组别例数 LVEDV(mL) 术后3 d术后6个月 LVESV(mL) 术后3 d术后6个月重构组 3490.26±13.64123.64±21.3948.06±8.1561.38±13.49非重构组6485.66±13.2785.62±15.0748.64±9.6646.75±14.62t值1.6883.466-0.2984.841P0.0950.001 0.7660.000组别 LVEDD(mm) 术后3 d术后6个月 LVEF(%) 术后3 d术后6个月 E/A 术后3 d术后6个月重构组 4.31±0.724.58±0.6252.42±7.3348.63±8.271.19±0.370.91±0.22非重构组4.36±0.654.34±0.5954.13±5.7956.66±7.621.17±0.261.16±0.18t值-0.3492.119-1.267-4.8200.312-6.051P 0.7280.037 0.208 0.0000.756 0.000
2.3 两组3D-STE应变参数检测结果比较 两组GCS比较,差异无统计学意义(P>0.05)。两组GLS、GAS、GRS比较,差异有统计学意义(P<0.05)。详见表3。

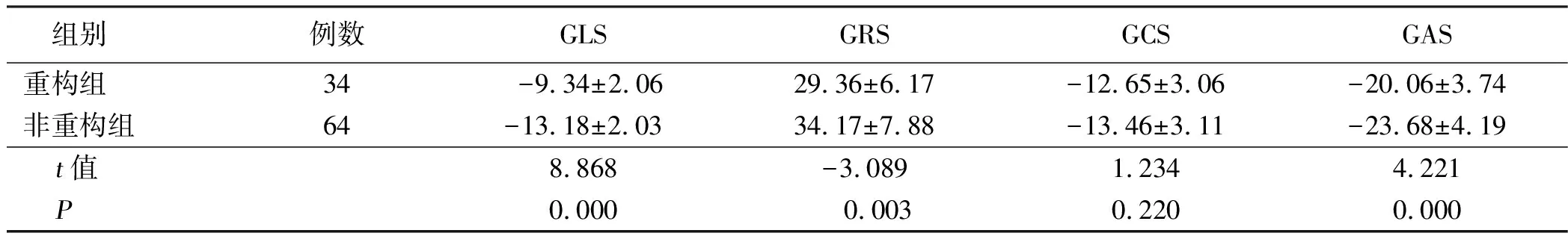
组别例数GLSGRSGCSGAS重构组34-9.34±2.0629.36±6.17-12.65±3.06-20.06±3.74非重构组64-13.18±2.0334.17±7.88-13.46±3.11-23.68±4.19 t值8.868-3.0891.2344.221 P0.000 0.0030.2200.000
2.4 单因素及多因素分析影响左室重构的因素 将病人一般资料、3D-STE应变参数等指标纳入单因素回归分析,结果显示年龄、cTnI、GLS、GRS、GAS均可能预测病人PCI术后6个月左室重构,进一步进行多因素回归分析,结果显示GLS、GAS、GRS为预测左室重构的独立预测指标。详见表4。
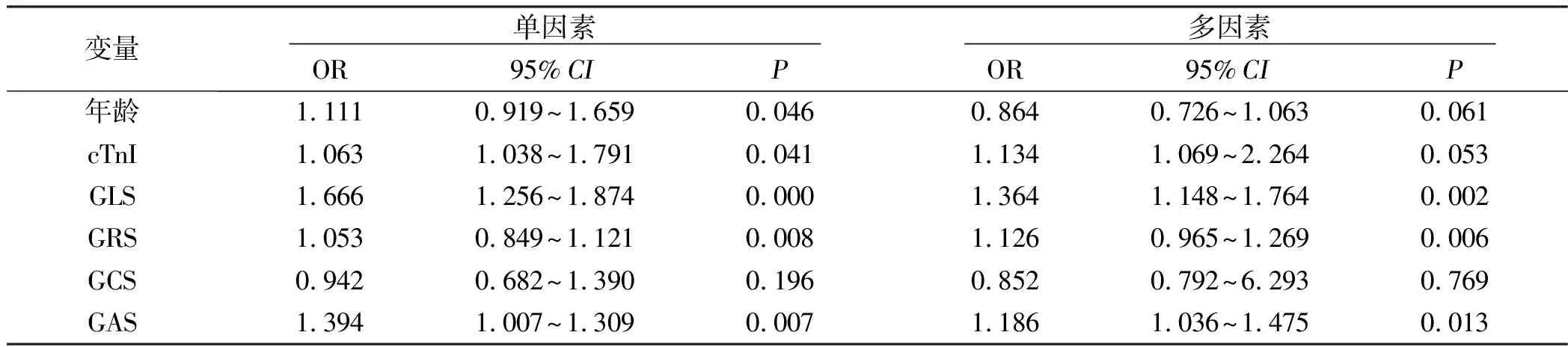
表4 单因素及多因素分析影响左室重构的因素
2.5 峰值应变参数预测左室重构ROC曲线分析 GLS、GAS、GRS 的AUC值分别为0.879、0.837、0.813。GLS截点值为-12.59,灵敏度为80.82%,特异度为60.20%;GAS截点值为-22.63,灵敏度为91.84%,特异度为51.02%;GRS截点值为33.74,灵敏度为87.75%,特异度为47.96%。详见图1、表5。
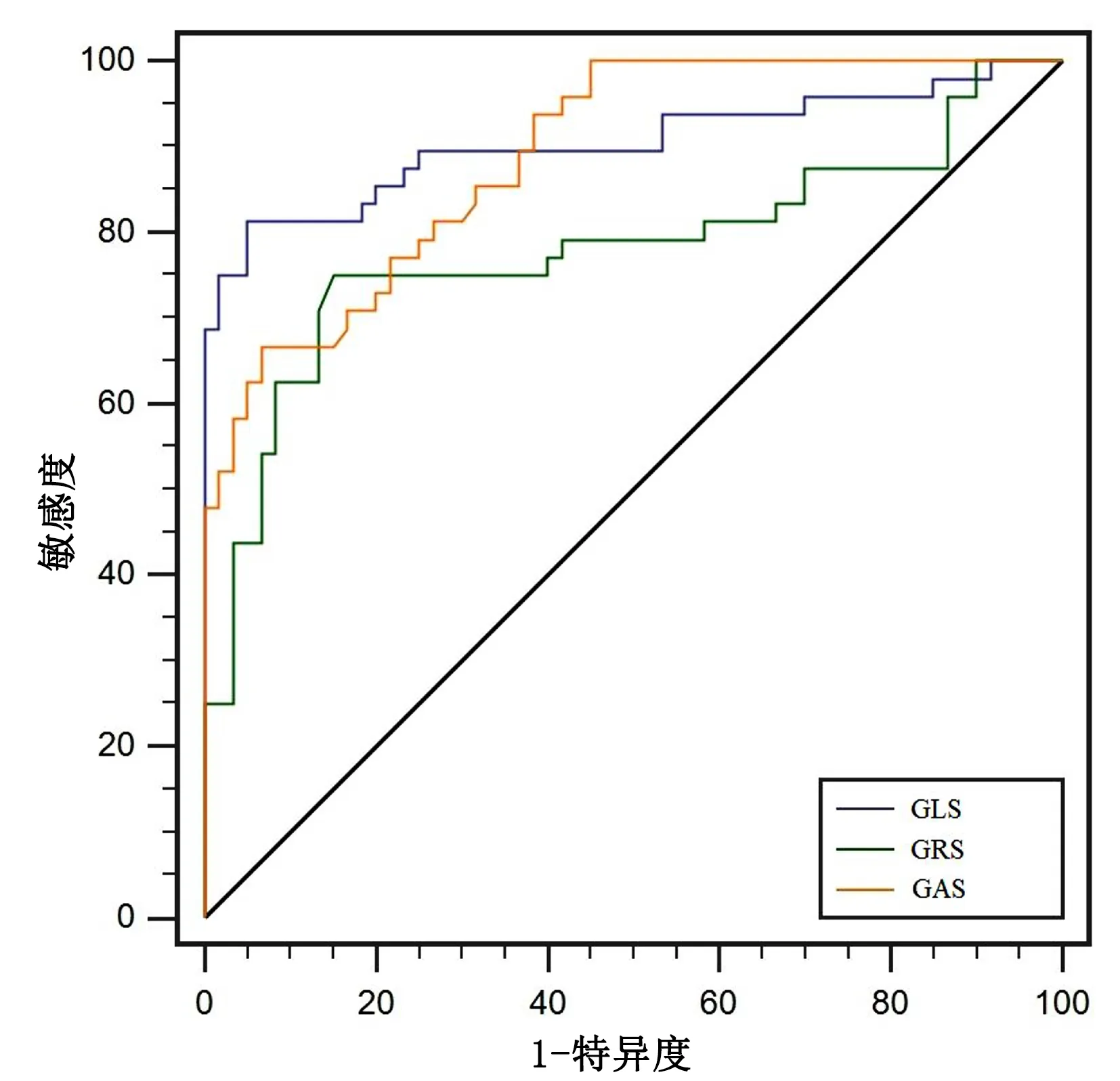
图1 GLS、GAS、GRS预测左室重构的ROC曲线
表5峰值应变参数预测左室重构的ROC曲线分析
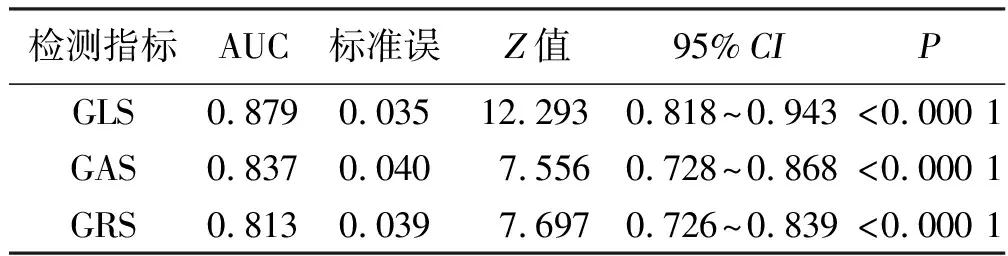
检测指标AUC标准误Z值95%CIPGLS0.8790.03512.2930.818~0.943<0.000 1GAS0.8370.0407.5560.728~0.868<0.000 1GRS0.8130.0397.6970.726~0.839<0.000 1
3 讨 论
临床研究显示心肌梗死到心室重构过程为动态演变过程,出现心肌梗死后,心肌内细胞大量坏死使心脏受损,在受到神经、免疫、炎症、机械牵引等作用下,心脏结构层面出现一系列改变,以适应心肌梗死后血流动力学变化,进而适应重新构建的新环境[6]。心脏结构的变化中,心室整体扩张最为常见,其为左室重构的主要形式。临床有关研究显示心肌梗死病人PCI术后发生心肌急性损伤会导致左室重构,这是心脏负荷增加的修复反应,但随着时间的延长,左室重构可影响病人预后[7]。因此,早期对左心室重构病人进行检测对于其预防、干预措施的制定十分重要。
心脏心肌主要受心肌纤维带组成,由右室肺动脉瓣下方至左室延伸连接主动脉,在机体发育中,心肌纤维不断进行包绕、扭转,最终心肌纤维形成双螺旋结构。在心脏周期中,心肌纤维的运动较复杂,包括径向、纵向、环向以及旋转运动,因此心肌纤维可以在中轴、横轴以及立体空间中进行伸长、增厚以及扭转运动[8]。冠状动脉血供方向由心外膜向心内膜进行,由于心内膜血管较细位于血管末端,因此,心肌缺血时会发生由心内膜向心外膜的心肌完全梗死,且缺血时间越长梗死面积越大[9]。本研究首先对病人进行常规超声心动图检测,结果显示术后6个月重构组LVEDV、LVESV、LVEDD高于非重构组,LVEF、E/A低于非重构组,表明左室重构病人心腔大小、容量均明显增大,进一步反映心肌细胞受损,使左心室大小、形态发生变化,局部收缩功能降低。在后续多因素分析中并未见其在左室重构中的预测价值,分析原因可能为以上参数由于受到机体因素或技术检测的限制,不能够反应心肌梗死区域存活心肌以及非梗死区域临床心肌功能障碍情况,因此不足以反应心肌梗死后心脏泵功能、左心室收缩功能情况。
GLS主要反映心脏长轴方面心肌形变情况,反映长轴方面心脏收缩功能情况,心肌纤维在长轴方向呈纵向排列,主要位于心内膜下方,冠状动脉血供方向由心外膜向心内膜进行,当心肌缺血时,与中层、心外膜心肌相比,心内膜对于心肌损伤更敏感,因此心脏在长轴方面的运动变化对于心肌缺血或心肌功能变化更为敏感[10]。既往研究显示,心脏长轴方向的收缩占整个心脏收缩的70%,说明心脏长轴方面功能下降更能代表整个心脏收缩能力的下降[11]。国外近期研究显示,GLS较3D-STE其他应变参数更能够评估心肌梗死病人梗死面积,灵敏度、特异度更高[12]。刘艳午等[13]研究认为,3D-STE检测中GLS在预测心脏不良事件中预测价值更高。本研究结果显示,左室重构病人GLS低于非重构组,多因素回归分析其为左室重构独立预测指标;ROC分析显示GLS AUC值为0.879,高于其他应变参数,临床预测价值最高,说明通过测定病人PCI术后GLS的变化可对左室重构进行预测,提示GLS为心血管疾病预后的潜在预测指标。
GRS主要反映心脏短轴方面心脏运动情况,能够代表左室壁增厚情况,因此在应变参数中为正数。有关研究显示,正常人心脏收缩时心室壁由外向内增厚,心内膜纤维占60%,因此当心内膜下心肌纤维发生收缩后,室壁发生增厚的概率较大,而当心内膜心肌损伤后,心外膜下心肌纤维加强收缩,弥补心内膜收缩功能的降低[14]。本研究结果显示,左室重构病人GRS低于非重构组,多因素回归分析其为左室重构独立预测指标,ROC分析显示GRS AUC值分别为0.813,临床预测价值较高,以上结果说明GRS对于左心室重构具有一定的价值,但其预测价值低于GLS,结合文献分析原因可能为心脏心内膜中心肌主要为纵形纤维,因此在心脏结构、功能发生变化时,纵向应变更敏感,能够反应左室收缩功能的变化[15]。
GAS主要反映心脏在短轴圆周、长轴轴向的运动状况,代表心动周期期间心内膜表面积变化情况,通过心内膜表面积变化情况可反映心肌缺血情况[16]。宋平梅等[17]研究显示GAS作为复合型参数能够更准确反映心肌形变情况,在心功能评估中价值更高。Chen等[18]在对心力衰竭病人进行心功能评估时发现,当其他应变参数还未发生改变时,GAS对早期心功能受损较敏感,且能够反应不同程度心力衰竭。本研究结果显示左室重构病人GAS低于非重构组,多因素回归分析其为左室重构独立预测指标,ROC分析显示GAS AUC值为0.837,具有一定的临床预测价值,但低于GLS,分析原因可能为GAS中包含圆周应变(CS),因此在预测时整体评价能力降低。
综上所述,ST段抬高型心肌梗死PCI术后发生左室重构病人心室功能发生改变,3D-STE在左室重构预测中具有较好的临床价值,其中GLS预测价值最高。但本研究也存在以下局限性,所选病人仅为ST段抬高型心肌梗死PCI术后病人,纳入样本量有限,3D-STE对图像质量以及病人要求较高,随访时间有限,不能预测左室重构病人长期预后,还需进一步开展相关工作进行验证。

