盐酸法富集低品位锰矿及酸介质高值再生工艺
吕东亚,马保中,陈永强,张永禄,王成彦,雷蒙恩
北京科技大学冶金与生态工程学院,北京 100083
世界锰矿资源总量比较丰富,但分布不均.全世界陆地锰矿床主要分布在南非、乌克兰、澳大利亚、加蓬、印度、巴西、中国、墨西哥等地区,这些国家锰矿资源的总和占到全球储量的94%左右[1].其中,我国的锰矿储量占世界锰矿总量的6.98%,且以碳酸锰矿为主,品位较低,而国外锰矿以氧化锰矿为主,矿石性质较好,锰品位在35%左右[2].在现代工业中,锰的应用非常广泛,约95%的锰应用于冶金工业,约5%的锰应用于化学工业、建筑材料、电子工业、环境保护和农牧业等其他领域[3-5].随着锰矿资源的不断消耗,高品位锰矿资源越来越少,而锰的需求却在日益增长,因而储量丰富的低品位锰矿的开发利用逐渐受到人们的重视.
开发利用低品位锰矿,首先要通过一定的富集工艺得到锰含量较高的锰精矿或含锰产品.目前常用的富集方法主要有洗矿、重选、磁选、浮选,以及火法富集、化学选矿法等[6-12].贺周初等[13]以硫铁矿作还原剂采用两矿酸浸法,用硫酸直接浸出锰质量分数为25%左右的低品位软锰矿,浸出率达到93%.彭荣华等[14]以低品位的软锰矿为原料,用生产钛白副产的硫酸亚铁直接浸锰,经过浸出液除杂、碳酸锰沉淀、碳酸锰焙烧及二氧化锰精制制备高纯二氧化锰.Mehta等[15]使用黑曲霉菌来浸出印度洋多金属锰结核,在一定条件下锰的浸出率可达91%.同时化学法富集会产生大量含钙废液,如将其用来生产硫酸钙广阔晶须,将会产生巨大的经济效益并减少环境污染,尤其是大长径比硫酸钙晶须的市场售价每吨高达8000~10000元,远高于普通高纯硫酸钙,具有较大的经济价值.硫酸钙晶须性能优良,用途广泛,是一种应用前景十分广阔的无机材料.较常用的制备方法主要有常压酸化法和水压热法等[16-18].
本文针对产自印度尼西亚的某低品位锰矿,开展矿物学分析与筛析,结合其矿物组成特点,提出一种粗碎筛分与盐酸浸出相结合的锰矿富集方法,探究并分析不同工艺参数对浸出锰精矿品位的影响.同时利用锰矿浸出液,在常温常压条件下制备硫酸钙晶须,并将再生的盐酸返回浸出锰矿,用以验证整个工艺流程的可行性.
1 实验材料
实验所用锰矿为印度尼西亚某低品位锰矿,该锰矿的元素化学分析结果如表1所示.主要组成元素Mn质量分数为20.00%,Ca质量分数为25.91%,其他元素含量较少.所用试剂为硫酸(分析纯,质量分数95%~98%)和盐酸(分析纯,质量分数36%~38%).

表1 锰矿化学成分分析(质量分数)Table 1 Chemical composition of manganese ore %
2 实验方法
将原矿粗碎浸泡后进行分级湿筛,得到不同粒度的锰矿,取样进行化学分析.取一定量经筛分得到的锰中矿磨细后与一定量的水一起加入到反应容器中,浆化均匀后在一定条件下滴加盐酸进行反应,反应结束后过滤得到浸出液和浸出渣,分别取样分析.锰矿浸出实验分别探究了浸出pH、浸出时间、搅拌转速、液固比对产出锰精矿品位的影响.固定搅拌转速为200 r·min-1,向适量浸出液中匀速滴加一定量与水等体积稀释过的硫酸,常温下反应2 h后过滤,得到再生的盐酸溶液和硫酸钙晶须,而后将硫酸钙晶须洗涤,60 ℃下干燥,然后进行X射线衍射分析,并用光学显微镜观察硫酸钙晶须微观形貌.用再生盐酸溶液在最优条件下浸出锰中矿,反应结束后过滤得到浸出液和浸出渣并取样分析.
3 实验结果与分析
3.1 锰矿矿物学分析
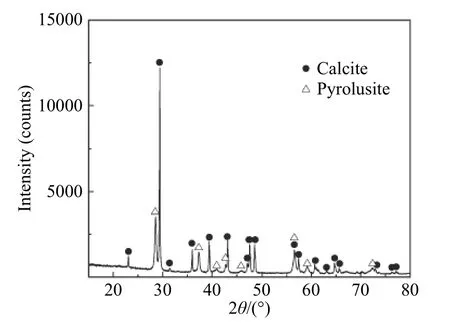
图1 锰矿X射线衍射图谱Fig.1 XRD pattern of the manganese ore
锰矿原矿综合样X射线衍射分析结果如图1所示.可以看出该锰矿矿物组成简单,主要物相为方解石和软锰矿.锰矿综合样扫描电镜图与主要元素的面分布如图2所示,软锰矿和方解石单体解离比较充分,部分软锰矿呈微粒单体产出.钙元素集中分布在方解石中,锰元素集中分布在软锰矿中,铝、镁、硅为杂质元素,含量较少,分布较为分散.图3为锰矿样的重要矿物产出特征,从图中可以看出,软锰矿和方解石是主要矿物.方解石呈粗粒状产出,与软锰矿共生关系不密切;软锰矿呈粒状或不规则状产出,结构较为松散.此外,还有少量的菱锰矿和褐铁矿,主要呈粒状产出.根据X射线衍射分析,光学显微镜、扫描电子显微镜以及元素化学分析结果,可以确定该矿中含锰矿物主要为软锰矿,偶见菱锰矿.其他矿物主要为方解石,其次为褐铁矿、高岭石等.
3.2 锰矿筛析
锰矿原矿经粗碎筛分得到的不同粒度锰矿的化学成分分布如图4所示.可以看出随着锰矿粒度的不断减小,锰的含量逐渐增加,钙和碳的含量逐渐减少,硅的含量略有增加,但增加幅度较小,硫的含量较少,且整体变化不大.锰矿粗碎后粒度大于2 mm的部分,锰含量较低(质量分数15%左右),钙、碳含量较多,结合之前的锰矿矿物组成分析结果,可以推知该部分锰矿主要矿物为方解石和软锰矿,其中方解石含量相对较多.粒度小于2 mm的部分锰含量整体得到提高,主要矿物为软锰矿和方解石,其中软锰矿含量大幅增加,含量也相对较多.若将原矿粗碎洗矿后用2 mm筛孔的筛子过筛,抛去大于2 mm的部分,锰质量分数从原矿的20.00%富集到33.32%,产率为61.8%,锰回收率为83.4%.经过筛分得到的锰中矿化学成分分析结果如表2所示,筛下的锰中矿锰含量明显提高,钙含量明显降低,主要矿物为软锰矿和方解石,杂质元素含量较少,达到了较好的富集效果.

图2 锰矿样的微观形貌和元素分布情况.(a) 扫描电镜图;(b)~(f) EDS元素面分布Fig.2 Microstructure and element distribution of the manganese ore samples: (a) SEM image; (b)~(f) EDS analyses of elements

图3 锰矿样不同区域重要矿物的产出特征Fig.3 Output characteristics of important minerals in the manganese ore sample at different zones
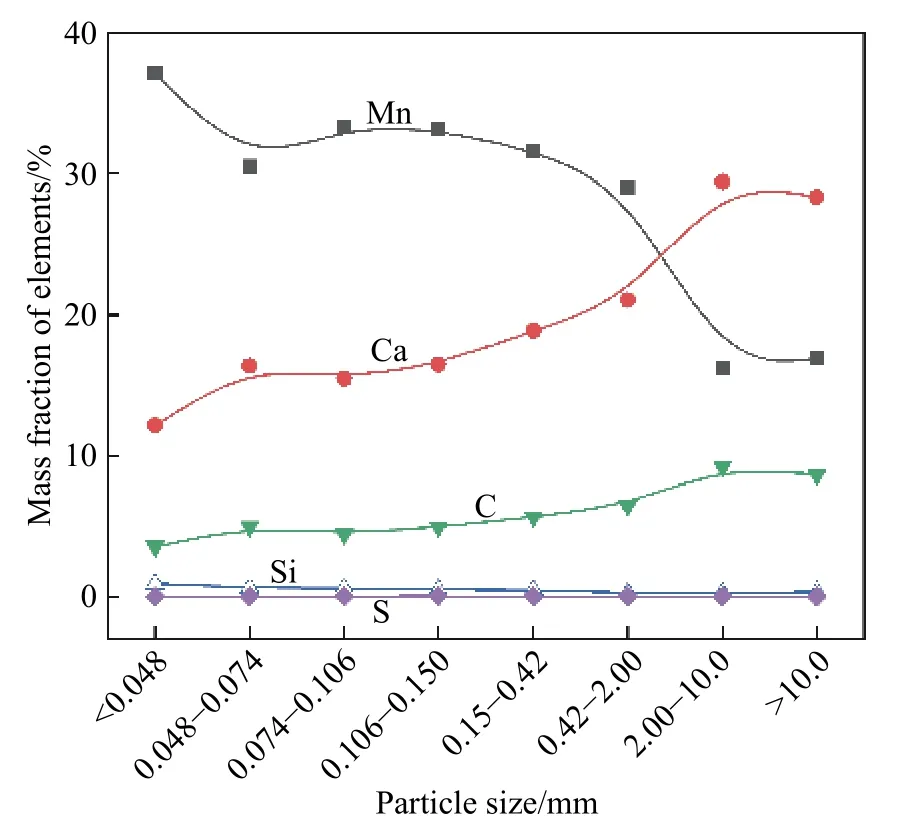
图4 不同粒度锰矿的化学成分分布Fig.4 Chemical composition distribution of the manganese ore with different particle sizes

表2 锰中矿化学成分分析(质量分数)Table 2 Chemical analyses results of the manganese middlings %
3.3 工艺流程的选择
基于锰矿矿物学分析与筛析结果,运用常温下方解石易溶于酸而软锰矿难溶于酸的性质,通过酸浸,就可轻易除去锰矿中的绝大部分方解石,从而达到化学法富集锰矿的目的.为减少酸耗量,可先对原矿进行选矿,选矿采用粗碎-洗矿-筛分的方法,并将经过2 mm筛孔的筛子筛下的锰中矿作为浸出原料.市面上盐酸的价格要高于硫酸,且不易储存与运输,但是锰矿浸出只能用盐酸而不能用硫酸,这是因为方解石主要成分为碳酸钙,与硫酸反应会生产难溶的硫酸钙.考虑到锰矿浸出滤液含大量氯化钙,可利用硫酸与氯化钙的反应,再生出盐酸的同时产出硫酸钙晶须,再生出的盐酸可返回锰矿浸出工序.结合印度尼西亚当地的气候地理条件,锰矿浸出与盐酸再生选择在常温(30 ℃)下进行,初始阶段使用工业盐酸直接浸出,而后通过盐酸再生实现氯循环.其中少量氯离子会损失于浸出渣残留,考虑用海水不断补充氯离子.图5为盐酸法富集低品位锰矿原则性工艺流程图,该工艺既能产出可直接用于出售的高品位锰精矿(锰品位>49%),又能产出高附加值产品硫酸钙晶须,实现了资源高效利用与无废排放,对环境友好.
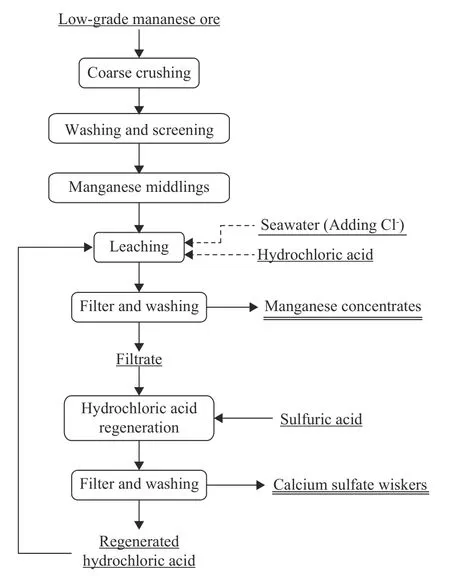
图5 低品位锰矿富集工艺流程图Fig.5 Process flow diagram of the beneficiation of low-grade manganese ore
3.4 锰中矿直接浸出
3.4.1 pH值的影响
锰中矿主要矿物为方解石和软锰矿,为使方解石溶出比较完全,就要适当降低浸出pH值.在浸出时间2 h,搅拌转速200 r·min-1,液固比4∶1 mL·g-1条件下,浸出pH值对产出锰精矿品位的影响如图6(a)所示.pH值为4时,由于酸度不足,导致方解石未能完全溶出,钙含量高,锰精矿品位偏低;pH值由4减小到3时,方解石大量溶出,钙含量减少,锰精矿品位大幅提高;pH值小于3时,锰精矿品位依然不断增加,但增量较小.这表明浸出pH值为3时,锰中矿中的绝大部分方解石已经溶出.对比不同pH值下的盐酸用量,pH值为3时酸耗较低(每吨矿耗酸780 kg),浸出渣的锰质量分数达到53.67%,钙、硅的质量分数分别为0.42%和0.92%,浸出效果较好.继续降低pH值虽然能继续提高锰精矿品位,但提高并不明显,而酸耗却在不断增加,pH值偏低也会对反应容器的耐腐蚀性提出更高要求,这些因素都会导致工业应用成本提高.因此,浸出pH值选择3较为合适.
3.4.2 浸出时间的影响
在浸出pH为3,搅拌转速200 r·min-1,液固比4∶1 mL·g-1条件下,浸出时间对产出锰精矿品位的影响如图6(b)所示.随着浸出时间的增加,锰精矿品位不断提高,钙含量因方解石的溶出而不断减少,但总体变化趋势较为平稳,锰精矿品位都在54%以上.锰矿盐酸浸出属于典型的液固反应,浸出时间越长,盐酸与可溶性物质反应就越充分,得到的锰精矿的品位也就越高.但考虑到生产效率,浸出时间不宜过长,且浸出时间大于1.5 h后,锰精矿品位已趋于稳定.当浸出时间为1.5 h时,锰精矿品位达到54.45%,钙、硅的质量分数分别为0.47%和1.30%,达到了很好的浸出效果,浸出时间选择1.5 h较为合适.
3.4.3 搅拌转速的影响
在浸出pH为3,浸出时间2 h,液固比4∶1 mL·g-1条件下,搅拌转速对产出锰精矿品位的影响如图6(c)所示.可以看出搅拌转速对锰精矿品位的影响较小,这是因为实验所用锰中矿已经经过磨细处理,矿粉比表面积大,比较容易做到均匀浆化,较有利于锰矿中方解石的溶出.搅拌转速低于200 r·min-1时,矿浆搅动变弱,传质条件变差,产出锰精矿品位偏低.搅拌转速大于200 r·min-1,锰精矿品位变化趋于稳定.工业应用时,搅拌转速过快,会增加矿浆对反应容器的磨损,搅拌转速不宜过高.因此搅拌转速选择200 r·min-1较为恰当,在此条件下,产出锰精矿品位为54.43%,钙、硅的质量分数分别为0.49%和1.29%.
3.4.4 浸出液固比的影响
在浸出pH为3,浸出时间2 h,搅拌转速200 r·min-1条件下,浸出液固比对产出锰精矿品位的影响如图6(d)所示.可以看出,适当提高液固比,可以提高锰精矿品位.当浸出液固比较小时,浸出效果较差,这是因为液固比较小时,矿浆较为浓稠,搅拌传质条件差,不利于液固反应的进行.随着浸出液固比的增加,传质条件变好,方解石溶出更加完全,钙含量不断减小,锰精矿品位不断提高.但实际工业应用时,浸出液固比过高会增加成本投入,降低生产效率,不宜采用较高的液固比.综合考虑,浸出液固比选择4∶1 mL·g-1较为合适,产出锰精矿品位为53.46%,钙、硅的质量分数分别为0.88%和0.84%.
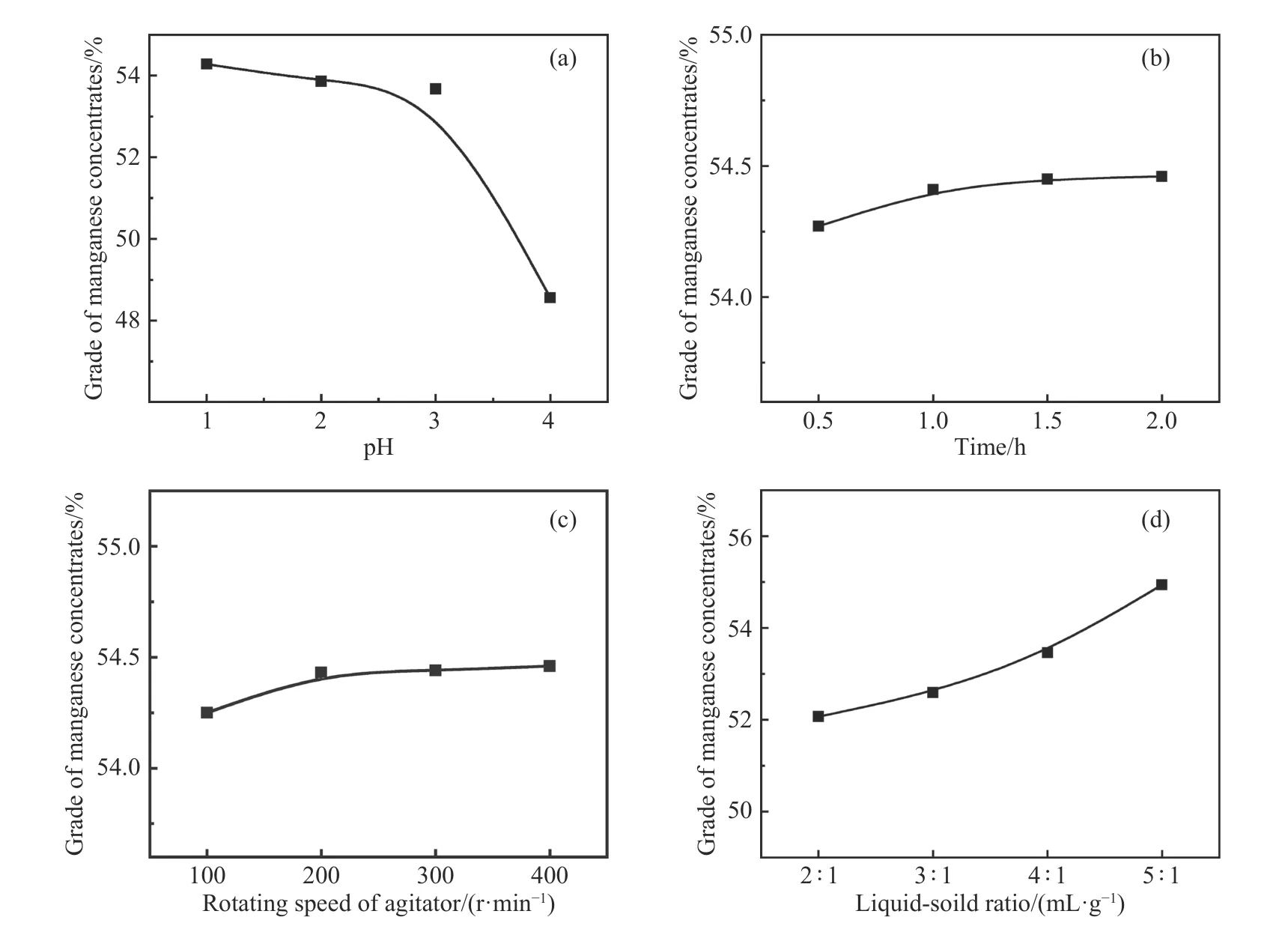
图6 不同浸出条件对锰精矿品位的影响.(a) pH;(b) 时间;(c) 搅拌转速;(d) 液固比Fig.6 Effect of different leaching conditions on the grade of manganese concentrates: (a) pH; (b) time; (c) rotating speed of agitator; (d) liquid-solid ratio
3.4.5 最优条件实验
通过以上条件实验,同时综合各种因素,可以确定锰中矿的最优浸出条件为:浸出pH为3,浸出时间1.5 h,搅拌转速200 r·min-1,液固比4∶1 mL·g-1.在此条件下进行实验,产出锰精矿的元素化学分析结果如表3所示.结果显示:最优条件下锰中矿经盐酸直接浸出,锰矿品位可从33.32%提高到54.50%,钙的相对质量分数从16.23%降低到0.57%.锰精矿中的C质量分数只有0.02%,对比原矿和中矿,C的脱除较为彻底.这是因为主要存在于方解石中的C随方解石的溶解而转化为二氧化碳气体脱离反应体系,且方解石的溶解较为完全.其他杂质元素含量普遍较低,浸出效果良好,浸出渣经适当处理后可直接作为高品位锰精矿出售(锰品位>49%).

表3 最优条件产出的锰精矿化学分析(质量分数)Table 3 Chemical analyses results of the synthesized manganese ore concentrate under optimal conditions %
3.5 盐酸再生与再生盐酸浸出锰中矿
使用不同硫酸加入量再生出的盐酸进行锰中矿浸出最优条件实验,产出的锰精矿品位如表4所示,其中硫酸加入量表示其与理论完全反应所需硫酸量的比值.可以看出硫酸加入量越少,产出的锰精矿品位越高.这是因为硫酸的相对加入量越少,再生盐酸浓度就越小,盐酸中溶解的硫酸钙也就越少.再生盐酸浸出锰中矿时,盐酸被消耗,部分溶解在盐酸中的硫酸钙析出,降低锰精矿的品位.为了达到浸出要求,选择硫酸加入量为理论量的80%.此条件下产出的锰精矿品位为52.16%,钙、硅的质量分数分别为1.39%和0.83%,符合高品位锰精矿标准(锰品位>49%),验证了本工艺流程的可行性.盐酸再生产出的硫酸钙晶须XRD分析结果如图7(a)所示,硫酸钙晶须物相为二水硫酸钙,纯度高,结晶度较好.二水硫酸钙晶须光学显微镜图片如图7(b)所示,晶须呈棒状或针状,形貌较好,长径比可达50以上(晶须长度和直径分别为650 μm和12.5 μm).
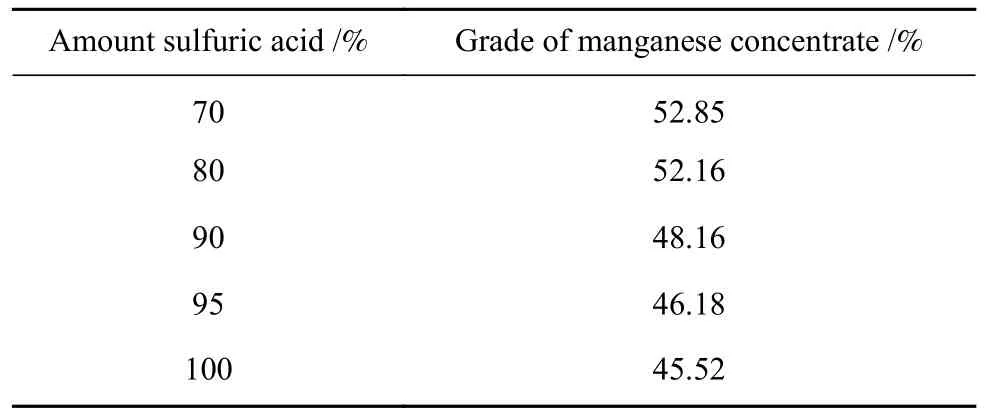
表4 硫酸加入量与锰精矿品位的关系Table 4 Relationship between the amount of added sulfuric acidand the grade of the manganese concentrate
3.6 产出锰精矿分析
产出的锰精矿X射线衍射分析结果如图8所示.可以看出,锰中矿经盐酸浸出,方解石已完全溶出,主要组成为软锰矿,此外还有很少量的褐铁矿.图9为锰精矿扫描电镜图与能谱分析.图9(a)中点1处为软锰矿,主要以细粒、微粒单体形式产出,并含有少量的杂质硅;点2处为褐铁矿与高岭石集合体,其中含有少量的锰.图9(b)中点3处为高岭石和软锰矿集合体,在电镜下呈不规则颗粒状;点4处为软锰矿与褐铁矿集合体,以细粒单体产出,锰含量高,并伴有少量铝、硅、钙等杂质.高岭石难溶于盐酸,且部分呈微粒状夹带于软锰矿中.部分褐铁矿与软锰矿或高岭石共生关系较为密切,或者包裹于软锰矿中.这些原因导致高岭石与褐铁矿等杂质矿物未能在盐酸环境下溶出而残留在锰精矿中,降低锰精矿品位.
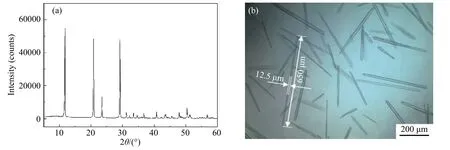
图7 二水硫酸钙晶须分析.(a) X射线衍射图;(b) 光学显微镜图Fig.7 Analyses of calcium sulfate dihydrate whiskers: (a) XRD pattern; (b) Optical microscope image
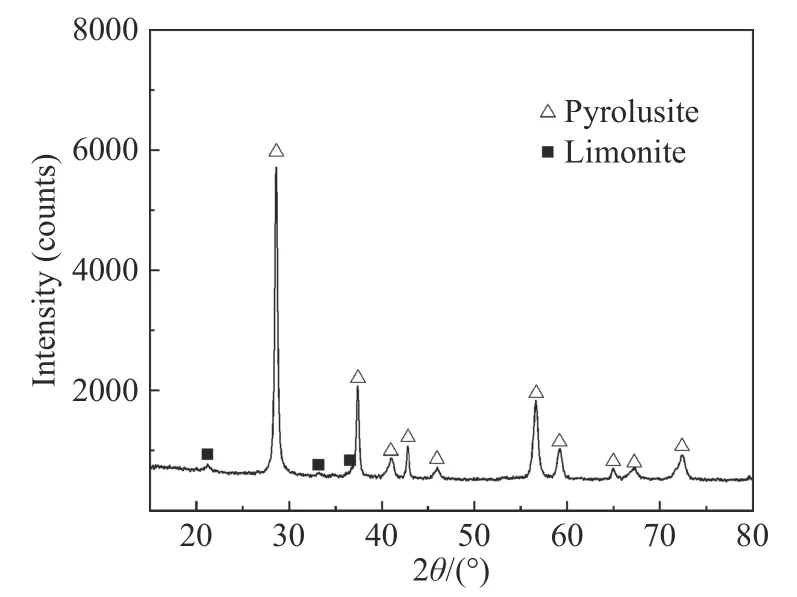
图8 锰精矿X射线衍射图谱Fig.8 XRD pattern of the manganese concentrates
3.7 酸介质的杂质积累与除杂
首次再生的盐酸介质主要杂质离子Mg2+、Al3+和Fe3+的质量浓度分别为202.3、8.6和0.01 mg·L-1.其中Mg2+质量浓度较高,优先考虑其循环积累情况.常温下MgCl2在水中溶解度为542 g·L-1[19],故饱和时的Mg2+质量浓度为138.2 g·L-1.为防止杂质因不断积累而饱和析出,进而影响锰矿浸出,需在酸介质循环一定次数后进行除杂.由Mg2+饱和浓度可推算出酸介质的循环次数约为680次,而实际上,由于同离子效应的存在,应选择Mg2+质量浓度达到饱和浓度的70%(96.74 g·L-1)时开始除杂,酸介质的循环次数约为480次.Mg2+、Al3+和Fe3+开始沉淀的pH值[19]分别为:9.4、3.3和1.6,完全沉淀pH值分别为:12.4、5.2和3.2.可以看出通过选用CaO为沉淀剂并准确调节pH值,即可分步沉淀除去杂质离子,并可使其得到回收利用.
4 结论
系统研究了印度尼西亚某低品位锰矿工艺矿物学,开展了筛析锰中矿盐酸浸出富集锰及盐酸再生耦合制备高值硫酸钙晶须的研究,得出如下结论:
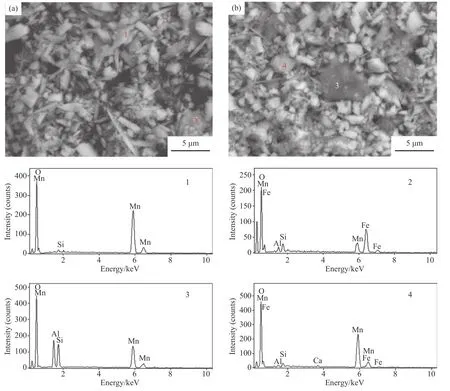
图9 锰精矿不同区域场发射扫描电镜图与能谱分析Fig.9 FESEM images and EDS analyses of the manganese concentrates at different zones
(1)锰矿矿物组成简单,含锰矿物主要为软锰矿,偶见菱锰矿,其他矿物主要为方解石,其次为褐铁矿、高岭石等,且较易实现软锰矿与方解石的分离.原矿经粗碎-洗矿后以2 mm筛孔的筛子过筛,筛下矿的锰质量分数从原矿的20.00%富集到33.32%,产率为61.8%,锰回收率为83.4%,锰矿得到初步富集,筛下锰中矿可用于盐酸浸出.
(2)锰中矿的盐酸直接浸出最佳工艺条件为:反应pH为3,反应时间为1.5 h,搅拌转速为200 r·min-1,反应液固比为4∶1 mL·g-1.在此条件下产出的锰精矿品位为54.50%,钙质量分数为0.57%.盐酸可在常温常压下由浸出液与硫酸溶液反应再生,产出的二水硫酸钙晶须结晶度好,呈棒状或针状,长径比可达50以上.再生盐酸浸出锰中矿产出的锰精矿品位为52.16%,钙质量分数为1.39%,少量溶解于再生盐酸中的硫酸钙在浸出时由于酸度降低而析出,导致锰精矿钙含量略高.产出的锰精矿主要组成为软锰矿,杂质矿物含量较少,主要为褐铁矿和高岭石等,可直接作为高品位锰精矿(Mn>49%)出售.酸介质循环再生,杂质镁铝铁将逐渐积累,当Mg2+质量浓度积累到96.74 g·L-1时进行除杂,此时酸介质的循环次数约为480次.除杂采用水解沉淀法,加入CaO调节pH值分步沉淀除去杂质离子.

