无机纳米颗粒在锂离子电池复合电解质中的应用
郭 健
(青岛科技大学 高分子科学与工程学院,山东 青岛 266042)
新能源技术的可持续发展是当今世界亟待解决的问题之一,锂离子电池作为新能源的储能设备,已被广泛的应用于便携式智能设备(手机、电脑)以及电动交通工具(电动汽车、混合电动汽车、电动飞机)[1-2]。但它们的能量密度和循环寿命仍然不足以满足日益提升的用户需求,特别是对于未来大规模可再生的能源存储和电动交通工具的发展[3-4]。电解质是锂离子电池的重要组成部分。液体电解质由于其较高的离子电导率以及与电极良好的相容性,几十年来在电化学储能中发挥着重要的作用。然而液体电解质具有明显的两个缺点:一是易泄露、高可燃性和化学稳定性较差等原因可能会导致燃烧甚至爆炸的危险;二是锂枝晶的产生和生长,缩短了电池的使用寿命。,相对于液体电解质,聚合物电解质的比表面积较高,且工作温度范围较宽,为生产高容量、大功率、长循环等良好性能的电池提供了有利条件;能适应在充放电过程中的体积变化,具有良好的电极界面相容性;与液体电池中的多孔隔膜相比,聚合物电解质有利于抑制锂枝晶的生长;此外,聚合物电解质能够有效促进离子的传输,综合性能优于普通隔膜;最后,聚合物电解质能够排除有机液体泄露,燃烧爆炸,腐蚀外壳等风险,大大提高了电池使用的安全性。是一种更富有发展前景的电池材料[5-6]:
理想的聚合物电解质应符合以下技术指标要求:(1)电导率应在10-3~10-2S·cm-1范围内,接近液体电解质;(2)较高的锂离子迁移数(≈ 1.0);(3)具有较宽的电化学窗口(> 4.5 V),减少分解反应的发生;(4)在电池工作温度范围内(- 40~150 ℃)具有良好的热稳定性和机械稳定性。但实际情况是,聚合物电解质的电导率往往低于液体电解质,因此如何提高聚合物电解质的电导率以及使其各项性能接近理想状态,是目前研究聚合物电解质的重要课题之一。自Weston和Steele首次报道具有α-Al2O3填料的复合电解质以来[7],将无机纳米材料引入聚合物基质,从而结合无机电解质和有机电解质的优势一直是研究的热点,人们普遍认为,陶瓷纳米颗粒能够促进聚合物基质局部结构改性,导致游离锂离子浓度增加,使其能够在陶瓷延伸表面的整个导电通路中快速移动,提高离子电导率,而且添加无机纳米颗粒还可以提高聚合物电解质的力学和热力学性能。因此,设计填料的组成、结构以及与聚合物的成膜工艺成为研究的热点。
1 无机纳米颗粒填充复合电解质
1.1 简单的陶瓷填料填充对复合电解质的影响
无机纳米颗粒的填充不仅提高了聚合物电解质热稳定性,而且由于其在整个聚合物电解质中分散良好,破坏了聚合物的结晶区域,增加了无定型区域的比例,从而增加了电解质的吸液量以及机械强度[8-10]。随着填料的发展,填料的结构也会影响聚合物电解质的性能,如中空结构、多孔结构等。制备工艺则是通过简单的相分离法,将无机纳米填料与特定的聚合物分散在有机溶剂中,然后将溶液涂布在玻璃板或聚四氟乙烯板上,干燥或浸入凝固浴中,最终得到复合电解质[11-12]。
Jayalekshmi等[13]通过将Al2O3掺杂进聚(环氧乙烷)(PEO)、碳酸亚乙酯(EC)和碳酸亚丙酯(PC)的共混膜中,发现添加Al2O3可以提高固态电解质(SPE)的离子电导率,Al2O3改性SPE薄膜的离子电导率为1.86×10-4S·cm-1,相比于对照组提高了一个数量级 (1.08×10-5S·cm-1).此外,对于掺杂8% Al2O3的复合电解质,观察到的锂离子迁移数约为0.9895,从电化学储能装置应用的角度来看,这是非常可观的实验结果。其原因是向聚合物中添加Al2O3作为活性填料导致表面官能化,在晶粒表面形成-OH基团,进而与迁移的离子形成氢键,提高了最终的离子导电性。

图1 电池中PVDF-co-HFP和PVDF-co-HFP / SiO2隔膜上锂离子的示意图Fig.1 The schematic illustration of lithium-ions across the PVDF-co-HFP and PVDF-co-HFP/SiO2 separators in the battery
He等[14]人通过直接固化工艺从纳米SiO2/丙酮单分散悬浮液和聚(偏二氟乙烯-共六氟丙烯)(PVDF-HFP)/丙酮凝胶的混合物中合成高度均匀的非均相复合电解质,如图1所示,将不同比例的SiO2纳米颗粒与PVDF-co-HFP分别溶于丙酮溶液中形成两个均相体系再进行共混。该技术使PVDF-co-HFP/SiO2复合凝胶电解质具有优异的微观结构均匀性。SiO2纳米颗粒的掺入有效降低了复合电解质的结晶度(降低≈ 27%),有效提高了电解质的润湿性(≈ 14%)、电解质吸收率(≈ 420%)和机械强度(> 14 MPa)。值得注意的是有效降低了LiFePO4/Li电池的极化提高了电池循环性能,使得0.5 C时室温容量高达165 mAh·g-1,在2 C下1500次充电/放电循环后只有5.2%容量衰减;并且提高了电池的热尺寸稳定性(160 ℃退火后收缩率约为4.5%)。
1.2 特殊结构的陶瓷填料填充对复合电解质的影响
Chen及其合作者[15]通过以Brij56为表面活性剂,HCl为pH调节剂的软模板法合成了中空SiO2纳米微球,微球具有较高的比表面积804.15 m2·g-1;在聚合物方面引入甲基丙烯酰氧基丙基三甲氧基硅烷(MPTMS)修饰的甲基丙烯酸甲酯(PMMA)与PVDF-HFP共混,将两者在丙酮溶液中形成均相体系,溶液浇铸成膜获得中空SiO2纳米微球掺杂的复合凝胶电解质。这种复合电解质具有至少两种特性,首先,在电池循环期间复合结构内部可以提高电解液的保留率;其次,纳米尺寸的颗粒使之形成多孔网状物,为锂离子提供传输路径,并防止中间产物在电极之间穿梭(如图2所示),有效改善了电池性能:1 C下初始放电容量在1277 mA h·g-1,100次循环后具有1143 mA h·g-1的超高比容量,容量保持率为89.5%。
Lanceros-Méndez等[16]通过以十六烷基三甲基溴化铵(CTAB)为软模板制备了尺寸约400 nm的介孔SiO2微球,作为填料其具有超高的比表面积1197 m2·g-1和密集的介孔结构。通过非溶剂诱导相分离法(NIPS)制备了SiO2/聚(偏二氟乙烯)(PVDF)复合电解质,在浸入水凝固浴中之前,将复合膜暴露在空气中不同时间,发现暴露于空气1分钟后制备的复合膜显示出最佳的离子电导率(0.9 mS·cm-1)。在2 C下循环50次后,观察到Li/CPE/LFP体系电池仍具有较高容量(95 mA h·g-1)和保持率(96%),倍率性能明显优于原始空白样。

图2 复合聚合物电解质的表面和横截面的SEM图像Fig.2 SEM images of the surface and cross-section of the composite polymer electrolyte
1.3 二元/多元金属氧化物填充对复合电解质的影响
除二氧化硅、二氧化钛、氧化铝等一元金属氧化物外,多元金属氧化物同样适用于填充复合电解质,其结构主要有烧绿石型、钙钛矿型和尖晶石型等。除了拥有一元陶瓷填料的固有优势外,复合多元金属氧化物具有较高的离子电导率。
Park等[17]通过将铝掺杂的钛酸锂镧(A-LLTO)固体电解质颗粒掺入PVDF-HFP聚合物基质中得到复合电解质。如图3所示,A-LLTO固体电解质用作分散相的无机填料,其具有室温下较高的离子电导率(2.99×10-3S·cm-1)、锂扩散系数、热稳定性和较宽的电化学窗口等优点。然而,A-LLTO与锂金属接触时化学性质不稳定,因此A-LLTO颗粒用超薄SiO2外壳封装,改性后的颗粒与锂金属接触时化学性质稳定,壳层足够薄,不会妨碍锂离子的传输,SiO2层的表面也有助于增强无机颗粒与聚合物基质之间的相容性。得到的复合电解质表现出1.22×10-3S·cm-1较高的离子电导率和高达5 V(VS.Li / Li+)的电化学稳定窗口,且Li/LiCoO2电池在0.5 C倍率下500次充/放电循环后容量保持率为80.5%,明显优异于对照组电池(32.6%)。
图3 (a-b)A-LLTO / m-SiO2核-壳结构颗粒的SEM、TEM图像(c)放大对应于标记区域的TEM图像;(d)在0.5 C的充放电速率下进行500次循环
Fig.3 (a) SEM,(b) TEM images of A-LLTO/m-SiO2core-shell structured particles,(c) magnified TEM images corresponding to the marked regions;(d) under the charge-discharge rate of 0.5 C for 500 cycles
Rajendran等[18]通过水热法成功制备了立方结构的BTiO3纳米颗粒,并作为填料掺杂在PVDF-HFP/醋酸乙烯酯(PVAc)/双三氟甲基磺酸亚酰胺锂(LiTFSI)/ EC的共混物中,制备锂离子电池的复合电解质。与空白样电解质相比,所有复合电解质电导率均显著增加。随着立方结构BTiO3陶瓷填料浓度的增加,复合膜的玻璃化转变温度和结晶度大大降低。掺杂7.5 %立方结构BTiO3的复合电解质显示5.4 V(VS.Li / Li+)电化学稳定窗口,显著提高了放电容量、循环稳定性和各倍率(0.2和0.5 C)下的库仑效率,而且复合电解质与锂电极具有良好的相容性,有效地抑制锂电极表面上锂枝晶的形成。
2 无机纳米颗粒涂层或夹层复合电解质
2.1 涂层工艺在复合电解质中的应用
为了保护聚合物电解质的表面,往往借助纳米填料与聚合物粘合剂在基材表面上形成网络结构的涂层工艺,这不仅增强了电解质表面的孔隙率、电解液吸液率和离子电导率,并且在提高循环容量方面也起着重要作用。无机纳米填料的耐高温性能可使复合电解质具有热稳定的涂层并提供有效的加热保护。用于改性膜的最常见无机纳米填料有二氧化钛[19]、二氧化硅[20-21]、氧化铝[22]等。
浸涂技术易于形成厚度可控且表面积较大的均匀涂层,并广泛应用于商业和非商业领域。制备涂层复合电解质的一般工艺如下:首先,通过超声处理将纳米颗粒分散在有机溶剂中;然后,在室温或高温下将特定的粘合剂加入搅拌器中形成均相体系,将聚合物浸入溶液中制备涂覆的复合电解质;最后,将其在特定温度下真空干燥。
Lee等[23]通过水热法和喷射研磨工艺成功制备了高纯度的超细α-Al2O3颗粒。将喷射研磨的Al2O3颗粒涂覆在常规聚乙烯(PE)隔膜上,研究Al2O3粒度对涂覆Al2O3的PE隔膜的涂覆性能的影响。在球磨过程中,首先将填料、粘结剂和丙酮混合2小时形成均相溶液,然后将PE隔膜浸入溶液中,最后在真空烘箱中干燥。他们发现,与未经研磨的颗粒相比,经过喷射研磨加工后可以生成纯度为99.99%的α-Al2O3颗粒。与涂有未研磨颗粒的对照组(其孔隙率为59%,吸液量为212%)相比,水热法制备的颗粒涂层为PE隔膜提供了较高的孔隙率(61%~63%)和较高吸液量(243%~244%)。在热性能上,PE隔膜表面的Al2O3涂层也显著降低了复合电解质的收缩率。
Kim等[24]合成了氨基官能化的SiO2(N-SiO2)颗粒并用于涂覆多孔聚乙烯隔膜的两侧,涂覆后的电解质表现出良好的润湿性,当用电解液浸泡后,复合电解质具有较高的离子导电性和优异的热稳定性。制备工艺流程如下:将氨基官能化的SiO2纳米颗粒溶解到具有聚PVDF-HFP粘合剂的N,N-二甲基甲酰胺(DMF)溶液中,并进行球磨24小时以制备均匀的浆料,然后将PE电解质浸渍其中使其两侧均有浆料涂覆,最后真空干燥。亲水性氨基官能化使SiO2涂层具有良好的均匀性和亚微米尺寸的多孔结构,有效的提高了复合电解质的热稳定性,而且作为粘结剂的PVDF-HFP能够增强电解液的吸收,使离子电导率达到0.81 mS·cm-1。与用常规PE隔膜或SiO2涂覆的复合电解质所制备的电池相比,采用N-SiO2涂覆的复合电解质的锂离子电池显示出优异的容量保持率、倍率性能和高温循环稳定性。
Li等[25]设计了一种由聚苯乙烯-聚(丙烯酸丁酯)共聚物包覆的SiO2核壳纳米颗粒,作为“热关闭开关”,涂在聚丙烯隔膜上,如图4所示。聚合物壳层在玻璃化转变温度(Tg)以上具有自粘性,能够有效的阻止电极之间的Li+传导,从而防止电池热失控,不仅如此,当电池温度持续升高时,纳米颗粒内核能够保护隔膜避免发生显著的热收缩,提高了复合电解质本身的热稳定性。涂覆的隔膜具有与商业隔膜相同的离子电导率和循环容量,并且对电化学性能没有负面影响,他们发现涂层电解质膜在80 ℃下工作不会发生容量损失。

图4 制备涂覆在多孔隔板上的PS-co-PBA @ SiO2的示意图Fig.4 Schematic diagram for the preparation of PS-co-PBA@SiO2 coated on porous separator
2.2 夹层工艺在复合电解质中的应用
除了无机纳米填料在商业聚合物电解质上的涂覆工艺以外,最近在两层聚合物电解质中间填充一层无机纳米填料的夹层工艺也被开发出来[26-27],以期解决锂离子电池中电解质的两个较为突出的问题:较低的离子电导率与锂枝晶的生长;一层由粘结剂与无机填料混合的高浓度无机纳米颗粒层不仅能够发挥某些二元金属氧化物填料的高电导率优势,也能够凭借其较高的机械强度有效抑制锂枝晶的生长。
Yang等[28]设计了一种聚合物/聚合物-钛酸锂镧(LLTO)/聚合物混合夹层结构的复合电解质。一方面,聚PVDF层可以避免LLTO同锂金属的化学反应并抑制锂枝晶生长,通过使用PVDF表层,可以改善LLTO对锂金属的化学稳定性。另一方面,制备的夹层电解质可以有效的降低锂离子电池的界面电阻。因此,复合电解质在室温下显示出优异的锂离子电导率(3.01×10-3S·cm-1)、较高的锂离子迁移数(tLi+= 0.74)、较低的界面电阻和较宽的电化学窗(~5.0 V)。此外,组装的钴酸锂(LiCoO2)/复合电解质/Li电池在2 C下表现出优异的倍率性能,在循环100次后,电池具有132 mA h·g-1的放电容量和91.8%容量保持率。

图5 (a)二氧化硅纳米粒子夹层隔板的SEM图像;(b)在相同条件下测试具有常规隔板(灰色曲线)和二氧化硅纳米颗粒夹层三层隔板(黑色曲线)的Li / Li电池的典型电压与时间的关系曲线
Fig.5 (a) SEM image of the silica nanoparticle sandwiched separator;(b) Typical voltage versus time profle of a Li/Li battery with a conventional separator (grey curve) and the silica nanoparticle sandwiched trilayer separator (black curve) tested under the same conditions
Cui等[29]通过将二氧化硅纳米颗粒夹在两个聚合物电解质(商业PP膜)之间来制备具有反应保护效果的复合电解质,如图5所示。该设计有三个优势,(1)SiO2/锂化SiO2(在Li枝晶渗透之后)不与活性阳极/阴极接触。(2)无机纳米颗粒的物理性质通常表现为将它们涂覆在聚合物电解质上来提高热稳定性,电解液的润湿性等,但是该设计证明了金属锂与SiO2可以发生反应,使填料拥有能够消耗锂枝晶的化学性质并显著延长电池循环寿命。(3)SiO2纳米粒子的夹层结构与聚合物良好的相容性使复合电解质更加坚固,杨氏模量较强的SiO2层抑制了渗透到电解质中的锂枝晶生长。凭借SiO2纳米颗粒的物理化学两种性质可以将电池的寿命延长大约五倍。另外,夹层复合电解质的制造可以通过使用传统浆料涂覆工艺完成,使其完全与制造锂离子电池的常规工艺兼容。
3 无机纳米颗粒原位生成复合电解质
由于原位聚合可以让填料更均匀的分散在聚合物基质中,使得制备原位生成含有无机纳米填料的复合电解质成为广受关注的热点之一,相比于简单的掺杂,原位聚合能更有效的破坏聚合物的结晶结构,改善其电化学性能。其制备工艺主要分为两种:一是通过无机填料与聚合物单体的混合使聚合物单体在充满无机填料的均相体系下聚合;二是将无机填料单体与聚合物混在有机溶液中,使填料在聚合物内部或者表面原位成核形成复合电解质。
3.1 聚合物单体在填料均相体系下原位合成

图6 (a)插入交联过程的PLxTF-GPE的原位制备方法;(b)PLxTF-GPE的可能的复合结构的示意图Fig.6 Schematic of the a) in situ preparation process of PLxTF-GPE with crosslinking process inserted;(b) possible composite structure of PLxTF-GPE
Wen等[30]以Li6.4Ga0.2La3Zr2O12为引发剂和离子导电填料,采用原位交联法设计合成了一种耐火复合凝胶电解质,如图6所示。先将填料与聚合物分别溶于有机溶剂中获得均相体系,共混搅拌6.0 h后,将共混物转入模具中聚合,所制得的复合凝胶电解质表现出优异的耐火性能。复合后的凝胶电解质在20 ℃下具有高达1.84×10-3S·cm-1的离子电导率,室温下电化学窗口高达4.75 V。此外,所获得的凝胶复合电解质与锂具有优异的兼容性。该方法制备的复合凝胶电解质简便且对环境无害,优异的安全性和电化学性能使其成为发展高安全性和高性能锂金属电池的潜在电解质。
Fan等[31]设计合成了三乙二醇二乙酸酯-2-丙烯酸丁酯(TEGDA-BA)的复合电解质(CPE),通过掺入Al2O3纳米颗粒(平均粒径10~20 nm)作为无机填料来原位聚合。将两种聚合物、引发剂及不同含量的Al2O3溶于有机溶剂中超声分散形成前驱体溶液,再转入玻璃模具中进行聚合。由于Al2O3纳米颗粒在聚合物中具有均匀的分散性,所以复合电解质的机械柔韧性和可弯曲性得到了显著改善。具有5 %Al2O3纳米颗粒的CPE在25 ℃下具有较高的离子电导率6.02×10-3S·cm-1、较高的Li+迁移数(0.675),以及较稳定的电化学窗口(> 4.5 V)。具有较高表面积的Al2O3可有效的增加电解液的润湿性并有助于捕获残留的痕量杂质,例如水、氧或电解质的分解产物,显著的改善了CPE与锂金属之间的相容性。
3.2 无机纳米颗粒在聚合物均相体系中原位合成
Cao等[32]通过在室温下静电纺丝聚合物溶液制备基于PVDF-HFP、热塑性聚氨酯(TPU)和PMMA的复合凝胶聚合物电解质:将不同含量的SiO2原料(TEOS)以及少量催化剂加入聚合物与丙酮的均相体系中,搅拌共混,通过静电纺丝技术得到复合电解质。含有2 %原位生成SiO2的复合电解质具有较高的离子电导率(8.5×10-3S·cm-1),在室温下电化学稳定窗口高达5.9 V(vs.Li+/Li)。含有2 %原位生成SiO2复合电解质制备的锂电池首次放电容量为168.5 mAh·g-1,约为磷酸铁锂(LiFePO4)理论容量的99%。并且它具有优异的机械稳定性、较高的拉伸强度(10.8 MPa)和断裂伸长率(86.4%),保证了复合电解质在锂离子电池中的操作安全。
Cui等[33]通过在PEO溶液中原位水解正硅酸四乙酯(TEOS)开发了PEO-单分散超细SiO2(MUSiO2)复合聚合物电解质(PEO-MUSiO2-CPE),如图7所示。在原位合成期间形成的MUSiO2球和PEO链之间的强化学/机械相互作用成功地抑制了PEO结晶度。此外,由于应用了精确控制的SiO2生长,可以实现更好的颗粒分布和单分散性,这增强了路易斯酸-碱相互作用的有效表面积。由于具有可控原位合成的所有优点,与无纳米填料掺杂的PEO相比,PEO-MUSiO2-CPE的离子电导率显著提高,甚至比通过简单机械混合的复合电解质还高1个数量级。电化学稳定性窗口拓宽至5.5 V。1 C倍率下分别在90 ℃和60 ℃下可以保持约120 mAh·g-1和100 mAh·g-1的LiFePO4容量,并且在80个循环内没有明显的容量衰减。
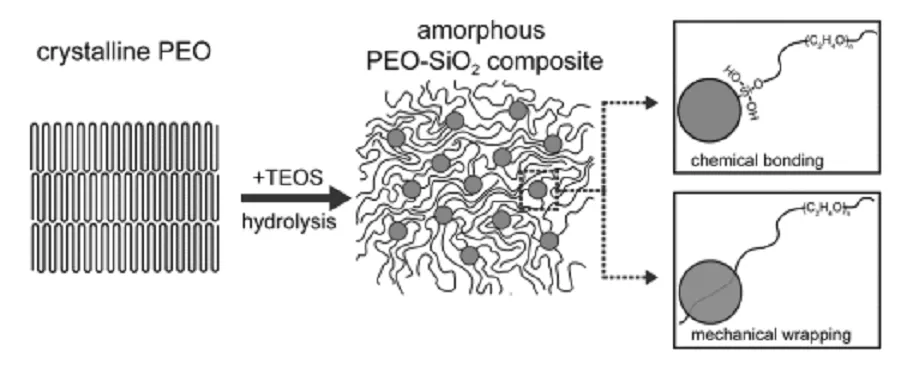
图7 两种可能的相互作用机制,在MUSiO2表面上PEO链的末端与羟基之间的化学键合,以及在MUSiO2球体生长期间PEO链的机械缠绕
Fig.7 Two possible interaction mechanisms are shown including chemical bonding between the ends of PEO chains with hydroxyl groups on MUSiO2surfaces and mechanical wrapping of PEO chains during the growth of MUSiO2spheres
4 无机纳米颗粒填充非织造复合电解质
传统非织造膜的缺点是具有大的孔径并且由于不充分的电解液保持能力,在长循环期间会发生较多的性能损失。为了解决这个问题,人们把研究方向转向了静电纺丝技术,该技术使电解质具有良好的润湿性和高孔隙率[34-35]。由于高度多孔结构和优异的吸液量,无机纳米颗粒可以有效的填充非织造膜。如今,静电纺丝是常见的制造较高电解液吸液量,较高孔隙率和优异电化学性能电解质的方法之一。
Yong等[36]通过在一步静电纺丝工艺中,将聚丙烯腈(PAN)聚合物和三种不同的有机聚硅氮烷(OPSZ)前驱体混合,制备了静电纺丝PAN/陶瓷复合电解质。电纺丝溶液中含有TEOS、DMF、PAN聚合物和某一种有机硅氮(OPSZ)前驱体,前驱体与TEOS的侧链交联,并且在纤维中形成了无机网络,从而为纤维膜提供了优异的机械强度和电化学性能。得到的复合电解质具有高达82±5%的孔隙率、1109±32%的电解液吸收率和电导率1.04±0.05 mS·cm-1。结果表明,具有交联无机网络结构的电解质显示出优异的机械和电化学性质,交联的无机填料影响聚合物的结晶能力,导致纤维内的无定形区域增加,无定形区域的增加导致电解液吸液收增加,提高了离子电导率和循环稳定性。
Cao等[37]通过静电纺丝技术成功制备了PVDF/SiO2复合非织造膜,并将其用作锂离子电池电解质,如图8所示。通过水解的TEOS与乙醇(1∶1体积比)在pH值=4.0下反应24 h制备二氧化硅溶胶,然后将7%PVDF溶液和SiO2溶胶以一定质量比(9∶1,10∶1)混合搅拌12 h得到纺丝原液,最终通过静电纺丝技术得到复合电解质。与商业PP隔膜相比,制备的复合电解质显示出较高的孔隙率(75 %~ 85%)和电解液吸液量(571% ~ 646 %)。更值得注意的是复合电解质由于耐热的PVDF非织造支撑体和无机SiO2成分的存在,在热收缩方面得到了显著的改善,有效提高了锂离子电池的安全性。

图8 对于(a)(9∶1)和(b)(10∶1)复合膜,在高和低放大倍数下的SEM图像;(c)在130 ℃和150 ℃下暴露1小时后分离器的照片。
Fig.8 SEM images at high and low magnifications for (9∶1) (a) and (10∶1) (b) composite membranes;(c)Photographs of the separators after exposure to 130 ℃ and 150 ℃ for 1 h.
Kim等[38]通过静电纺丝技术制备了含有6 %Al2O3纳米颗粒的PVDF-HFP复合电解质,吸收电解液后作为凝胶聚合物电解质(GPE)用于锂离子电池。将PVDF-HFP与Al2O3溶于丙酮/N,N-二甲基乙酰胺(7/3)组成的溶液用于制备纤维膜。与纯GPE相比,GPE- Al2O3复合电解质显示出优异的电化学稳定性和离子电导率。相对于GPE空白样,具有GPE- Al2O3复合电解质的电池在0.1 C倍率下显示出更高的可逆性,结果表明它们具有更高的放电容量和优异的循环稳定性。
Zhang等[39]使用沸石作为纳米填料制备复合电解质,沸石通过共聚物与纤维膜化学结合。首先,将合成的氟化共聚物PC4SA-co-PMMA-co-PMPS和PVDF加入到溶有沸石的二甲基乙酰胺(DMAc)/丙酮混合均相体系中,然后将溶液加入到静电纺丝机中进行静电纺丝。合成的共聚物与PVDF进行了自键合,并与共聚物形成共价键,提高了纳米纤维分散体的分散性,对PVDF膜的力学性能有良好的影响。三维纤维结构提供了较高的孔隙率、优异的热稳定性和较高的吸液量(378%),由于沸石的高表面积,复合电解质与纯PVDF空白样相比,具有高达1.72 mS·cm-1的锂离子电导率。复合电解质组装的电池显示出优异的倍率性能(5 C下为110 mAh·g-1)和良好的循环性(0.5 C下200次循环后容量保持率为93.8%)远远优于商业膜。
Cui等[40]设计了一种含有良好排列的无机Li+导电纳米线填料的复合电解质,如图9所示。首先制备Li0.33La0.557TiO3(LLTO)纳米线,随后加入适量的聚乙烯吡咯烷酮(PVP), 通过剧烈搅拌获得浓度为12 %PVP的前驱体溶液,由静电纺丝技术得到纳米线,再通过光刻法制造交叉指型电极,在Pt电极上煅烧规则排交叉列的纳米线,然后在纳米线上涂覆含有PAN-LiClO4的DMF溶液,最后烘干成膜。与随机分散的纳米线相比,良好排列的纳米线具有较高的锂离子电导率(30 ℃时为6.05×10-5S·cm-1)。此外,通过使用纳米线也改善了聚合物电解质的结构稳定性,为设计新型纳米结构改善固体电解质离子电导率提供了具有应用前景的参考方法。

图9 锂离子传导途径的比较。a-c,复合聚合物电解质中的锂离子传导途径,具有纳米颗粒(a);随机纳米线(b);和排列的纳米线(c);无机纳米粒子(NPs)和纳米线(NWs)的表面区域作为锂离子传导的高速通道(d)
Fig.9 The comparison of possible Li-ion conduction pathways.a-c,Li-ion conduction pathways in composite polymer electrolytes with nanoparticles (a);random nanowires (b);and aligned nanowires (c); The surface region of inorganic nanoparticles (NPs) and nanowires (NWs) acts as an expressway for Li-ion conduction(d)
5 结论与展望
本文主要介绍了无机填料在聚合物电解质中的应用,包括复合电解质的四种制备工艺以及无机填料的结构、成分和含量对复合电解质性能的影响。随着对电池安全性能以及电化学性能要求越来越高,聚合物电解质必须有较强性能来应对收缩与结构破坏,同时需要其具有较高的化学稳定性,不与电解质反应,以及较高的离子迁移数和电导率。目前,向聚合物电解质中添加无机填料制备复合电解质是最为可行的方法之一,首先,无机填料的均匀分布破坏了聚合物的结晶区域,增加复合电解质的润湿性,从而提高电导率与离子迁移数;其次,部分无机填料表面的基团可以和聚合物发生路易斯酸-碱反应,从而提高锂盐的解离性;最后,部分多元金属氧化物其本身也具有较高的导电性,从而提高复合电解质的电导率。不过我们也清晰的认识到,复合电解质还不足以同时满足多个物理化学性能,想要获得理想的复合电解质还需进一步优化填料的成分、结构,尝试开发新的制备工艺。填料结构从简单的实心结构到复杂的中空、介孔结构,电解质制备工艺从机械的填充涂覆到多孔的原位生成和静电纺丝技术,无论填料或电解质,孔体积的增加能够有效的提高复合电解质的电化学性能,因此,复合电解质的多孔性在未来的发展中将是人们研究的热点。复合电解质的产业化必将为锂离子电池发展做出重大贡献。
--先进无机材料论坛例记(Ⅰ)

