复方酮酸微丸胶囊的制备及其稳定性影响因素研究
徐 欣,刘哲鹏
(1.上海信谊金朱药业有限公司技术中心,上海 201506;2.上海理工大学医疗器械与食品学院制药工程教研室,上海 200093)
慢性肾病患者日常治疗中,在低蛋白饮食的基础上给予复方酮酸(含有氨基酸和酮酸)提供人体必需氨基酸,由于酮酸不含氨基,利用非必需氨基酸的氮在体内转化为氨基酸,从而减少氮的摄入,减少尿素合成,避免因蛋白质摄入不足导致的营养不良[1]。这种治疗方法在控制慢性肾病进程的临床研究中取得了较大进展[2]。本研究的复方酮酸制剂中含有多种人体必需氨基酸及酮酸,包括L-醋酸赖氨酸、L-苏氨酸、L-色氨酸、L-组氨酸、L-酪氨酸、酮缬氨酸钙、消旋酮异亮氨酸钙、酮亮氨酸钙、消旋羟蛋氨酸钙和酮苯丙氨酸钙,成分复杂。市场上已有的复方酮酸保健产品中的氨基酸和酮酸在储存过程中含量下降,给用药效果与用药安全带来隐患[3-4]。本研究根据相容性研究结果,将氨基酸和酮酸分别制成微丸,再装填胶囊,得到复方酮酸微丸胶囊,为慢性肾病患者提供一种补充必需氨基酸的制剂,也为相关制剂的临床开发奠定一定的理论基础。
1 仪器和试药
1.1 仪器 WL-300型制丸机、LBL-1型流化床(重庆市科旭制药机械设备制造有限公司);安捷伦1200高效液相色谱仪(配DAD二极管阵列检测器)、辛烷基硅烷键合硅胶色谱柱[安捷伦科技(中国)有限公司]、氢型阳离子交换色谱柱[赛默飞世尔科技(中国)有限公司];Milli-Q超纯水机(美国密理博公司)。
1.2 药品和试剂 醋酸赖氨酸、苏氨酸、色氨酸、组氨酸和酪氨酸(无锡晶海氨基酸有限公司);酮缬氨酸钙、消旋酮异亮氨酸钙、酮亮氨酸钙、消旋羟蛋氨酸钙、酮苯丙氨酸钙(开原亨泰制药有限公司);预胶化淀粉(卡乐康包衣材料有限公司);交联聚维酮、聚维酮K30(美国国际特品公司);滑石粉(桂林桂广滑石开发有限公司);醋酸赖氨酸对照品、苏氨酸对照品、色氨酸对照品、组氨酸对照品、酪氨酸对照品(中国食品药品检定研究院);酮缬氨酸钙对照品、消旋酮异亮氨酸钙对照品、酮亮氨酸钙对照品、消旋羟蛋氨酸钙对照品、酮苯丙氨酸钙对照品(上海理工大学医疗器械与食品学院自制);四氢呋喃、甲醇和乙腈为色谱纯;其余试剂均为优级纯。
2 方法和结果
2.1 氨基酸含量测定
2.1.1 氨基酸溶液的配制 取待测样品(氨基酸颗粒或复方酮酸微丸),研细,混匀后取适量,精密称定,置100 ml量瓶中,加入0.1 mol/L盐酸溶液适量,溶解,用0.1 mol/L盐酸溶液稀释至刻度,摇匀,过滤,作为供试品溶液。另分别称取组氨酸、苏氨酸、酪氨酸、色氨酸和醋酸赖氨酸对照品适量,用0.1 mol/L盐酸溶液溶解并配制成浓度为0.2、0.25、0.15、0.1和0.5 mg/ml的溶液,摇匀,作为对照品溶液。
2.1.2 氨基酸含量测定的色谱条件 采用辛烷基硅烷键合硅胶色谱柱(250 mm×4.6 mm,5 μm);流动相A:取1.64 g醋酸钠,加0.18 ml三乙胺和3 ml四氢呋喃,加水至1000 ml,混匀,用1%的醋酸溶液调节pH值至7.2;流动相B:取1.64 g醋酸钠,加200 ml水使溶解,用1%的醋酸调pH值至7.2,加入400 ml乙腈和400 ml甲醇,混匀,进行梯度洗脱:0~10 min流动相A 90%→80%,10~20 min流动相A 80%→50%,20~25 min流动相A 50%→20%,25~26 min流动相A 20%→0%,26~27 min流动相A 0%→90%,27~30 min流动相A 90%;柱温40 ℃;检测波长338 nm[5]。
2.1.3 样品处理和进样检测 分别取氨基酸对照品溶液和供试品溶液按以下方法进行柱前衍生化和进样检测。(1)硼酸缓冲液的配制:取2.48 g硼酸和1.14 g氢氧化钠,加水溶解并稀释至100 ml,用2 mol/L氢氧化钠溶液调节pH值至10.2,备用。(2)邻苯二甲醛(OPA)溶液的配制:称取120 mg OPA,加1 ml乙腈和7 ml硼酸缓冲液(pH 10.2)溶解后,加入150 μl的3-巯基丙酸,混匀,备用。(3)系统适用性实验:吸取10 μl硼酸缓冲液,2 μl的OPA溶液,2 μl氨基酸对照品溶液或供试品溶液,将14 μl溶液以最大速度混合,按2.1.2项下色谱条件进样检测,得到5种氨基酸的HPLC谱图,见图1。出峰顺序依次为组氨酸、苏氨酸、酪氨酸、色氨酸、赖氨酸,理论塔板数按组氨酸峰计算≥3000,相邻色谱峰之间的分离度均>1.5。
2.2 酮酸含量测定
2.2.1 酮酸溶液的配制 取待测样品(酮酸颗粒或复方酮酸微丸),研细,混匀后取适量,置250 ml量瓶中,加水适量溶解,定容,摇匀,滤过,作为供试品溶液。另分别称取酮缬氨酸钙、消旋酮异亮氨酸钙、酮亮氨酸钙、消旋羟蛋氨酸钙和酮苯丙氨酸钙对照品适量,分别用水溶解并配制成浓度为0.05、0.04、0.06、0.04和0.04 mg/ml的溶液,作为对照品溶液。
2.2.2 酮酸含量测定的色谱条件 采用氢型阳离子交换色谱柱(380 mm×7.8 mm,9 μm);精密吸取0.67 ml浓硫酸,加水稀释至1000 ml,即得0.012 5 mol/L的硫酸溶液作为流动相;检测波长205 nm;流速0.5 ml/min;柱温25 ℃[6]。
2.2.3 系统适用性实验 精密量取酮酸供试品溶液和对照品溶液各10 μl,注入HPLC仪,得到5种酮酸的HPLC谱图(见图1)。理论塔板数按酮苯丙氨酸钙计算≥2000,相邻色谱峰之间的分离度均>1.5。
2.4 标准曲线的绘制
2.4.1 氨基酸的标准曲线 分别称取醋酸赖氨酸、苏氨酸、色氨酸、组氨酸和酪氨酸对照品52.54、26.64、11.37、19.12和15.26 mg,置20 ml量瓶中,加0.1 mol/L盐酸溶液适量使溶解,稀释至刻度,作为对照品储备液。分别精密量取对照品储备液1.0、1.5、2.0、2.5、3.0 ml,分别置10 ml量瓶中,加0.1 mol/L盐酸溶液稀释至刻度,作为系列浓度标准曲线工作液。按2.1.2项下色谱条件进样检测,记录色谱图。以峰面积(A)对浓度(c)进行线性回归,计算标准曲线,得到醋酸赖氨酸、苏氨酸、色氨酸、组氨酸、酪氨酸的线性回归方程见表1,结果表明5种氨基酸在线性范围内线性关系良好。

表1 氨基酸和酮酸含量测定的方法学考察结果
2.4.2 酮酸的标准曲线 分别精密称取28.94 mg酮缬氨酸钙对照品、24.09 mg消旋酮异亮氨酸钙对照品、33.25 mg酮亮氨酸钙对照品、17.56 mg消旋羟蛋氨酸钙对照品和18.54 mg酮苯丙氨酸钙对照品,置50 ml量瓶中,加水适量,超声使对照品完全溶解,定容,摇匀,作为对照品储备液。精密量取对照品储备液0.5、1、2、5、8、10和12.5 ml,分别置50 ml量瓶中,加水稀释并定容至刻度,摇匀,作为系列浓度标准曲线工作液,按2.2.2项下色谱条件进样,记录色谱图。
以各组分的峰面积(A)对浓度(c)进行线性回归,计算标准曲线,得到酮缬氨酸钙、消旋酮异亮氨酸钙、酮亮氨酸钙、消旋羟蛋氨酸钙和酮苯丙氨酸钙的线性回归方程见表1,表明5种酮酸在线性范围内线性关系良好。
2.5 精密度实验 精密量取供试品溶液,重复进样6次,结果5种氨基酸和5种酮酸的RSD均<2%(见表1),表明精密度良好。
2.6 重复性实验 按2.1.1项和2.2.1项下方法,分别配制氨基酸或酮酸对照品溶液和6份供试品溶液,按2.1.2项和2.2.2项下色谱条件,测得5种氨基酸和5种酮酸含量的RSD均<1.5%(见表1),表明方法重复性良好。
2.7 回收率实验 (1)氨基酸的回收率:按处方组成称取各种辅料和酮酸,混匀后作为模拟空白辅料,将模拟空白辅料分别加入到标示含量为80%、100%和120%的各种氨基酸对照品中,每组平行3份,加0.1 mol/L盐酸溶液使主成分溶解,过滤,作为供试品溶液。按2.1.2项下色谱条件进样,测得各种氨基酸含量测定的平均回收率在98.62%~100.45%,表明氨基酸的回收率良好。(2)酮酸的回收率:按处方组成称取各种辅料和氨基酸,混匀后作为模拟空白辅料,将模拟空白辅料分别加入到标示含量为80%、100%和120%的各种酮酸对照品中,每组平行3份,加水使主成分溶解,滤过,作为供试品溶液。按2.2.2项下色谱条件,测得各种酮酸含量测定的平均回收率在99.14%~101.45%,表明酮酸的回收率良好。
2.8 稳定性实验 精密量取供试品溶液,每2 h测定一次,连续测定12 h,结果5种氨基酸和5种酮酸的RSD均<2%,表明供试品溶液在12 h内稳定。
2.9 相容性实验 将5种氨基酸和5种酮酸共10种组分混匀,另分别将5种酮酸混匀,将5种氨基酸混匀,将混匀后样品进行影响因素试验(高温60 ℃),以相对于0 d的性状和含量变化作为考察指标。10种组分混合样品、5种氨基酸混合样品以及5种酮酸混合样品的高温相容性实验结果见表2。10种组分混合样品在60 ℃放置10 d,性状由白色粉末变为黄色粉末。由表2可见,醋酸赖氨酸、色氨酸、酮亮氨酸钙和酮苯丙氨酸钙的含量有显著变化。而5种氨基酸、5种酮酸分别制粒后混合,60 ℃放置10 d,各种氨基酸和酮酸的含量和混合物的性状均无明显变化。由此可见,酮酸和氨基酸之间存在相互作用,因此为保证微丸中药物稳定性,本研究考察了将氨基酸和酮酸分别制颗粒、再混合后的影响因素试验,结果见表2。将酮酸与氨基酸分别制颗粒后,60 ℃放置10 d,各组分含量均无明显变化,说明将氨基酸与酮酸分别制粒,样品相容性较好。因此,本研究将氨基酸和酮酸分别制丸,装填胶囊,以保证其稳定性。

表2 氨基酸和酮酸混合样品在高温60 ℃的相容性 (%)
2.10 微丸的制备
2.10.1 氨基酸微丸的制备 取处方量的醋酸赖氨酸、苏氨酸、色氨酸、组氨酸、酪氨酸(见表3),过80目筛,混匀,取部分混合物,加入5%聚维酮K30溶液制软材,过60目筛制粒,流化床干燥,60目筛网整粒,收集60~80目颗粒,置于制丸机中。开动制丸机,以7 ml/min流量喷入15%聚维酮K30乙醇溶液,同时不断加入剩余混合物,制丸。控制雾化压力<0.3 MPa,转速250~350 r/min,温度35 ℃~45 ℃,加料结束后,维持制丸机温度15 min,加入适量滑石粉混匀。

表3 复方酮酸微丸胶囊的处方组成 (mg/粒)
2.10.2 酮酸微丸的制备 取处方量的酮缬氨酸钙、消旋酮异亮氨酸钙、酮亮氨酸钙、消旋羟蛋氨酸钙、酮苯丙氨酸钙及辅料(见表3),过80目筛,混匀,取部分混合物,加入5%聚维酮K30溶液制软材,过60目筛制粒,流化床干燥,60目筛网整粒,收集60~80目颗粒,置于制丸机中。开动制丸机,以7 ml/min流量喷入10%聚维酮K30乙醇溶液,同时不断加入剩余混合物,制丸。控制雾化压力<0.3 MPa,转速250~350 r/min,温度35 ℃~45 ℃,加料结束后,维持制丸机温度15 min,加入适量滑石粉混匀。
2.10.3 复方酮酸微丸胶囊的制备 分别取上述氨基酸微丸和酮酸微丸,装填胶囊,制备得到每粒含氨基酸微丸270 mg、酮酸微丸460 mg的复方酮酸微丸胶囊。
2.11 影响因素试验 将制备得到的复方酮酸微丸胶囊进行高温(60 ℃)、高湿(相对湿度92.5%)和强光照射(4500 Lx)影响因素试验,0、5和10 d取样,检测各组分含量变化,结果见表4。由表4可见,复方酮酸微丸胶囊在上述条件下放置10 d,各组分稳定性良好。
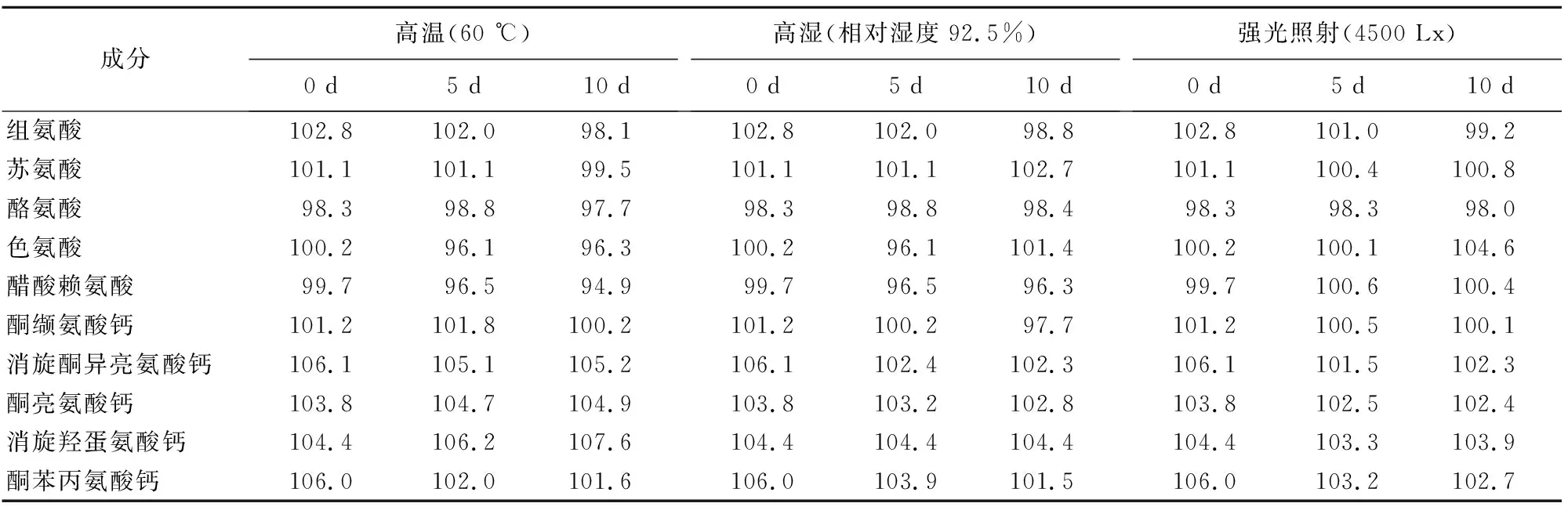
表4 复方酮酸微丸胶囊含量的影响因素试验结果 (%)
3 讨 论
本研究发现,复方酮酸组分中的醋酸赖氨酸、色氨酸、酮亮氨酸钙与酮苯丙氨酸钙之间存在相容性配伍问题,因此在制备工艺中采用将氨基酸和酮酸分别制丸后再装填胶囊的方式,可以较好地解决复方产品组分的稳定性问题。有研究表明,高温、高湿、强光照射、原辅料相容性因素等会影响产品质量[7],在产品开发中,首先应通过相容性研究,明确各组分在高温、高湿和强光照射等外界苛刻条件下的稳定性以及处方中各组分是否存在相容性问题,再以此为基础选择合适的工艺条件开发产品,从而可以有效确保复方制剂的产品质量。本研究制备的复方酮酸微丸胶囊稳定性良好,可用于慢性肾病患者必需氨基酸的补充。

