实验室制取二氧化碳
张翠然
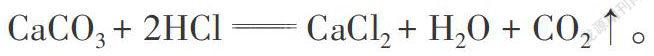
实验室制取二氧化碳是初中化学的重点内容,也是中考考查的热点。在实验室如何制取二氧化碳呢?实验中都有哪些注意事项呢?下面加以归纳。
[夯实基础]
1.实验药品:稀盐酸和大理石(或石灰石)。
2.反应原理:CaCO3 + 2HCl [ ] CaCl2 + H2O + CO2↑。
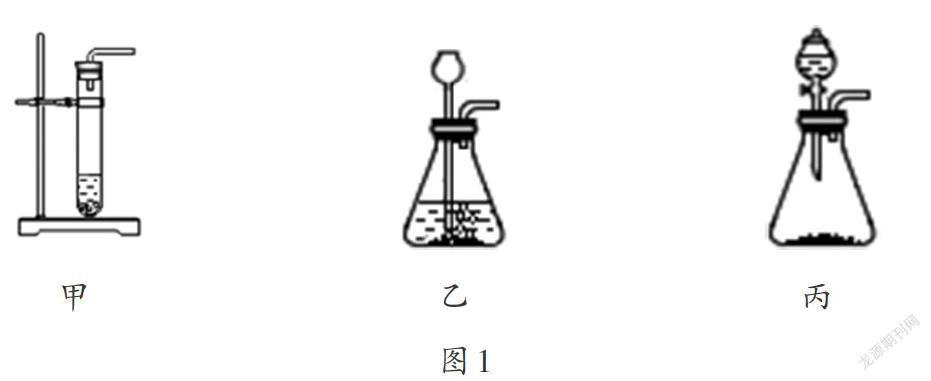
3.發生装置:如图1中的三组装置均可作为实验室制取二氧化碳的发生装置。
(1)选择依据:反应物状态和反应条件;
(2)各装置特点:
图1甲装置简单,但不便于添加稀盐酸;
图1乙装置便于添加稀盐酸,长颈漏斗的下端管口应伸到液面以下,防止二氧化碳从长颈漏斗逸出;
图1丙装置使用了分液漏斗,便于添加稀盐酸,还可以通过控制滴加液体药品的速率来控制反应速率;
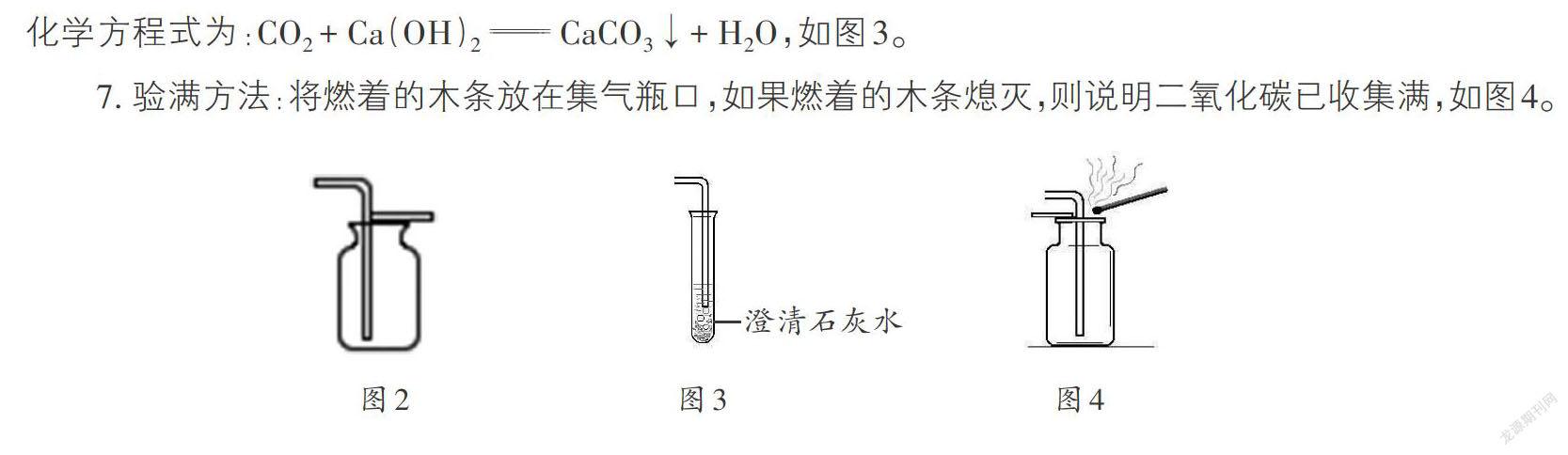
4. 收集装置:二氧化碳是一种能溶于水且与水反应、密度比空气大的气体,故应采用向上排空气法收集,如图2。
5. 操作步骤:连(连接仪器)→查(查气密性)→装(装药品)→收(收集气体)→验(验满)。
6. 检验方法:将生成的气体通入澄清石灰水中,如果澄清石灰水变浑浊,则证明气体是二氧化碳,化学方程式为:CO2 + Ca(OH)2 [ ] CaCO3↓+ H2O,如图3。
7. 验满方法:将燃着的木条放在集气瓶口,如果燃着的木条熄灭,则说明二氧化碳已收集满,如图4。
[注意事项]
1. 药品的选用:
(1)不能用浓盐酸替代稀盐酸,因为浓盐酸有挥发性,会导致制取的气体不纯,生成的CO2中会混有氯化氢(HCl)气体;
(2)不能用稀硫酸替代稀盐酸,因为稀硫酸与碳酸钙反应生成的硫酸钙微溶于水,会覆盖在大理石的表面,阻碍反应的进行;
(3)不能用纯碳酸钙或碳酸钠粉末替代大理石或石灰石,因为它们与稀盐酸反应速率太快,不利于控制反应的速率及气体的收集;
2.药品的取用:
要用镊子夹取石灰石或大理石,在装入锥形瓶或大试管等时,要注意“一横、二放、三慢竖”。
3. 制取装置:
(1)在使用长颈漏斗时,长颈漏斗的下端管口应伸到液面以下,防止二氧化碳从长颈漏斗逸出,这样就起到了液封的作用;
(2)导气管不要伸入容器太长,更不能伸入液面以下,只需露出橡胶塞少许即可,以便导出气体;
(3)收集气体的导管应伸到集气瓶底部,以利于收集到较纯净的气体。
4. 检验气体:
不能用燃着的木条检验收集的气体是否为二氧化碳,因为能使燃着的木条熄灭的气体不一定是二氧化碳,还可能是氮气等。
[实战演练]
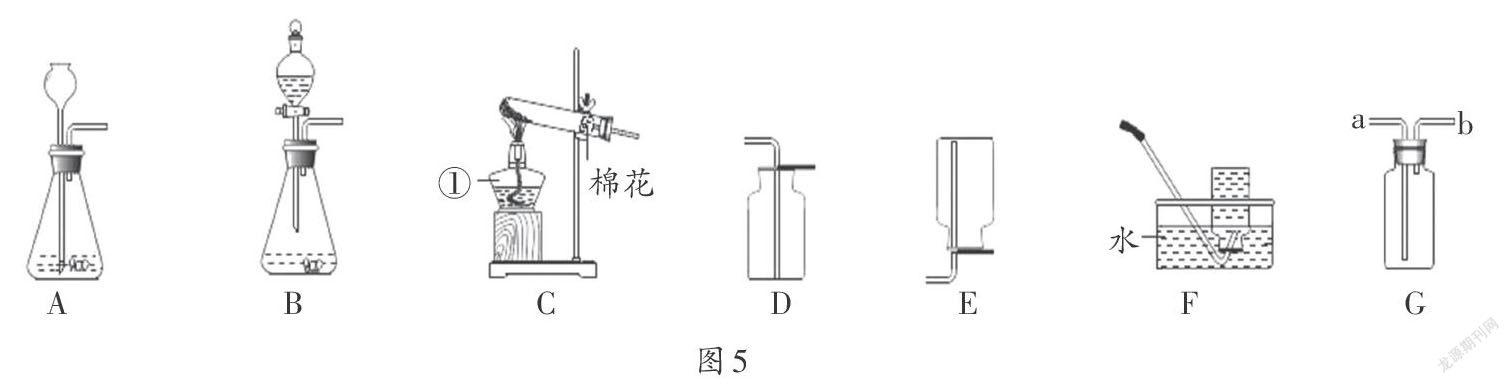
请你根据所学知识并结合图5所示装置,回答下列问题。
(1)指出标号仪器的名称:① ;
(2)实验室制取二氧化碳药品是 ,其反应的化学方程式为 ,实验开始之前应先 ,然后再加药品,且先加 ,再加 。
(3)A装置中长颈漏斗必须伸入液面以下的原因是 ;
(4)装置A与B都能用于制取二氧化碳气体,你认为装置B的优势是 ;
(5)用D装置收集二氧化碳时,检验气体收集满的方法是 。欲制得干燥的二氧化碳,还需将气体通过盛有 (填药品名称)的洗气瓶G;集满二氧化碳的集气瓶应 (填“正”或“倒”)放在桌面上。若用G装置收集二氧化碳,应从 (填“a”或“b”)通入。
答案:(1)酒精灯 (2)稀盐酸和大理石(石灰石) CaCO3 + 2HCl [ ] CaCl2 + H2O + CO2↑ 检查装置的气密性 固体药品 液体药品 (3)防止气体从长颈漏斗逸出 (4)便于添加稀盐酸,还可以控制反应的速率 (5)用燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳收集满 浓硫酸 正 a

