蜂蜜中氯霉素残留基体标准物质的研制
施海燕 宋美洁 赵玲玲 齐素贞 吴黎明 薛晓锋
(1 中国农业科学院蜜蜂研究所,北京 100093;2 北京百花蜂业科技发展股份公司,北京 100176)
氯霉素是从微生物代谢物中分离的一种广谱抗生素,目前通过人工合成已广泛用于动物各种传染性疾病的治疗。但是氯霉素有较强的毒副作用,它能抑制人体骨髓造血功能而引起再生障碍性贫血症和粒状白细胞缺乏症等疾病,因此动物食品中的氯霉素残留对人类健康构成了潜在危害[1]。联合国粮农组织于1994年决定禁止使用氯霉素,许多国家禁止此药用于生产食品动物,并规定了其在畜产品中最高限量。其中,各国对蜂蜜中氯霉素的残留限量作了严格规定,如美国0.3μg/kg、日本5μg/kg、加拿大1μg/kg及欧盟0.1μg/kg[2]。我国农业农村部公告第250号《动物性食品中兽药最高残留限量》规定氯霉素在蜂蜜中不得检出。氯霉素残留检测已经成为进出口蜂产品的重点监测指标[3,4],保证氯霉素残留检测结果的准确、可靠,对于提高监管机构执法能力和保障企业的合法利益具有重要的意义。
基体标准物质是分析技术重要的技术物质保障。加快农业领域基体标准物质研发,是提高农业科技创新能力、促进农业高质量发展和增强我国农产品市场竞争力的必然要求。基体标准物质在保证分析方法的准确性及可溯源性方面具有重要作用[5]。在日常的检测工作中,检测人员经常通过人为添加药物到基体中形成一个“阳性”样品,并通过测定回收率来评判方法和检测结果的可靠性。然而,药物在生物体内代谢复杂,结合形式多样,在提取方法、提取溶剂的使用方面同人为添加药物残留的检测不同,因此,人为添加的样品不一定真实反映药物在基体的实际情况,不能完全保证检测结果真实可靠[6]。自然基体标准物质要求其候选材料获取于天然基体,目标物和基体结合情形与真实检测样品完全一致,可有效避免基体效应对物质成分分析的影响。
我国已有多种食品分析用基体标准物质,已经广泛应用于各类食品的实验室能力考核、检测机构能力比对、企业实验室的数据质量控制等[7]。但关于蜂蜜基体标物研究较少,仅有蜂蜜中磺胺和羟甲基糠醛的基体标物有报道,目前尚未见蜂蜜中氯霉素基体标准物质的研制报道。本文以洋槐蜂蜜为基体,通过实际的蜂场饲喂方式,研制了蜂蜜中的氯霉素残留基体标准物质。
1 实验部分
1.1 仪器和试剂
Aglient 1260液相色谱(美国Aglient公司);AglientUltivo Tripe Auad MS 6465B(美国Aglient公司);METTLER XS105十万分之一天平,METTLER AL104万分之一天平,50ml、25ml棕色容量瓶(均为A级),10ml棕色容量瓶(B级),2.0ml单标线吸量管(A级),1000μl可调移液器(最大允许误差为1.0%)、100μl可调移液器(最大允许误差为2.0%)均已通过北京市计量检测科学研究院校准和检定;高速冷冻离心机(美国Thermo公司);Vortex-Genie 2型涡旋混合器(美国Scientific Industries公司);BAKERBOND固相萃取仪(美国Waters公司);水浴氮吹仪(美国Organomation公司,N-EVAPTM 111,OA-SYSTM水浴加热装置)。
甲醇、乙腈、乙酸乙酯、氨水(LC-MS级别,美国Fisher公司);甲酸(LC-MS级别,德国Sigma公司);实验室用水为经Milli-Q净水系统(0.22μm过滤膜)过滤的去离子水;氯霉素购自中国农科院质量标准研究所,为国家二级标准物质,编号GBW(E)082557,标准值100mg/l,不确定度3mg/l(k=2);氯霉素标记标准品(D5-氯霉素)纯度为100mg/l,德国Dr.Ehrenstorfer公司。SPE萃取小柱:Oasis HLB柱(6ml 200mg,美国Waters公司)。Bond ElutQuEChERS试剂盒(型号:5982-0032)及QuEChERS d-SPE EMR-lipid(part no.5982-5158)均购于安捷伦科技有限公司(Santa Clara,USA)。
1.2 氯霉素阳性样品的制备
选取两个蜂场,取18kg洋槐蜂蜜,人工加入2kg果糖混合进一步调节葡萄糖和果糖的比例,防止蜂蜜结晶。饲喂该添加果糖的蜂蜜样品获得空白样品;再通过添加1μg/kg的氯霉素药物于该饲喂的蜂蜜混合物中,饲喂蜜蜂一周后,取部分样品经初步测试,作为样品的基体标物候选物。
1.3 样品的分析方法
1.3.1 样品的前处理方法
蜂蜜基体标准物质解冻后震荡均匀,准确称取5.0g(精确至0.1mg)于50ml塑料离心管中,按照标准曲线中添加的内标浓度,准确量取200μg/kg的氯霉素-D5溶液23.0mg(约25μl,准确记录天平质量),涡旋30s后4℃平衡1h。
提取与净化:在离心管中加入5ml水,涡旋震荡混匀1min;再加入10ml 1%氨水乙腈溶液(V/V)提取,涡旋提取1min;加入Agilent 5982-0032盐包一袋,涡旋混匀2min,4℃ 8000r/min离心5min;取6ml上层提取液加入Agilent 5982-5158净化包中,涡旋净化1min,4℃ 8000r/min离心5min;取上层净化液2ml,氮气吹干,最后加入准确称取的50%乙腈水溶液1.0g,充分溶解,溶解液过0.22μm滤膜,上机。
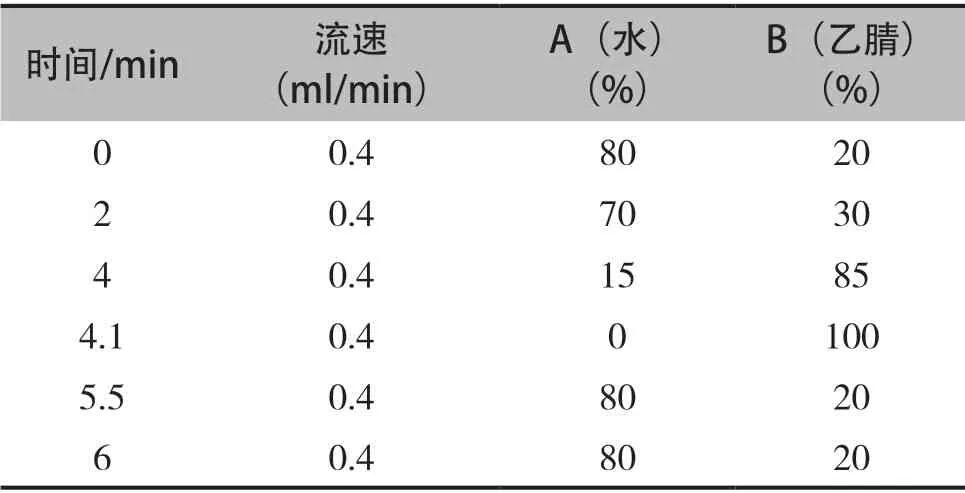
表1 液相色谱洗脱程序
1.3.2 仪器分析条件
液相色谱条件:Agilent ZORBAX Eclipse Plus C18(2.1×50mm,1.8μm)色谱柱;流动相A为水,流动相B为乙腈。温度:40℃。优化洗脱程序,确定梯度洗脱程序如表1所示。
质谱条件:AJS ESI离子源负离子模式,多反应离子监测(MRM);电离电压:3500V;雾化器和碰撞气:氮气;雾化器温度:300℃;雾化器流速:6l/min;雾化器压力40psi;气帘气流速:12l/min;气帘气温度:350℃;定量离子对信息如表2所示。
1.4 样品的均匀性和稳定性检验
1.4.1 均匀性检验
根据《一级标准物质技术规范》(JJF 1006-1994)和《标准物质定值的通用原则及统计学原理的要求》(JJF 1343-2012),对标准物质进行均匀性检验。记总体单元数为N,当N≤200时,抽样单元数不少于11个。从标准物质的包装中随机抽取11个包装,记录编号为CAP-X(X为1,2,3,…),每个包装样品测定3个子样,每个子样中最小取样量为5.0g,平行测定3次。按照液相色谱同位素稀释质谱法进行测试并对测量的数据进行方差分析(具体方法及参数见标准物质定值部分)。方差分析法是用来统计检验均匀性最常用的方法,通过组间方差和组内方差的比较来判断不同包装单元蜂蜜中氯霉素含量的测量值之间有无系统性差异。如果二者的比小于统计检验的临界值,则认为样品是均匀的。
1.4.2 稳定性检验
稳定性是标准物质的基本属性,用于描述标准物质的特性量值随时间变化的性质,即描述标准物质特性的时间分布特征。为考察蜂蜜中氯霉素基体标准物质在长期储存条件以及外部环境变化条件影响下,物质物理化学性质和特性量值保持不变的能力,本研究根据JJF 1343-2012《标准物质定值的通用原则及统计学原理》的要求,采用直线拟合法对蜂蜜中氯霉素基体标准物质的量值开展长期和短期的稳定性评估考察。
1.5 样品的定值和不确定评估
1.5.1 定值方法
本项目蜂蜜中氯霉素基体标准物质的研制,采用液相色谱-同位素稀释-串联质谱法作为测量方法,8家实验室联合定值。8家实验室的定值数据经过科克伦检验和格布拉斯检验,数据等精度、无界外值,可保留并参与最终定值。
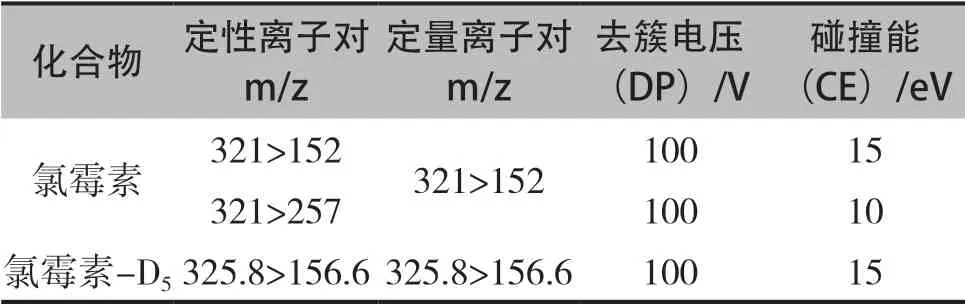
表2 氯霉素及其内标物MRM离子对信息

表3 洋槐蜂蜜原料的基本理化指标
1.5.2 不确定评估
蜂蜜中氯霉素基体标准物质研制过程中引入的不确定度来源主要由3部分组成:标准物质的均匀性引入的不确定度、标准物质长期稳定性和短期稳定性引入的不确定度和、标准物质定值引入的不确定度。
2 结果与讨论
2.1 基体标物材料的制备
根据已有研究及不同品种蜂蜜的性质,当果糖和葡萄糖比例(果葡比)大于1.3∶1时,蜂蜜不易结晶[8]。由于洋槐蜂蜜富含果糖且在长期保存过程中稳定不易结晶,杂质少且质地均匀,更适宜作为基体标物的原料。因此,本研究取洋槐蜜作为基体,通过饲喂意大利蜂种蜜蜂以获得含有氯霉素药物残留的蜂蜜基体样品。
选择符合监测浓度的样品(与市场上监测的氯霉素阳性样本平均含量接近)经过摇蜜、过滤、均质、混匀等一系列工艺过程,得到约3500g的蜂蜜样本。获取的洋槐蜜的各项基本理化指标参数如下表3所示。
将获得的蜂蜜基体原料通过初步测试,其不易结晶,容易均质均匀。通过蜂蜜均质分装仪用铝袋真空分装并封口,得到200单元每袋约15g的基体标物样本,于-20℃冷冻条件下储存,进行后续的标物均匀性、稳定性和定值等。
2.2 均匀性检验
氯霉素蜂蜜基体标准物质的均匀性检验结果见表4。
上述实验数据表明,蜂蜜中氯霉素特性量值均通过F检验,表明基体标准物质均匀性良好,满足技术规范要求。
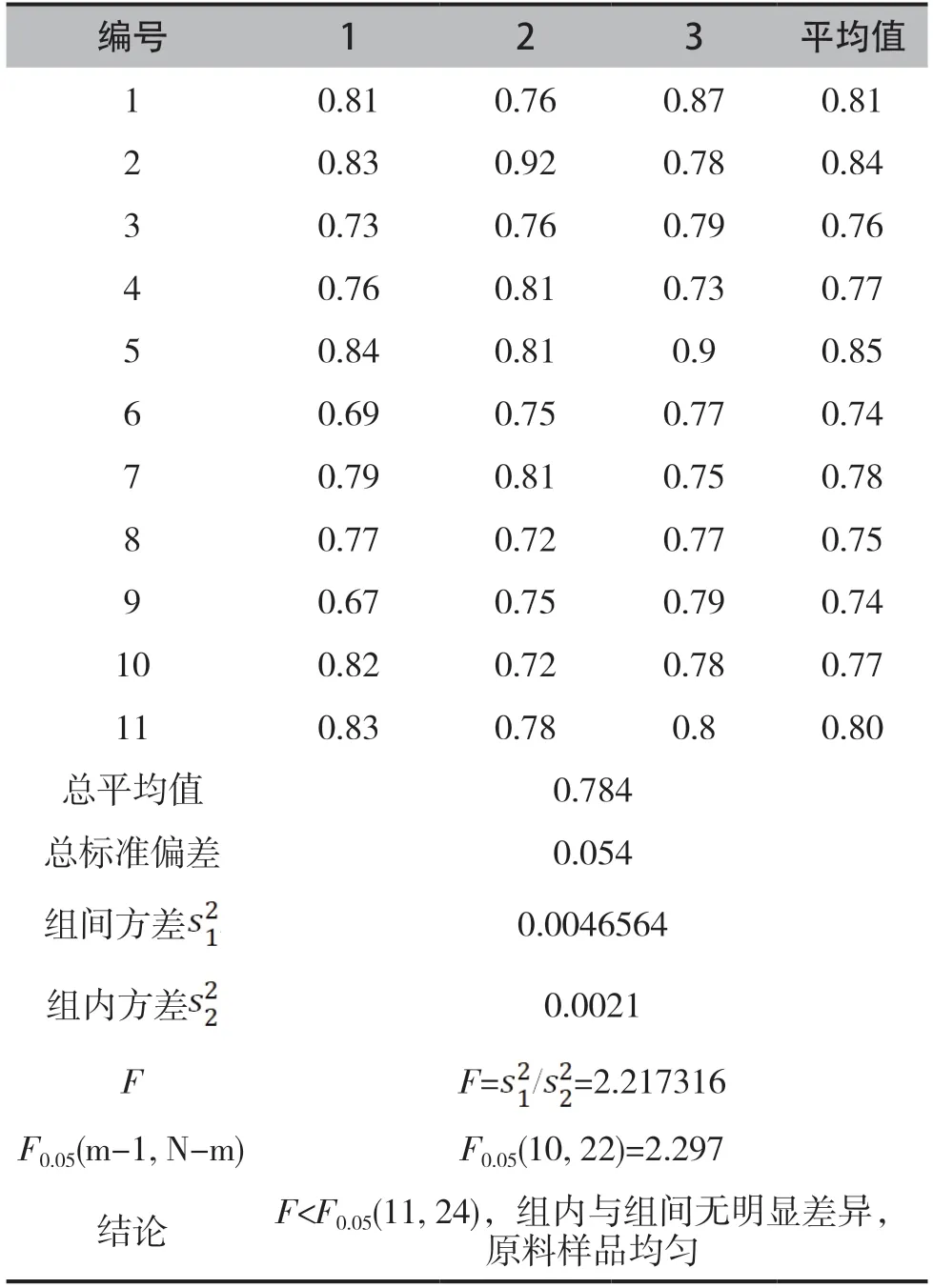
表4 蜂蜜中氯霉素基体标准物质的均匀性检验结果(µg/kg,n=3)
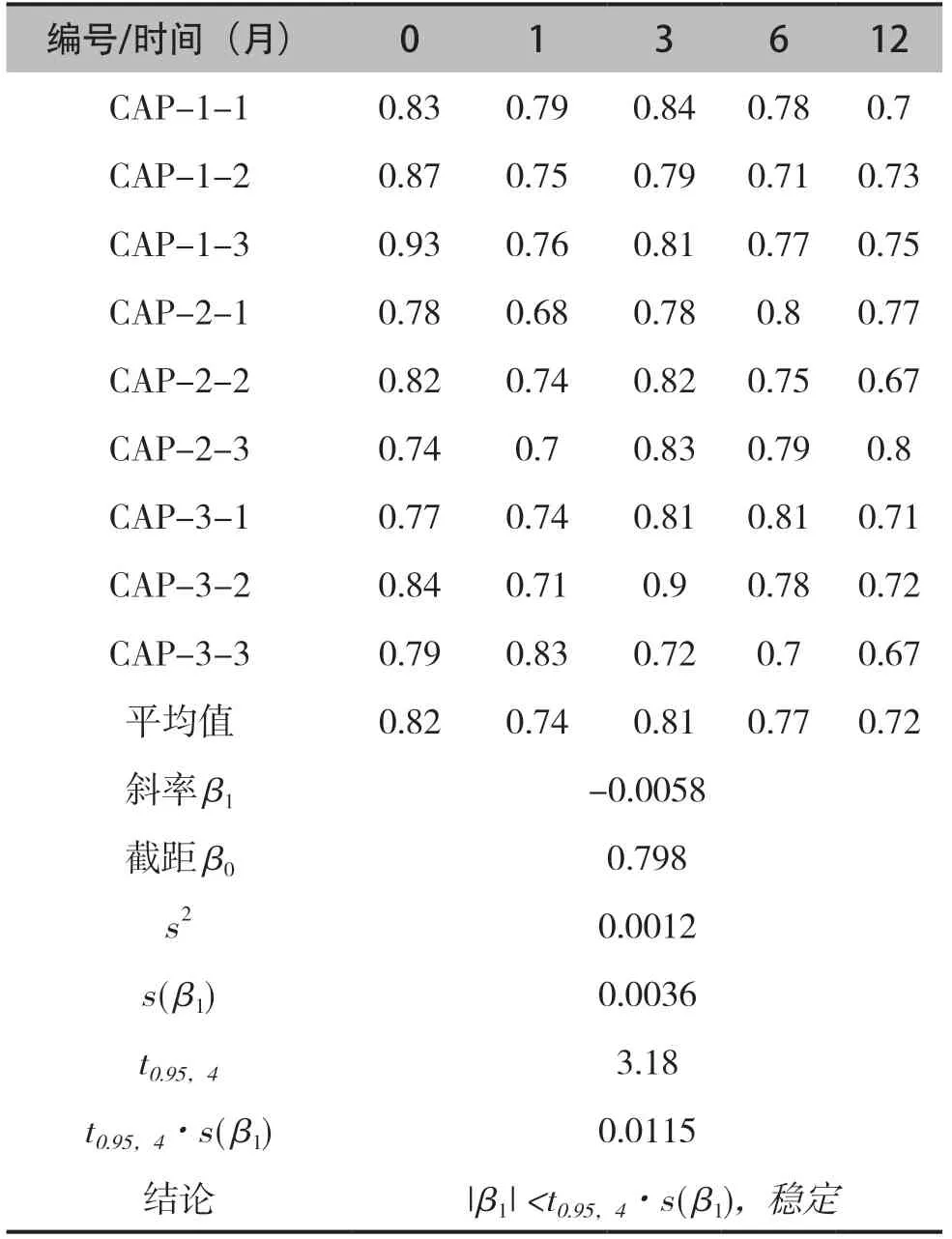
表5 蜂蜜中氯霉素基体标准物质的长期稳定性监测结果(µg/l)
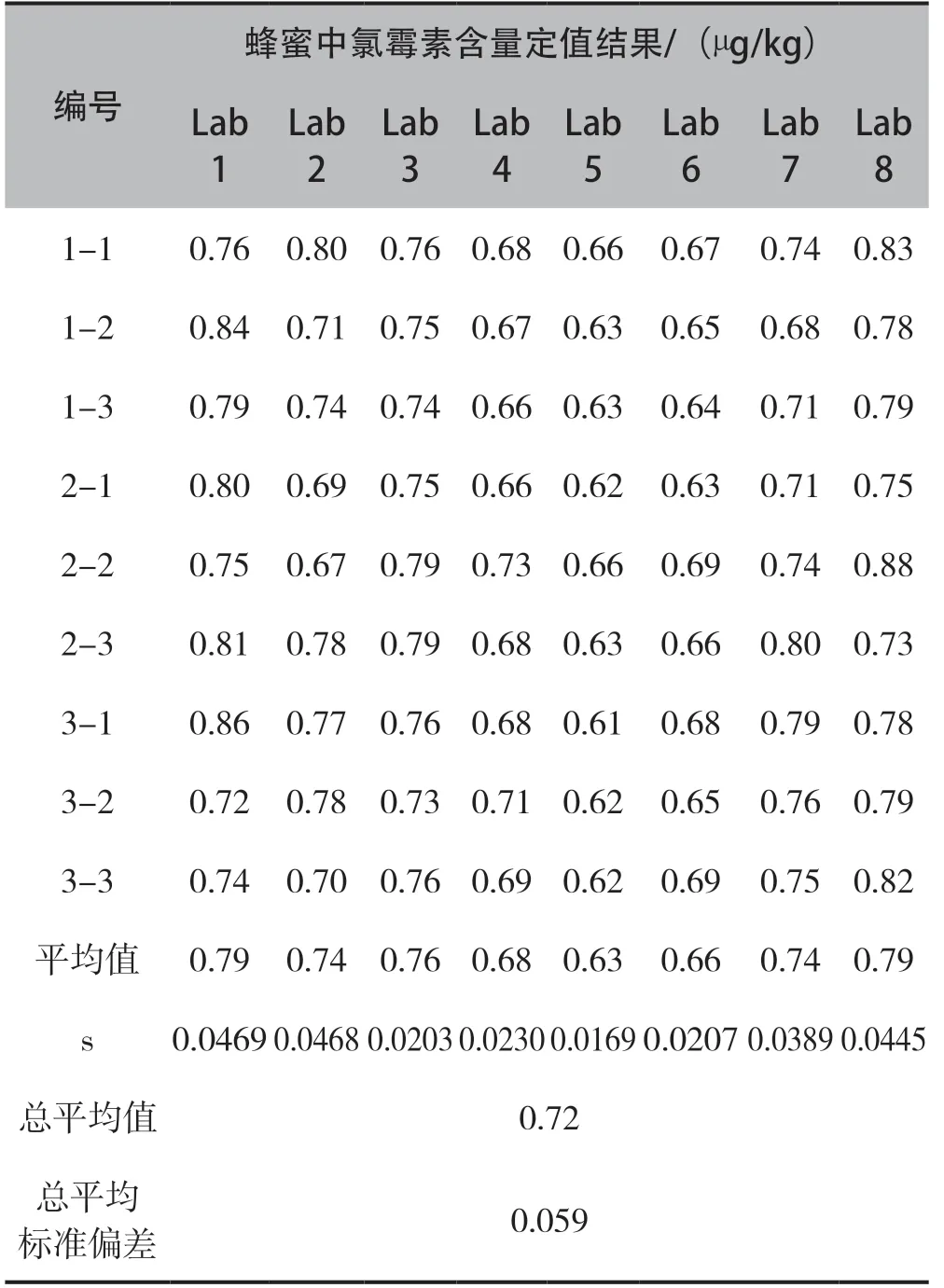
表6 蜂蜜中氯霉素基体标准物质多家合作定值结果
2.3 稳定性检验
将分装的标准物质置于冰箱-20℃冷冻条件下保存,从2018年8月开始到2019年8月,本标准物质已进行了12个月的稳定性考察,考察结果显示在该包装储存条件下,标准物质在12个月内是稳定的,结果见表5。
采用趋势分析对监测数据进行考察,4℃、20℃(常温)和40℃条件下氯霉素浓度可保持14天无明显变化,在3种不同温度条件下氯霉素浓度标准偏差无明显差别,因此,本基体标准物质对运输过程中温度要求并不严格,可以在低于40℃条件下短期运输。
2.4 定值与不确定评估
2.4.1 联合定值
根据JJF 1006-1994一级标准物质技术规范要求,针对一级标准物质定值可采用两种不同原理的方法同时定值,或者采用一种方法多家实验室联合定值的方式。国际物质量咨询委员会(CCQM)将同位素稀释质谱法(IDMS)定位于具有绝对测量性质的方法,IDMS方法是唯一公认的痕量和超痕量分析权威测量方法[9]。然而,复杂基体标准物质一般难以满足两种不同原理方法同时定值,通常采用国际计量领域公认的、权威的绝对测量方法——IDMS结合多家实验室联合定值的方式[10]。另外,同位素内标法可以减少仪器及样品提取率等一系列误差和基质干扰。因此,本实验室采用建立的高准确度的IDMS方法对蜂蜜中的氯霉素进行定值测定,定值结果由国内8家检测实验室验证。
8家实验室的定值数据经过科克伦检验和格布拉斯检验,数据等精度、无界外值,可保留并参与最终定值,结果见表6。
根据《GB/T 4883-2008数据的统计处理和解释-正态样本离群值的判断和处理》,首先采用狄克逊准则对各实验室定值数据进行统计检验,将定值结果按照由小到大的顺序排列:
x(1)=0.61,x(2)=0.62,x(3)=0.62,
……
x(n-2)=0.84,x(n-1)=0.86,x(n)=0.88
又因为
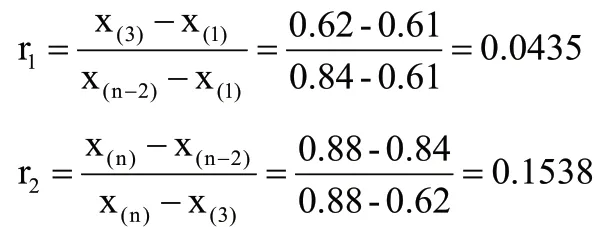
同时,8家实验室均采用同位素稀释液相色谱质谱方法作为定值方法,可以认为属于同等精度方法。从这一点出发,进一步采用科克伦(Cochran)准则判断这8组数据有无哪一组是可疑数据,按照标准,这里n取多数实验室的测量次数9。
根据科克伦准则,计算统计量:
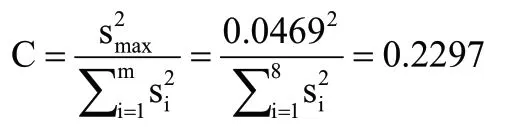
查表得C(0.05,8,8)=0.3043,则C<C(0.05,8,3),判断无可疑数据。经过狄克逊和科克伦检验,数据等精度、无界外值,均符合定值要求。因此,蜂蜜氯霉素标准物质的特性量为多家联合定值结果平均值0.72mg/kg。
2.4.2 不确定评估
蜂蜜中氯霉素的基体标准物质定值结果的不确定度是由均匀性、稳定性和定值引入的不确定度3部分组成,标准物质的合成相对不确定度计算结果如下:即
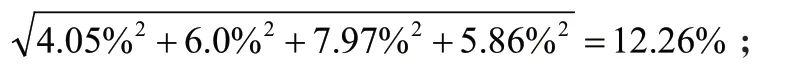
k=2时的相对扩展不确定度:
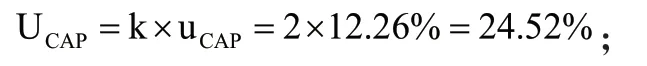
3 结论
本研究通过蜂场饲喂给药方式获得了适合浓度的氯霉素自然污染的阳性样品。采用同位素稀释质谱法和多家实验室联合定值的方式,制备了蜂蜜氯霉素残留基体标准物质。所获得的氯霉素基体标物,量值可靠,均匀性和稳定性良好。可以用于实验室蜂蜜中氯霉素残留检测能力比对、实验室数据质量控制以及进出口企业原料蜂蜜中氯霉素残留检测的质控样品。本项目研究的蜂蜜基体标物对进一步开展蜂蜜中的各类残留基体标物的研制具有参考价值。

