唑来膦酸联合89SrCl2 治疗前列腺癌骨转移的Meta 分析
马平川, 程光华*, 储昭阳
(1. 皖南医学院弋矶山医院核医学科, 安徽 芜湖241001; 2. 超声医学科)
前列腺癌是导致男性罹患癌症而死亡的常见原因[1], 目前我国前列腺癌发病率呈现出逐年上升的态势。 晚期前列腺癌容易转移至骨骼, 其发生率可高达70%, 由此所带来一系列临床症状,严重降低了患者的生存质量[2]。 姑息性治疗是当前前列腺肿瘤骨转移的主要治疗方法, 旨在缓解患者的骨痛及预防骨相关事件(SREs) 的发生发展[3]。 唑来膦酸作为较新一代的双磷酸盐类药物,被广泛应用于骨转移患者SREs 的防治[4]。89SrCl2(氯化锶) 是治疗性放射性核素的典型代表, 可以释放β 射线用于前列腺癌等恶性肿瘤骨转移的治疗, 持久有效地缓解疼痛[5-6]。 两者虽然发挥作用的药理机制不同, 但皆在骨转移治疗上获得了较为广泛的认可。 目前临床上以单独使用唑来膦酸或89SrCl2治疗骨转移居多, 关于两者联用的临床效果和安全性的观点并不统一, 而且对于单一肿瘤的研究也相对不多, 笔者期望通过Meta 分析来系统评价与讨论唑来膦酸联合89SrCl2治疗前列腺癌骨转移的疗效与安全性。
1 资料与方法
1.1 纳入标准与排除标准 纳入标准: (1) 研究类型: 唑来膦酸联合89SrCl2治疗前列腺癌骨转移的随机对照试验(RCT), 语言限定为中英文文献,对于重复发表的研究, 纳入数据较新或较完全的一篇。 (2) 研究对象: 通过临床及病理确诊为前列腺癌骨转移的患者。 (3) 干预措施: 试验组接受唑来膦酸联合89SrCl2联合治疗, 对照组接受唑来膦酸及89SrCl2其中一种或是两者其中之一联合其他治疗方法, 并且2 组的其他治疗方法必须相同(也包括相同的药物剂量)。 (4) 结局指标: 骨痛缓解率、 骨转移灶控制率、 5 年总生存期、 毒副反应发生率。
排除标准: (1) 诊断标准、 疗效及安全性的标准不明确; (2) 资料收集的方法不明确; (3)没有原始数据或者数据不完整; (4) 未能获取全文的研究; (5) 回顾性分析、 个案报道及综述类研究; (6) 若纳入的研究是3 组或以上数据, 则只提取本研究相关的数据, 排除其他不相关数据。
1.2 检索策略 计算机分别检索英文及中文数据库,具体包括PubMed、 Web of Science、 Ovid Medline、EMbase、 Cochrane Library、 CNKI、 Wanfang Database、 VIP Database、 CBM, 检索唑来膦酸联合89SrCl2治疗前列腺癌骨转移患者的RCT 研究, 检索起止时间为建库至2020 年3 月止。 中文及英文数据库的检索都采取主题词联合自由词的方式, 英文检索词包括Zoledronic Acid、 Bisphosphonates、Zoledronate、89SrCl2、 Sr-89、89Sr、 strontium chloride、Metastron、 prostate cancer/carcinoma/neoplasm 等,中文检索词包括唑来膦酸、89锶、 氯化锶、 美他特龙、 前列腺癌/前列腺肿瘤、 骨转移等。
1.3 文献筛选、 资料提取及偏倚风险评价 将初步检索的结果导入到EndNoteX8 文献管理软件中,首先剔除重复文献, 再阅读题干和摘要排除无关文献, 最后阅读全文以筛选出符合标准的文献。提取资料包括研究者、 发表时间、 年龄、 分组例数、 干预方法、 治疗剂量及结局指标等。 以上工作交由2 位研究者同时独立进行, 最后将资料汇总整合, 产生分歧处通过双方讨论或交由第3 位研究者裁决解决。 质量学评价采取Cochrane Handbook的风险偏倚评价工具。
1.4 统计学方法 Meta 分析采用RevMan 5.3 软件, 特异危险度(risk difference, RD) 作为评价临床疗效的指标, 相对危险度(risk radio, RR)作为评价毒副反应的效应指标, 风险比(hazard ratio, HR) 作为总生存期的效应指标, 所纳研究之间需要进行异质性检验, 利用P 值及I2判断异质性的大小, 当P>0.1 且I2<50%时采用固定效应模型, 当P<0.1 且I2>50%时, 分析异质性产生的原因, 并选用随机效应模型进行分析。 利用漏斗图分析发表偏倚。 当P<0.05 为有统计学意义。
2 结果
2.1 文献检索结果及基本特征 初步检索了207篇文献, 包括PubMed 36 篇, Embase 5 篇, The Cochrane Library 19 篇, Ovid Medline 12 篇, Web of Science 30 篇, CBM 7 篇, VIP Database 31 篇,CNKI 36 篇, WanFang Database 31 篇, 通过阅读摘要及全文剔除重复、 个案报道、 综述类等不符合条件的文献198 篇, 最终纳入9 篇文献[7-15]。 纳入的文献中共包括735 例患者, 其中试验组351 例,对照组384 例。 各研究均较为详细地描述了研究对象分组的方法及数量, 各研究中试验组及对照组的唑来膦酸、89SrCl2的药物剂量及给药方法基本相同, 患者随访时间大致相仿, 关于结局指标的评价标准大致相同。 纳入研究的基本特征见表1。
2.2 纳入文献的方法学质量评价 除2 篇文献未提到“随机” 外, 剩下的7 篇文献在文中提到“随机”, 5 篇文献设计了具体的随机试验方案(如数字法、 简单随机法等), 9 篇文献均未对盲法、 结果数据的完整性、 选择性报告及其他偏倚来源等情况进行系统的描述。 所纳文献的整体质量不高, 但由于研究者对试验对象的纳入标准及结局评价上都做了较为严格的筛选, 试验结果的可信度较高。 文献的质量评价表见图1。
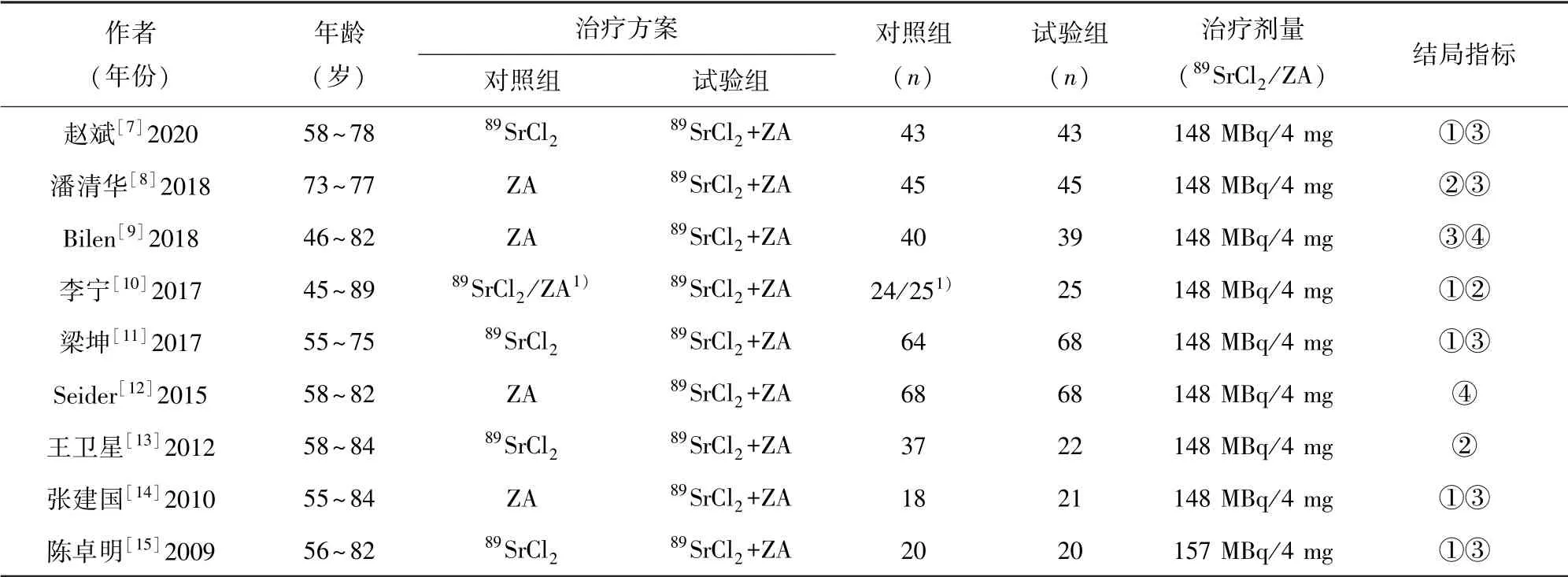
表1 纳入文献基本特征

图1 偏倚风险百分比图及偏倚风险汇总图
2.3 Meta 分析结果
2.3.1 骨痛缓解率 共有5 篇文献报告了骨转移疼痛缓解率, 结果显示各组间均无明显异质性,试验组既比单用唑来膦酸组的骨痛缓解率高(RD=0.17, 95%CI: 0.01 ~0.32, P<0.05) (图2),又比单用89SrCl2组骨痛缓解率高 (RD =0.14,95%CI: 0.05~0.23, P<0.01) (图3)。
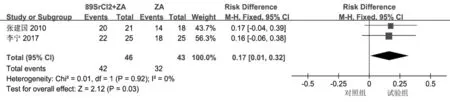
图2 试验组与单用唑来膦酸组骨痛缓解率比较的森林图

图3 试验组与单用89SrCl2组骨痛缓解率比较的森林图
2.3.2 骨转移灶控制率 共有3 篇文献报告了骨转移灶控制率, 由于各组间异质性较高, 采用随机效应模型进行分析。 结果显示, 试验组比单用唑来膦酸组的骨转移灶控制率高 (RD =0.31,95%CI: 0.07~0.54, P<0.05) (图4), 也要比单用89SrCl2组高(RD =0.25, 95%CI: 0.02 ~0.49,P<0.05) (图5)。
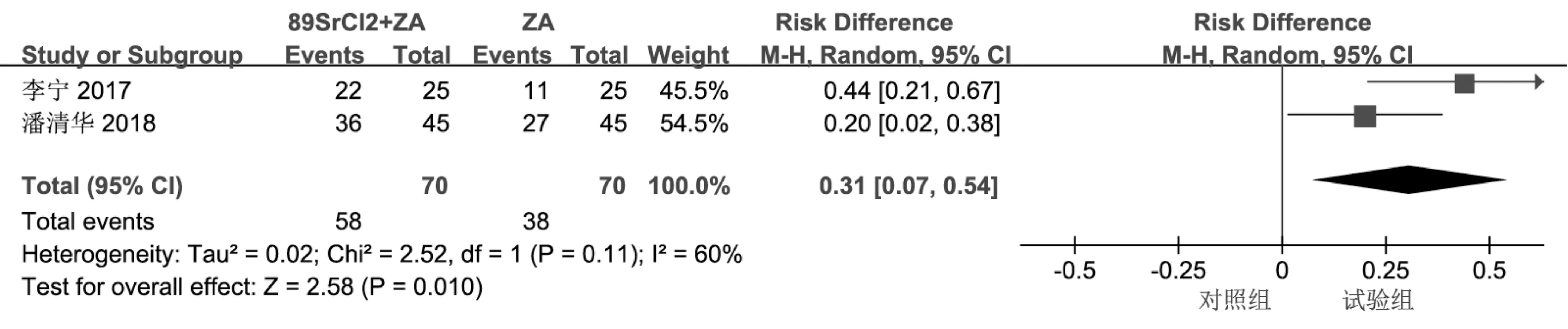
图4 试验组与单用唑来膦酸组骨转移灶控制率比较的森林图
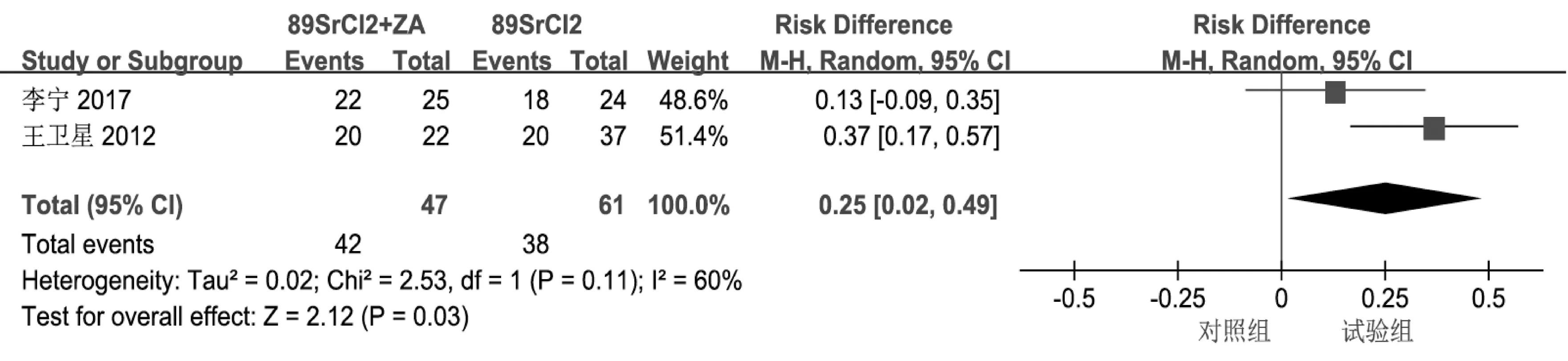
图5 试验组与单用89SrCl2组骨转移灶控制率比较的森林图
2.3.3 5 年总生存期 2 篇文献在试验组与单用唑来膦酸组的研究中比较了患者5 年总生存期的情况, 组间无显著异质性, 合并结果显示, 试验组与单用唑来膦酸组在5 年总生存期上差异无统计学意义(HR =1.01, 95%CI: 0.74 ~1.38, P >0.05) (图6)。
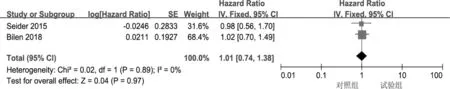
图6 试验组与单用唑来膦酸组5 年总生存期比较的森林图
2.3.4 毒副反应发生率 共有6 篇文献报道了毒副反应的发生率。 在试验组与单用唑来膦酸组的研究中, 3 篇文献对全身症状及胃肠道症状做了比较。 在试验组与单用89SrCl2的研究中, 3 篇文献还对血液及骨髓系统毒副反应进行了比较。 各组间均无明显异质性, 亚组及合并分析结果显示, 试验组与单用唑来膦酸组或单用89SrCl2组的毒副反应(仅包括全身、 胃肠道症状和血液及骨髓系统的毒副反应) 发生率的差异无统计学意义(P>0.05)(图7 和8)。
2.4 敏感性及偏倚分析 逐一剔除各组间的单个研究进行敏感性分析, 结果显示Meta 分析的结果较为稳定, 骨转移灶控制率在所纳入大多数研究中都有报道, 我们用这个指标来分析发表偏倚,结果显示漏斗图对称性良好, 提示研究结果受到发表偏倚的影响可能较小(图9)。
3 讨论
据报道, 将近70%的晚期前列腺癌患者发生了骨转移[16], 唑来膦酸及89SrCl2作为临床上治疗骨转移的标志性用药得到了较为广泛的认可。 目前研究认为89SrCl2缓解骨转移疼痛的主要机制可能是: (1) 减轻肿瘤体积, 降低受累骨膜和骨髓腔的压力; (2) 辐射生物效应干扰疼痛信号的传导并抑制前列腺素等炎性介质的产生[17], 它还能在癌灶中积蓄发射β 射线, 利用辐射效应杀死骨骼内肿瘤细胞而缩小病灶[18]。 唑来膦酸作为一种破骨细胞的有效抑制剂, 主要通过抑制骨破坏来减轻恶性肿瘤骨转移所致的疼痛等骨相关事件。 临床上常以单独使用这两种药物之一进行治疗居多,关于两者联合应用的研究目前尚少, 其临床效果与安全性未能得到广泛认可。 此外, 大多数研究将罹患多种不同类型肿瘤的患者作为一个整体,而针对单一类型肿瘤(例如前列腺肿瘤、 乳腺肿瘤) 的研究相对较少。
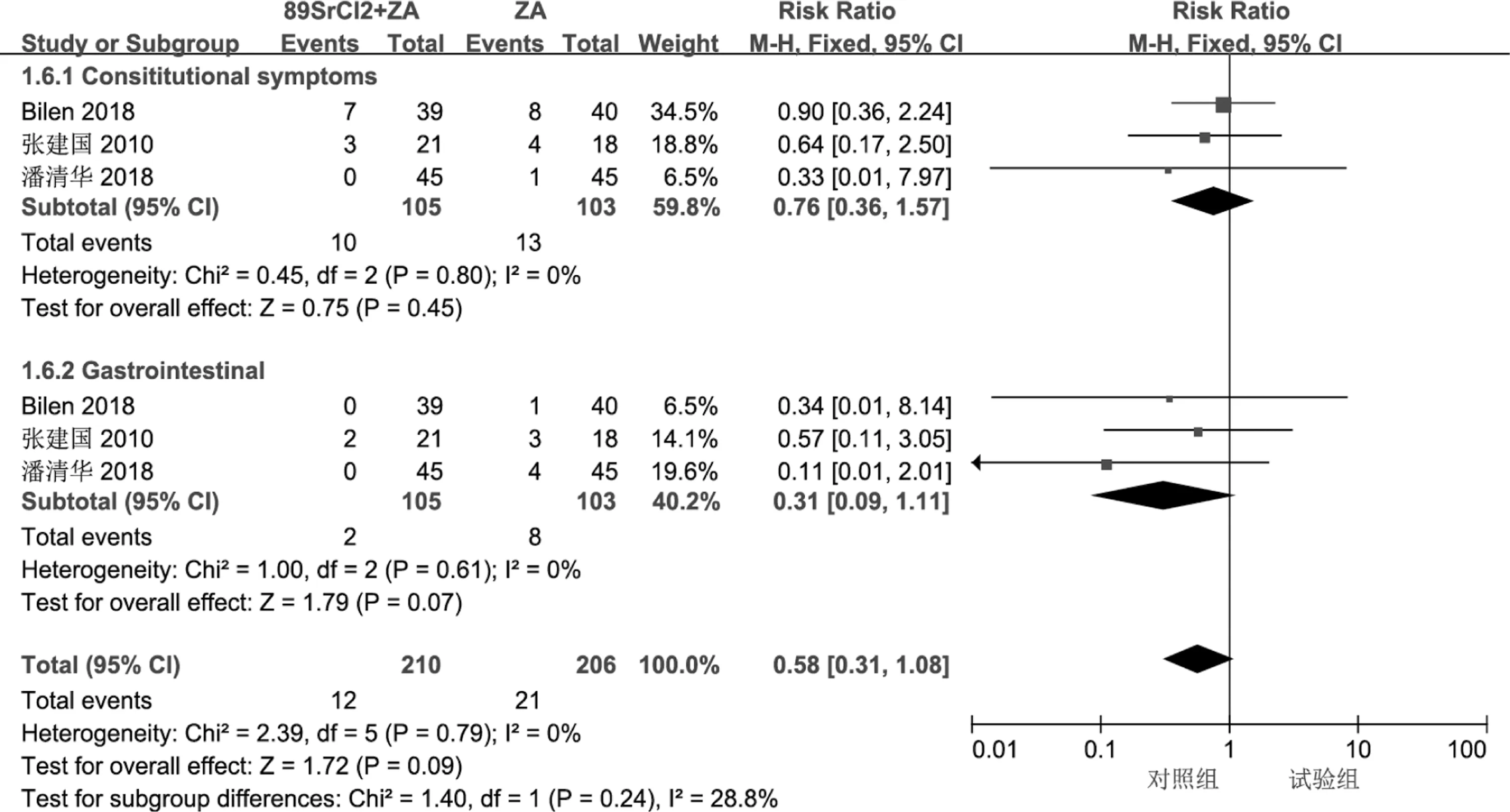
图7 试验组与单用唑来膦酸毒副反应发生率比较的森林图

图8 试验组与单用89SrCl2毒副反应发生率比较的森林图
本研究纳入9 项RCT, 共735 例前列腺癌骨转移的患者。 Meta 分析结果显示, 试验组(联合应用唑来膦酸及89SrCl2) 与单药组(单独使用唑来膦酸或89SrCl2) 相比, 其骨痛缓解率与骨转移灶控制率均显著高于单药组, 提示联合用药的疗效较为确切, 两者结合可以用于治疗前列腺癌骨转移, 这也与张青菊等[19]的观点一致。 虽然联合用药可以改善患者的生活质量, 但本研究发现, 试验组相对于单药组(唑来膦酸) 并未改善患者的5 年总生存期。 本研究分析了几种常见的毒副反应, 与单药组相比, 试验组未增加毒副反应, 且发生的毒副反应都为轻度反应, 患者能够耐受并在一定时间内可自行恢复, 这与Furubayashi 等[20]的报道一致。 我们还对此次研究进行了敏感性及偏倚分析, 结果表明此次Meta 分析的结果具有一定的可靠性。
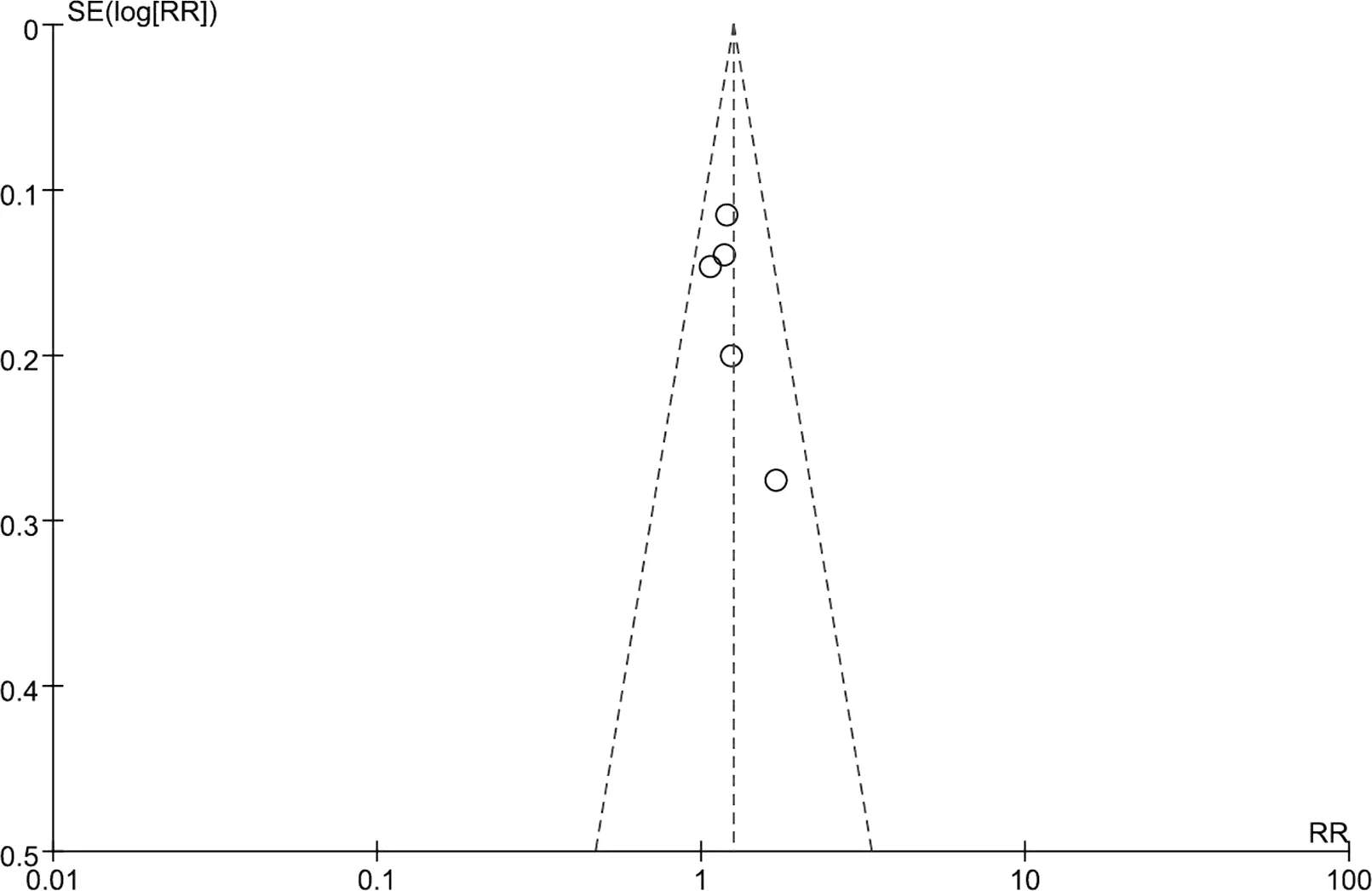
图9 骨转移灶控制率的漏斗图
该系统评价的局限性: (1) 纳入文献中评价骨痛缓解率的指标主要依靠观察者的视觉及患者感觉, 主观性较强; (2) 由于目前关于本文相关问题的研究较少, 纳入文献数量及样本量依旧较少, 加上整体文献质量偏低, 可能会对结果的可靠性产生一定影响; (3) 纳入研究中涉及的毒副反应种类较多, 故不能够做到全方位的分析。 笔者今后会对唑来膦酸联合89SrCl2治疗不同类型的肿瘤的疗效与安全性展开更加细致的研究, 以期为临床治疗发展提供更具体的方案。
综上所述, 唑来膦酸联合89SrCl2治疗前列腺癌骨转移的临床效果较好, 无不良反应的增加。 由于本研究所纳文献质量及数量等方面存在局限性,今后还需要更多大样本量、 高质量及长期随访的RCT 辅以验证。

