高分辨电感耦合等离子体质谱测量氯化锶[89Sr]原料中铝含量
苏冬萍,梁帮宏,罗 婷,张劲松,陈云明,罗 宁,甘 泉,李顺涛,曾俊杰
(中国核动力研究设计院 第一研究所,四川 成都 610005)
氯化锶[89Sr]溶液为转移癌性骨痛的治疗剂,一次给药,止痛时间长,副作用轻微,主要用于前列腺癌、乳腺癌等晚期恶性肿瘤继发骨转移所致骨痛的缓解,是骨转移癌止痛的一种疗法,具有良好的市场前景。生产89Sr主要有两种方法:一是通过88Sr(n,γ)89Sr反应,用热中子照射浓缩88Sr2CO3靶制备89Sr,是国际上通常采用的生产方式;二是通过89Y(n,p)89Sr反应,用天然Y2O3靶制备89Sr。
在88Sr2CO3靶制备89Sr过程中,88Sr2CO3原料、辐照靶管、化学试剂和容器等均可能产生杂质元素铝,氯化锶[89Sr]注射液中的铝含量是重要的质量控制指标。研究表明,脑组织对铝元素有亲和性,脑组织中的铝沉积过多,可使人记忆力减退、智力低下、行动迟钝等。2020版《中国药典》已纳入氯化锶[89Sr]注射液,对产品质量提出了明确要求:氯化锶[89Sr]注射液中铝的含量不得超过2 μg/mL[1]。为了控制注射液中的铝含量,需要严格控制氯化锶[89Sr]原料中的铝含量,一般要求锶[89Sr]原料中铝的含量远低于药典限值。因此,准确测量氯化锶[89Sr]原料中铝含量是控制产品质量和指导生产工艺改进的基础,具有重要意义。
氯化锶[89Sr]原料中锶基体含量高、铝元素含量低,铝和锶的含量相差约4个数量级,测量难度大。2020版《中国药典》规定氯化锶[89Sr]注射液中铝的浓度测量方法为紫外-可见分光光度法,以2 μg/mL的铝标准溶液作为基准溶液进行合格性判定[1]。该方法具有较好的普适性和通用性,操作简单,仪器价格便宜,但具有测量体系复杂、分析速度慢、灵敏度低等缺点,测量结果易受显色温度、时间和样品酸度影响,不能充分满足工艺过程样品快速分析和产品质量高精度定量测定的要求。《欧洲药典》(EP 9.0)和《英国药典》(BP 2016)中采用原子发射光谱法测量注射液中铝含量[2-3],该方法快速准确,但检出限较高,当原料中铝含量较低时可能会低于仪器检出限。《美国药典》(USP 40)中采用原子吸收光谱法[4],该法选择性好、分析速度快,检出限介于原子发射光谱和质谱之间,但标准工作曲线的线性范围窄,铝的原子化温度高,易对石墨炉造成损坏,影响仪器使用寿命。此外,在食品业和农业中,铝的测量也多采用以上三种方法[5-10],个别采用四极杆等离子体质谱法(ICP-MS)[11-14]。高分辨电感耦合等离子体质谱仪(HR-ICP-MS)是一种电场、磁场双聚焦的大型质谱,该仪器价格昂贵、配套实验室和人员要求高,操作较为复杂。但其灵敏度和分辨率高、线性范围宽、干扰少、谱线简单,并可多元素同时测定,在分析微量杂质方面有其独特优势。将HR-ICP-MS应用于氯化锶[89Sr]原料溶液中铝含量测量,有助于在工艺改进和产品质量趋势分析中获得更加准确的数据。针对氯化锶[89Sr]注射液中铝的分析测试,各国药典给出了多种方法,具有较好的适应性和可推广性,便于规模化生产中推广应用。质谱因其昂贵的价格、苛刻的配套实验室要求,并未被列入药典的测量方法,但其优异的微量元素测量能力使其在氯化锶[89Sr]原料溶液中铝含量测量方面有着巨大的应用潜力。与其他方法相比,其分析精密度更高、样品消耗量更小、检出限更低,也更适于高放射性浓度氯化锶[89Sr]原料的测量。
本文研究氯化锶[89Sr]溶液中铝含量测定的样品准备方法,确定质谱条件,研究基体、质谱干扰和本底等影响测量准确性的因素,建立测量流程和方法,以期快速准确测量铝含量,用于氯化锶[89Sr]原料生产工艺改进和产品质量控制。
1 仪器与试剂
1.1 主要仪器
高分辨电感耦合等离子体质谱仪(HR-ICP-MS):Thermo Scientific Element XR,美国热电公司,动态线性范围1012,最高分辨率20 000(FWHM);超纯水装置:Q-POD Element终端精制器,德国默克密理博;器皿:均用10%硝酸浸泡6 h后清洗,超纯水润洗后备用。
1.2 主要试剂
氯化锶[89Sr]原料溶液:热中子照射浓缩88Sr2CO3靶制备的89Sr原料,中国核动力研究设计院产品;调谐液:Tune-Up Solution Element,德国不莱梅Thermo Scientific生产,元素浓度1 μg/L;高纯硝酸:70%(质量浓度),UP-S级,苏州晶瑞化学股份有限公司;药用盐酸:四川合升创展医药有限责任公司;铝标准溶液(浓度为1 000 mg/L)、锶标准溶液(浓度为1 000 mg/L):国家有色金属及电子材料分析测试中心;超纯水:电阻率大于18.2 MΩ·cm,由Q-POD Element终端精制器制备。
2 实验方法
2.1 仪器工作参数
质谱仪开机预热72 h以上,点火。测量调谐液及铝标准溶液,调整仪器参数,在分辨率300(峰谷高度为峰高的10%),检测器计数模式下,实时扫描峰形和峰高,使质谱峰两侧对称、中间平坦,低分辨率下铝灵敏度达2×105s-1/(μg·L-1)以上。然后进行三种检测模式的交叉校正,完成低、中、高三种分辨率下的质量校正,得到优化的仪器工作参数列于表1。

表1 仪器工作参数Table 1 Working parameters of HR-ICP-MS
2.2 溶液制备
2.2.1标准溶液 为避免容量瓶中的铝在酸性条件下溶出,导致配制的铝标准溶液浓度发生变化,每次测量的标准溶液均是现配现用,配制好后转移至洁净的塑料瓶中储存。标准溶液配制过程中的超纯水均由元素终端精制器生产。实验所用铝标准溶液为1 000 mg/L,需多次稀释。首先用移液枪准确移取铝标准溶液500 μL于洁净的100 mL容量瓶中,以0.5%(V/V)高纯硝酸定容至刻度线,得到5 mg/L的铝标准溶液。再将该溶液逐级稀释,以0.5%(V/V)高纯硝酸溶液定容,得到5、10、20、50 、100 μg/L铝标准溶液。
2.2.2样品 将氯化锶[89Sr]溶液用0.5%(V/V)药用盐酸溶液稀释至溶液总溶解固体(TDS)小于1 000 mg/L,控制溶液中铝含量为10 μg/L量级。每个样品至少配制2个平行样,测量时,两个平行样数据相对偏差应小于5%,否则应重新制样测量,直到两个样品平行为止。
2.3 测量
采用中分辨,triple模式进行铝含量测量。钇作为内标,50%峰宽,测量时需确保质谱峰居中,两侧对称。每个样品测量至少6组,每组6次。测量时,样品进样时间大于30 s。先测低浓度样品,再逐一测量高浓度样品。每次测量高浓度样品后需使用0.5%硝酸冲洗仪器2 min以上,避免样品间的交叉污染。
样品分析时,首先测量0.5%(V/V)高纯硝酸和药用盐酸,作为空白样品,测量标准和样品溶液时分别予以扣除。然后再分别测量0、5、10、20、50、100 μg/L铝标准溶液,标准曲线应过零点,R2大于0.999 5,没有明显的异常点,否则应重新配制或测量标准溶液。样品测量时,应实时监测质谱峰,确认质谱峰未明显偏离中心,相对标准偏差应小于2%,否则应重新测量或制样。
3 结果与讨论
3.1 本底及扣除
微量铝含量测量时,水和试剂中的铝本底会使测量结果偏大。特别是稀释倍数较大的样品,铝本底会被放大。为此,测量相关试剂和水的铝本底,减小铝本底影响,并在计算时予以扣除。常用试剂、水和容器中的铝本底测量结果列于表2,从表2结果可知,去离子水、稀盐酸的本底均为每升微克级,因此测量时宜采用超纯水,且待测样品中铝的浓度尽可能控制在10 μg/L以上。容量瓶浸泡后铝含量会增加,因此铝标准溶液现配现用,并尽快转移至塑料容器中。

表2 常用试剂和水中的铝本底Table 2 The background of Al in reagent and water
为了减小微量铝测量的本底影响,在测量时应扣除本底。测量系列铝标准溶液时,测量值应扣除0.5%高纯硝酸本底再拟合标准曲线,所得标准曲线应接近通过原点,若纵坐标截距较大,则本底扣除不准确,需重新测量或制样。样品测量时,应制备流程空白,样品测量值需减去流程空白本底。
3.2 盐酸体系对铝含量测量的影响
用于质谱测量的样品一般采用硝酸体系,有利于减小多原子离子干扰和对仪器的腐蚀。但由于氯化锶[89Sr]溶液是盐酸体系,在生产全流程中统一使用药用盐酸,为了在工艺样品和产品检验过程中不引入新的铝本底污染,提高工艺标准化和生产效率,测量时仍然采用相同的药用盐酸稀释。因此,需评价盐酸体系样品是否对铝含量测量有影响。
分别采用0.5%药用盐酸和0.5%硝酸配制相同浓度的铝溶液,并以相同的质谱参数测量样品中铝含量,对两种体系下铝的计数率进行比较,实验结果列于表3。由表3数据可知,相同浓度的铝在两种酸体系下的计数率一致,表明盐酸体系对铝含量测量无显著影响。采用盐酸体系后,为了减小氯离子对仪器的腐蚀,需控制样品中的盐酸浓度,采用PFA抗酸进样系统替换原有的石英进样系统,将镍锥更换为铂锥。

表3 盐酸和硝酸体系下铝的计数率Table 3 The counting rate of Al in hydrochloric acid and nitric acid
3.3 酸度对铝含量测量的影响
铝是两性金属,当溶液酸度太低时,会形成氢氧化铝胶体,造成溶液不均匀,测量信号波动较大,甚至堵塞进样管路;酸度过高时,又加大了氯离子对仪器的腐蚀。因此,需通过实验优选合适的盐酸浓度。
采用不同浓度的盐酸对样品进行稀释定容,配制的样品中均含有相同浓度的铝,分别测量不同样品中铝的计数率,测量结果列于表4。由表4中数据可知,直接用超纯水稀释定容,铝的计数率略小。0.5%盐酸体系下,铝计数率趋于稳定,样品澄清透明,测量过程中铝计数率稳定,震荡溶液质谱计数率无变化。因此,最终选择0.5%盐酸体系配制样品。

表4 不同酸度时铝的计数率Table 4 The counting rate of Al in different concentration of hydrochloric acid
3.4 锶基体对铝测量的影响
由于质谱离子聚焦系统内的空间电荷效应导致质量歧视,基体离子排斥目标离子,重离子排斥轻离子,从而影响目标离子传输效率,空间电荷效应是电感耦合等离子体质谱基体效应的主要根源,在基体离子的质量大于分析离子时尤为严重。
本次测量的氯化锶[89Sr]原料是由88Sr2CO3辐照产生,因此样品中的主要基体为锶,稀释待测样品中锶的浓度约为100 mg/L量级,铝约为10 μg/L量级,浓度相差约4个量级,部分样品接近5个量级。锶离子质荷比大于铝离子,更加剧了基体效应。为此需研究基体效应对铝测量的影响,并加以修正。配制锶基体浓度不同的系列铝标准溶液,锶浓度分别为0、0.1、1、10、100、1 000 mg/L,系列标准中铝浓度均为20 μg/L。测量铝计数率,结果列于表5。从表5结果可知,锶基体浓度超过10 mg/L后,对测量结果的影响较大,需采用内标法进行修正。

表5 不同锶基体浓度下20 μg/L铝的计数率Table 5 The counting rate of 20 μg/L Al in different strontium concentration
3.5 内标的选择
内标法是用待测元素与内标元素在仪器上对应的信号比来补偿分析信号的波动,能有效降低基体效应和仪器波动的影响,以提高测定的精密度和准确度。根据常用的内标元素选择原则,选择质量数、第一电离能相近的元素,并重点考虑样品中没有的元素,最终选取Sc、Ge、Y、Rh、In、Bi作为备选内标元素开展对比实验。分别配制两份5、50、200 μg/L Al标准溶液,其中一份加入1 g/L锶基体。使用在线内标分别测量无基体和有基体时铝和内标元素的计数率,计算有基体时的信号响应率,实验结果列于表6。从表6中可知,钇(Y)与铝在加入基体后的信号响应率最为接近,钪(Sc)次之。因此,优选钇作为内标元素,修正基体对样品的影响。

表6 锶基体中铝及内标元素的信号响应率Table 6 The response rate of Al and internal standard elements in strontium substrate
3.6 质谱干扰及排除
铝测量的主要质谱干扰列于表7。由表7可知,54Fe++与27Al+质量相差最小,为0.012 u。根据分辨率定义可知,将54Fe++分开要求分辨率大于2 250。因此,仪器设置为分辨率4 000(峰谷高度为峰高10%),可将所有干扰分开。

表7 铝的质谱干扰及质量Table 7 The mass and mass spectrum interference of Al
本实验采用高分辨质谱,其特有的电场和磁场双聚焦分析器具备104的分辨率,可将常见的复合离子、双电荷离子等干扰分开。而常规的四极杆质谱只有约500的分辨率,只能通过碰撞/反应池排除部分干扰,干扰排除能力较弱。因此,高分辨电感耦合等离子体在铝测量时的抗干扰能力强,具有独特优势。
3.7 灵敏度及检出限
HR-ICP-MS分辨率越高,则灵敏度越低,即选择性和灵敏度二者不可兼得。根据优化的质谱条件,在分辨率为4 000时测量铝的灵敏度为1.82×104s-1/(μg·L-1)。
根据检出限定义,对样品制备全流程空白测量11次,3倍标准偏差即为铝测量的检出限。样品测量时,主要为分取、稀释、定容等操作,全流程空白主要基体为0.5%盐酸。测量结果列于表8。从表8中数据可知,方法检出限为39 ng/L,决定测量方法检出限高低的关键因素为流程空白中的铝本底。

表8 方法检出限测量值Table 8 The measured value of detection limits in the established method
3.8 测量结果
根据优化的质谱条件,设置分辨率为4 000,得到铝的标准曲线,如图1所示,R2为0.999 95。从氯化锶[89Sr]原料中移取微升级样品稀释103倍初测浓度,然后根据标准曲线范围和仪器最佳响应范围计算合适的稀释倍数,再次移取适量原料准确定容稀释后上机测量,稀释后样品中铝浓度控制在10 μg/L量级。某批次氯化锶[89Sr]原料测量数据列于表9。从表9中数据可知,原料中铝含量为0.52 μg/mL。若按照《中国药典》2020版的“放射性浓度不小于3.7×107Bq/mL”要求[1]进行等效计算,本批次产品中铝含量为药典要求(2 μg/mL)的1/40,远低于国内外药典指标要求[1-4]。
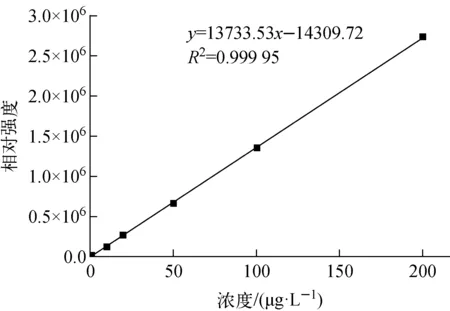
图1 铝标准曲线Fig.1 The standard curve of Al

表9 氯化锶[89Sr]原料中铝含量测量结果Table 9 Result of Al concentration in the raw material of strontium chloride[89Sr]
3.9 不确定度评定
氯化锶[89Sr]溶液中铝含量测量的不确定度分量分别为样品定容、标准溶液配制、标准曲线拟合、测量重复性、试剂空白,其相对不确定度分别为0.05%、0.1%、2%、1%、0.04%,相对扩展不确定度为4.5%(k=2)。
4 结论
以0.5%盐酸体系稀释氯化锶[89Sr]溶液至总溶解固体小于1 g/L,4 000分辨率下,选择钇为内标元素,该方法测量铝的检出限为39 ng/L,测量相对扩展不确定度为4.5%(k=2)。
本研究工作在国内首次开展并成功应用于实际生产,实现了高基体氯化锶[89Sr]原料中的微量铝含量测量。与药典方法相比,本文基于HR-ICP-MS建立的测量方法具有灵敏度高、检出限低、分析速度快、操作简单、样品消耗量小等优点,满足氯化锶[89Sr]原料生产工艺改进和产品质量控制需求,该方法还可应用于88Sr2CO3靶料、氯化锶[89Sr]注射液中铝含量的检验。

