麸炒北苍术饮片粉末的色度值与质量指标的相关性分析及其炮制时间研究
鲁云 洪婉敏 姚晓璇 纪玉华 梁丽金 钟文峰 刘燎原

中圖分类号 R283.1 文献标志码 A 文章编号 1001-0408(2021)21-2605-08
DOI 10.6039/j.issn.1001-0408.2021.21.08
摘 要 目的:分析麸炒北苍术饮片粉末的色度值与质量指标的相关性,并对其炮制时间进行确定。方法:制备16批麸炒北苍术饮片炮制过程样品(S0~S15,S0为北苍术生品),并测定所有样品粉末的色度值[明度值(L*)、黄蓝色值(b*)、红绿色值(a*)];分析样品的超高效液相色谱(UPLC)指纹图谱,并测定其浸出物、挥发油含量。对样品粉末色度值与质量指标(UPLC指纹图谱中各色谱峰的相对峰面积以及水溶性浸出物、醇溶性浸出物、挥发油含量)进行Pearson相关性分析,并以色度值和质量指标进行多元统计分析(主成分分析、聚类分析、偏最小二乘法判别分析),进一步结合灰色关联度法对麸炒北苍术饮片的炮制时间进行确定。结果:北苍术饮片在麸炒过程中,随着炮制时间的延长,饮片粉末的L*、b*呈下降趋势,a*呈先升高后下降的趋势;峰1、峰2的相对峰面积先增加后减少,峰3(5-羟甲基糠醛)的相对峰面积增加,其余色谱峰的相对峰面积均减少;浸出物含量变化不明显,挥发油含量呈一定的下降趋势。相关性分析结果显示,峰2~27的相对峰面积、醇溶性浸出物含量以及挥发油含量与色度值呈一定相关性,峰1的相对峰面积和水溶性浸出物含量与色度值无线性相关关系。多元统计分析结果显示,样品可聚为炮制轻度(S0~S5)、过度(S12~S15)、适度(S6~S11,即炮制时间为18~33 min)3类;灰色关联度法结果显示,麸炒北苍术饮片的炮制时间应控制在18~24 min范围内,且最优炮制时间为18 min。结论:麸炒北苍术饮片粉末的色度值与27个色谱峰的相对峰面积以及浸出物、挥发油的含量具有一定相关性。建议尽量控制炮制时间为18 min。
关键词 麸炒北苍术饮片;指纹图谱;色度值;浸出物;挥发油;相关性;炮制
ABSTRACT OBJECTIVE: To analysis the correlation between chromaticity value and quality index of Atractylodis chinensis decoction piece powder stir-fired with bran, and to determine its processing time. METHODS: The processed samples of 16 batches of A. chinensis decoction piece stir-fired with bran (S0-S15, S0 is the raw product of A. chinensis) were prepared, and chromaticity values of all samples were determined, such as lightness value (L*), yellow blue value (b*), red green value (a*). UPLC fingerprint of sample were analyzed, and the contents of extract and volatile oil were also determined. Pearson correlation was used to analyze the correlation between the chromaticity value and quality index (relative peak area of each chromatographic peak in UPLC fingerprint, water-soluble extract content, alcohol-soluble extract content and volatile oil content). Multivariate statistical analysis (principal component analysis, cluster analysis, partial least squares discriminant analysis) was carried out with chromaticity value and quality index, and the processing time of A. chinensis decoction piece stir-fired with bran was determined by grey correlation method. RESULTS: In the process of bran frying, with the extension of processing time, L* and b* of decoction pieces powder decreased, and a* increased first and then decreased; relative areas of peak 1 and peak 2 increased first and then decreased, while relative areas of peak 3 (5-hydroxymethyl furfural) increased, and the areas of the other peaks decreased. The content of the extract did not change significantly with time, and the content of the volatile oil decreased. The results of correlation analysis showed that the relative peak area of peak 2-27, alcohol-soluble extract content and volatile oil content had a certain correlation with the chromaticity value, while the relative peak area of peak 1 and water-soluble extract content had no linear correlation with the chromaticity value. Results of multivariate statistical analysis showed that the samples were divided into mild (S0-S5), excessive (S12-S15), moderate (S6-S11, processing time of 18-33 min). The results of grey correlation method showed that the processing time of A. chinensis decoction piece stir-fired with bran should be controlled in the range of 18-24 min, and the optimal processing time was 18 min. CONCLUSIONS: There is a correlation between chromaticity value of A. chinensis decoction piece powder stir-fired with bran and the relative peak area of 27 chromatographic peaks, and content of extract and volatile oil. It is suggested that the processing time should be 18 min.
KEYWORDS Atractylodis chinensis decoction piece stir-fired with bran; Fingerprint; Chromaticity value; Extract; Volatile oil; Correlation; Processing
苍术为菊科植物茅苍术Atractylodes lancea (Thunb.)DC.或北苍术Atractylodes chinensis (DC.) Koidz.的干燥根茎[1]。苍术的炮制方法较多,常用的有麸炒法、土炒法、酒制法、醋炒法、姜汁法等[2]。目前在2020年版《中国药典》中主要收载麸炒苍术这一种炮制品[1]。苍术生品辛温,具有燥湿、祛风散寒的作用,用于治疗湿阻中焦、脘腹胀满、泄泻、水肿等症[2]。经麸炒后,苍术性味和化学成分均发生了相应的变化,且其健脾养胃以及保肝作用均增强、燥湿作用减弱,可用于治疗脾胃不和、腹痞满等症[3]。
苍术的化学成分复杂,在麸炒过程中,其表观颜色与内在质量均发生了一定程度的变化,而苍术内在质量的变化可在一定程度上影响其临床治疗效果[4]。随着现代科学技术的不断发展,色差分析仪在传统中药研究中的应用越来越广泛,可实现对中药饮片及其粉末颜色的客观量化[5-7],为中药饮片的炮制程度量化分析及质量控制提供技术支持[8]。基于此,本研究以北苍术为研究对象(由于苍术产地差异以及基原不同等原因[9-10],苍术中所含的成分也存在一定差异,故本研究明确所用苍术药材基原为北苍术),对其炮制过程样品粉末的色度值与质量指标[指纹图谱(前期研究已建立[11])中各色谱峰的相对峰面积、水溶性浸出物含量、醇溶性浸出物含量、揮发油含量]的相关性进行研究,以期为北苍术饮片麸炒过程的质量控制及炮制时间的确定提供参考。
1 材料
1.1 主要仪器
本研究所用主要仪器有H-class型超高效液相色谱(UPLC)仪(美国Waters公司)、KQ-700DE型数控超声波清洗器(昆山市超声仪器有限公司)、Milli-Q Direct型超纯水系统(美国Merck公司)、ME204E型万分之一天平(瑞士Mettler-Toledo公司)、DHG-9147A型电热恒温干燥箱(上海精宏实验设备有限公司)、ARB52B+型红外测温仪(东莞万创电子制品有限公司)、HP-C220型精密色差仪(深圳汉谱光彩科技有限公司)、HK-168型中药切片机(广州赛豪机械设备有限公司)、CZ40型超导电加热炒药机(北京霍氏机械制造有限公司)。
1.2 主要药品与试剂
本研究所用5-羟甲基糠醛(5-HMF,批号111626- 201912,纯度99.2%)、绿原酸(批号110753-201817,纯度96.8%)、咖啡酸(批号110885-201703,纯度99.9%)、阿魏酸(批号110771-201915,纯度97.7%)、苍术素(批号111924-201605,纯度99.8%)的对照品均购自中国食品药品检定研究院;甲醇为分析纯,甲酸为色谱纯,其余试剂为实验室常用规格,水为纯净水。
北苍术药材均购自哈尔滨福顺堂药材有限公司,经广东一方制药有限公司魏梅主任药师鉴定为菊科植物北苍术A. chinensis(DC.)Koidz.的干燥根茎。
2 方法与结果
2.1 麸炒北苍术饮片炮制过程样品的制备
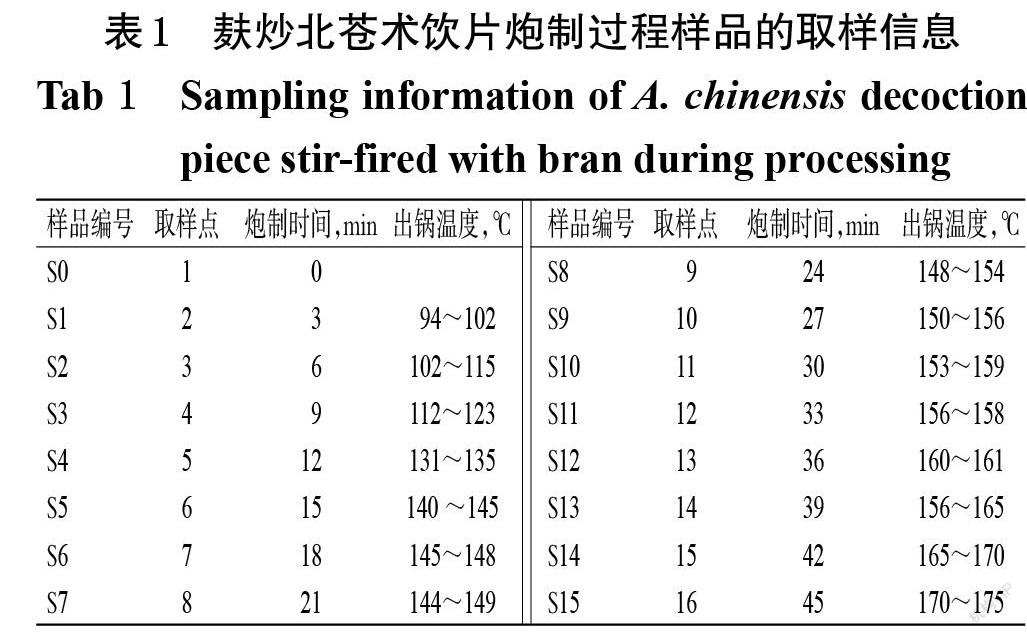
参考2020年版《中国药典》[1]北苍术【炮制】项下的规定制备北苍术饮片,再按麸炒法制备不同炮制时间的麸炒北苍术饮片。具体麸炒方法如下:设置炒药机加热温度为250 ℃,待锅内温度稳定在200 ℃时,投入麦麸1.5 kg,炒至冒白烟时,投入北苍术饮片10 kg进行翻炒;从投入北苍术饮片后开始计时,每隔3 min取样1次,共炮制45 min,并采用红外测温仪测定出锅时该饮片表面的温度。本研究在炒制过程中共取样16次,各时间点样品记为S0~S15(其中S0为北苍术生品)。具体取样信息见表1。
2.2 麸炒北苍术饮片炮制过程样品的表观性状及颜色变化
2.2.1 表观性状观察 取麸炒北苍术饮片炮制过程样品(S0~S15)进行表观性状观察,结果见表2、图1。
由表2和图1可知,随着炮制时间的延长,麸炒北苍术饮片断面的整体颜色逐渐加深,由黄棕色变为深黄色再变为棕褐色;饮片断面的油室颜色逐渐加深,由黄棕色变为棕褐色,且断面上焦斑的颜色也越来越深。
2.2.2 色度值测定 取麸炒北苍术饮片炮制过程样品(S0~S15)的粉末(过三号筛,下同)适量,压制成厚度约1 mm的薄片(表观变化见图2),采用国际照明委员会认可的D65光源进行照射,经白板校正后,平行拍照3次。观察并记录各样品粉末的色度值[包括明度值(L*)、红绿色值(a*)、黄蓝色值(b*),其数值由大到小分别表示粉末颜色由明变暗、由红变绿、由黄变蓝],计算总色值(E*ab)、总色差值(ΔE*a)[E*ab=(L*2+a*2+b*2)1/2,ΔE*ab=(ΔL*2+Δa*2+Δb*2)1/2,式中ΔL*=炮制品的L*-生品的L*,Δa*=炮制品的a*-生品的a*,Δb*=炮制品的b*-生品的b*],结果见表3。由表3可知,随着炮制时间的延长,麸炒北苍术饮片粉末的L*、b*呈下降趋势,a*呈先升高后下降的趋势; ΔE*ab逐渐增大,当ΔE*ab>6时(即炮制9 min后),可与生品明显区分[6],详见表3。
分别以色度值L*、a*、b*为纵坐标(y),以炮制时间为横坐标(x,min)进行回归分析,结果见图3。由图3可知,L*、b*与炮制时间呈线性关系,a*与炮制时间呈二元回归关系。
2.3 麸炒北苍术饮片炮制过程样品的UPLC指纹图谱分析
本课题组前期研究采用UPLC法建立了麸炒北苍术饮片炮制前后的指纹图谱[11],详见图4。其中S0样品(即北苍术生品)检测到26个色谱峰(峰2~峰27),S1~S15样品共检测到27个色谱峰(峰1~峰27,其中峰2、峰3仅部分样品中检测到)。基于此,本研究不再对方法学考察等内容进行赘述,而主要对麸炒北苍术饮片炮制过程样品间的相似度进行评价,并分析27个色谱峰的相对峰面积在炮制过程中的动态变化情况(未检测到的色谱峰的相对峰面积以0计算)。
2.3.1 相似度评价 以S0样品的色谱图为参照图谱,采用《中药色谱指纹图谱相似度评价系统(2012A版)》进行相似度评价。结果显示,S0~S15样品的相似度分别为1.000、0.999、0.993、0.990、0.973、0.925、0.887、0.872、0.762、0.612、0.530、0.461、0.444、0.284、0.214、0.088。由此可知,麩炒北苍术饮片随着炮制时间的延长,其样品相似度呈逐渐降低的趋势,这表明北苍术饮片经炮制后化学成分发生了明显变化。
2.3.2 色谱峰的相对峰面积测定 结合本课题组前期研究可知,峰1为北苍术麸炒后所产生的新成分[11],基于此,峰1以S1样品的色谱峰峰面积作为基准“1”,其余色谱峰均以S0样品的各色谱峰峰面积作为基准“1”,采用相对峰面积进行相对定量,测定麸炒北苍术饮片炮制过程样品的27个色谱峰的相对峰面积,结果见表4。
由表4可知,随着炮制时间的延长,麸炒北苍术饮片炮制过程样品的色谱峰相对峰面积呈一定动态变化规律:峰1、峰2的相对峰面积先增加后减少;峰3(5-HMF)的相对峰面积增加;峰4~峰27的相对峰面积均减少,且炮制45 min后,峰15已无法检出。
2.4 麸炒北苍术饮片炮制过程样品的浸出物、挥发油含量的测定
2.4.1 水溶性浸出物和醇溶性浸出物的含量测定 (1)水溶性浸出物:取麸炒北苍术饮片炮制过程样品(S0~S15)粉末约2 g,精密称定,置于150 mL的锥形瓶中,加水50 mL,参考2020年版《中国药典》(四部)通则“2201浸出物测定法”项下的水溶性浸出物测定法中的热浸法进行测定[12],结果见表5。(2)醇溶性浸出物:取麸炒北苍术饮片炮制过程样品(S0~S15)粉末约2 g,精密称定,置于150 mL的锥形瓶中,加乙醇50 mL,参考2020年版《中国药典》(四部)通则“2201浸出物测定法”项下的醇溶性浸出物测定法进行测定[12],结果见表5。
2.4.2 挥发油的含量测定 取麸炒北苍术饮片炮制过程样品(S0~S15)粉末约60 g,精密称定,置于1 000 mL的圆底烧瓶中,加水360 mL,参考2020年版《中国药典》(四部)通则“2204挥发油测定法”项下的甲法进行测定[12],结果见表5。
由表5可知,随着炮制时间的延长,麸炒北苍术饮片炮制过程样品的浸出物含量变化不明显,挥发油含量呈一定的下降趋势;当炮制至45 min时,挥发油含量相较于炮制0 min时下降约52%。
2.5 麸炒北苍术饮片炮制过程样品粉末的色度值与质量指标的相关性分析
将麸炒北苍术饮片炮制过程样品粉末的色度值、UPLC指纹图谱中27个色谱峰的相对峰面积(未检出的色谱峰相对峰面积以0计算)以及水溶性浸出物、醇溶性浸出物、挥发油的含量,分别采用SPSS 25.0软件进行Pearson相关性分析,结果见表6。
由表6可知,峰4~峰6、峰11~峰13、峰15~峰27的相对峰面积以及挥发油含量与L*、b*均呈正相关,表明随着L*、b*的减少,上述19个色谱峰的相对峰面积以及挥发油含量均随之减少。峰2、峰7~10的相对峰面积以及醇溶性浸出物含量与L*、a*、b*均呈一定的相关性:当L*、b*与质量指标均呈正相关时,a*与质量指标则呈负相关(例如峰7~峰10的相对峰面积随着L*、b*的减少而减少,随着a*的减少而增加);当L*、b*与质量指标呈负相关时,a*与质量指标则呈正相关(例如峰2的相对峰面积以及醇溶性浸出物含量随着L*、b*的减少而增加,随着a*的减少而减少)。峰14的相对峰面积与b*呈正相关,即随着b*的减少,峰14的相对峰面积也随之减少。峰1的相对峰面积以及水溶性浸出物含量与L*、a*、b*均无线性相关关系。
2.6 麸炒北苍术饮片炮制过程样品的多元统计分析
本研究以麸炒北苍术饮片炮制过程样品的色度值以及质量指标等33个变量为指标,采用Simca 14.1软件进行多元统计分析[主成分分析(PCA)、聚类分析(HCA)、偏最小二乘法判别分析(PLS-DA)][13]。
2.6.1 PCA和HCA 对麸炒北苍术饮片炮制过程样品进行PCA时,共提取了4个特征值>1的主成分因子,其特征值和方差贡献率见表7,PCA得分图见图5。由表7和图5可知,这4个主成分的作用显著,可用于反映麸炒北苍术饮片炮制过程样品90%以上的特征信息。
以平方欧氏距离为测度,进行HCA,结果见图6。由图6可知,麸炒北苍术饮片炮制过程样品可聚为3类:S0~S5样品聚为一类,S6~S11样品聚为一类,S12~S15样品聚为一类。基于此,笔者将与生品(S0)接近的样品拟定为炮制轻度样品(S0~S5),与S15样品(该样品中峰15丢失,其原因可能为炮制过度)接近的样品拟定为炮制过度样品(S12~S15),其余为炮制适度样品(S6~S11,炮制时间为18~33 min)。
2.6.2 PLS-DA 对麸炒北苍术饮片炮制过程样品进行PLS-DA后,其模型得分图见图7。由图7可知,麸炒北苍术饮片炮制过程样品可聚为3类,聚类结果与HCA结果一致。PLS-DA模型中R2Y=0.86,Q2=0.69,表明该模型拟合程度好、预测能力强[14]。进一步对该模型中33个指标的变量投影重要性(VIP)进行分析,结果见图8。选择VIP值大于1的指标作为麸炒北苍术饮片炮制过程中的重要质量指标[15],得到a*和峰2、19、9、7、8、10、13、1、4、21的相对峰面积是该饮片炮制过程中的重要质量指标。
2.7 麸炒北苍术饮片的炮制时间研究
结合“2.6”项下结果可知,麸炒北苍术饮片炮制适度的时间为18~33 min,但该时间范围较宽,无法较好地确定麸炒北苍术饮片的炮制时间。基于此,本研究参考灰色关联度法[15],将“2.6”项下的重要质量指标a*和峰2、19、9、7、8、10、13、1、4、21的相对峰面积以及峰3(5-HMF,其具有一定毒性[16])的相对峰面积作为评价指标,进行麸炒北苍术饮片炮制过程样品的综合质量评价,以确定其炮制时间,具体步骤如下。
第一,确定分析序列。将麸炒北苍术饮片炮制过程的16批样品组成16个评价单元序列xi(k)(i=1,2,3……m;k=1,2,3……n。本研究中m=16,n=12),并以炮制18 min的S6样品作为最优参考序列xs(k)。
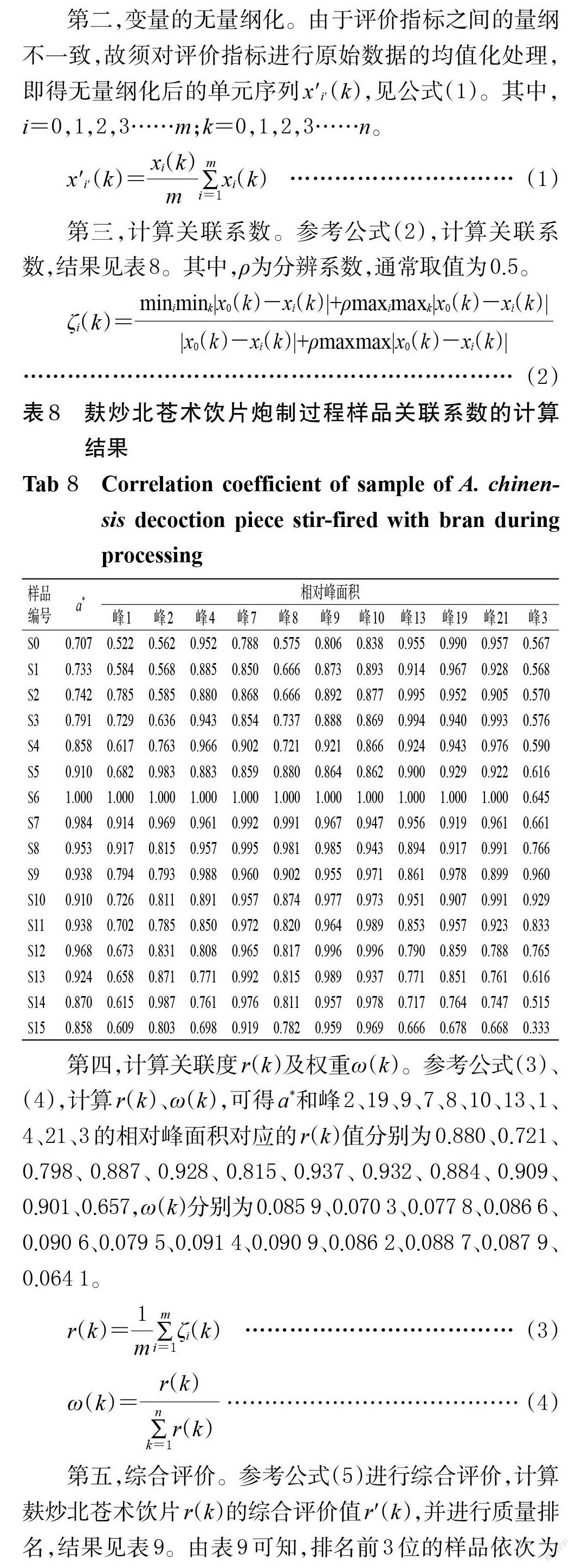
第二,变量的无量纲化。由于评价指标之间的量纲不一致,故须对评价指标进行原始数据的均值化处理,即得无量纲化后的单元序列x′i′(k),见公式(1)。其中,i=0,1,2,3……m;k=0,1,2,3……n。
3 讨论
3.1 麸炒北苍术饮片炮制辅料用量的考察
本课题组前期对麸炒北苍术饮片炮制辅料(麦麸)的用量(0、15%、30%)进行了考察,结果发现,辅料的用量对麸炒北苍术饮片粉末的L*、a*、b*并无明显影响。另外,随着辅料用量的增加,一方面可以抑制峰1的相对峰面积增加,且当麦麸用量为30%时,峰1的相对峰面积增加不明显;另一方面可以促进峰2、峰3的相对峰面积的增加,且当麦麸用量为30%时,这2个峰的相对峰面积均增加不明显。因此,本研究在炮制北苍术饮片时,麦麸的用量选择15%。
3.2 麸炒北苍术饮片粉末的色度值与质量指标的相关性
本研究前期对麸炒北苍术饮片进行色度值测定时发现,该饮片由于存在油室、外皮及焦斑的性状,导致所测色度值偏差较大。后续本课题组参考文献[17]方法,选择颜色特征更为均一的饮片粉末色度值与质量指标进行相关性分析。本研究结果显示,随着炮制时间的延长,麸炒北苍术饮片粉末的L*、b*呈现下降趋势,a*呈现先升高后下降的趋势,表明样品表观亮度由明变暗、颜色逐渐变深。进一步将麸炒北苍术饮片粉末的色度值与指纹图谱中27个色谱峰的相对峰面积以及水溶性浸出物、醇溶性浸出物、挥发油的含量进行相关性分析发现,随着L*、b*的降低,峰4~6、峰11~13、峰15~27的相对峰面积以及挥发油含量也随之减少,峰7、8(咖啡酸)、9、10(阿魏酸)的相对峰面积也随之减少,而峰2的相对峰面积、醇溶性浸出物含量却随之增加;随着a*的降低,峰2的相对峰面积、醇溶性浸出物含量随之减少,而峰7~10的相对峰面积却随之增加;随着b*的降低,峰14的相对峰面积以及醇溶性浸出物含量也随之减少;峰1的相对峰面积及水溶性浸出物含量与L*、a*、b*均无线性相关关系。由此表明,随着麸炒北苍术饮片色度值的变化,色谱峰(峰2~27)的相对峰面积、醇溶性浸出物含量以及挥发油含量也随之呈规律性变化,实际炮制工艺中可结合该饮片炮制品粉末的色度值对其质量指标的变化进行监测。
3.3 麸炒北苍术饮片炮制时间评价指标的确定
经HCA、PLS-DA发现,麸炒北苍术饮片可聚为炮制轻度(S0~S5)、适度(S6~S11)、过度(S12~S15)3类;再根据VIP值大于1,筛选出重要质量指标为a*和峰2、19、9、7、8、10、13、1、4、21的相对峰面积。相关研究发现,北苍术饮片中含有大量的果糖和葡萄糖[18],在炮制过程中可能发生降解,生成5-HMF(峰3),而该成分具有一定的副作用(如刺激性、肾毒性等)[19]。基于此,本研究将峰3和上述重要质量指标共同作为麸炒北苍术饮片炮制时间的评价指标,进一步经灰色关联度分析后发现,麸炒北苍术饮片的炮制时间应控制在18~24 min范围内。
綜上所述,麸炒北苍术饮片粉末的色度值与27个色谱峰的相对峰面积以及浸出物、挥发油的含量具有一定相关性。建议麸炒北苍术饮片的炮制时间范围为18~24 min,且可尽量控制在18 min。由于药材在生产炮制过程中,存在炮制规范、取样量、炮制仪器等差异,因此在实际炮制过程中仍需结合具体的炮制参数来控制饮片质量。
参考文献
[ 1 ] 国家药典委员会.中华人民共和国药典:一部[S]. 2020年版.北京:中国医药科技出版社,2020:168-169.
[ 2 ] 刘芬.基于炮制原理的麸炒苍术药效及作用机制研究[D].武汉:湖北中医药大学,2018.
[ 3 ] 于艳, 袁媛, 贾天柱,等.苍术炮制前后化学成分及药理作用研究近况[J].时珍国医国药,2016,27(1):195-197.
[ 4 ] 邓爱平,李颖,吴志涛,等.苍术化学成分和药理的研究进展[J].中国中药杂志,2016,41(21):3904-3913.
[ 5 ] 梁志毅,黄贵发,崔婷,等.狗脊微波炮制过程中指标成分与粉末颜色关联性分析[J].中成药,2020,42(6):1548- 1552.
[ 6 ] 张雪,李晓庆,王云,等.焦栀子炒制过程中HPLC图谱变化与外观颜色的动态关联研究[J].中草药,2018,49(17):4029-4037.
[ 7 ] 石典花,戴衍朋,苏本正,等.基于一测多评和色度识别的侧柏炭内外在质控方法研究[J].中国中药杂志,2020,45(24):5996-6002.
[ 8 ] 张天翼,郭成杰,郭宁,等.药效相关的中药感官指标测定方法的研究进展[J].中草药,2021,52(2):594-602.
[ 9 ] 曾敏.苍术饮片规格及其质量评价标准研究[D].武汉:湖北中医药大学,2013.
[10] 邹小兴.苍术属植物药用亲缘学研究[D].北京: 北京中医药大学,2010.
[11] 洪婉敏,陈丹燕,纪玉华,等.北苍术麸炒前后指纹图谱与色度值的差异研究[J/OL].中药材,2021[2021-03-04].https://doi.org/10.13863/j.issn1001-4454.2021.02.013.
[12] 国家药典委员会.中华人民共和国药典:四部[S]. 2020年版.北京:中国医药科技出版社,2020:232,252.
[13] 李晶峰,兰梦,边学峰,等.基于聚类分析与多元统计分析的东北林蛙油及其类似品、伪品的聚丙烯酰胺凝胶电泳图谱鉴别[J].中国实验方剂学杂志,2019,25(24):111- 117.
[14] 郭丽,杨忠杰,于晓涛,等.南、北五味子药材的HPLC指纹图谱建立及化学模式识别分析[J].中国药房,2020,31(18):2224-2229.
[15] 石海培,包贝华,黄胜良,等.川芎饮片的HPLC指纹图谱建立、聚类分析及偏最小二乘判别分析[J].中国药房,2019,30(8):1066-1071.
[16] 刘吉爽,段连政,徐文慧,等.灰色关联度法优化葵花盘“精准炮制”饮片的加工炮制一体化工艺[J].中国药房,2019,30(24):3413-3418.
[17] 林琳,林铌,凌亚豪 ,等. 5-羟甲基糠醛的急性毒性和细胞毒性研究[J].中国药物警戒,2018,15(4):205-209.
[18] 杨丽,龚燚婷,许铭珊,等.基于“表里关联”的大黄炭炮制过程颜色和成分变化关系研究[J].中草药,2020,51(22):5705-5713.
[19] 刘苗苗,陈祥胜,陈琪瑶,等.苍术麸炒过程中5-羟甲基糠醛的转化机制研究[J].中草药,2016,47(8):1327-1331.
(收稿日期:2021-06-29 修回日期:2021-08-30)
(编辑:唐晓莲)

