枣核活性炭的制备及其铀吸附性能
谢 宇 楚焕焕 李光英 陶 鹏 林晓艳
(1. 西南科技大学生命科学与工程学院 四川绵阳 621010; 2. 西南科技大学生物质材料教育部工程研究中心 四川绵阳 621010; 3. 西南科技大学材料科学与工程学院 四川绵阳 621010)
近年来,核能作为一种清洁高效的新型能源备受重视。核能的开发离不开核燃料,铀作为核燃料中重要的一种,其需求量也在不断增加。与此同时,随着核能的开发利用,产生的含铀放射性废水也越来越多[1],含铀废水若直接排放会造成严重的环境污染。因此,对含铀废水中的铀进行处理既可满足环保的要求,又能提高铀资源的利用率。在含铀废水的众多处理方法中吸附法具有成本低、效果好等优势[2]。
活性炭是由木质、煤质和石油焦等含碳的原料经热解、活化加工制备而成的,具有发达的孔隙结构、较大的比表面积和丰富的表面化学基团的特异性吸附能力较强的炭材料的统称。活性炭在治理放射性废水污染方面有着其他吸附材料不可比拟的优势[3]。活性炭具有较大的比表面积和丰富的孔隙结构,不仅原料广、可再生、制备方法简单,而且在热稳定性、耐辐照性、吸附容量、对铀的选择性等方面明显优于其他吸附材料[4-5]。我国枣树种植面积广,枣的产量大。枣核中富含木质素及矿物质,是一种制备活性炭的优质原料[6]。刘世军等[7]通过煅烧法制备枣粉木质活性炭,测定其碘吸附值及亚甲基蓝脱色力,此法工艺简单,但吸附性能有待提高。Suresh[8]研究了CO2和磷酸活化制备海枣核活性炭,其亚甲基蓝吸附效果比前者有很大提高,表明活化剂有利于增加官能团,从而提高吸附效果。杨晓霞等[9]采用 ZnCl2活化法制备枣核活性炭并研究其对阳离子杂环染料罗丹明 B 的吸附性能,证明吸附过程为化学吸附协同颗粒内扩散作用。国内外关于枣核生物炭材料对染料和碘的吸附性能研究较多,而对铀离子的吸附性能研究报道很少[10-12]。
本文选用新疆大红枣加工后副产物枣核进行活性炭制备,力求制备成本低廉、工艺简单的活性炭材料。通过对枣核活性炭进行适当的氧化改性处理,探究其对模拟含铀废水中铀离子的吸附效果及最佳的吸附条件,分析其吸附过程热力学和动力学模型,为枣核利用和工业化处理含铀废水提供理论依据。
1 实验
1.1 材料与仪器
枣核,和田大枣公司;KOH,NaOH,成都市科龙化工试剂厂;浓HCl,浓HNO3,成都市科隆化学品有限公司;偶氮胂-Ⅲ,梯希爱(上海)化成工业发展有限公司;硝酸双氧铀,湖北楚盛威化工有限公司。
DECO—PBM—V—4L球磨机,长沙德科仪器设备有限公司;SLD1700—8D金顿电炉,上海升利测试仪器有限公司;TM—3000型台式扫描电子显微镜,日本日立公司;Nicolet—6700型傅里叶变换红外吸收光谱仪,美国 Thermo Fisher 科技有限公司;JW—BK112型比表面分析仪,北京精微高博科学技术有限公司;PHS—3CW型精密酸度计,上海般特仪器制造有限公司。
1.2 枣核活性炭材料制备
洗去枣核表面杂质,在50 ℃条件烘干水分,用球磨机粉碎枣核过60目筛。取适量干的枣核粉于管式炉内,设置管式炉实验温度以5 ℃/min的升温速度从40 ℃升至450 ℃,保温1 h,使之碳化60 min。自然冷却后用研钵磨细,加入KOH和去离子水,50 ℃水浴下磁力搅拌2 h后于120 ℃烘箱内干燥。烧结2次后,将烧杯90 ℃水浴加热于磁力搅拌器上,磁力搅拌1 h,在室温下冷却后研磨,加入1 mol/L的盐酸洗涤,再次用去离子水洗涤抽滤,洗涤至溶液无色且pH值接近7,在真空干燥箱内50 ℃真空干燥12 h,得到初步的枣核活性炭。枣核活性炭加入适量的浓HNO3在140 ℃油浴24 h,抽滤,洗涤至中性,在50 ℃真空干燥12 h,得到最终氧化枣核活性炭。制备流程如图1所示。

图1 枣核活性炭材料的制备流程Fig.1 Preparation process of jujube nucleus activated carbon material
1.3 枣核活性炭吸附性能研究
称取枣核活性炭(0.005,0.010,0.015,0.020,0.025 g)于20 mL模拟铀废水溶液中,考察溶液pH值、吸附时间、温度等条件对吸附 U(VI) 的影响。通过式(1)、式(2)计算枣核活性炭对U(VI) 的吸附量qe和去除率Re。
(1)
(2)
式中:c0,ce分别为初始铀离子浓度和吸附达到平衡铀离子浓度,mg/L;V为模拟铀废水溶液体积,L;m为吸附剂加入量,g。
1.4 枣核活性炭材料的表征
扫描电镜(SEM)分析:观察不同活性炭材料与氢氧化钾质量比制备的枣核活性炭以及浓硝酸氧化改性前后及吸附 U(VI)后的氧化枣核活性炭的微观形貌。
比表面积(BET)测定:采用氮气吸附-脱附法进行比表面积以及孔径分布测试,用BJH脱附等温线的低压段得到孔径分布,用 BET 法计算材料的比表面积。
傅里叶变换红外吸收光谱(FT-IR)分析:将改性前后和吸附 U(VI)后的氧化枣核活性炭用玛瑙研钵研磨后与溴化钾粉末压片,在500~4 000 cm-1波数范围扫描。
2 结果与讨论
2.1 活化剂用量对枣核活性炭吸附U(Ⅵ)的影响
活化剂KOH用量直接影响枣核活性炭的孔结构和孔隙率以及表面官能团等表面特性,从而影响活性炭的吸附容量。枣核/活化剂质量比对枣核活性炭吸附U(Ⅵ)的影响结果如表1所示。当枣核质量与活化剂的质量比从1∶1降低到1∶5,即活化剂用量逐渐提高时,枣核活性炭对U(Ⅵ)的吸附量逐渐增加,但比例1∶4降到1∶5时吸附量增加不明显。最终选择质量比为1∶4的活化剂用量来活化枣核活性炭。
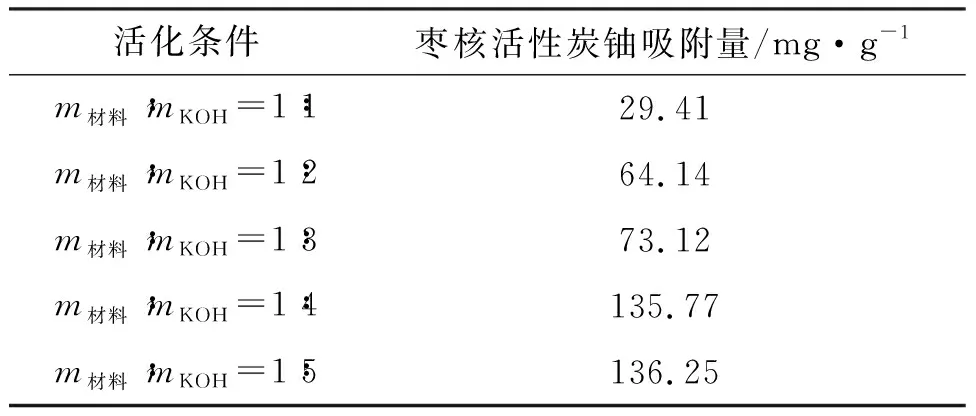
表1 枣核/活化剂质量比对枣核活性炭吸附铀的影响Table 1 Effect of jujube nucleus/activator mass ratio on uranium adsorption by jujube nucleus activated carbon
2.2 枣核活性炭材料的形貌表征
2.2.1 比表面积和孔结构
采用低温氮气吸附脱附对枣核活性炭材料的孔结构进行表征。硝酸氧化前后的 N2吸附-脱附等温线如图2所示。当相对压力P/P0<0.1时,氧化前的枣核活性炭对N2的吸附量迅速增加,表明它有大量的微孔结构。P/P0为0.1~0.3时,从吸附等温线特性可以判断氧化前的枣核活性炭有大量的微孔和介孔结构。此外,图中其他特征表明,氧化前的枣核活性炭有大量的大孔结构。氧化前后枣核活性炭的比表面积、N2脱附总体积、平均脱附孔径以及微孔体积如表2所示。氧化前的枣核活性炭比表面积、孔体积、微孔体积都比氧化后的大,但孔径略小,说明氧化前的枣核活性炭内部有丰富的孔结构,经过酸化处理导致部分孔结构坍缩,但依然保留了大孔和介孔结构。

表2 硝酸氧化前后枣核活性炭的比表面积、孔体积、孔径及微孔体积Table 2 Specific surface area, pore volume, pore diameter and micropore volume of activated carbon from jujube nucleus before and after nitric acid oxidation
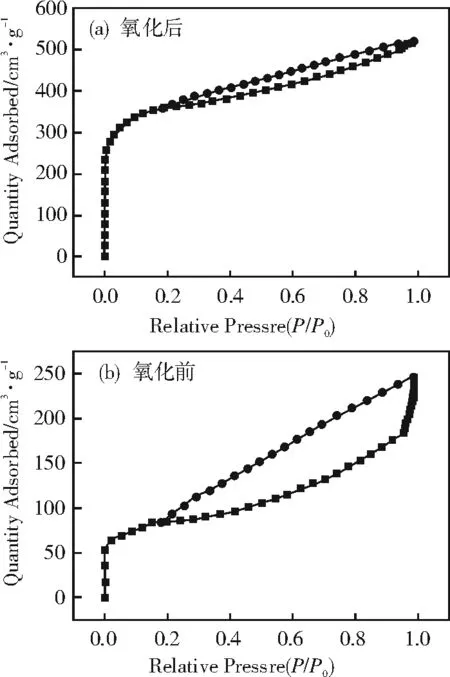
图2 枣核活性炭氮气吸附-解吸等温线 Fig.2 Nitrogen adsorption-desorption isotherm of jujube nucleus activated carbon
2.2.2 微观形貌
硝酸氧化前后的枣核活性炭的 SEM图片如图3 所示。未氧化的枣核活性炭有大量的片状中空管状结构,图3 (c) 上有一些独立的颗粒,这些颗粒有孔洞结构。由图3(d)、图3(e)、图3(f)可以看出,经过氧化后的枣核活性炭多为独立的颗粒,这些颗粒上有很多密集的小孔呈现蜂窝状,在一些地方有大孔出现,并且可以看出孔边缘变得粗糙。

图3 枣核活性炭的 SEM图Fig.3 SEM images of jujube nucleus activated carbon
2.3 枣核活性炭材料对U(Ⅵ)的吸附性能
2.3.1 溶液pH值对吸附U(Ⅵ)的影响
pH值对枣核活性炭吸附U(Ⅵ)的影响结果如图4所示。pH值为1.5~5.5时,吸附量随着pH值增大而增大,pH=5.5时,吸附量达到了最大值146.4 mg/g。在pH值为5.5~6.0时,吸附量随着pH值的增大而减小。当pH值较低时,溶液中含有较多的H+,吸附剂表面被较多的质子所占据,溶液中的H+与U(Ⅵ)存在着竞争关系,共同竞争活性炭上的活性位点[13]。因为pH 值较低,H+的浓度较高,而随着pH值的升高,U(Ⅵ)逐渐占据上风,所以吸附量增大[14]。随着pH值升高,H+的数量减少,质子与U(Ⅵ)之间的竞争减少,枣核活性炭对铀酰离子的吸附量逐渐增大。当pH值大于5.5时,铀酰离子产生沉淀,所以吸附量下降。因此枣核活性炭对U(Ⅵ)的吸附宜在pH 值为5.5条件下进行。
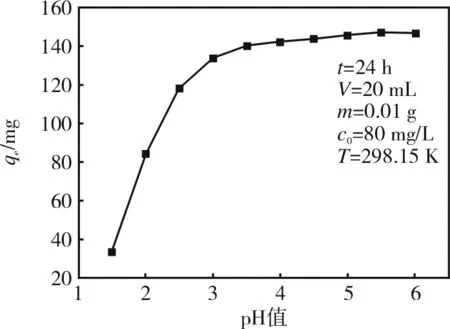
图4 pH 值对枣核活性炭吸附 U(VI)的影响Fig.4 Effect of the pH on the adsorption of uranium(VI) by jujube nucleus activated carbon
2.3.2 吸附剂用量对吸附U(Ⅵ)的影响
枣核活性炭投料量从0.005 g增加到0.025 g时,对U(Ⅵ)的吸附量和去除率的影响实验结果如图5所示。由图5 可以看出,在U(Ⅵ)浓度为80 mg/L,吸附剂用量为0.005~0.010 g时,枣核活性炭对铀溶液中铀酰离子的去除率上升,而吸附量下降。因为在U(Ⅵ)浓度一定时,增加吸附剂用量相当于为吸附U(Ⅵ)提供了更多的吸附接触位点,去除率增加,而单位质量的吸附剂的吸附容量降低,所以吸附量下降[15]。当吸附剂用量大于0.010 g时,去除率接近平衡。枣核活性炭的吸附量随着吸附剂的增加逐渐降低。因为吸附剂用量过多,导致吸附位点过多,吸附位点没有得到充分利用,部分吸附位点达不到饱和,使单位质量的吸附剂吸附量减少[16]。当吸附剂用量为0.010 g时,对铀酰离子的去除率已达到96%,而吸附剂用量增加为0.025 g时,铀的去除率为97.1%,只增加了1.1%。综上,考虑铀的去除率和吸附量的影响以及对枣核活性炭的合理利用,选择吸附剂用量为0.010 g。

图5 吸附剂用量对枣核活性炭吸附 U(VI)吸附量及去除率的影响Fig.5 Effect of adsorption dosage on the adsorption capacity and removal efficiency of U(VI) by jujube nucleus activated carbon
2.3.3 吸附时间对吸附U(Ⅵ)的影响及动力学模型分析
吸附时间对枣核活性炭吸附U(Ⅵ)的吸附量影响实验结果如图6所示。当t<3 h时,吸附量迅速增加。当t在3~11 h 时,吸附量先减小后增加再减小,最后趋于平衡,最大吸附量为147.8 mg/g。因为吸附时间小于3 h 时,活性炭上有很多活性位点没有被占据,此时溶液中铀酰离子也很多。当吸附时间在3~11 h 时,活性炭表面的活性位点已被占据,只有内部还有吸附能力,此时铀离子的浓度降低,要扩散到活性炭内部需要更高能量,所以吸附变慢。
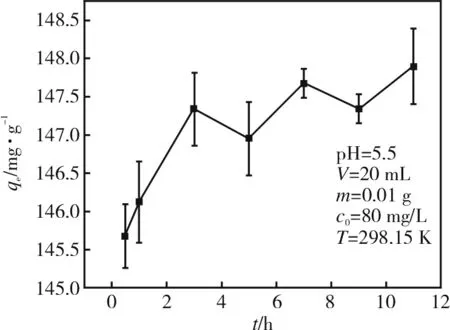
图6 吸附时间对枣核活性炭吸附 U(VI)的影响Fig.6 Effect of adsorption time on the adsorption of U(VI) by jujube nucleus activated carbon
采用准一级和准二级动力学模型对吸附铀过程拟合结果如表3所示。准二级和准一级动力学模型拟合的R2分别为0.999和 0.599,表明准二级模型的拟合度高于准一级模型。由准二级模型得出的平衡吸附量147.9 mg/g接近于实际平衡吸附量147.8 mg/g,说明枣核活性炭吸附过程符合准二级动力学模型,该吸附过程以化学吸附为主[17]。此过程主要依赖枣核活性炭上的吸附位点,而不是吸附质浓度,推断与枣核活性炭和铀离子之间共用电子对或电子转移有关,还需进一步验证。

表3 枣核活性炭吸附 U(VI)的准一级和准二级动力学拟合参数Table 3 Fitting parameters of the quasi-first- and quasi-second-order kinetics of U(VI) adsorption by jujube nucleus activated carbon
2.3.4 初始浓度对吸附U(Ⅵ)的影响及等温吸附模型分析
不同铀溶液的初始浓度对枣核活性炭吸附U(Ⅵ)的影响如图7所示。在288.15 ~328.15 K温度范围内,当初始浓度增大时,吸附量均增大。在同一温度下,吸附量随着铀初始浓度的增大而增大。

图7 铀初始浓度对枣核活性炭吸附 U(VI)的影响Fig.7 Effect of initial uranium(VI) concentration on the adsorption of uranium(VI) by jujube nucleus activated carbon
在铀浓度较小时,活性炭上的吸附位点没有被完全占据,随着铀浓度的增大,吸附量一直保持增长的趋势。可能是由于溶液中U(Ⅵ)浓度增大,使 U(Ⅵ)与吸附剂碰撞机会增加。表明初始浓度对枣核活性炭吸附铀酰离子起主要作用。
用Langmuir和Freundlich 等温吸附模型来描述达到平衡时被吸附物质的分布情况。拟合结果如图8、图9 所示,发现线性Langmuir等温模型的R2高于其它模型,说明等温吸附数据更符合线性Langmuir等温模型。枣核活性炭吸附剂吸附铀酰离子主要是单分子层吸附[18]。

图8 枣核活性炭吸附 U(VI)的 Langmuir 模型的线性和非线性拟合图Fig.8 The linear and nonlinear fitting diagrams of the Langmuir model for U(VI) adsorption by jujube nucleus activated carbon
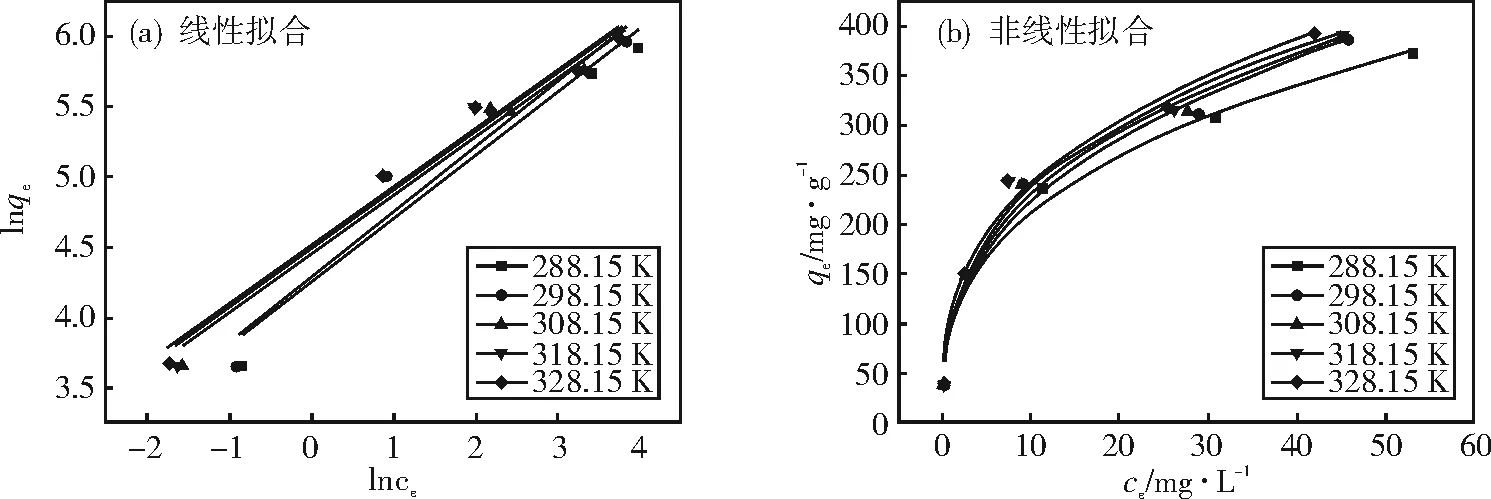
图9 枣核活性炭吸附 U(VI)的 Freundich 模型的线性和非线性拟合图Fig.9 The linear and nonlinear fitting graphs of the Freundich model for U(VI) adsorption by jujube nucleus activated carbon
2.3.5 温度对吸附U(Ⅵ)的影响及热力学模型分析
在288.15~328.15 K温度范围内,温度对吸附量的影响实验结果如图10和表4所示,在较低铀浓度时,随温度的升高,吸附量变化不大。在较高铀浓度时,吸附量随着温度的升高而稍微升高,但变化不大。考虑吸附量及耗能,选择枣核活性炭吸附温度在室温 298.15 K进行。
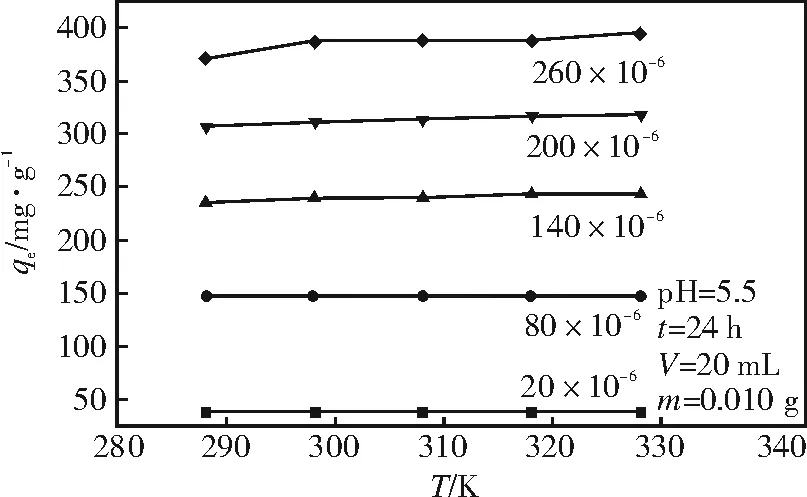
图10 温度对枣核活性炭吸附 U(VI)的影响Fig.10 Effect of temperature on the adsorption of U(VI) by jujube nucleus activated carbon
根据热力学公式计算得出不同温度下的参数如表4所示。根据公式计算得到K0。从表4中得出:△H0>0,△G0<0,△S0>0,说明吸附过程是一个自发进行无序程度增加的吸热过程。

表4 枣核活性炭吸附 U(VI)的热力学参数Table 4 The rmodynamic parameters of U(VI) adsorption by jujube nucleus activated carbon
2.3.6 枣核活性炭的脱附再生
用1.0 mol/L盐酸对枣核活性炭的U(Ⅵ)进行解吸,如图11所示。枣核活性炭经过5次吸附-脱附循环实验后,去除率仍有96.25 %,说明其对铀酰离子仍有良好的吸附效果,表明枣核活性炭稳定性良好,吸附U(VI)过程对其破坏不大[19]。

图11 枣核活性炭的吸附再生试验Fig.11 Adsorption regeneration test of jujube nucleus activated carbon
2.3.7 枣核活性炭吸附机理分析
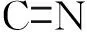
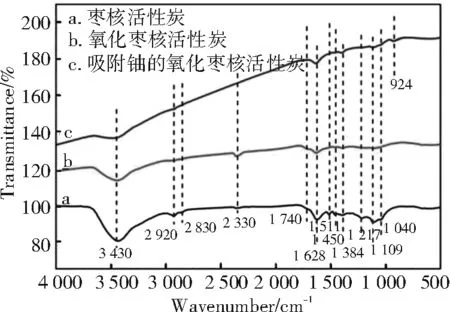
图12 枣核活性炭的傅里叶红外吸收光谱图Fig.12 FT-IR spectra of jujube nucleus activated carbon

通过图3(d)-图3(i) 可以发现,吸附铀之后的枣核活性炭与氧化后的活性炭在形貌结构上并没有改变,这说明吸附铀的主要作用基团在氧化后活性炭的表面。
2.3.8 枣核活性炭与其他生物碳材料吸附性能比较
枣核活性炭与其他生物碳材料的吸附比较如表 5所示。表5表明枣核活性炭的吸附性能要优于目前报道的其他生物碳材料,可能是枣核活性炭表面富含更多数量的含氧官能团。
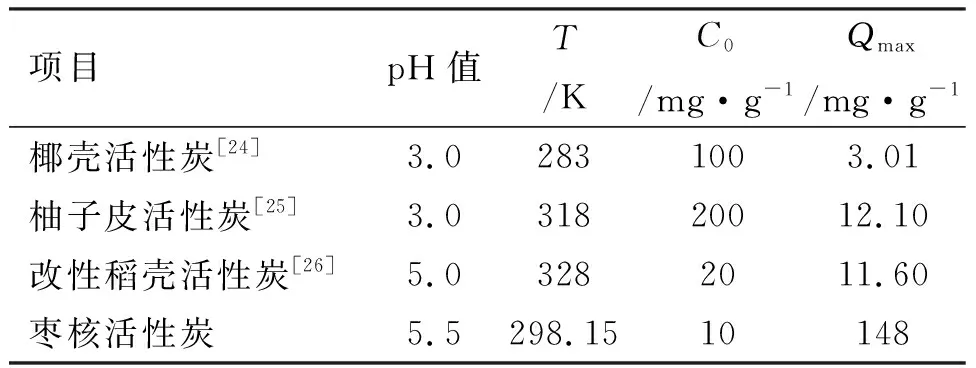
表5 几种活性炭材料对U (VI)最大吸附量Qmax比较Table 5 Comparison of the maximum adsorption capacity (Qmax) of U (VI) by several activated carbon materials
3 结论
(1)枣核活性炭材料具有丰富的孔隙结构。当温度为298.15 K,溶液 pH值为5.5,吸附剂量为 0.010 g,吸附时间为 11 h时,枣核活性炭对 U(VI)吸附效果最佳,最大吸附量为148 mg/g。
(2)枣核活性炭对 U(VI)的吸附行为符合准二级动力学模型和线性 Langmuir等温吸附模型,枣核活性炭吸附过程主要依赖于活性位点,吸附主要以化学吸附为主。吸附过程为自发进行熵增加的吸热反应。
(3)枣核活性炭对铀的吸附机理中存在离子交换和表面络合吸附,参与吸附的活性主要官能团为材料表面的含氧官能团。

