甘露子化学成分及其对鼻黏膜上皮细胞的影响
张灵敏, 李静波, 蔡纪堂, 郑琳靖
(河南省中医院,河南 郑州 450002)
甘露子为唇形科水苏属植物甘露子StachyssieboldiiMiq.的全草,又称地牯牛、草石蚕、旱螺蛳、地环儿等[1],主要分布于山西、河北、河南、山东、山西等地,其药性甘平,具有润肺补肾、活血散瘀、清热利湿的功效,用于肺炎、肺结核、风热感冒、气喘、黄疸、小便短涩[2],主要化学成分包括黄酮类、有机酸类、三萜类、甾体类[3],具有抗氧化、抗菌、抗疲劳、抗肿瘤等作用[4]。郭淑云等[5]报道,甘露子对创伤黏膜组织具有显著的修复作用。本研究对甘露子90%乙醇提取物进行分离、纯化,得到15个化合物,均为首次从甘露子中分离得到,其中化合物1、5可提高鼻黏膜上皮细胞的相对存活率。
1 材料
PT2025型超导核磁共振仪(瑞士Metrolab公司);Daltonics1300型质谱仪(德国Bruker Daltonics公司);60~100、300~400目柱色谱硅胶(青岛海洋化工有限公司);UV-3000型暗箱式紫外分析仪(上海昶钲电子科技有限公司);UHT87Y型旋转蒸发仪(郑州长城科工贸有限公司);NYJ96型超声波清洗器(山东新玛自动化科技有限公司);XY-2C型分析天平(常州德普纺织科技有限公司);BSA116S型全自动离心机(济南欧莱博电子商务有限公司)。SephadeX LH-20凝胶(瑞典Pharmacia公司)。苯环喹溴铵(上海闪谱生物科技公司);二甲基亚砜(DMSO,山东瑞港化工有限公司);噻唑蓝(MTT,广东翁江化学试剂有限公司)。所用试剂均为分析纯。
甘露子采自河南省郑州市,经河南中医药大学第二附属医院李静波教授鉴定为甘露子StachyssieboldiiMiq.的全草。
2 提取与分离
取干燥的甘露子21.4 kg,粉碎后加入90%乙醇加热回流提取3次,每次2 h,合并上述提取液,减压浓缩得甘露子总浸膏2.6 kg,超声分散在水中,采用石油醚、二氯甲烷、丙酮和正丁醇依次萃取,减压回收溶剂,得石油醚部分浸膏(Fr.A)173.6 g、二氯甲烷部分浸膏(Fr.B)186.2 g、丙酮部分浸膏(Fr.C)217.3 g、正丁醇部分浸膏(Fr.D)251.4 g。取Fr.B,经硅胶柱分离,以石油醚-二氯甲烷-乙酸乙酯 (50∶50∶0~30∶70∶0~10∶80∶10)梯度洗脱,得到7个流分Fr.B1~Fr.B7,Fr.B2 (7.8 g) 经硅胶柱,以石油醚-二氯甲烷-丙酮 (40∶60∶0~20∶80∶0~10∶80∶10)梯度洗脱,得到8个组分Fr.B2-1~Fr.B2-8,Fr.B2-2 (843 mg) 经硅胶柱,以石油醚-二氯甲烷-乙酸乙酯 (30∶60∶10) 洗脱,得化合物3(27 mg)、6(21 mg);Fr.B2-4 (649 mg) 经硅胶柱,以石油醚-二氯甲烷-乙酸乙酯 (20∶70∶10)洗脱,得化合物8(16 mg)、10(25 mg);Fr.B2-5 (437 g) 经硅胶柱,以石油醚-二氯甲烷-乙酸乙酯 (10∶80∶10)洗脱,得化合物1(22 mg)、7(19 mg);Fr.B2-7 (624 mg) 经Sephadex LH-20柱,以甲醇洗脱,得化合物11(21 mg)。取Fr.C,经硅胶柱分离,以二氯甲烷-丙酮-甲醇 (80∶20∶0~30∶70∶0~20∶70∶10) 梯度洗脱,得到5个流分Fr.C1~Fr.5,Fr.C3 (9.3 g) 经硅胶柱分离,以二氯甲烷-丙酮-甲醇 (80∶20∶0~30∶70∶0~20∶70∶10)梯度洗脱,得到7个组分Fr.C3-1~Fr.C3-7,Fr.C3-2 (763 mg) 经硅胶柱分离,以二氯甲烷-乙酸乙酯-甲醇 (10∶80∶10)洗脱,得化合物2(18 mg)、5(34 mg);Fr.C3-4 (591 mg) 经硅胶柱分离,以二氯甲烷-乙酸乙酯-甲醇 (30∶60∶10)洗脱,得化合物4(19 mg);Fr.C3-6 (341 mg) 经结晶、重结晶,得化合物15(26 mg),Fr.C4 (11.5 g) 经硅胶柱分离,以二氯甲烷-丙酮-甲醇 (70∶30∶0~20∶80∶0~10∶80∶10) 梯度洗脱,得到6个组分Fr.C4-1~Fr.C4-6,Fr.C4-2 (473 mg) 经硅胶柱分离,以二氯甲烷-丙酮-甲醇 (10∶80∶10)洗脱,得化合物13(19 mg);Fr.C4-4 (316 mg) 经Sephadex LH-20色谱柱,以甲醇洗脱,得化合物12(23 mg)。取Fr.D,经硅胶柱分离,以二氯甲烷-丙酮-甲醇(20∶80∶0~10∶80∶10~0∶60∶40)梯度洗脱,得到6个流分Fr.D1~Fr.D6,Fr.D3 (815 g) 经硅胶柱分离,以二氯甲烷-乙酸乙酯-甲醇(10∶90∶0~10∶80∶10~0∶50∶50) 梯度洗脱,得到6个组分Fr.D3-1~Fr.D3-6,Fr.D3-2 (514 mg) 经硅胶柱,以二氯甲烷-乙酸乙酯-甲醇 (10∶80∶10)洗脱,得化合物14(23 mg);Fr.D3-4 (613 mg) 经Sephadex LH-20色谱柱,以甲醇洗脱,得化合物9(23 mg)。
3 结构鉴定
化合物1:黄色胶状,ESI-MSm/z:266.1[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.92 (1H,d,J=7.6 Hz,H-5),6.71 (1H,d,J=7.6,1.6 Hz,H-6),6.58 (1H,d,J=7.6 Hz,H-8),6.39 (1H,d,J=7.6 Hz,H-1),6.26 (1H,d,J=7.6 Hz,H-3),3.81 (3H,s,4-OCH3),2.63 (4H,s,H-9,10);13C-NMR (CD3OD,150 MHz)δ:108.2 (C-1),157.3 (C-2),99.6 (C-3),161.2 (C-4),130.2 (C-5),115.0 (C-6),156.3 (C-7),113.7 (C-8),31.2 (C-9),31.3 (C-10),140.1 (C-1a),116.5 (C-4a),126.3 (C-5a),146.1 (C-8a),55.4 (4-OCH3)。以上数据与文献[6]基本一致,故鉴定为coelonin。
化合物2:白色胶状,ESI-MSm/z:201.2[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.69 (1H,d,J=9.6 Hz,H-6),7.03 (1H,s,H-3),6.72 (1H,d,J=9.6 Hz,H-5),2.52 (3H,s,H-10),2.38 (3H,s,4-OCH3);13C-NMR (CD3OD,150 MHz)δ:113.1 (C-1),164.5 (C-2),120.1 (C-3),150.4 (C-4),119.2 (C-5),1322.4 (C-6),195.7 (C-8),199.6 (C-9),28.1 (C-10),22.4 (4-OCH3)。以上数据与文献[7]基本一致,故鉴定为1-(2-hydroxy-4-methylphe-nyl)propan-1,2-dione。
化合物3:白色粉末,ESI-MSm/z:174.8[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:9.68 (1H,s,H-7),7.38 (2H,dd,J=9.6,7.6 Hz,H-2,6),6.92 (1H,d,J=9.6 Hz,H-5),3.81 (3H,s,4-OCH3);13C-NMR (CD3OD,150 MHz)δ:129.2 (C-1),130.4 (C-2),150.1 (C-3),160.3 (C-4),111.4 (C-5),117.2 (C-6),56.1 (4-OCH3),192.8 (7-CHO)。以上数据与文献[8]基本一致,故鉴定为3-羟基对甲氧基苯甲醛。
化合物4:白色粉末,ESI-MSm/z:272.8[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:6.46 (1H,d,J=9.6 Hz,H-13a),5.48 (1H,d,J=7.6 Hz,H-13b),4.25 (1H,m,H-8),4.05 (1H,t,J=9.6 Hz,H-4),0.97 (3H,d,J=9.6 Hz,H-14),0.81 (3H,s,H-15);13C-NMR (CD3OD,150 MHz)δ:45.1 (C-1),26.4 (C-2),30.4 (C-3),83.7 (C-4),44.3 (C-5),36.5 (C-6),47.4 (C-7),83.4 (C-8),44.7 (C-9),31.7 (C-10),139.1 (C-11),170.4 (C-12),119.3 (C-13),20.5 (C-14),19.3 (C-15)。以上数据与文献[9]基本一致,故鉴定为2-desoxy-4-epi-pulchellin。
化合物5:白色胶状,ESI-MSm/z:176.8[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:6.58 (1H,d,J=9.6 Hz,H-4),6.15 (1H,m,H-5),5.76 (1H,s,H-2),5.41 (1H,ddd,J=9.6,7.6,1.6 Hz,H-8),5.03 (1H,m,H-6),3.25 (1H,m,H-7b),1.72 (1H,m,H-7a);13C-NMR (CD3OD,150 MHz)δ:175.4 (C-1),114.0 (C-2),164.2 (C-3),121.7 (C-4),140.3 (C-5),64.8 (C-6),39.2 (C-7),79.3 (C-8)。以上数据与文献[9]基本一致,故鉴定为aquilegiolide。
化合物6:白色粉末,ESI-MSm/z:190.8[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.63 (1H,d,J=9.6 Hz,H-5),7.35 (1H,dd,J=9.6,7.6 Hz,H-6),6.85 (1H,d,J=7.6 Hz, H-2),3.72 (3H,s,7-OCH3);13C-NMR (CD3OD,150 MHz)δ: 119.5 (C-1),116.2 (C-2),148.4 (C-3),145.1 (C-4),122.6 (C-5),114.3 (C-6),167.2 (C-7),53.6 (7-OCH3)。以上数据与文献[10]基本一致,故鉴定为3,4-二羟基苯甲酸甲酯。
化合物7:白色粉末,ESI-MSm/z:599.1[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:5.43 (1H,dd,J=9.6,7.6 Hz,H-6),5.02 (1H,d,J=9.6 Hz,1-Glc),1.22 (3H,d,J=9.6 Hz,21-CH3),1.14 (3H,s,19-CH3),0.85 (3H,s,18-CH3),0.69 (3H,d,J=7.6 Hz,27-CH3);13C-NMR (CD3OD,150 MHz)δ:32.8 (C-1),28.1 (C-2),75.2 (C-3),40.1 (C-4),139.2 (C-5),122.4 (C-6), 33.1 (C-7),32.4 (C-8),47.6 (C-9),38.2 (C-10),22.4 (C-11),39.4 (C-12),40.8 (C-13),58.1 (C-14),31.7 (C-15),82.6(C-16),62.5 (C-17),17.1 (C-18),20.4 (C-19),43.1 (C-20),16.1 (C-21),111.2 (C-22),34.1 (C-23),30.1 (C-24),33.5 (C-25),68.1 (C-26),18.2 (C-27)及1个葡萄糖 (δ:101.1,76.2,80.6,73.1,81.2,64.3)。以上数据与文献[11]基本一致,故鉴定为3-epi-diosgenin-3-β-D-glucopyranoside。
化合物8:白色粉末,ESI-MSm/z:351.2[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.86 (2H,d,J=9.6 Hz,H-2′,6′),7.69 (1H,d,J=9.6 Hz,H-7),7.22 (1H,dd,J=7.6 Hz,H-6),7.18 (2H,d,J=7.6 Hz,H-2),6.92 (2H,d,J=9.6 Hz,H-3′,5′),6.75 (1H,d,J=7.6 Hz,H-5),6.43 (1H,d,J=9.6 Hz,H-8),5.79 (2H,s,H-8′),3.76 (3H,s,10-OCH3);13C-NMR (CD3OD,150 MHz)δ:126.3 (C-1),111.7 (C-2),149.5 (C-3),151.6 (C-4),117.4 (C-5),124.1 (C-6),146.3 (C-7),117.2 (C-8),167.4 (C-9),129.1 (C-1′),130.2 (C-2′),114.2 (C-3′),164.3 (C-4′),114.2 (C-5′),130.2 (C-6′),191.5 (C-7′),66.2 (C-8′),56.3 (10-OCH3)。以上数据与文献[12]基本一致,故鉴定为4′,8′-二羟基苯乙酮-8-O-阿魏酸酯。
化合物9:黄色油状,ESI-MSm/z:207.3[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:6.73 (1H,s,H-2),6.57 (1H,s,H-5),6.46 (1H,dd,J=9.6,7.6 Hz,H-6),3.37 (2H,s,H-7),3.12 (3H,s,9-OCH3);13C-NMR (CD3OD,150 MHz)δ:127.4 (C-1),116.8 (C-2),146.8 (C-3),143.1 (C-4),115.1 (C-5),122.5 (C-6),40.9 (C-7),76.2 (C-8),54.2 (9-OCH3)。以上数据与文献[13]基本一致,故鉴定为3,4-二羟基苯乙酸甲酯。
化合物10:白色结晶,ESI-MSm/z:509.2[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.93 (1H,d,J=9.6 Hz,H-2),6.72 (1H,d,J=7.6 Hz,H-8),6.37 (1H,d,J=7.6 Hz,H-6),6.19 (1H,d,J=7.6 Hz,H-3),5.31 (1H,d,J=7.6 Hz,H-1″),5.08 (1H,d,J=9.6 Hz,H-1′),3.93 (1H,dd,J=7.6,1.6 Hz,H-2″),3.79 (2H,m,H-6′),3.71 (1H,dd,J=9.6,7.6 Hz,H-2′),3.51 (1H,t,J=7.6 Hz,H-3′),3.42(1H,m,H-5′),3.27 (1H,dd,J=7.6,1.6 Hz,H-4′),1.18(1H,d,J=7.6 Hz,H-6″);13C-NMR (CD3OD,150 MHz)δ:131.2 (C-1),162.4 (C-2),113.5 (C-3),183.7 (C-4),164.1 (C-5),102.3 (C-6),165.1 (C-7),97.4 (C-8),160.2(C-9),107.3 (C-10),99.2 (C-1′),80.4 (C-2′),83.6 (C-3′),72.3 (C-4′),79.1 (C-5′),63.5 (C-6′),102.8 (C-1″),73.1 (C-2″),74.5(C-3″),72.6 (C-4″),69.3 (C-5″),19.2 (C-6″)。以上数据与文献[14]基本一致,故鉴定为5,7-dihydroxychromone-7-O-neohesperidoside。
化合物11:黄色粉末,ESI-MSm/z:278.6[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.38 (2H,t,J=9.6 Hz,H-3,5),7.24 (2H,t,J=9.6 Hz,H-2,6),7.06 (1H,t,J=9.6 Hz,H-4),4.85 (1H,d,J=9.6 Hz,H-glc-1),3.92 (1H, dd,J=9.6,7.6 Hz,H-glc-6a),3.24~3.81 (5H,m,H-glc-2,3,4,5,6b);13C-NMR (CD3OD,150 MHz)δ:161.4 (C-1),16.2 (C-2),127.4 (C-3),120.8 (C-4),127.4 (C-5),116.2 (C-6),99.7 (C-glc-1),72.8 (C-glc-2),75.6 (C-glc-3),70.2 (C-glc-4),77.1 (C-glc-5),61.2 (C-glc-6)。以上数据与文献[15]基本一致,故鉴定为phenyl β-D-glucopyranoside。
化合物12:黄色针晶,ESI-MSm/z:339.1[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:8.17 (2H,d,J=7.6 Hz,H-2′,6′),6.93 (2H,d,J=7.6 Hz,H-3′,5′),6.28 (1H,s,H-6),3.41(3H,8-OCH3);13C-NMR (CD3OD,150 MHz)δ:115.4 (C-1),147.1(C-2),135.8 (C-3),175.3 (C-4),156.4 (C-5),100.2(C-6), 156.3 (C-7),129.1(C-8),150.2(C-9),103.8 (C-10),124.1 (C-1′),129.6 (C-2′),115.3 (C-3′),159.3 (C-4′),115.3 (C-5′),129.6 (C-6′),62.1 (8-OCH3)。以上数据与文献[16]基本一致,故鉴定为8-甲氧基山萘酚。
化合物13:黄色片晶,ESI-MSm/z:351.3[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:13.17 (1H,s,5-OH),7.93 (2H,d,J=7.6 Hz,H-2′,6′),7.18 (2H,d,J=7.6 Hz,H-3′,5′),6.39 (1H,d,J=1.6 Hz,H-8),6.28 (1H,d,J=1.6 Hz,H-6),3.82 (3H,s,4′-OCH3),3.79 (3H,s,7-OCH3),3.71 (3H,s,3-OCH3);13C-NMR (CD3OD,150 MHz)δ:179.1 (C-1),163.2 (C-2),161.6 (C-3),162.4 (C-4),155.1 (C-5),156.2 (C-6),139.4 (C-7),129.7 (C-8),121.4 (C-9),113.6 (C-10),105.4 (C-11),96.3 (C-12),93.4 (C-13),56.2 (3-OCH3),55.7 (7-OCH3),60.8 (4′-OCH3)。以上数据与文献[17]基本一致,故鉴定为5-羟基-3,7,4′-三甲氧基黄酮。
化合物14:黄色粉末(甲醇),ESI-MSm/z:363.1[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:7.91 (1H,d,J=7.6 Hz,H-2),6.72 (1H,d,J=7.6 Hz,H-6),6.47 (1H,d,J=7.6 Hz,H-8),6.17 (1H,d,J=7.6 Hz,H-3),4.96 (1H,d,J=7.6 Hz,H-glc-1),3.72 (1H,dd,J=9.6,7.6 Hz,H-glc-6a), 3.21-3.64 (5H,m,H-glc-2,3,4,5,6b);13C-NMR (CD3OD,150 MHz)δ:121.3 (C-1),157.4 (C-2),111.2 (C-3),183.5 (C-4),162.3 (C-5),100.4 (C-6), 164.2 (C-7),95.1 (C-8),156.4 (C-9),107.2 (C-10),99.8 (C-glc-1),72.1 (C-glc-2), 76.3 (C-glc-3),70.2 (C-glc-4),75.1 (C-glc-5),59.4 (C-glc-6)。以上数据与文献[18]基本一致,故鉴定为7-β-D-glucosyloxy-5-hydroxy-chromone。
化合物15:白色粉末,ESI-MSm/z:342.7[M+Na]+。1H-NMR (CD3OD,600 MHz)δ:5.41 (1H,t,J=9.6 Hz,H-14),4.91 (1H,brs,H-17a),4.63 (1H,brs,H-17b),4.08 (2H,d,J=5.5 Hz,H-15),1.72 (3H,s,H-16),1.18 (3H,s,H-20),0.62 (3H,s,H-18);13C-NMR (CD3OD,150 MHz)δ:40.1 (C-1),19.7 (C-2),39.2 (C-3),45.1 (C-4),57.4 (C-5),27.5 (C-6),39.1 (C-7),149.5 (C-8),57.2 (C-9),41.3 (C-10),21.8 (C-11),39.2 (C-12),139.6 (C-13),123.1 (C-14),60.2 (C-15),17.1 (C-16),107.2 (C-17),30.4 (C-18),183.2 (C-19),13.4 (C-20)。以上数据与文献[19]基本一致,故鉴定为isocupressic acid。
4 化合物对鼻黏膜上皮细胞的影响
选取2021年1月至2月在河南省中医院耳鼻喉科行鼻内镜术患者5例,经知情同意后取其下鼻甲黏膜,生理盐水冲洗,除去表层血及组织黏液后进行粉碎,加入胶原酶,在36.8 ℃下培养4 h,5 ℃、3 000 r/min离心 5 min,吸弃上层清液,加入DMEM培养基,在36.8 ℃下培养4 h,去除成纤维组织,将悬浮细胞置于96孔板中,在36.8 ℃下培养36 h,再用含生长因子的培养基培养8 d。取鼻黏膜上皮细胞,随机分为化合物组(80 mg/L LPS+1、5、10 mg/L化合物)、对照组(80 mg/L LPS+等体积生理盐水)、阳性组(80 mg/L LPS +1 mg/mL苯环喹溴铵),采用 MTT法[20]测定化合物1、5、12、15对鼻黏膜上皮细胞的影响,将其置于96孔板中,在36.8 ℃下培养36 h后加入LPS+化合物1、5、12、15,80 mg/L LPS+等体积生理盐水,80 mg/L LPS +1 mg/mL苯环喹溴铵,孵育36 h后,加入15 μL含6 mg/mL MTT的PBS溶液,继续孵育4.0 h,移弃上层培养液,每孔加入100 μL DMSO,轻轻摇匀,在510 nm波长处检测光密度,计算细胞相对存活率,公式为细胞相对存活率=(化合物组光密度/对照组光密度)×100%。结果,5、10 mg/L化合物1及1、5、10 mg/L 化合物5可提高鼻黏膜上皮细胞的相对存活率,见表1。
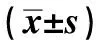
表1 各化合物对鼻黏膜上皮细胞的相对存活率的影响
5 讨论
本研究从甘露子中分离得到15个化合物,均为首次从该植物中分离得到,其中化合物1、4~5、10~11、14~15为首次从该属植物中分离得到。另外,5、10 mg/L化合物1及1、5、10 mg/L化合物5对鼻黏膜细胞具有保护作用。本研究丰富了甘露子化学成分的资料库,为修复鼻黏膜新药的开发提供了参考。

