信迪利单抗联合化疗对晚期非小细胞肺癌肿瘤标志物及免疫功能的影响
陈良新,孙 鹏,胡中舟
信阳市中心医院肿瘤内科,河南信阳 464000
肺癌是呼吸系统最常见的恶性肿瘤之一,病理类型多为非小细胞肺癌(NSCLC),占肺癌总发病率的80%以上[1]。晚期NSCLC主要以化疗为主,但是患者对化疗药物的反应和副作用各不相同,因此化疗的疗效和安全性存在显著差异[2]。随着基因技术的不断进步,越来越多的晚期NSCLC患者开始应用靶向药物治疗[3]。某些基因检测,如XPG基因检测,可作为NSCLC个体化治疗策略的预测指标[4]。目前,细胞程序性死亡受体-1(PD-1)/细胞程序性死亡受体-配体1(PD-L1)单克隆抗体广泛用于肺癌的治疗。信迪利单抗作为PD-1单克隆抗体可以与T细胞表面的PD-1特异性结合,进而阻断T细胞表面的PD-1与肿瘤细胞PD-L1的结合,使T细胞和自身免疫反应发挥正常功能,从而消除肿瘤细胞[5]。本研究通过对比晚期NSCLC治疗前后的肿瘤标志物和免疫功能的变化,旨在评价信迪利单抗联合化疗对晚期NSCLC的疗效,现报道如下。
1 资料与方法
1.1一般资料 经本院医学伦理委员会批准后,选取2019年11月至2020年11月本院收治的180例具有完整随访记录的晚期NSCLC患者,按照随机抽签法将患者分为观察组和对照组,每组90例。纳入标准:(1)符合晚期NSCLC的诊断标准[6];(2)患者无明显认知障碍,且签署知情同意书。排除标准:(1)伴糖尿病、心脑血管疾病等严重基础疾病者;(2)伴精神障碍,无法配合完成研究者;(3)伴其他恶性肿瘤等影响肿瘤标志物水平者;(4)伴慢性炎症性疾病、自身免疫性疾病等影响免疫因素水平者。2组性别构成、年龄、体质量和美国东部肿瘤协作组(ECOG)评分比较,差异均无统计学意义(P>0.05),具有可比性,见表1。

表1 2组一般资料比较
1.2方法 对照组接受常规GP(吉西他滨+顺铂)方案化疗,化疗前进行常规生化和血常规检查,血白细胞明显减少的患者另外行增加白细胞的药物治疗,化疗前1 d行水化治疗以降低不良反应。第1、8天静脉注射吉西他滨(1 g/m2),第1、2、3天静脉注射顺铂(25 mg/m2)。化疗期间,所有患者均接受心电监护、补液、不良反应处理等对症治疗。以21 d为1个疗程,持续治疗3个疗程[7]。观察组在接受常规GP化疗的基础上加用信迪利单抗200 mg静脉注射,每个疗程1次[8],持续治疗3个疗程。
治疗期间最常见的药物不良反应包括恶心、呕吐和胃溃疡。采用水化治疗、奥美拉唑等抑酸剂及以胃蛋白酶为代表的胃黏膜保护剂,防止胃溃疡和止吐。对于急性呕吐的患者,采用地塞米松或托烷司琼治疗。
1.3观察指标 观察并记录2组治疗前后患者血清肿瘤标志物[细胞角质蛋白19片段抗原21-1(CYFRA21-1)、癌胚抗原(CEA)、糖类抗原125(CA125)]、T细胞亚群指标(CD3+、CD4+、CD8+T细胞比例及CD4+/CD8+比值)变化及治疗后6个月时的临床疗效(近期疗效)。临床疗效判断标准[9]:完全缓解(CR),病变完全消失,肿瘤标志物检测结果恢复正常,并维持4周以上;部分缓解(PR),病变体积减小30.0%以上,维持4周以上;病情稳定(SD),病变体积减小<30.0%或增大<30.0%;病变进展(PD),病变体积增加30.0%以上或出现新病变;总有效率(RR)=(CR例数+PR例数)/患者例数×100.0%。

2 结 果
2.12组治疗前后血清肿瘤标志物变化 2组治疗后CCYFRA211、CEA、CA125水平均低于治疗前,且观察组低于对照组,差异均有统计学意义(P<0.05),见表2。
2.22组治疗前后T细胞亚群变化 观察组治疗后CD3+、CD4+T细胞比例及CD4+/CD8+比值高于治疗前,对照组则低于治疗前,且观察组高于对照组,差异均有统计学意义(P<0.05),见表3。
2.32组临床疗效比较 观察组CR率和RR高于对照组,PD率低于对照组,差异均有统计学意义(P<0.05),见表4。
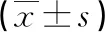
表 2 2组治疗前后血清肿瘤标志物水平比较
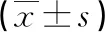
表3 2组治疗前后T细胞亚群水平比较

表4 2组临床疗效比较
3 讨 论
目前,化疗、靶向治疗和免疫治疗是晚期NSCLC的主要治疗方案,对于部分晚期NSCLC患者,化疗可改善预后和生存率,但也可能出现明显的不良反应[10]。有研究结果表明,联合治疗优于单独化疗,其安全性高,不良反应少[11]。近年来,越来越多的肺癌诊疗指南推荐使用靶向药物和免疫药物联合治疗晚期NSCLC患者[12],与靶向药物直接攻击肿瘤细胞靶点不同,免疫治疗的主要目的是调节患者自身免疫状态,从而清除肿瘤细胞。PD-1主要在免疫细胞表面表达,而PD-L1主要在肿瘤细胞表面表达,PD-1和PDL-1结合激活了免疫细胞的信号通路,使肿瘤细胞逃避了免疫系统的攻击[13]。
以生物标志物为导向的靶向治疗和免疫治疗提高了转移性NSCLC患者的总生存率[14]。PD-1单克隆抗体作为免疫治疗药物,已获国家食品药品监督管理局批准用于NSCLC患者的临床治疗,它特异性地阻断PD-1抑制途径,恢复T细胞的免疫功能,进而抑制肿瘤细胞[15]。刘双庆等[16]的研究证实了免疫检查点阻断治疗在NSCLC中取得了明显的临床效果。在本研究中,观察组治疗后T细胞亚群CD3+、CD4+T细胞比例及CD4+/CD8+比值较治疗前升高,且观察组高于对照组,差异均有统计学意义(P<0.05);观察组CR率和RR高于对照组,PD率低于对照组,差异均有统计学意义(P<0.05)。研究结果证明PD-1单克隆抗体有助于改善和调节细胞免疫功能,发挥杀死肿瘤细胞、抑制肿瘤进展的作用,在此基础上可以获得满意的临床疗效。有研究表明,CEA联合CYFRA211有助于肺腺癌的辅助诊断,CA125与转移有关,肿瘤标志物的降低也表明治疗有效,患者预后良好[17]。在本研究中,观察组治疗后血清肿瘤标志物CCYFRA211、CEA、CA125水平比对照组下降更明显,差异均有统计学意义(P<0.05),提示信迪利单抗联合化疗比单纯化疗效果更好。但本研究存在一些局限性,如研究样本量小,随访时间短。下一步将扩大样本量、延长随访时间,进一步研究信迪利单抗联合化疗对晚期NSCLC肿瘤标志物及免疫功能的影响。
综上所述,信迪利单抗联合GP化疗方案治疗晚期NSCLC疗效显著,该方案可显著降低血清肿瘤标志物水平,提高患者免疫功能和治疗总有效率,值得临床推广。

