辛鹅温敏原位凝胶经鼻给药后木兰脂素血浆含量的测定及药动学研究
颜红 彭志荣 高司琪 骆慧婷 欧阳威


〔摘要〕 目的 建立辛鵝温敏原位凝胶经鼻给药后大鼠血浆中木兰脂素的液相色谱-串联质谱(liquid chromatography mass spectrometry/mass spectrometry, LC-MS/MS)检测方法,并探讨其在大鼠体内的药动学特性。方法 大鼠滴鼻给予辛鹅鼻用温敏原位凝胶(1.5 mL/kg)后于不同时间点腹主动脉取血,应用梯度洗脱程序进行色谱分离,用LC-MS/MS技术检测,以采样时间对血药浓度建立药-时曲线,采用DPS 15.10软件计算药动学参数。结果 在2~500 ng/mL范围内,木兰脂素与内标的峰面积比值与浓度的线性关系良好。大鼠滴鼻给予辛鹅鼻用温敏原位凝胶,其主要药动学参数分别为达峰时间T为(0.46±0.03) h,达峰浓度C为(230.83±55.17) ng/mL,半衰期T为(2.98±0.43) h,体内平均驻留时间MRT为(4.30±0.62) h,药-时曲线下面积值AUC为(1 035.34±200.65) ng·h/mL、AUC为(1089.22±201.00) ng·h/mL,总清除率CL为(1278.30±226.46) L/(kg·h)。结论 建立的LC-MS/MS检测方法灵敏度高、专属性强,适用于大鼠体内的木兰脂素药动学研究。辛鹅温敏原位凝胶经鼻给药后,木兰脂素在大鼠体内的过程符合一室模型。
〔关键词〕 原位凝胶;辛夷;鹅不食草;木兰脂素;药动学;液相色谱-串联质谱;血药浓度
〔中图分类号〕R285.5 〔文献标志码〕A 〔文章编号〕doi:10.3969/j.issn.1674-070X.2022.04.009
Study on content determination and pharmacokinetics of magnolin in rat plasmafrom Xinyi (Magnoliae Flos)-Ebushicao (Centipedae Herba) thermosensitive in situ gels after intranasal administration
YAN Hong, PENG Zhirong, GAO Siqi, LUO Huiting, OUYANG Wei
(School of Pharmacy, Hunan University of Chinese Medicine, Changsha, Hunan 410208, China)
〔Abstract〕 Objective To establish a liquid chromatography mass spectrometry/mass spectrometry (LC-MS/MS) method for determination of magnolin and study its pharmacokinetics after intranasal delivery of Xinyi (Magnoliae Flos)-Ebushicao (Centipedae Herba) thermosensitive in situ gels. Methods Blood samples were taken from abdominal aorta at different time points after intranasal delivery of Xinyi (Magnoliae Flos)-Ebushicao (Centipedae Herba) thermosensitive in situ gels in rats (1.5 mL/kg). The gradient elution program was used for chromatographic separation. The LC-MS/MS was applicated for detection. The plasma drug concentration-time curve was established by the sampling time to blood drug concentration. The pharmacokinetic parameters were obtained calculated with DPS 15.10 software. Results There was a good linear relationship between peak area ratio and concentration of magnolin and internal standard within range of 2~500 ng/mL. After intranasal administration of Xinyi (Magnoliae Flos)-Ebushicao (Centipedae Herba) thermosensitive in situ gels in rats, the main pharmacokinetics parameters were as follows: the peak time T was (0.46±0.03) h, the peak concentration C was (230.83±55.17) ng/mL, the half-life T was (2.98±0.43) h, the average residence time MRT was (4.30±0.62) h, the area under the drug-time curve AUC was (1035.34±200.65) ng·h/mL, AUC was (1089.22±201.00) ng·h/mL, and the total clearance CL was (1278.30±226.46) L/(kg·h). Conclusion The established LC-MS/MS method has the high sensitivity and strong specificity, and it can be used for the pharmacokinetic study of magnolin in rats. The process of magnolin in rats conforms to one-compartment model after intranasal delivery of Xinyi (Magnoliae Flos)-Ebushicao (Centipedae Herba) thermosensitive in situ gels.
〔Keywords〕 in situ gel; Xinyi (Magnoliae Flos); Ebushicao (Centipedae Herba); magnolin; pharmacokinetics; liquid chromatography mass spectrometry/mass spectrometry; plasma concentration
辛鹅鼻用温敏原位凝胶源于临床经验方[1],由辛夷与鹅不食草两味药材组方而成,辛夷的主要有效成分为木兰脂素,鹅不食草的主要成分为挥发油类。辛夷与鹅不食草均具有发散风寒、宣通鼻窍之功效[2-5],临床多用于治疗风寒头痛、鼻塞流涕、鼻鼽、鼻渊等。温敏原位凝胶剂是一种具有临界相转变温度的原位凝胶,它可在临界相转变温度附近由液体状态突变为半固体状态,可使凝胶黏附于鼻黏膜表面,具有延长药物滞留时间、使用方便、组织相容性和生物黏附性好等优点[6-9]。
本实验前期已成功制备了辛鹅鼻用温敏原位凝胶,其pH值、胶凝温度、黏度均适宜,常温下呈液体,预期给药后可迅速在鼻黏膜上形成凝胶,体外释药实验表明其具有一定的缓释作用,可延长药物在鼻腔内滞留的时间[10]。为进一步考察辛鹅鼻用温敏原位凝胶经鼻给药后的体内过程,为制剂的开发提供参考,本项目建立了辛鹅温敏原位凝胶经鼻给药后大鼠血浆中木兰脂素的液相色谱-串联质谱(liquid chromatography mass spectrometry/mass spectrometry, LC-MS/MS)检测方法,并开展了其药动学研究。
1 材料
1.1 仪器与试剂
Agilent 1290超高效液相色谱系统串联6460三重四级杆质谱仪(美国安捷伦科技有限公司);TG16MW台式高速离心机(湖南赫西仪器装备有限公司);UGC-24CF防腐型24位圆形氮吹仪(北京优晟联合科技有限公司)。
辛鹅鼻用温敏原位凝胶(实验室自制);木兰脂素对照品(中国食品药品检定研究院,批号:110882-201708,纯度:96.5%);托特罗定(上海紫霞生物科技有限公司,批号:E013520,纯度:94%);甲醇(美国斯百全公司,批号:3HG0013,纯度:99.9%);乙腈(美国天地公司,批号:21125090,纯度:99.9%)为色谱纯;甲酸(国药集团化学试剂有限公司,批号:40023774,纯度:99.5%)为分析纯。
1.2 实验动物
雄性SD大鼠66只,体质量230~270 g,由湖南斯莱克景达实验动物有限公司提供,许可证号SCXK(湘)2016-0002,实验动物使用环境合格证号SYXK(湘)2013-0005。
2 方法
2.1 辛鹅鼻用温敏原位凝胶的制备
课题组前期已开展辛鹅鼻用温敏原位凝胶的制备工艺与处方的优选[10],具体操作如下:称取处方量2%辛夷与鹅不食草复方提取物、0.4%混合挥发油、1%吐温-80、15% 1,2-丙二醇、0.04%苯扎溴铵溶于双蒸水中,加入处方量15%泊洛沙姆P407、1% P188作为基质,补加双蒸水至总处方量,置于4 ℃冰箱中冷藏过夜,即得凝胶。
2.2 大鼠血浆中木兰脂素LC-MS/MS测定
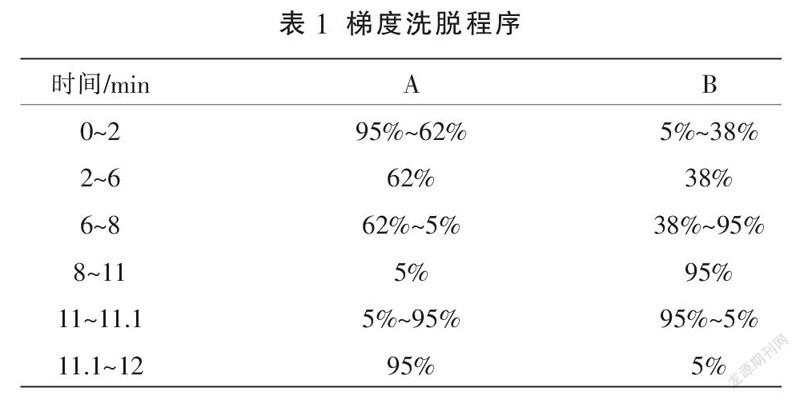
2.2.1 色谱与质谱条件 色谱柱为Zorbax RRHD Extend-C(2.1 mm×50 mm,1.8 μm),流动相为0.1%甲酸水溶液(A相)-乙腈(B相),柱温35 ℃,体积流量0.3 mL/min,进样量2 μL,梯度洗脱程序见表1。
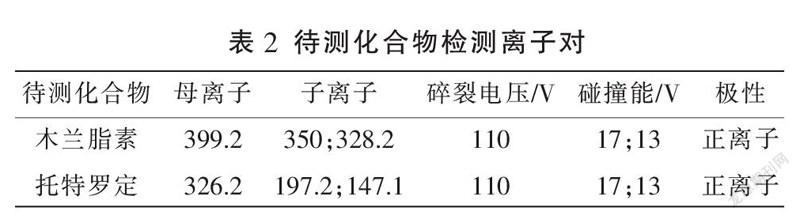
质谱检测采用电喷雾离子化正离子(ESI+)模式,多反应监测(multiple reaction monitoring, MRM)方式。毛细管电压为4 kV,离子源干燥气温度为345 ℃,干燥气气流12 L/min,雾化气50 psi。待测化合物检测离子对见表2。
2.2.2 對照溶液的配制 木兰脂素对照品母液:精确称取0.010 1 g木兰脂素对照品(纯度为96.5%)置10 mL容量瓶中,甲醇定容至刻度,即得0.974 7 mg/mL的木兰脂素对照品母液。内标托特罗定对照品母液:精确称取0.005 0 g托特罗定对照品(纯度为94.0%)置25 mL容量瓶中,甲醇定容至刻度,即得0.188 0 mg/mL的内标托特罗定对照品母液。
2.2.3 大鼠血浆样品的处理 取大鼠血浆,精确吸取100 μL血浆样品于EP管中,加入20 μL托特罗定溶液作为内标(3 μg/L),再加入370 μL乙腈沉淀蛋白,涡旋振荡3 min,超声15 min,以12 000 r/min离心10 min(离心半径6 cm),取上清液400 μL至EP管,置于氮吹仪中,用氮气吹干后加入160 μL乙腈复溶,涡旋震荡5 min,12 000 r/min离心10 min(离心半径6 cm),过0.22 μm有机膜,上机检测。
2.2.4 方法学考察[11-13] (1)专属性考察:取大鼠空白血浆,除不加内标溶液外,其余按“2.2.3”项下方法处理,上机检测,获得空白血浆MRM图;将一定浓度托特罗定内标溶液和木兰脂素对照品溶液加入大鼠空白血浆中,同法操作,上机检测,获得空白血浆加内标与木兰脂素对照品的MRM图;取大鼠给药后的血浆,同法操作,上机检测,获得给药后大鼠含药血浆的MRM图。
(2)线性关系和定量下限的考察:精确吸取100 μL空白血浆,加入20 μL托特罗定作为内标(3 μg/L)和10 μL含有不同质量木兰脂素对照品的单标,再加入370 μL乙腈沉淀蛋白,涡旋3 min,超声15 min,12 000 r/min离心10 min(离心半径6 cm),取出上清液400 μL,氮气吹干后加入160 μL乙腈复溶,涡旋5 min,12 000 r/min离心10 min(离心半径6 cm),配制成含木兰脂素不同质量浓度(2、5、10、25、50、125、250、500 ng/mL)的基质单标溶液。分别进样测定,记录峰面积。
(3)精密度考察:取“2.2.4(2)”项下制备的低、中、高3个质量浓度(5、50、500 ng/mL)的基质单标溶液,分别在24、48 h内重复进样6次,进样检测,记录峰面积,计算各浓度峰面积的RSD值。
(4)加样回收与基质效应试验:取大鼠空白血浆,按“2.2.4(2)”项下方法处理,分别加入含不同浓度的木兰脂素乙腈溶液,配制成浓度为5、50、500 ng/mL的样品,计算各化合物的实际质量浓度和理论质量浓度的比值作为加样回收率。
精确吸取100 μL空白血浆于EP管中,加入400 μL乙腈沉淀蛋白,涡旋3 min,超声15 min,12 000 r/min离心10 min(离心半径6 cm),得到基质提取液,再用基质提取液稀释木兰脂素标准储备液至低、中、高3个质量浓度(5、50、500 ng/mL),每个浓度平行6份,进样检测记录峰面积。此外,将木兰脂素标准储备液用乙腈稀释得5、50、500 ng/mL 3个浓度,每个浓度平行6份。以基质提取液稀释的木兰脂素峰面积与乙腈稀释的木兰脂素峰面积的比值计算基质效应。
(5)稳定性试验:取“2.2.4(2)”项下制备的低、中、高3个质量浓度(5、50、500 ng/mL)的基质单标溶液,每个浓度平行6份,分别考察4 ℃放置0、12、24 h,样品-70 ℃冰冻21 d以及冻融稳定性。在设定的考察时间进样检测,记录峰面积,计算RSD值。
2.3 大鼠滴鼻给予辛鹅鼻用温敏原位凝胶药动学实验
2.3.1 给药方法 受试大鼠隔夜禁食后,每只大鼠两鼻各滴鼻给予辛鹅鼻用温敏原位凝胶1.5 mL/kg。
2.3.2 樣品采集 每6只大鼠分为一平行时间组,分别于给药后0、5、15、30 min及1、1.5、2、4、8、12、24 h腹主动脉取血,置于肝素化的离心管中,3 000 r/min离心10 min(离心半径6 cm),分离上层血浆,置
-70 °C冰箱中保存待测。
2.3.3 血药浓度测定 采用LC-MS/MS技术,按所建立的血药浓度检测方法测定大鼠经滴鼻给予辛鹅鼻用温敏原位凝胶后血浆中的木兰脂素浓度。
2.3.4 数据处理 主要药动学参数达峰浓度(Cmax)、达峰时间(T)为实测值,药-时曲线下面积(AUC)、半衰期(T)、清除率(CL)、体内平均驻留时间(MRT)经DPS 15.10拟合计算。
3 结果
3.1 方法学考察
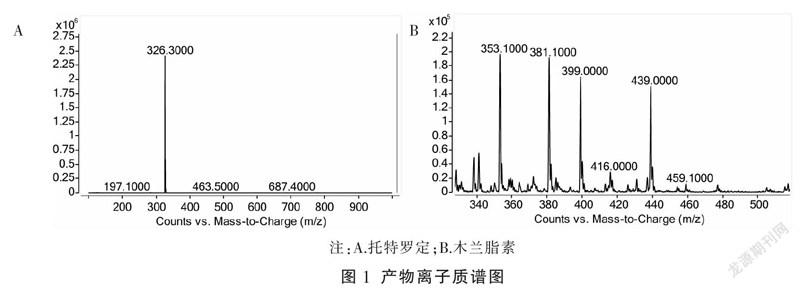
3.1.1 方法的专属性 在本实验所采用的色谱条件下,木兰脂素的保留时间约为4.82 min,内标托特罗定的保留时间约为2.65 min。木兰脂素、内标托特罗定峰形良好,无杂峰干扰测定,基线平稳,分析方法具有良好的专属性。产物离子质谱图及MRM图分别见图1、图2。
3.1.2 标准曲线、线性范围及定量下限 以对照品与内标的峰面积之比为纵坐标(Y),对照品浓度为横坐标(X),进行线性回归,木兰脂素在2~500 ng/mL范围内线性关系良好,标准曲线方程为:Y=0.4494X+5.134 1(R=0.999 8),权重系数W为1/c。血浆中木兰脂素最低定量限为2 ng/mL。
3.1.3 精密度试验结果 木兰脂素的低、中、高3个质量浓度(5、50、500 ng/mL)的基质单标溶液在24 h内峰面积的RSD值分别为2.35%、3.20%、2.57%;48 h内峰面积的RSD值分别为5.58%、2.11%、1.47%。
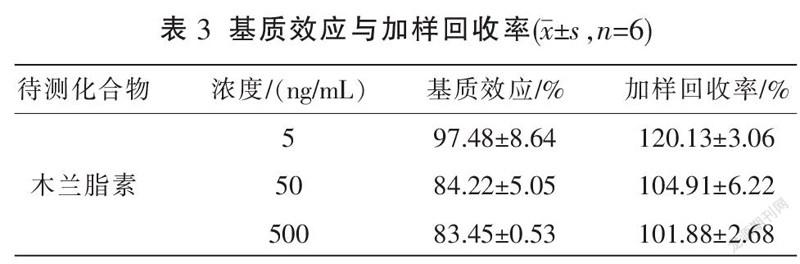
3.1.4 加样回收与基质效应试验结果 木兰脂素在低、中、高3个质量浓度下(5、50、500 ng/mL)的基质效应分别为97.43%、84.15%、83.45%,均在80%~120%范围之内,表明本方法可有效避免基质对木兰脂素测定的影响。同时,木兰脂素的低、中、高3个质量浓度的加样回收率分别为120%、105%及102%,符合生物样品分析要求,加样回收与基质效应结果见表3。
3.1.5 稳定性试验结果 木兰脂素的低、中、高3个质量浓度(5、50、500 ng/mL)的基质单标溶液4 ℃放置峰面积的RSD值分别为4.23%、3.51%、4.21%,表明木兰脂素在该条件下稳定;-70 ℃短期冰冻低、中、高3个质量浓度测定结果RSD分别为1.59%、2.75%、2.54%,表明样品在-70 ℃冰冻环境下可短期稳定存放;低、中、高3个质量浓度在反复3次冻融后的测定结果RSD分别为3.70%、1.48%、2.17%,表明样品在反复冻融3次后仍保持稳定。
3.2 血药浓度时间曲线
大鼠两鼻经滴鼻给予辛鹅鼻用温敏原位凝胶(1.5 mL/kg)后30 min左右达最大吸收,Cmax约为230 ng/mL,木兰脂素的平均血药浓度时间曲线见图3。
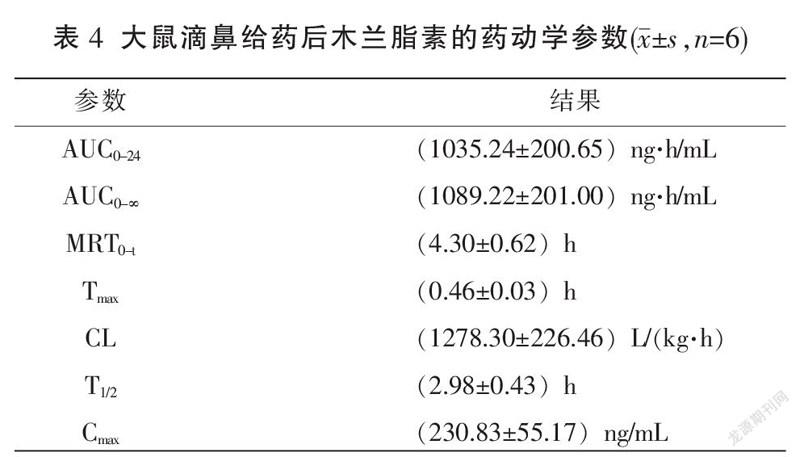
3.3 药动学参数
DPS数据处理系统一室模型拟合决定系数为94.02%(>90%),且拟合系数较其他模型更高,故采用一室模型拟合计算大鼠给药后的药动学参数,所得药动学参数见表4。
4 讨论
温敏原位凝胶剂是一种具有临界相转变温度的原位凝胶,其在临界相转变温度附近,可由液体状态突变为半固体状态,形成凝胶黏附于鼻黏膜表面,具有延长药效、工艺简单、生物相容性好等优点,是一种具有良好应用前景的新型鼻用制剂[14-17]。
木兰脂素为制剂中辛夷的主要有效成分,本实验采用LC-MS/MS技术建立了大鼠血浆中木兰脂素的检测方法。结合预实验结果,采用梯度洗脱对组分进行分离,采用MRM模式,以托特罗定为内标[M+H]+(m/z 326.2 /147.1)对血浆中木兰脂素进行检测,木兰脂素、内标托特罗定峰形良好,无杂峰干扰测定,基线平稳,专属性强;分析方法可消除制剂中其他成分及血浆内源性物质的干扰,无明显的基质效应;在血浆用量100 μL的情况下检测灵敏度可达2.0 ng/mL,相比于文献报道[18]的高效液相色谱法更灵敏。精密度及加样回收率测定结果均符合现行生物分析方法的相关规定[19-20]。建立的检测方法可为辛鹅鼻用温敏原位凝胶在大鼠体内的药动学分析提供一种有效手段。此外,目前关于木兰脂素活性单体的系统研究甚少,作为辛夷的主要有效成分,本实验亦可为辛夷制剂的研究奠定药动学基础。
本实验首次采用LC-MS/MS检测方法对中药制剂给药后大鼠体内的木兰脂素进行药动学研究,实验结果表明大鼠经滴鼻给予辛鹅鼻用温敏原位凝胶(1.5 mL/kg)后,主要有效成分木兰脂素在体内的过程符合一室模型,T为(0.46±0.03) h,C为(230.83±55.17) ng/mL,T为(2.98±0.43) h,MRT为(4.30±0.62) h,AUC为(1035.34±200.65) ng·h/mL,CL为(1278.30±226.46) L/(kg·h),以上药动学实验结果可为制剂的临床用药方案提供实验依据。
参考文献
[1] 广东省科技成果展览会医疗卫生馆.中草药处方选编[M].广州: 广东省科技成果展览会医疗卫生馆,1970:52.
[2] 周毅叶,王 祺,贾妍卓,等.基于网络药理学的辛夷治疗过敏性鼻炎作用机制研究[J].中國中医药信息杂志,2021,28(3):33-39.
[3] 张莉莉,金籽杉,于同月,等.辛夷、鹅不食草、苍耳子治疗鼻炎:仝小林三味小方撷萃[J].吉林中医药,2020,40(12):1553-1555.
[4] 赵晓华,顾成娟,朴春丽,等.态靶辨证在过敏性鼻炎风寒湿型的运用:麻黄附子细辛汤加鹅不食草、辛夷[J].辽宁中医杂志,2020,47(7):3-5.
[5] 汪 娟,陈 涛.辛夷汤结合督脉灸治疗过敏性鼻炎临床疗效及对炎症因子及免疫因子、复发情况影响研究[J].四川中医,2021,39(11):196-199.
[6] 韩胜男,李喜香,闫治攀,等.原位凝胶剂的研究概况[J].西部中医药,2021,34(1):153-157.
[7] 许 欢,张永萍,程 纯,等.原位凝胶给药系统的研究进展[J].湖北民族大学学报(医学版),2021,38(3):81-85.
[8] 宋 亚,祁小乐,沙 康,等.温度敏感型原位凝胶药物递送系统的研究进展[J].国际药学研究杂志,2019,46(4):245-255..
[9] 杨博渊,陈 斌,徐 朋,等.原位凝胶技术的发展和相关产品研究进展[J].中国新药杂志,2020,29(17):1964-1971.
[10] 袁佳敏,黄星雨,周宇婷,等.辛鹅鼻用温敏原位凝胶的制备[J].中成药,2018,40(12):2656-2662.
[11] ZHOU Q, YAN H, LI R, et al. A sensitive LC-MS-MS method for quantification of 1,6-O,O-diacetylbritannilactone in rat plasma and its application in a pharmacokinetic study[J]. Journal of Chromatographic Science, 2018, 56(3): 242-247.
[12] 王培乐,孙会婷,高梅梅,等.UPLC-MS/MS测定特发性肺纤维患者血浆中吡非尼酮及其代谢物的含量及药动学研究[J].中国药学杂志,2021,56(8):675-681.
[13] 夏丽琼,徐长琼,任秋芸,等.基于UPLC-MS/MS技术的张氏消肿定痛膏物质基础研究[J].湖南中医药大学学报,2021,41(11):1705-1710.
[14] 朱卫丰,刘水婷,王万春,等.黄白温敏型原位凝胶的处方筛选与评价[J].中草药,2021,52(7):1914-1923.
[15] 张利竣,吴盈盈,吴瑾瑾,等.灯盏花素温敏型鼻用原位凝胶的体外释放和生物黏附性考察[J].中国现代应用药学,2020,37(23):2863-2867.
[16] YU Y, CHENG Y, TONG J, et al. Recent advances in thermo-sensitive hydrogels for drug delivery[J]. Journal of Materials Chemistry B, 2021, 9(13): 2979-2992.
[17] 丛志新,樊慧敏,吴春芝,等.原位凝胶剂的研究现状与应用前景[J].中南药学,2018,16(9):1185-1190.
[18] 俞 瑜,袁浩宇,曾健鹏.木兰脂素在大鼠体内的药动学研究[J].中国药房,2015,26(25):3522-3524.
[19] 刘淑洁,闻 镍,王 宇,等.高效液相色谱-串联质谱法定量测定大鼠血浆中LMV-12(HE003)及其代谢产物M4[J].中国医药生物技术,2021,16(5):426-432.
[20] CHEN Y H, BI J H, XIE M, et al. Classification-based strategies to simplify complex traditional Chinese medicine (TCM) researches through liquid chromatography-mass spectrometry in the last decade (2011-2020): Theory, technical route and difficulty[J]. Journal of Chromatography A, 2021, 1651: 462307.

