基于系统思维培养的“盐类水解”内容分析与教学建议
纪崧杰 卢姗姗 杜明成
摘要: 在界定盐类水解系统的基础上,阐述系统思维的具体内涵与水平,从复杂系统的结构、行为和功能三方面解析盐类水解系统。基于系统思维的识别系统组织、分析系统行为和建立系统模型三个维度进一步阐释教材内容并提供若干教学建议。
关键词: 系统思维; 盐类水解; 内容分析; 教学建议
文章编号: 10056629(2022)07002805
中图分类号: G633.8
文献标识码: B
盐类水解是中学化学教学的重点和难点。《普通高中化学课程标准(2017年版)》(简称“课程标准”)对盐类水解内容的教学建议是促进学生认识水溶液中的平衡以此培养学生的系统思维能力[1]。该内容蕴含着培养学生系统思维能力的价值,学生具备系统思维能够更好地理解盐类水解,从而克服学习困难。
1 系统与系统思维
“系统”,是系统科学中的基本概念。在自然辨证法中,系统是指由若干个相互联系、相互作用的要素构成的有机整体;而化学科学中常把以一定质量和种类的物质组成的整体看作系统[2]。例如,像溶液这类由一定质量和种类的溶质与溶剂构成的均一、稳定的混合物就是一种系统。对一个自然或人为的系统,Jaradat等人(2015)[3]认为需要从三个方面进行研究: (1)从系统的结构来看,系统具有复杂性、相互联系性、整合性和模糊性;(2)从系统的行为来看,系统具有动态性和发展性;(3)从系统的功能来看,系统具有不确定性和非预期性。一个系统之所以被认为是复杂的,也是由这三个方面引起的[4]。
系统思维与系统之间则是思维方式和思维对象的关系。系统思维的起源可以追溯到为解决复杂问题而产生的系统理论,虽然在学术界没有统一的定义,但在发展过程中逐渐被生物学、教育学、心理学和社会学等诸多学科接受,产生了不同的内涵。从哲学的视角来看,系统思维是一套可以用来整理思想的概念框架,能够让个体将所研究的对象看作系统,既考察对象的整体性,又注重把握系统内各部分之间的互动关系,进而形成系统化的思维成果[5]。从心理学相关研究看,系统思维作为一种高阶思维能力,使个体在思考过程中关注不同要素之间的关系,随后将各要素整合成一个整体来研究,与个体心智模型的发展、思维过程与问题解决过程都存在联系[6]。
在科学教育领域,Mambrey等人(2020)[7]总结学生的系统思维包括三个方面: (1)识别系统组织及结构;(2)分析系统行为;(3)建立系统模型。这一内涵也在化学教育领域得以发展和应用[8]。首先,识别系统组织及结构。识别是对系统中要素的准确把握和区分,应能准确判断和知道复杂系统中的要素,具体表现为能够确定系统中的要素,能够知道要素在系统中的地位,能够理解系统中的隐藏要素;其次,分析系统行为。分析是将系统中的要素拆分后,找出要素的本质属性以及彼此之间的关系,具体表现为能够明确哪些要素之间会发生关系,哪些要素之间不会发生关系,能够分析系统内部的动态关系,理解系统循环及发展的本质;最后,建立系统模型。模型有助于学生认识系统的功能和对系统达到整体性的认识。当学生面临新的问题情境时,对系统建立的模型则具有认知功能,帮助学生形成分析问题和解决问题的整体思路。
2 盐类水解的内容分析
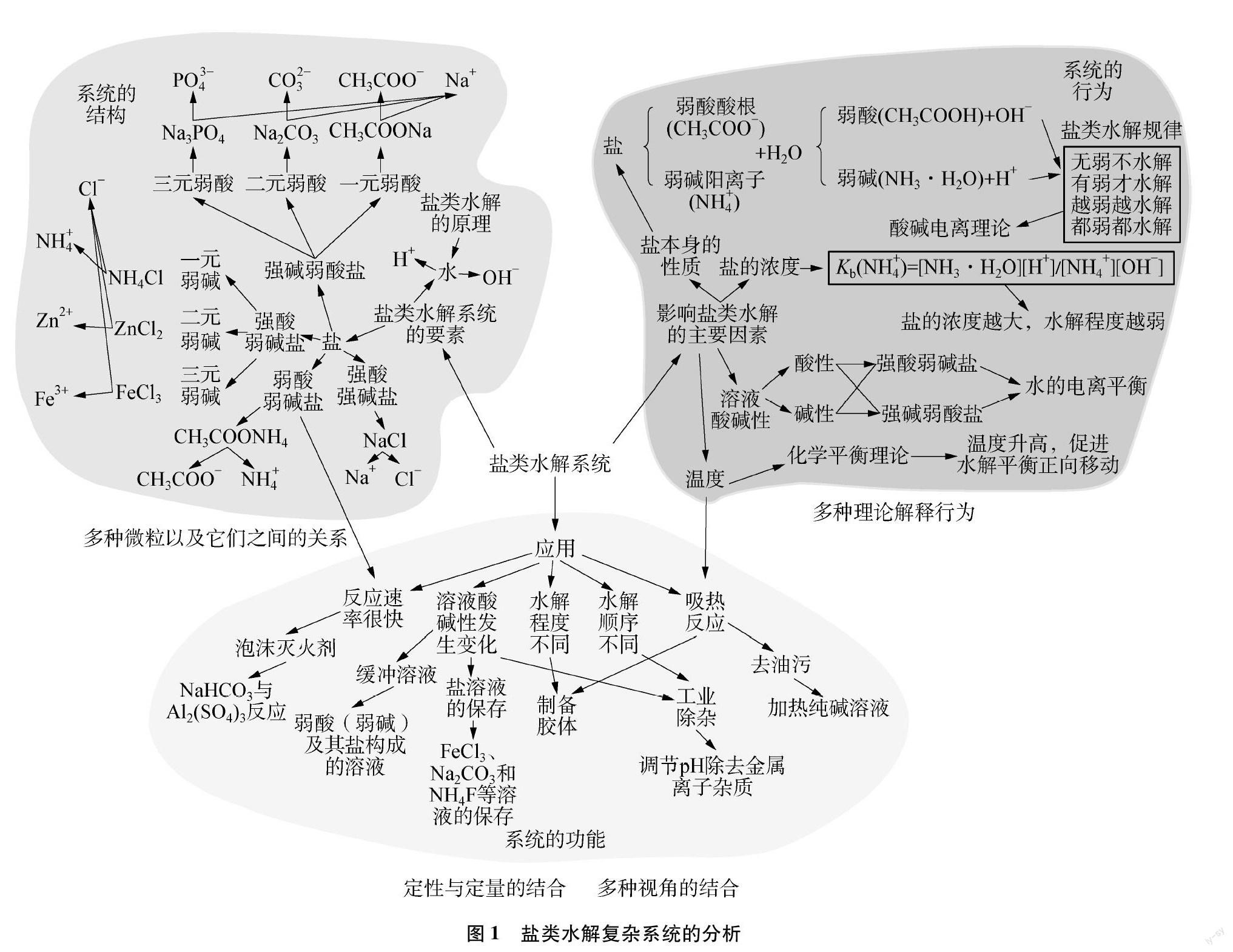
根据以上对系统的定义,盐类水解是盐和水组成的系统整体表现出的一种特性,属于水溶液体系中的一种。将盐类水解看作系统,按照上述Jaradat等人的分析标准,对该系统的结构、行为和功能所涉及到的课程内容进行分析。整体结果如图1所示。
2.1 系统的结构: 涉及多种微粒及相互作用
从系统的结构来看,盐类水解系统涉及到弱电解质的电离和水的电离两个子系统,原理是盐电离产生的弱酸酸根离子或弱碱阳离子对水的电离平衡的影响,涉及到多种类型的微粒(要素)以及微粒(要素)之间不同形式的相互关系。具体来说:
(1) 系统的要素是复杂的。从水溶液体系来看,包括溶质(盐)和溶剂(水)。盐包含四类,不同类型的盐电离出来的离子又具有不同的性质,例如强碱弱酸盐电离产生弱酸酸根离子(如CH3COO-)和强碱阳离子(如Na+)。分子包括弱电解质分子(例如CH3COOH、 NH3·H2O和H2O)。如果从多元酸或者碱的角度看,离子变得更加复杂,例如二元弱酸酸根CO2-3,在水解过程中还会生成HCO-3。
(2) 微粒间的相互联系是复杂的。包括溶剂对溶质的作用,例如水分子对构成盐的离子作用发生盐的溶解和电离,水分子对弱电解质的分子作用发生弱电解质电离;又包括溶质与溶质的作用,例如两种及两种以上盐溶液的离子间发生离子反应;还包括溶质对溶剂的相互作用,例如弱电解质离子对水分子作用发生水解;另外,水分子与水分子之间相互作用也存在电离平衡。
(3) 結构具有整合性。需要对溶液中微粒及存在数量、存在状态进行整体把握。盐类水解是水的电离平衡、弱电解质的电离平衡、溶解平衡等各种情况的综合体现。涉及到电荷守恒、物料守恒和质子守恒等关系。
(4) 结构具有模糊性。由于盐类水解反应的程度非常微小,有些微粒在溶液中存在的量非常少,在处理复杂系统的时候可以忽略不计,但是不代表这些微粒不存在,至于在什么情况下将这些微粒忽略不计是模糊的。
2.2 系统的行为: 涉及多种理论加以解释
从复杂系统的行为来看,在盐类水解系统中两种弱电解质(水和弱酸或弱碱)的电离平衡竞争溶液中的H+或OH-,改变条件(例如温度、浓度、酸碱性等)会影响两种电离平衡状态,从而产生不同的水解结果。具体来说:
(1) 系统具有动态性。盐类水解系统的动态属性是各种平衡状态的集合,这种平衡属于动态平衡。平衡状态下,系统中发生的水解反应正、逆反应速率相等,各微粒的浓度不再发生变化。但溶液中各微粒间的动态关系依然存在并始终发生着微粒间的相互作用。对盐类水解动态平衡的把握和解释需要综合用到酸碱电离理论、化学平衡理论等。
(2) 系统具有发展性。系统在发展过程中具有复杂性,具体体现在改变不同的条件对系统的发展趋势的影响是不同的,于是形成了各种原理和规律。例如,盐的浓度越大,水解程度越小;温度越高,水解程度越大。这种发展趋势可以用盐类水解的规律来把握,例如“无弱不水解,有弱才水解”“越弱越水解,都弱都水解”以及水解平衡常数Kh。
2.3 系统的功能: 涉及多种视角解决问题
从复杂系统的功能来看,盐类水解系统在生产、生活实际中有着广泛的应用,例如净水、工业除杂、人体内的酸碱平衡等。这些应用与盐类水解反应的基本特征和反应结果相关。从能量变化和物质变化的角度看,盐类水解反应为吸热反应,反应程度很小且反应速率很快。由于弱酸酸根(弱碱阳离子)对应的弱酸(弱碱)酸(碱)性不同,这就使不同的盐类水解反应对溶液酸碱性的改变程度不同,反应结果存在差异。此外,在多种离子共存的溶液中,离子之间的水解程度和水解顺序也不同。这些性质在应用于生产、生活实际的过程中会使系统受到情境的影响。
(1) 系统具有不确定性。在不同情境下,系统有着不确定的内容,会影响个体对系统功能和相互关系的理解。例如,学生若不知道人体血液中存在着H2CO3NaHCO3等体系,便无法进一步理解人体中缓冲溶液系统具有的行为和相互关系。
(2) 系统具有非预期性。由于系统本身的复杂性、相互联系性和模糊性等属性,导致系统中有些结果很难预料到,或者与自己预期的结果不同。盐类水解系统的非预期性着重体现在对不同情境中盐溶液的分析上。例如,学生在判断陌生的酸式盐溶液的酸碱性时,需要分析具体的盐溶液中酸式盐酸根离子电离程度和水解程度的相对大小才能够作出判断,无法直接根据盐类水解的规律预测溶液的酸碱性。不同的酸式盐酸根离子电离程度与水解程度不同,如HSO-3的电离程度大于水解程度,而HCO-3的水解程度大于电离程度。
盐类水解系统在与生产、生活实际相结合后更具不确定性和非预期性。因此,从学生学习的角度来看,则需要利用系统思维分析不同情境中的电解质溶液,利用盐类水解相关知识开展更高水平的迁移创新活动。
3 盐类水解的教学建议
学生系统思维的发展需要课程内容的输入和学习活动的参与。课程标准中的内容要求是学生预期要学习的主题内容,学业要求代表着学生学习完主题内容后应该具有的素养发展表现。内容要求与学业要求二者之间具有“输入”和“输出”的承接关系[9]。从学习内容的“输入”到“输出”,隐含着学生系统思维能力的发展和提升。基于学生系统思维的培养,开展盐类水解的教学,提出以下几点建议。
3.1 引导学生准确识别微粒的特性,理解盐类水解原理
(1) 全面识别系统中的要素。这一点是认识盐类水解首要的并且非常关键的一步。根据已有对学生盐类水解的学习困难分析发现,学生经常会忽视H+、 OH-、 H2O三类要素。一个原因是由于H+、 OH-在水溶液的数量很少,学生对少量的微粒缺乏重视;另一个原因是学生从初中溶液的学习过程中就经常性地忽视水分子在系统中的作用。而理解盐类水解反应的关键,恰好是在学生容易忽视的三种微粒上。在教学中可以让学生以不同盐溶液的酸碱性为基础,利用宏观水平上溶液pH的差异认识到溶液中H+、 OH-和H2O的存在。初步根据溶液酸碱性差异分析溶液中存在的微粒和预测微粒间可能发生的相互作用。
(2) 区别不同微粒的特征及相互之间的关系。盐溶液中的微粒,并不是全部参与水解反应,学生在全面识别系统要素的基础上,还要准确把握不同微粒的特征,并且能够识别出发生水解的关键微粒。在以往的教学中,通常以CH3COONa和NH4Cl溶液为例,直接告知或者通过启发引导学生得出发生反应的微粒是CH3COO-和NH+4。但从培养学生系统思维的视角来看,应引导学生首先对不同微粒的特征进行分析,例如对Na+的分析,它是带有一个正电荷的阳离子,在水溶液中不与其他微粒结合形成分子或者沉淀;CH3COO-是带有一个负电荷的阴离子,对应的酸为弱电解质,能在溶液中与H+结合建立动态平衡。从而识别并明确微粒间的电离平衡、水解平衡和离子反应等关系,依据这些关系理解溶液中哪些微粒参与水解反应,哪些微粒不参与水解反应,并从微观层面认识水解反应的最终结果是H+和OH-浓度的关系发生了变化。
(3) 认识到盐溶液体系中包含隐藏的维度。第一,在中学化学阶段,盐类水解相关内容是根据电离理论的框架来解释的。盐类水解系统中所发生的真实情况也不一定与教材中的描述完全一致。例如,酸碱质子理论则认为H+以水合离子的形式存在。第二,不同类型的盐溶液具有不同的结构和关系。由于多元弱酸酸根和多元弱碱阳离子的水解反应较为复杂,教材内容仅要求学生了解其分步水解的特点,能够利用化学符号描述此类盐溶液中发生的水解反应,对于分步水解的具体过程并不细究。
3.2 引导学生动态分析系统的行为,理解盐类水解的影响因素
系统是存在于一定条件下的状态,条件越多系统的行为就越复杂。盐类水解系统是特定的盐在一定的温度、浓度、酸碱性等条件下达到平衡的综合状态。当外在条件发生改变时,系统的行为就会改变,发展成为新条件下达到平衡的一种综合状态。
(1) 综合利用各种理论解释系统的行为。利用系统思维去认识盐类水解系统的行为,需要借助化学理论和原理去分析、解释盐类水解的行为,具体包括化学平衡理論、电离理论、弱电解质的电离、水解规律等,学生能够理解盐溶液体系中各种微粒的动态性,以及这些微粒之间最终达到一种相对稳定的平衡状态;学生能够分析出微粒之间相互作用的直接结果和间接结果,总结盐类水解反应的一些规律;学生能够理解盐溶液体系循环及发展的本质,从而认识和分析不同条件对盐类水解程度的影响。
(2) 认识到不同影响因素产生不同的变化规律。从系统思维的视角,影响盐溶液体系的因素是多方面的,既包括内在因素(盐本身的性质),也包含外在因素(温度、浓度等)。内外因素作用于盐溶液体系时,都会影响盐类水解的水解程度,使系统产生不同的行为。在教学过程中引导学生认识到弱酸酸性和弱碱碱性对水解程度的影响,从动态平衡的视角理解盐类水解反应,理解盐本身的性质对水解程度的影响和水解反应规律。借助水解平衡常数Kh与Kw、 Ka的关系,从定性和定量两个角度理解盐本身的性质对水解程度的影响。此外,温度、浓度和溶液酸碱性对盐类水解系统的影响需要运用化学平衡原理进行解释。认识温度、浓度与外加酸碱三种外部因素能够使水解平衡发生移动,影响盐类水解的程度。学生借助化学平衡理论,从能量变化和反应限度两个角度解释水解平衡的移动,不仅能认识盐类水解反应吸热、可逆的特征,同时能够理解盐溶液体系的动态性和循环及发展的本质[10]。
(3) 具体分析各种影响因素对系统行为的影响。运用系统思维分析系统行为还需考虑复杂系统内部的相互关系变化情况。不同影响因素对盐溶液体系中各个平衡的影响程度是不同的。例如,在Na2CO3溶液中存在CO2-3、 HCO-3的水解平衡和HCO-3、 H2O的电离平衡。其中,HCO-3的水解平衡和电离平衡进行程度很小,可忽略不计。当温度升高时,溶液中H2O的电离平衡正向移动程度大于CO2-3的水解平衡正向移动程度,最终导致溶液的pH减小而非增大。
因此,在教学过程中需引导学生在理解盐溶液体系动态性和发展性的基础上具体分析内外因素对溶液中水解平衡和电离平衡的影响,明确溶液中各个平衡移动的相对大小,进而理解系统行为的变化。
3.3 引導学生逐步建立系统的模型,分析和解决生产生活实际问题
盐类水解的应用与系统思维中系统模型的建立密切相关。学生在新情境中面对的复杂系统既包含学科知识又包含其他要素。学生若没有掌握有关分析盐类水解复杂系统的模型,则很难建立起盐类水解知识与实际应用之间的联系以及理解新情境中复杂系统的因果关系。
在具体教学中,逐步启发学生从分析溶液的组成和相互作用的角度认识盐溶液体系,综合运用电离、盐类的水解和离子反应等核心概念,掌握并外显分析复杂溶液体系的一般思路。之后,学生以制备胶体、净水和除污为目的开展实验探究,认识盐类水解的应用,体会模型在不同的情境要素中发挥的作用可能是不同的。在面对生产、生活中与电解质溶液相关的问题时,促进学生对新情境中的盐溶液体系或系统进行综合分析和预测。
参考文献:
[1]中华人民共和国教育部制定. 普通高中化学课程标准(2017年版)[S]. 北京: 人民教育出版社, 2018: 35.
[2]夏征农. 辞海(中)[M]. 上海: 上海辞书出版社, 1999: 3249.
[3]Jaradat R.M.. Complex system requires systems thinking-how to find systems thinkers [J]. International Journal of System of Systems Engineering, 2015, 6(1~2): 53~70.
[4]Mehren R., Rempfler A., Buchholz J., et al.. System competence modelling: Theoretical foundation and empirical validation of a model involving natural, social and human-environment systems [J]. Journal of Research in Science Teaching, 2018, 55(5): 685~711.
[5]苗东升. 系统思维与复杂性研究[J]. 系统辩证学学报, 2004, (1): 1~5, 29.
[6]Assaraf B.Z., Orion N.. Development of system thinking skills in the context of earth system education [J]. Journal of Research in Science Teaching, 2005, 42(5): 518~560.
[7]Mambrey S., Timm J., Landskron J.J., et al. The impact of system specifics on systems thinking [J]. Journal of Research in Science Teaching, 2020, 57(10): 1632~1651.
[8]Chiu M.H., Mamlok-Naman R., Apotheker J.. Identifying Systems Thinking Components in the School Science Curricular Standards of Four Countries [J]. Journal of chemical education, 2020, 96(12): 2814~2824.
[9]郑长龙. 2017年版普通高中化学课程标准的重大变化及解析[J]. 化学教育(中英文), 2018, 39(9): 41~47.
[10]靳卫霞. “盐类的水解”教学难点分析及解决策略[J]. 山东教育, 2013, (Z2): 84~86.

