安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化疗效的meta分析
陈创欢 王振常2 甘钧元

[摘要] 目的 采用系统评价方法评价安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化的疗效。 方法 通过计算机检索中国知网、维普、万方及PubMed、Eambase、Cochrane數据库公开发表文献,检索时间自建库至2021年10月,检索关于安络化纤丸(ALX)联合恩替卡韦(ETV)治疗慢性乙型肝炎肝纤维化的随机对照试验(RCT)文献,对纳入文献采用Cochrane评价工具进行偏倚风险评价,采用Revman5.3版软件进行meta分析。 结果 共有10个RCT纳入本研究。Meta分析显示,HA[MD=-67.75,95%CI(-83.02,-52.47),Z=8.69,P<0.00001]、LN[MD=-45.20,95%CI(-64.12,-26.29),Z=4.68,P<0.00001]、PCⅢ[MD=-57.86,95%CI(-76.47,-39.24),Z=6.09,P<0.00001]、Ⅳ-C[MD=-46.47,95%CI(-60.31,-32.63),Z=6.58,P<0.00001]、ALT[MD=-17.92,95%CI(-29.87,-5.9),Z=2.94,P=0.003]、脾脏厚度[SMD=-0.92,95%CI(-1.33,-0.52),Z=4.46,P<0.00001]。两组患者在改善门静脉内径方面比较,差异无统计学意义(P>0.05)。 结论 安络化纤丸联合恩替卡韦能显著改善慢性乙型肝炎肝纤维化患者的血清肝纤维化指标、谷丙转氨酶及脾脏厚度。
[关键词] 安络化纤丸;恩替卡韦;肝纤维化;慢性乙型肝炎;Meta分析
[中图分类号] R575.2 [文献标识码] A [文章编号] 1673-9701(2022)15-0016-05
Meta-analysis of therapeutic effect of Anluohuaxian pill combined with entecavir in treatment of chronic hepatitis B liver fibrosis
CHEN Chuanghuan WANG Zhenchang GAN Junyuan
1.Guangxi University of Traditional Chinese Medicine,Nanning 530001,China;2.Department of Spleen, Stomach and Liver Diseases, Guangxi International Zhuang Medicine Hospital, Nanning 530219,China
[Abstract] Objective To evaluate the therapeutic effect of Anluohuaxian pill combined with entecavir in the treatment of chronic hepatitis B liver fibrosis. Methods Published literatures in CNKI, VIP, Wanfang, PubMed, Embase and Cochrane databases were searched by computer. Retrieval time was from when the databases were set up to October 2021. The randomized controlled trials (RCTS) of Anluohuaxian pill (ALX) combined with entecavir (ETV) in the treatment of chronic hepatitis B liver fibrosis were reviewed. The Cochrane evaluation tool was used to evaluate the risk of bias for the included literatures, and the Revman5.3 software was used for meta-analysis. Results A total of 10 RCTs were included in this study. Meta-analysis showed HA [MD=-67.75,95%CI(-83.02,-52.47),Z=8.69,P<0.00001], LN[MD=-45.20,95%CI (-64.12, -26.29),Z=4.68,P<0.00001], PC Ⅲ[MD=-57.86, 95%CI (-76.47, -39.24), Z=6.09, P<0.00001],Ⅳ-C[MD=-46.47, 95%CI (-60.31,-32.63),Z=6.58,P<0.00001], ALT [MD=-17.92,95%CI(-29.87,-5.9),Z=2.94,P=0.003], and the spleen thickness [SMD=-0.92, 95%CI (-1.33,-0.52),Z=4.46,P<0.00001]. No statistically significant difference was observed in improving portal vein inner diameter between the 2 groups(P>0.05). Conclusion Anluohuaxian pill combined with entecavir can significantly improve the serum liver fibrosis index, glutamic-pyruvic transaminase and spleen thickness in patients with chronic hepatitis B liver fibrosis.7E529C55-1736-46C6-B833-FD90115C963E
[Key words] Anluohuaxian pill; Entecavir; Liver fibrosis; Chronic hepatitis B; Meta-analysis
肝纖维化(hepaticfibrosis,HF)是由于病毒感染、寄生虫、药物等多种因素在多分子通路的协同作用下引起细胞外基质(extracellularmatrix,ECM)过度沉积或降解而导致肝功能异常的一种可逆的肝组织损伤过度修复反应[1]。随着病程进展,不加以控制,会发展成为肝硬化[2],甚至肝癌(hepaticcellcarcinoma,HCC)的发生[3]。据研究报道,全球约20亿人感染乙型肝炎病毒[4],而我国是世界上感染人数最多的国家,据研究表明,我国超过60% HF及80% HCC均与乙型肝炎病毒(hepatitis B virus,HBV)感染相关[5]。据研究报道,早期肝纤维化是可逆的,因此预防肝病发展的关键在于早期干预及阻止HF的发展[6],针对HBV感染所致的HF,核苷酸类和干扰素抗病毒为目前的主流用药,其次有效控制HBV复制,降低肝硬化及肝癌的发生率,甚或改善肝纤维化的作用。但是,单纯的抗病毒治疗容易产生耐药性及不良反应增多。祖国传统医学在治疗肝纤维化方面具有独到见解处。近年来,在抗病毒、抑制肝纤维化及改善肝功能等方面的文献报道中,安络化纤丸联合恩替卡韦疗效显著,但仍缺乏高质量的系统评价证据支持。本文通过全面检索关于安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化患者的文献,采用Cochrane系统评价方法,对纳入研究进行meta分析,以期为临床治疗决策提供参考。
1 资料与方法
1.1 文献检索
检索国内外发表的安络化纤丸联合恩替卡韦治疗慢性乙型肝炎肝纤维化(randomized controlled trial,RCT)的文献,检索时间自建库至2021年10月。以中文检索词“肝纤维化、乙型肝炎、安络化纤丸、恩替卡韦”为检索词,在中国知网、万方、维普三个中文数据库进行检索;以“Liver Cirrhosis、Hepatitis B、AnluoHuaxian、Entecavir”为检索词,在PubMed、Eamaese及Cochrane三个英文数据库进行检索。检索方式采用主题词与自由词相结合。
1.2 文献的纳入及排除标准
1.2.1 纳入标准 (1)研究类型:安络化纤丸与恩替卡韦两者联合治疗慢性乙型肝炎肝纤维化的RCT试验。(2)研究对象:诊断符合《慢性乙型肝炎防治指南》(2010年版)[7]的慢性乙型肝炎肝纤维化患者。(3)干预措施:试验组为安络化纤丸联合恩替卡韦、对照组为单用恩替卡韦。(4)疗程≥48周。(5)结局指标:①肝纤四项:透明质酸(HA)、层黏连蛋白(LN)、Ⅲ型前胶原(PCⅢ)、Ⅳ型胶原(Ⅳ-C);②肝功能指标:谷丙转氨酶(ALT);③影像学指标:门静脉内径、脾脏厚度。纳入文献语言限定中英文。
1.2.2 排除标准 满足以下1条或多条者予排除:①文献类型:综述、动物实验等;②由其他原因引起的肝纤维化,如肝吸虫感染、酒精等;③合并甲、丙等病毒性肝炎及肝恶性肿瘤、肝性脑病等严重肝病;④数据缺失及研究方案不完整;⑤重复发表文献。
1.3 文献筛选及数据提取
以2位研究员单独进行文献筛选,遇分歧时,由第3位研究员进行复核确认。对纳入研究进行数据提取与整理,采用Cochrane评价工具进行偏倚风险性评价,以“低风险”“中风险”及“高风险”三个标准,对下列6个条目[8]的具体内容进行评价,评价条目包括:(1)是否随机分配以及随机方法;(2)是否分配隐藏;(3)是否采用盲法(单盲、双盲);(4)结果数据的完整性;(5)选择性报告研究结果;(6)其他偏倚来源。
1.4 统计学方法
对纳入文献的统计资料,采用Revman5.3版本软件进行meta合并分析。效应量方面,采用95%可置信区间(confidenceinterval,CI)表示,纳入结局指标中HBV-DNA转阴率为二分类变量,则采用相对危险度(relative risk,RR)作为疗效分析统计量;肝纤四项、ALT、门静脉内径及脾脏厚度为连续型变量,则采用均数差(meandifference,MD)或标准均数差(standard mean difference,SMD)作为疗效分析统计量。异质性方面,若I2>50%,提示有显著异质性,则采用随机效应模型进行meta分析。若I2≤50%,提示无显著异质性,则采用固定效应模型进行meta分析。采用倒漏斗图法分析是否存在发表偏倚。
2 结果
2.1 文献检索结果及纳入文献基本特征
通过计算机共检索出140篇文献,初筛符合文献共59篇,复筛文献共28篇,然后仔细对全文进行阅读,最终纳入10篇RCT文献[9-18]。纳入研究的干预组与对照组患者的年龄、性别、病程等无统计学差异,基线具有可比性。干预组恩替卡韦联合安络化纤丸治疗,对照组单用恩替卡韦治疗,疗程为48周、6个月或12个月。
2.2 纳入文献的质量评价
所纳入10项RCT中,在随机分配方法方面,均采用随机分组,有3项研究[16-18]描述采用数字随机方法,余研究未详细描述随机方法;在结果数据的完整性方面,其中1项研究[13]存在数据不完整,对照组有1例患者脱落出组,余研究数据均完整;在分配隐藏、盲法及随访方面,均未提及。综上,说明本文纳入的文献质量不高,在一定程度上会降低本研究的证据强度及可信性。
2.3 meta分析结果
2.3.1 透明质酸 共有10项RCT报道透明质酸,经异质性检验(P<0.00001,I2=93%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,MD=-67.75[-83.02,-52.47],Z=8.69,两组差异有统计学意义(P<0.05),表明恩替卡韦联合安络化纤丸组在降低透明质酸方面明显高于单用恩替卡韦组。见图1。7E529C55-1736-46C6-B833-FD90115C963E
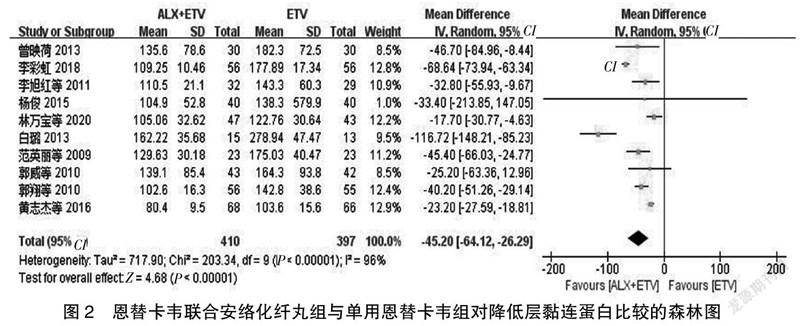
2.3.2 层黏连蛋白 共有10项RCT报道层黏连蛋白,经异质性检验(P<0.00001,I2=96%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,MD=-45.20[-64.12,-26.29],Z=4.68,两组差异有统计学意义(P<0.05),表明恩替卡韦联合安络化纤丸组在降低层黏连蛋白方面明显高于单用恩替卡韦组。见图2。
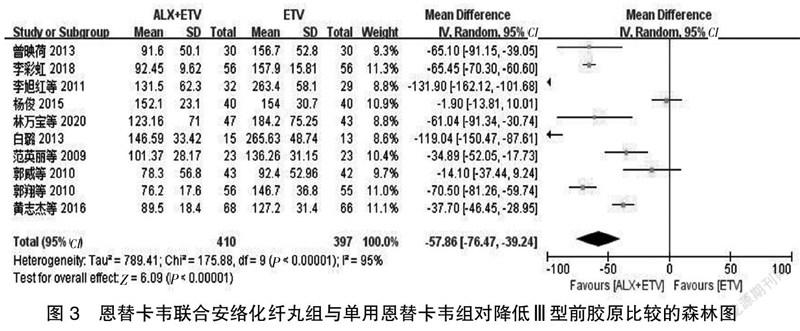
2.3.3 Ⅲ型前胶原 共有10项RCT报道Ⅲ型前胶原,经异质性检验(P<0.00001,I2=95%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,MD=-57.86[-76.47,-39.24],Z=6.09,两组差异有统计学意义(P<0.05),表明恩替卡韦联合安络化纤丸组在降低Ⅲ型前胶原方面明显高于单用恩替卡韦组。见图3。
2.3.4 Ⅳ型胶原 共有9项RCT报道Ⅳ型胶原,经异质性检验(P<0.00001,I2=91%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,MD=-46.47[-60.31,-32.63],Z=6.58,两组差异有统计学意义(P<0.05),表明恩替卡韦联合安络化纤丸组在降低Ⅳ型胶原方面明显高于单用恩替卡韦组。见图4。
2.3.5 谷丙转氨酶 共有9项RCT报道谷丙转氨酶,经异质性检验(P<0.00001,I2=98%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,MD=-17.92[-29.87,-5.9],Z=2.94,两组差异有统计学意义(P=0.003<0.05),表明恩替卡韦联合安络化纤丸组在降低谷丙转氨酶方面明显高于单用恩替卡韦组。见图5。
2.3.6 门静脉内径 共有5项RCT报道门静脉内径,经异质性检验(P<0.00001,I2=92%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型进行meta分析,结果显示,SMD=-0.57[-1.31,0.16],Z=1.53,两组差异无统计学意义(P>0.05),表明恩替卡韦聯合安络化纤丸组在降低门静脉内径方面与单用恩替卡韦组无差别。见图6。
2.3.7 脾脏厚度 共有5项RCT报道脾脏厚度,经异质性检验(P=0.002,I2=76%),提示异质性显著,以用药方案及疗程进行亚组分析后,异质性仍高,故采用随机效应模型,结果显示,SMD=-0.92,[-1.33,-0.52],两组差异有统计学意义(P<0.05),表明恩替卡韦联合安络化纤丸组在降低脾脏厚度方面明显高于单用恩替卡韦组。见图7。
2.3.8 倒漏斗图分析 以透明质酸指标作倒漏斗图进行发表偏倚观察,结果提示漏斗不对称,存在一定的发表偏倚。见图8。
3 讨论
肝纤维化在祖国传统医学上并无确切记载,但按其症状可归属“黄疸”“胁痛”“积聚”“鼓胀”等范畴,致病因素有外感六淫疫毒、内括七情内伤等[19],以“毒”“瘀”“痰”“虚”致正虚邪盛,邪毒入络,肝络受损,气滞血瘀为主要病机。临床研究表明,活血化瘀、滋补肝肾等治疗方法可有效延缓或逆转肝纤维化发展[20]。近些年来报道中医药治疗肝纤维化的相关文献日益增多,因中药复方具有多成分、多靶点、不良反应小的优势[21],且在改善血清肝纤维指标、缩小脾脏等方面疗效出色,目前已成为治疗肝纤维化的新方向,其中以安络化纤丸等中药复方为代表[22]。安洛化纤丸由三七、牛黄、地黄、水蛭、鸡内金、瓦楞子、白术、郁金、牡丹皮、水牛角、僵蚕、地龙等中药组成,全方以肝脾双补为主要特点,共奏凉血散结、养肝活血之功。其中,三七具有活血化瘀之功效,其提取物三七总皂苷对肝纤维化的肝组织有保护作用[23]。恩替卡韦是目前治疗主要的抗病毒药物之一,需长期服药[24],且无法有效阻止肝纤维化进展及降低肝癌发生率,故仅采取针对病因的方式进行抗病毒治疗仍不够,还需联合抗纤维化药物。石栓柱等[25]研究表明,安络化纤丸联合恩替卡韦能促使肝纤维降解吸收,减缓纤维化进程。聂红明等[26]研究表明恩替卡韦联合安络化纤丸能显著激活角质酶,加速纤维化的分解,进而可以缓解,甚至逆转纤维化。本meta研究共纳入10篇RCT,分析结果显示,安络化纤丸联合恩替卡韦能有效降低肝纤维化血清学标志物(透明质酸、层黏连蛋白、Ⅲ型前胶原、Ⅳ型胶原)、谷丙转氨酶及脾脏厚度,与大多数临床研究结果相符,但是在降低门静脉内径方面,没有明显的作用。
本研究也存在一些不足与局限性:①关于偏倚风险,鉴于本文纳入的RCT在盲法、分配方法及分配隐藏上均未提及,总体质量不高,故在一定程度上会造成偏倚,影响证据的可信度。②关于异质性,本文在大部分结局指标进行合并分析时,发现异质性过高,按用药和疗程两个组内因素进行亚组分析时,异质性居高不下,这可能与纳入病例的肝纤维化分级的不同有关。故应从整体上提高RCT的质量,在试验中心、样本量、随机盲法设计等层面上严格限制,才能为高质量的meta分析提供前期基础,为临床提供强有力的循证医学证据,进一步指导临床。
[参考文献]
[1] 徐列明,刘平,沈锡中,等.肝纤维化中西医结合诊疗指南(2019年版)[J].临床肝胆病杂志,2019,35(7):1444-1449.
[2] Rafael Lozano. Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: A systematic analysis for the global burden of disease study 2010[J].The Lancet,2012,380(9859):2095-2128.7E529C55-1736-46C6-B833-FD90115C963E
[3] Goldstein Susan Tl. A mathematical model to estimate global hepatitis B disease burden and vaccination impact[J].International Journal of Epidemiology,2005,34(6):1329-1339.
[4] 谢晓,陆伦根.乙型肝炎肝硬化抗病毒治疗的进展[J].实用肝脏病杂志,2018,21(1):140-144.
[5] Wang Fu-Sheng.The global burden of liver disease:The major impact of China[J].Hepatology (Baltimore,Md.),2014, 60(6):2099-2108.
[6] Yoav Lurie,Muriel Webb,Ruth Cytter-Kuint,et al.Non-invasive diagnosis of liver fibrosis and cirrhosis[J].World Journal of Gastroenterology,2015,21(41):11 567-11 583.
[7] 中华医学会肝病学分会和感染病学分会.慢性乙型肝炎防治指南(2010年版)[J].实用肝脏病杂志,2011,14(2):81-89.
[8] 谷鸿秋,王杨,李卫.Cochrane偏倚风险评估工具在随机对照研究meta分析中的应用[J].中国循环杂志,2014, 29(2):147-148.
[9] 范英丽,冯志成,袁勇.恩替卡韦联合安络化纤丸治疗乙肝肝纤维化23例临床研究[J].云南中医中药杂志,2009,30(7):9-10,88.
[10] 郭威,周莹,鲁有水,等.恩替卡韦联合安络化纤丸治疗慢性乙型肝炎肝纤维化43例[J].医药导报,2010,29(9):1157-1159.
[11] 郭翔.恩替卡韋联合安络化纤丸治疗慢性乙型肝炎56例[J].实用肝脏病杂志,2011,14(6):444-445.
[12] 李旭红,赖江琼,李奕鑫,等.恩替卡韦联合安络化纤丸治疗乙型肝炎肝硬化32例疗效分析[J].传染病信息,2011,24(1):51-54.
[13] 白璐. 恩替卡韦联合安络化纤丸治疗乙型肝炎肝硬化的临床观察[J].中外健康文摘,2013,(11):133.
[14] 曾映荷.恩替卡韦联合安络化纤丸治疗乙型肝炎肝纤维化的临床研究[J].湖北中医杂志,2013,35(6):11-12.
[15] 杨俊.安络化纤丸治疗乙肝肝硬化患者的疗效观察[J].医药论坛杂志,2015,36(3):143-144.
[16] 黄志杰,曾翠萍.恩替卡韦联合安络化纤丸治疗HBeAg阳性慢性乙型肝炎肝纤维化134例[J].中西医结合肝病杂志,2016,26(2):74-75.
[17] 李彩虹,连琳琳,高菲,等.安络化纤丸联合恩替卡韦对老年活动性代偿期乙肝肝硬化患者肝功能、肝纤维化及肝脾影像学指标的影响[J].实用医院临床杂志,2018, 15(4):232-234.
[18] 林万宝,陈海燕,殷光辉,等.安络化纤丸联合恩替卡韦片治疗慢性乙型病毒性肝炎肝纤维化临床研究[J].新中医,2020,52(1):80-82.
[19] 张美军,杨胜辉.中医药治疗肝纤维化研究进展[J].湖南中医杂志,2019,35(10):173-176.
[20] 刘成海,赵志敏,吕靖.中医对肝纤维化逆转的认识与治疗[J].临床肝胆病杂志,2019,35(4):728-733.
[21] 王乐,丁腾,龚伟玲,等.调控TGF-β1/Smads信号通路抗肝纤维化的中药有效成分研究进展[J].中国中药杂志,2019,44(4):666-674.
[22] 陈艳,杨永平.中医药阻断逆转肝纤维化的现状、希望与挑战[J].临床肝胆病杂志,2018,34(4):689-693.
[23] 王京凯,王艳春,王振宇.三七总皂苷对肝纤维化小鼠转化生长因子β-1及重组人SMAD家族成员3的调控作用研究[J].中国临床药理学杂志,2021,37(10):1163-1166.
[24] Lucio Boglione.Sequential therapy with entecavir and pegylated interferon in a cohort of young patients affected by chronic hepatitis B[J].Journal of Medical Virology,2016, 88(11):1953-1959.
[25] 石栓柱,陈翛然,古玉茹,等.安络化纤丸联合恩替卡韦对乙型肝炎肝硬化患者门静脉系统血流动力学研究[J].中西医结合肝病杂志,2016,26(6):336-337,373.
[26] 聂红明,王灵台.安络化纤丸抗肝纤维化的研究进展[J].中西医结合肝病杂志,2016,26(3):185-187.
(收稿日期:2021-11-12)7E529C55-1736-46C6-B833-FD90115C963E

