Cu2+掺杂TiO2/伊利石复合材料对亚甲基蓝去除能力的研究
丁浩洋, 金秀颖, 麻新宇, 姜男哲,
(1.延边大学 工学院, 吉林 延吉 133002; 2.延边大学 理学院, 吉林 延吉 133002)
0 引言
印染废水是工业废水的主要来源之一.近年来纳米级TiO2不仅因具有成本低廉、生态友好、空穴夺电子能力强和化学稳定性好等优点,而且还因具有较大的比表面积和优于TiO2的光催化活性而受到学者的关注[1-3].但目前纳米级TiO2在实际应用中仍存在一些问题:①纳米级TiO2具有团聚趋势[4],进而会减少其比表面积和降低其光催化活性[5];②纳米级TiO2在水溶液中易分散,难以分离回收[6].对此,一些学者通过引入蒙脱土[7]、高岭土[8]等黏土类载体来阻止颗粒间的团聚和解决分离回收问题,并取得了良好的效果.研究表明,在TiO2晶体中掺杂Ag+、 Cu2+、 Al3+、 Zn2+等金属阳离子(形成缺陷空位)可延长电子-空穴对的寿命,进而能够提高催化剂的光电转化效率[9-12];同时引入金属阳离子还可以使晶体结构生成杂质能级[13],进而可减小半导体材料能级间的带隙,拓宽晶体的吸光范围,提高TiO2可见光区的利用率.由于伊利石精粉在水溶液中具有良好的分散性,且对染料有着较好的吸附能力,因此本文选用伊利石精粉作为载体,Cu2+作为掺杂阳离子,采用溶胶-凝胶法制备了一种Cu2+-TiO2/伊利石复合材料,并利用扫描电镜(XRD)、透射电镜(SEM)等对样品进行了表征.另外,本文还以亚甲基蓝(MB)作为污染源,在可见光下探究了Cu2+掺杂TiO2/伊利石复合材料对MB溶液的去除作用.
1 实验
1.1 试剂和仪器
硝酸(分析纯),天津市大茂化学试剂厂;四异丙氧基钛(TTIP,分析纯), Acros organics公司;无水乙醇(分析纯),辽宁泉瑞试剂有限公司;冰乙酸(分析纯),天津市北方天医化学试剂厂;三水硝酸铜(分析纯), Damas-beta公司;伊利石由吉林省安图县工信局提供; 20 nm纳米TiO2(P25),上海阿拉丁生化科技股份有限公司; MB,国药集团化学试剂有限公司.
塑料注射器,江苏长城医疗器械有限公司;HJ-10多头磁力搅拌器,金坛市科析仪器有限公司;光化学反应器,上海岩征实验仪器有限公司;UV-2600型紫外分光光度计,日本岛津公司;SU3500型扫描电镜,日本日立公司; JEM-2100 plus型透射电镜,日本日立公司; X射线衍射仪(XRD)、 X射线荧光衍射仪(XRF), PANalytical公司.
1.2 实验方法
1.2.1伊利石精粉的制备
浮选、球磨伊利石矿石原料,干燥后过筛,取粒径小于10 μm的精粉作为实验中的反应材料(记为IPR).
1.2.2Cu2+掺杂TiO2纳米溶胶的制备
取8 mL TTIP溶于10.5 mL无水乙醇中,充分搅拌30 min后加入冰乙酸(与TTIP摩尔数比为0.4∶1, 作为抑制TTIP水解的稳定剂),继续搅拌30 min后得到透明溶液A.取0.974 mL水和1.252 mL硝酸溶于5.3 mL无水乙醇中,然后加入三水硝酸铜(与TTIP摩尔数比为0.009∶1),搅拌30 min后得到溶液B.在持续搅拌下将溶液B滴入溶液A中,均匀混合后即得Cu2+掺杂的淡蓝色透明纳米溶胶.
1.2.3Cu2+掺杂TiO2/伊利石复合材料的制备
在高速搅拌下,将6.3 g IPR加入到Cu2+掺杂的TiO2纳米溶胶中并持续搅拌4 h; 将所得混合物在室温下静置60 min后干燥(60 ℃烘箱中),干燥后的固态混合物再经研磨和煅烧5 h (马弗炉中, 550 ℃)即得Cu2+掺杂的TiO2/伊利石复合材料(记为CTIP).另外,制备了未经掺杂负载的TiO2纳米颗粒(记为TNP),用以与CTIP进行对比.
1.3 样品的性能表征
1.3.1样品表征测试
使用XRD测定Cu2+掺杂TiO2/伊利石复合光催化材料的物相组成及晶型结构,使用SEM测定Cu2+掺杂TiO2/伊利石复合光催化材料的微观形貌特征.
1.3.2光催化性能评价
在光化学反应器中,以氙灯模拟自然可见光, 以20 mg/L的MB溶液模拟污染源.打开光化学反应器冷却循环装置,在装有80 mL MB溶液的石英管中分别放入CTIP和P25 (2个石英管分别记为A和B).用塑料注射器在A和B石英管中各抽取5 mL 混合溶液移入离心管中,然后利用光化学反应器进行吸附-降解MB (通过调节光源功率旋钮使氙灯的照射功率保持在500 W).
离心混合溶液(5 000 r/min, 5 min),取上清液后在MB的最大吸光度波长(λ= 664 nm)下用紫外分光光度计测定其吸光度A0.按上述方法每隔15 min测定一次溶液的吸光度A(共进行6次),并计算各时间段CTIP和P25对MB的去除率(Rp).去除率的计算公式[14]为:
Rp= (1-A/A0)×100%.
2 结果与讨论
2.1 XRD分析
图1为TNP、 IPR和CTIP的XRD图谱.由图1可知:①在TNP的XRD图谱中,在25.34°、38.03°、 48.05° 处附近出现了衍射峰,这些峰分别对应的是锐钛矿的(101)、(004)、(200)衍射面,其他杂峰则对应的是锐钛矿的其余衍射面,由此说明所得的TiO2为纯净的锐钛矿.②在IPR的XRD图谱中出现多种衍射峰,其原因是伊利石中存在钾、钠、铝、镁等金属氧化物.③在CTIP的XRD图谱中同时出现了TiO2和伊利石的特征峰,但未出现氧化铜或硅化铜的特征衍射峰,这可能是由于Cu2+含量过少,且铜元素半径(0.073 nm)与钛元素半径(0.068 nm)相似所致(Cu2+虽然可插入到TiO2的晶格中取代钛元素,但并不影响TiO2与伊利石间的晶型结构).④CTIP中的TiO2仍为单一的锐钛矿相,伊利石的特征峰强度明显减弱,但没有发生偏移,这说明TiO2已负载到伊利石表面,但并未破坏伊利石的层间结构.所得的TiO2为单一锐钛矿相的可能原因是:TTIP水解时, Ti原子与伊利石表面的负电氧原子形成紧密的化学键,由此使晶型的转变条件变得更加苛刻[15].
为了进一步探究在伊利石上负载TiO2对TiO2结构生长所带来的影响,使用Debye-Scherrer公式[16]计算了CTIP中TiO2晶粒(101)面的尺寸,结果显示其尺寸为15.21 nm.而TNP对应的TiO2(101)面的尺寸为21.65 nm,这说明在伊利石上负载TiO2可限制TiO2晶粒(101)面的生长[14].

图1 TNP、IPR和CTIP的XRD图
2.2 SEM形貌分析
图2为TNP、IPR、CTIP的SEM图.由图可以看出: TNP(图2(a))中的TiO2颗粒分布均匀,但存在轻微团聚现象; IPR(图2(b))中的伊利石片层结构呈有序堆叠状态; CTIP(图2(c))中的伊利石片层结构呈无序状态,且在图中难以观察到TiO2颗粒.TiO2颗粒在图中难以观察到的原因是负载到伊利石片层上的TiO2粒径较小,且TiO2颗粒是以化学键的形式结合到伊利石表面上.上述原因也是图1中伊利石的特征峰未发生偏移的原因.

图2 TNP(a)、IPR(b)、CTIP(c)的SEM图
图3为CTIP的SEM-mapping图.由图可以看出, Si、Ti、Cu元素在材料中分布较为均匀(但Cu元素含量较少),这说明Cu元素已成功掺杂到复合材料中.

图3 CTIP的SEM-mapping图
表1为CTIP的元素含量表(由SEM-EDX实验获得).由表1也可看出, Cu元素已成功掺杂进该复合材料中,但其占比较少(质量分数为0.339%), 仅为Ti元素质量分数的1.98%.该结果与SEM-mapping图相符.

表1 CTIP的元素含量
2.3 复合材料的光催化性能测定
CTIP、 P25、 IPR对MB的去除率如图4所示.由图可知: IPR对MB的去除效果最差,其原因是IPR不具备光催化活性.光照时间为90 min时, CTIP和P25对MB溶液的去除率分别为93.2% 和92.1%.由于在CTIP中TiO2与伊利石的质量比为1∶3, 因此可知在含等量的TiO2的复合材料中, CTIP去除MB的效率约是P25的4倍.这可能是由以下因素共同形成的:
1)伊利石的吸附作用与改性TiO2的降解作用相互促进,加快了MB的去除过程;
2)较低pH环境有利于CTIP中的TiO2颗粒均匀覆盖在伊利石表面[14];
3)Cu2+的加入提供了空穴捕获中心,延长了非平衡载流子寿命,进而提高了晶体对可见光的利用率[17].

图4 CTIP、P25、IPR对MB的去除率
为了考察CTIP对不同浓度MB溶液的去除率,将0.15 g CTIP分别置于5、10、15、20、25 mg/L的MB溶液中,去除率结果如图5所示.由图5可知,光照90 min后CTIP对MB溶液的去除率分别为86.7%、 87.5%、 91.1%、 93.3%、 90.0%.在实验初期,去除率随着溶液浓度的升高而增加,其原因是MB与TiO2结合后可改善复合材料的光催化活性[18].当浓度大于20 mg/L时, CTIP对MB溶液的去除率出现下降,其原因可能是高浓度溶液中的MB分子会阻碍光的传播[19],进而会降低溶液中CTIP的光催化活性.

图5 CTIP对不同浓度MB溶液的去除率
不同复合材料用量及光照时间对MB的去除率如图6所示.由图6可知,光照时间为15 min、 复合材料用量分别为0.05、0.10、0.15、0.20、0.25 g时,其对MB的去除率分别为30.9%、50.8%、70.1%、 85.9%、 90.0%.当光照时间为90 min时,复合材料用量对MB的去除率出现先增高后降低的趋势(分别为80.7%、93.3%、94.7%、94.4%、93.8%).MB去除率出现下降的原因可能是随着光照时间增加,复合材料对MB的去除率达到饱和,进而出现光催化效率随复合材料用量的增加而降低的现象[20].

图6 不同复合材料用量及不同光照时间对MB的去除率
图7是CTIP的循环稳定性测试图.由图可以看出, CTIP对溶液中MB的去除率虽然呈逐渐降低趋势,但3次测试所得结果均超过90%,由此说明CTIP复合材料的稳定性较好.去除率逐渐降低的原因是回收过程中复合材料出现一定的损失.

图7 不同循环次数下CTIP对MB的去除率
图8为CTIP的XPS谱图.由图8可见,在933.5 eV处出现了Cu 2p3/2的特征峰,该特征峰与Cu2+的结合能相对应,这说明铜是以二价离子的形态掺杂进TiO2/伊利石复合材料中.Cu2+掺杂进TiO2/伊利石复合材料中后,由于Cu2+与Ti4+的半径大小相近,因此Cu2+会取代原TiO2晶格中的Ti4+,并生成空穴捕获中心.研究[17]表明,Cu2+掺杂后所产生的缺陷位置会吸引带正电荷的光生空穴(h+),进而可抑制TiO2晶体中的光生电子-空穴的复合,由此可提高TiO2/伊利石复合材料的光催化效率.
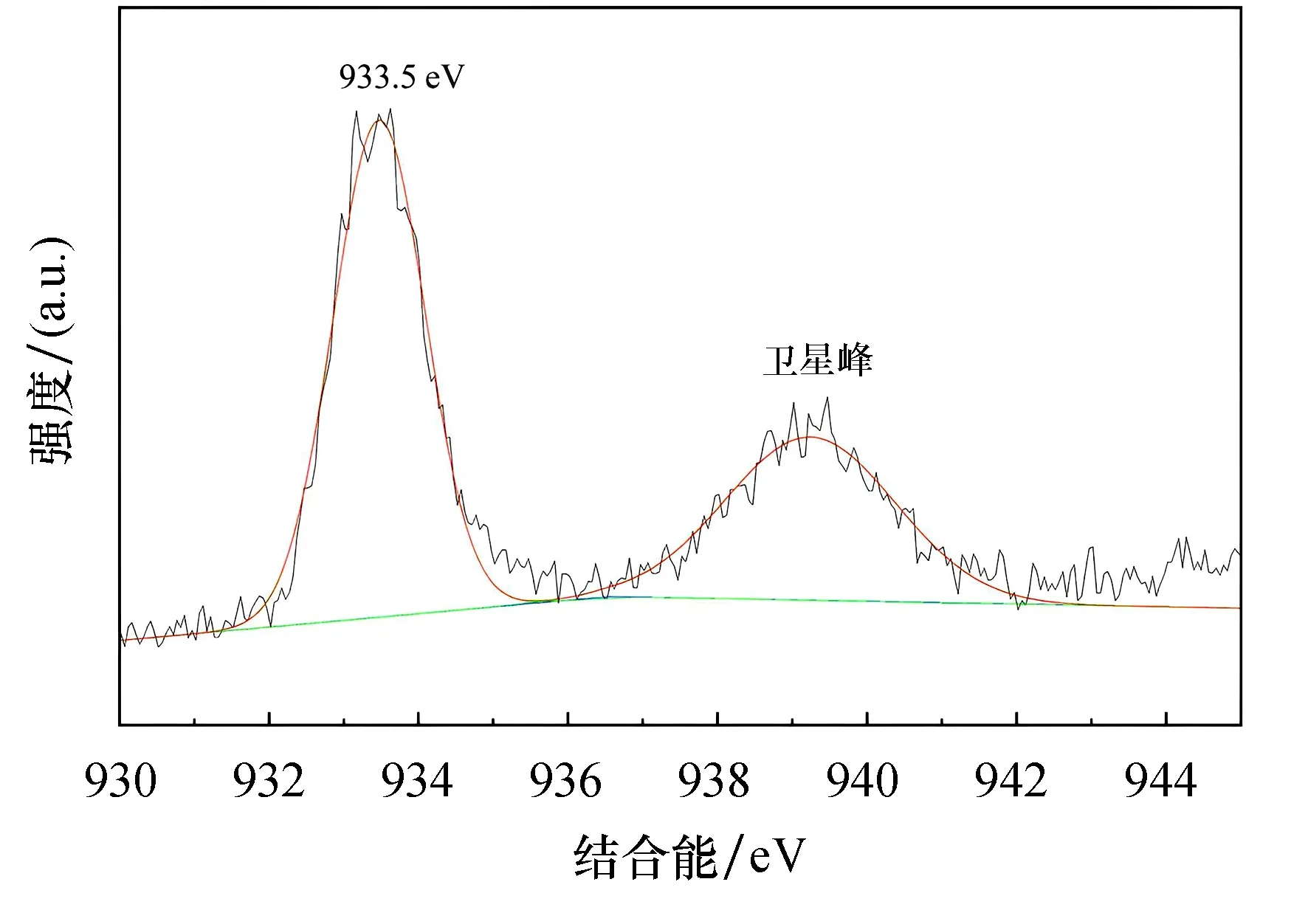
图8 CTIP的XPS谱图
3 结论
本文研究表明, CTIP复合材料不仅可解决纳米TiO2易于团聚的问题,还可以提高材料的使用率.复合材料中所掺杂的Cu2+可有效延长载流子寿命,并使复合材料的光催化能力显著优于P25; 因此,本文研究结果对利用复合材料处理染料废水具有良好的参考价值.在今后的研究中我们尝试对CTIP复合材料中的TiO2进行缺陷工程处理,即通过在TiO2晶体中引入氧空位与钛空位以进一步提高复合材料的光催化效果.

