两性离子共聚物PCBMA的合成及分析
武超群,郑久汉,胡建华,3
(1. 上海民航职业技术学院,上海 200232; 2. 复旦大学-金张科技联合实验室,上海 200082;3. 复旦大学 高分子科学系,上海 200433)
聚甲基丙烯酸羧酸甜菜碱(Polycarboxybetaine, PCB)的共聚物是研究较多的两性离子聚合物之一。PCB含有一个带正电的季铵基团和带负电的羧酸基团,其化学结构与调节机体渗透压的主要化合物甘氨酸甜菜碱(glycine-betaine)的结构十分相似。每天人体会摄入0.1~0.25克的甘氨酸甜菜碱,因此PCB被认为是一种具有良好生物相容性的重要仿生材料。蒋绍毅课题组的研究表明,PCB也具有优异的抗非特异性蛋白质黏附、微生物/细菌吸附和生物膜形成的抗生物污染性能[1-3]。另外,由于PCB中含有大量的羧酸基团,这将有利于通过简单的酯化反应将含有氨基的生物分子引入到PCB修饰的材料表面,实现对其表面的进一步功能化[4-6]。这使得PCB与聚甲基丙烯酸磺酸甜菜碱(Polysulfobetaine, PSB)相比,具有更为广阔的应用前景。
为了构建结构稳定,性能优异的两性离子抗污表面,材料的表面性能和接枝密度是决定两性离子聚合物功能性的重要因素[7-10]。目前,研究大多针对于表面引发聚合(ATRP)制备PSB和PCB抗污表面,蒋绍毅课题组在这方面做出了突出的成绩[1-3]。研究结果表明,表面引发聚合可以制备出接枝度高且性能优异的抗污表面,其在血液中的长循环性和稳定性优势也有了显著的发挥[11-12]。但是,关于两性离子聚合物的其他相关制备方法却研究甚少[13-14]。
本研究首先制备出两性离子单体甲基丙烯酸羧酸甜菜碱(CBMA),利用RAFT聚合方法研究CBMA与其他功能性单体的聚合反应条件和相关性能。以CBMA为两性离子模型,制备具有可替换的功能性单体和PEG基团的三元无规共聚物。在单因素实验基础上,对聚合反应体系的链转移剂(CTA),溶剂,单体浓度,反应时间及反应温度进行筛选,以聚合反应的程度为考察依据筛选出最佳的反应条件。利用甲基丙烯酸五氟苯酯(PFMA)等不同单体与CBMA进行RAFT聚合尝试,以期制备出同时具有两性离子和其他功能性基团的响应性抗生物污染的共聚物,同时也对三元共聚进行了探索。与此同时,为了实现两性离子聚合物的可控性抗污性能的研究[15-17],本研究也利用具有pH和CO2/N2响应性的单体2-(二甲氨基)乙基甲基丙烯酸酯(DMAEMA)与两性离子发生聚合反应,对两性离子聚合物的多方向应用进行了研究。
1 实验部分
1.1 原料和试剂
2-(二甲氨基)乙基甲基丙烯酸酯(DMAEMA)、β丙内酯(β-propiolactone)、甲基丙烯酸聚乙二醇醚(PEGMEMA)、五氟苯酚、甲基丙烯酰氯、2,6-二甲基吡啶、2-(十二烷基三硫代碳酸酯基)-2-甲基丙酸(CTA)、偶氮二异丁腈(AIBN)、N,N-二乙基乙胺(TEA): 分析纯,购自上海阿拉丁生化科技股份有限公司;氨基二茂铁(Aminoferrocene): 分析纯,TCI;N,N-二甲基甲酰胺(DMF)SuperDry: 分析纯,购自百灵威科技有限公司;正己烷,乙醇,丙酮,甲苯,二氯甲烷: 分析纯,购自国药集团化学试剂有限公司。
原料前处理:
丙酮: 丙酮中加入适量无水硫酸钙搅拌过夜后蒸馏,瓶中放入活化的分子筛并通入氮气备用。
二氯甲烷: 经CaH2干燥回流后蒸出,现蒸现用。
甲基丙烯酸聚乙二醇醚(PEGMEMA): 过碱性氧化铝柱去除阻聚剂后使用。
偶氮二异丁腈(AIBN): 用乙醇35℃重结晶两次后25℃减压干燥2 d,避光保存。
N,N-二乙基乙胺(TEA): 先经KOH干燥数天,在CaH2存在下回流蒸出,现蒸现用。
1.2 测试与表征
核磁共振: 超导核磁共振仪,在Varian Mercury 300, JEOL ECZ 400s, Bruker Avance 400和Bruker Avance 500上完成(1H NMR,19F NMR, 13C NMR)。溶剂包括: 氘代氯仿和重水,四甲基硅(TMS)为内标。
凝胶渗透色谱仪(GPC)测定聚合物分子量及分子量分布: 实验仪器为Waters 1515凝胶渗透色谱仪[HR3(500~30 000 g/mol),HR4(5 000~600 000 g/mol),HR5(5 000~4 000 000 g/mol)],采用Waters 2410示差折光检测器和Waters 2487紫外检测器。用THF将聚合物配成1 mg/mL的溶液,淋洗液为THF,流速1 mL/min,采用线性聚苯乙烯(PS)和聚甲基丙烯酸甲酯(PMMA)标样对分子量进行校正。
高分辨质谱: 美国安捷伦液质联用仪: 液相1260,串联飞行时间6230高分辨质谱(TOF),ESI源,5 μm色谱柱,masshunter工作站。
元素分析: 元素分析仪,Elemantar VARIOEL,Heraeus 1106,Carlo-erba 1108。
高效液相色谱(HPLC): 安捷伦LC 1100液相色谱仪,产品型号: Agilent 1100。用水和甲醇混合溶液配制流动相,流动相流速1.0 mL/min,定量分析采用峰面积定量。
1.3 单体的制备
1.3.1 CBMA单体的制备
取500 mL三口圆底烧瓶内置转子和恒压滴液漏斗,整个体系真空火烤-通氮气-冷却操作3次排除反应瓶中的氧气和水蒸气。将β-丙内酯(0.87 g,12 mmol,0.76 mL)充分溶解于10 mL干燥丙酮中置于恒压滴液漏斗中,DMAEMA(1.57 g,10 mmol,1.68 mL)充分溶解于50 mL干燥丙酮置于圆底烧瓶中。调整滴加速度使β-丙内酯丙酮溶液缓慢的滴加至圆底烧瓶中,反应置于15 ℃水浴中反应约5 h。得到的产物抽滤,白色粉末用100 mL干燥乙醚和50 mL干燥丙酮反复洗涤,真空干燥过夜,2~8 ℃下低温保存(反应式(1)),产率80.7%。
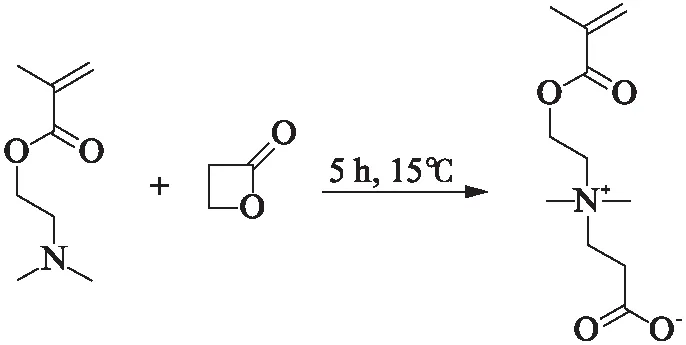
(1)
1.3.2 甲基丙烯酸五氟苯酯(PFMA)单体的制备
取500 mL三口圆底烧瓶内置转子和恒压滴液漏斗,整个体系真空火烤-通氮气-冷却操作三次排除反应瓶中的氧气和水蒸气。五氟苯酚(5.4 g,29.3 mmol)和2,6-二甲基吡啶(3.5 mL,30.0 mmol)溶于50 mL二氯甲烷(现蒸现用),充分溶解后加入圆底烧瓶中,置于冰浴中,在0 ℃下,用恒压滴液漏斗缓慢滴加甲基丙烯酰氯(3.0 mL,32.7 mmol)并持续搅拌3 h,去除冰浴后恢复至室温反应过夜。反应产物抽滤去除固体,滤液用30 mL水洗2次,加入无水硫酸镁干燥过夜。抽滤去除滤液中的硫酸镁,旋蒸浓缩后,配制展开剂,点板湿法过硅胶柱(反应式(2)),产率83.2%。
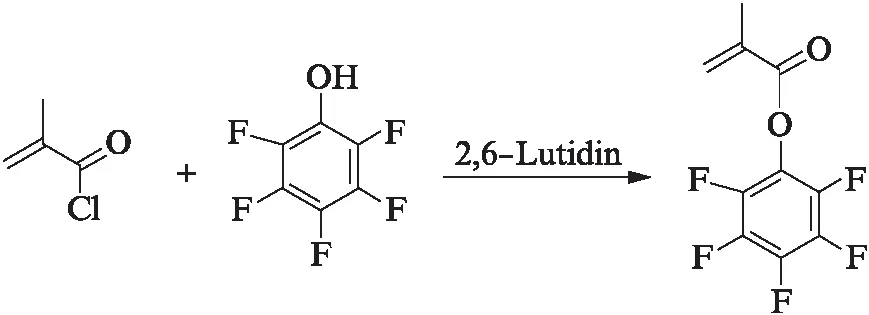
(2)
1.4 两性离子聚合物的制备
1.4.1 两性离子共聚物PCB-co-PPFMA-co-PEGMEMA的合成
共聚物PCB-co-PPFMA-co-PEGMEMA的RAFT聚合过程:nCBMA∶nPFMA∶nPEGMEMA=a∶b∶c(其中a,b,c是各单体的可变量,如表1所示),nM∶nCTA∶nAIBN=60∶3∶1。向一预置搅拌子的25 mL Schlenk瓶(使用前真空火烤两次)中加入AIBN(0.41 mg,0.002 5 mmol)、CTA(2.74 mg,0.007 5 mmol)和CBMA(n1mmol),抽真空通氮气3次后,加入超干DMF(2.0 mL)、PFMA(n2mmol)和PEGMEMA(n3mmol),经3次冷冻-抽真空-融解通氮气循环以除去反应液中氧气。将Schlenk瓶置于恒温的70 ℃油浴中加热,氮气保护下反应24 h 后液氮淬灭。用适量THF溶解后,以正己烷为沉淀剂沉淀3次,得到一定量的粉红色黏稠状固体,真空干燥过夜备用(反应式(3))。
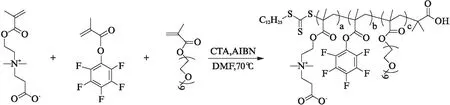
(3)
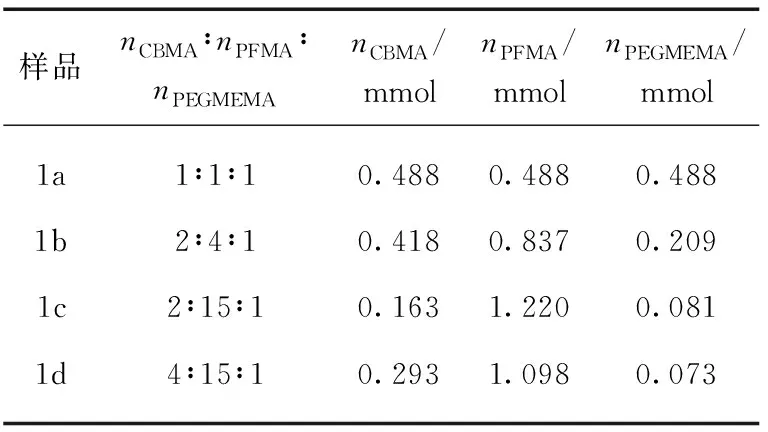
表1 制备不同比例PCB-co-PPFMA-co-PEGMEMA共聚物的实验参数
1.4.2 氨基二茂铁对两性离子共聚物PCB-co-PPFMA-co-PEGMEMA的修饰
向一预置搅拌子的25 mL Schlenk瓶(使用前真空火烤两次)加入共聚物1 d(15 mg)和干燥的DMF(10 mL),随后加入氨基二茂铁(1.0 mmol,2.0 mg)和TEA(1.0 mmol,140 μL)。反应管置于恒温45 ℃油浴中加热反应36 h后,浓缩反应液,用适量水溶解后,在水中透析2 d,得到的产物真空干燥,将铁锈色的产物密封保存备用(反应式(4))。
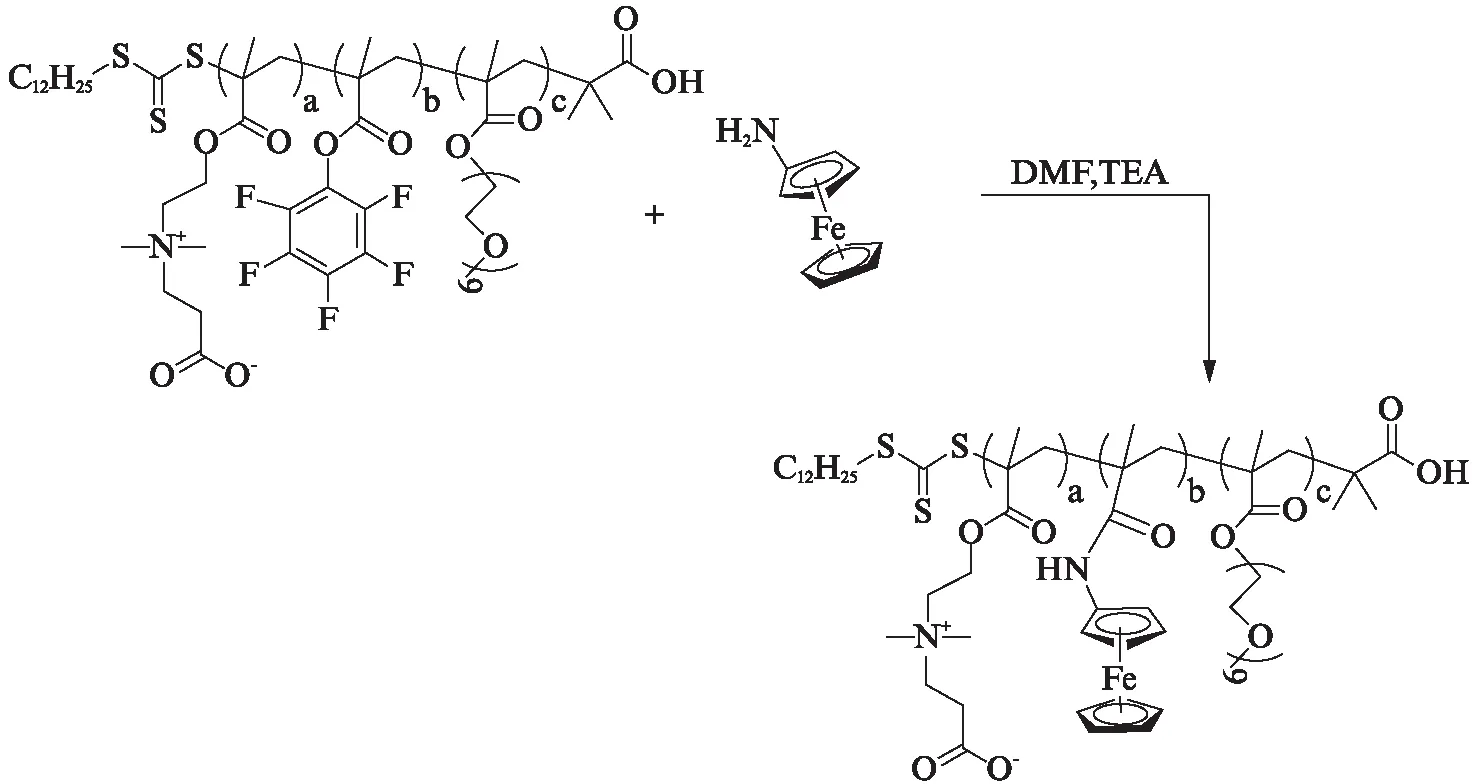
(4)
1.4.3 两性离子共聚物PCB-co-PDMAEMA-co-PEGMEMA的合成
共聚物PCB-co-PDMAEMA-co-PEGMEMA的RAFT聚合过程:nCBMA∶nDMAEMA∶nPEGMEMA=a∶b∶c(其中a,b,c是各单体的可变量,见表2),nM∶nCTA∶nAIBN=60∶3∶1。向预置搅拌子的25 mL Schlenk瓶(使用前真空火烤两次)中加入AIBN(0.41 mg,0.002 5 mmol),CTA(2.74 mg,0.007 5 mmol)和CBMA(n1mmol)抽真空通氮气3次后,加入超干DMF(2.0 mL),DMAEMA(n2mmol)和PEGMEMA(n3mmol),经3次冷冻-抽真空-融解通氮气循环以除去反应液中氧气。将Schlenk瓶置于恒温的70 ℃油浴中加热,氮气保护下反应24 h后液氮淬灭。用适量THF溶解后,以正己烷为沉淀剂沉淀3次,得到一定量的粉红色粘稠状固体,真空干燥过夜备用(反应式(5))。
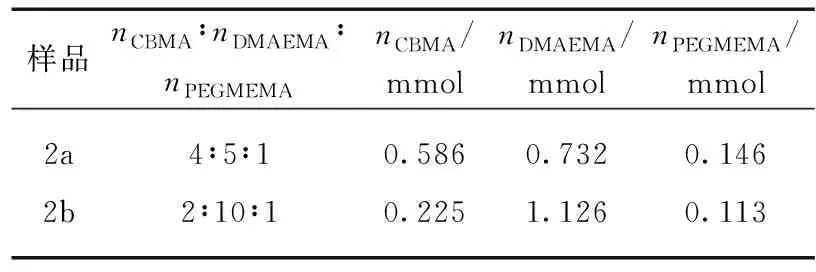
表2 制备不同比例PCB-co-PDMAEMA-co-PEGMEMA共聚物的实验参数
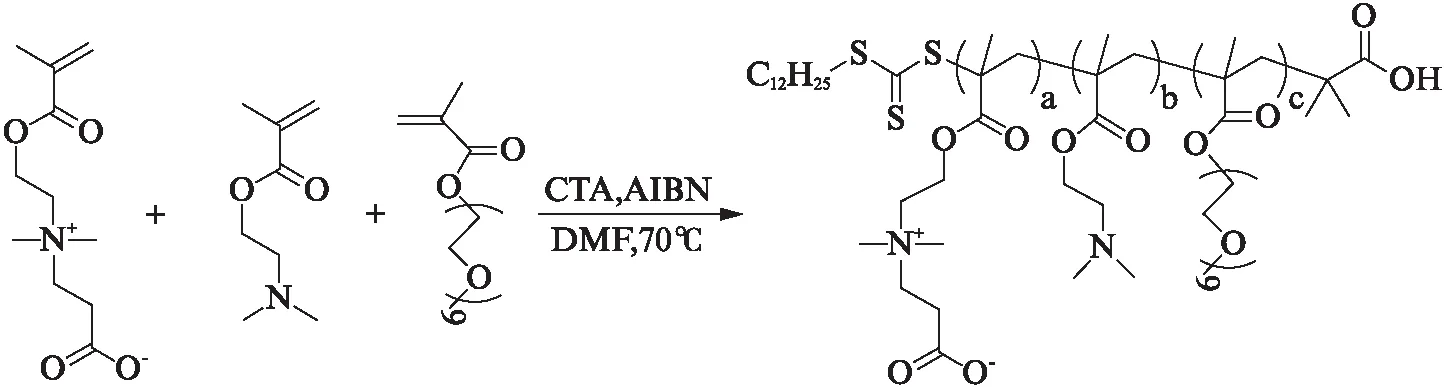
(5)
2 结果与讨论
2.1 单体CBMA的合成分析
我们通过商业化的N,N-二甲基氨基甲基丙烯酸乙酯与β-丙内酯反应合成含有羧酸甜菜碱的甲基丙烯酸酯单体CBMA,并利用通过1H NMR和高分辨质谱手段对所制备的单体进行结构表征(图1(a))。1H NMR(300 MHz,D2O): 6.03(s,1H,=CH),5.65(s,1H,=CH),4.67(t,2H,OCH2),3.66(t,2H,CH2N),3.55(t,2H,NCH2),3.19(s,6H,NCH3),2.60(t,2H,CH2COO),1.81(s,3H,=CCH3)。核磁的分析结果与文献中的结果一致[18],即认为成功合成了CBMA单体。高分辨质谱结果中CBMA的相对分子质量(Mr)为231.1。图1(b)为CBMA的红外光谱图,通过分析可以得出CBMA在1 724 cm-1位置处出现了酯基吸收峰中C=O的伸缩振动峰,3 424 cm-1处代表—OH的伸缩振动峰,对比分析红外结果充分证明CBMA单体的存在[19],与核磁的结果一致。
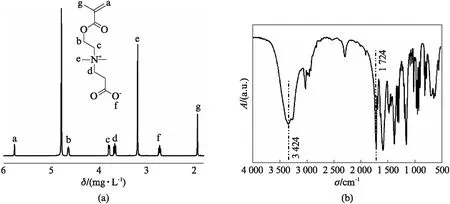
图1 D2O中CBMA的1H NMR和红外光谱图Fig.1 1H NMR and FT-IR spectrums of CBMA in D2O
2.2 单体PFMA的合成分析
为了成功制备含有二茂铁基团的无规共聚物,同时五氟苯酯(PFMA)有利于二茂铁基团的替换,因此我们也成功制备了PFMA,并利用通过1H NMR和19F NMR对所制备的单体进行结构表征(图2)。1H NMR(CDCl3): 6.43(1H,t,JHH=2 Hz),5.89(1H,t,JHH=1.5 Hz),2.06(3H,t,JHH=1.5 Hz);19F NMR(CDCl3): -162.90(2F,dd,JFF=12/18 Hz),-158.63(1F,t,JFF=15 Hz),-153.17(2F,d,JFF=15 Hz);核磁所得结果与文献一致,即认为成功合成了PFMA单体[19]。HPLC得到的PFMA单体纯度达到99%。
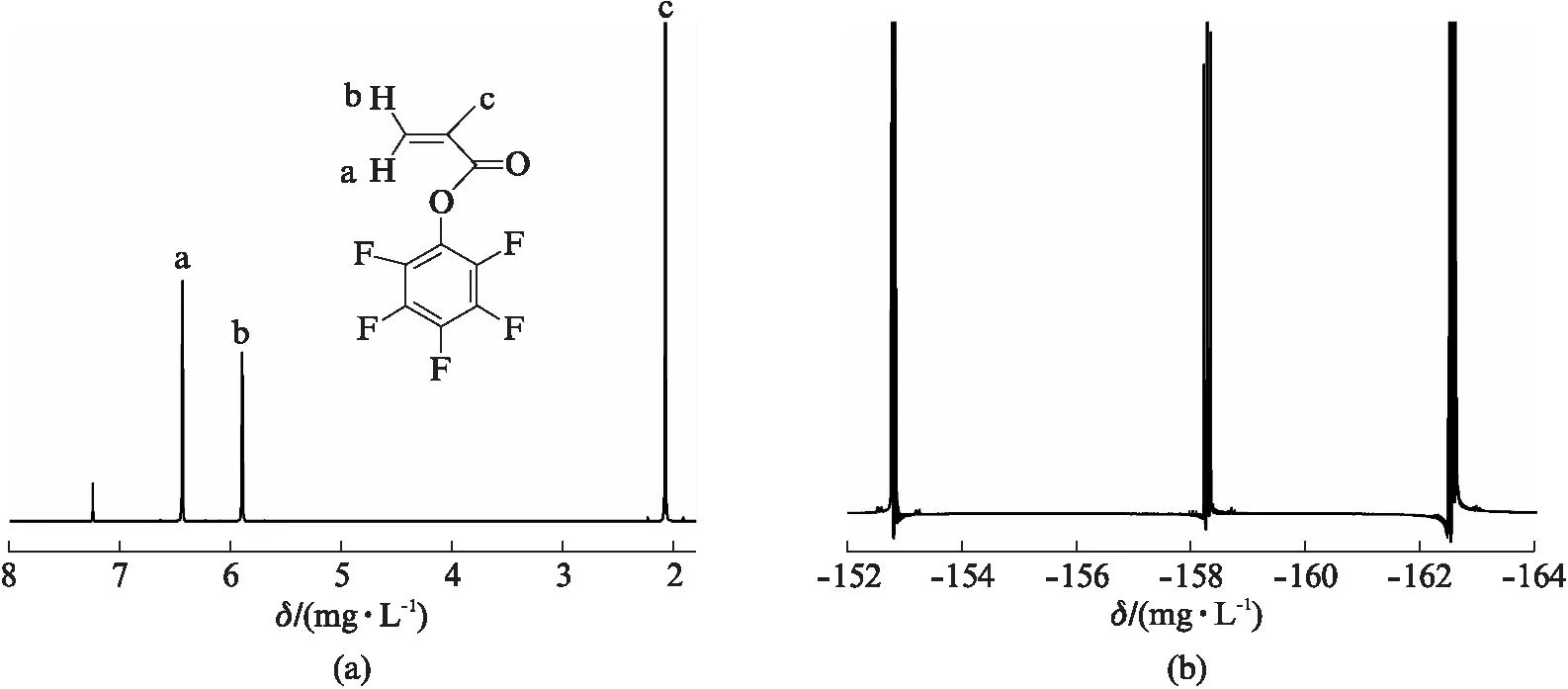
图2 CDCl3中PFMA的1H NMR和19F NMR谱图Fig.2 1H NMR and19F NMR spectrums of PFMA in CDCl3
2.3 PCB-co-PPFMA-co-PEGMEMA的合成分析
通过调整3种单体的组成比,制备出了4种比例的PCB-co-PPFMA-co-PEGMEMA共聚物。每种聚合物分别进行了核磁和GPC的测试分析,但是1a和1b样品的GPC曲线均显示出两种分子量聚合物的存在,且较小的分子量恰好与PPEGMEMA的分子量相对应,因此怀疑反应产物中仍有未反应的PPEGMEMA。下面继续采用透析的方法来去除反应中多余的单体,选用截留分子量为3 500的透析袋,将产物加入1 mL DMF溶解后加入透析袋中,在蒸馏水中透析24 h,将透析后的产物进行提纯进行GPC分析,所得结果如图3所示,GPC曲线呈对称的单峰(Mw/Mn<1.4),这说明透析后的产物为单纯的聚合产物。分别将透析后的1a和1b样品进行氢谱分析,如图4(见第90页)为共聚物不同单体比列的1H NMR,1b的1H NMR也与1a的结果一致,图中只出现了单体PEGMEMA的特征峰,与单体PEGMEMA均聚反应的1H NMR图(见第90页图5)一致。其他两种单体的特征峰并没有显示出来,说明这种组分的单体并没有形成我们所需要的两性离子共聚物,由于两性离子单体的加入会限制另外两种单体的共聚反应,因此将组分中两性离子的比例降低,PFMA单体的比例增加,合成出的样品分别为1c和1d。同样对这两种样品进行核磁和GPC的测试分析,结果如图3所示,1c和1d样品经过共聚之后能够形成单一的聚合物,GPC曲线呈对称的单峰(Mw/Mn<1.35),说明经过对单体比例的调整可以发生稳定的共聚反应,且产物均一。两种比例样品的氢谱和氟谱数据(图4)显示PFMA和PEGMEMA两种单体均发生了聚合反应,1H NMR和19F NMR中只出现了两种单体的特征峰,但是两性离子的特征峰却没有出现。通过对比分析可以看出,3种单体的共聚反应一定要协调好组分比和竞聚率之间的平衡关系,两性离子在聚合反应中的活性低且添加量不能过高,这样矛盾的两种因素限制了两性离子RAFT共聚的应用。另外两种单体的RAFT共聚活性高,但是也会出现组成比不同而导致最终聚合物中单体剩余的情况,仍然需要探索不同的两性离子聚合物的制备方法。
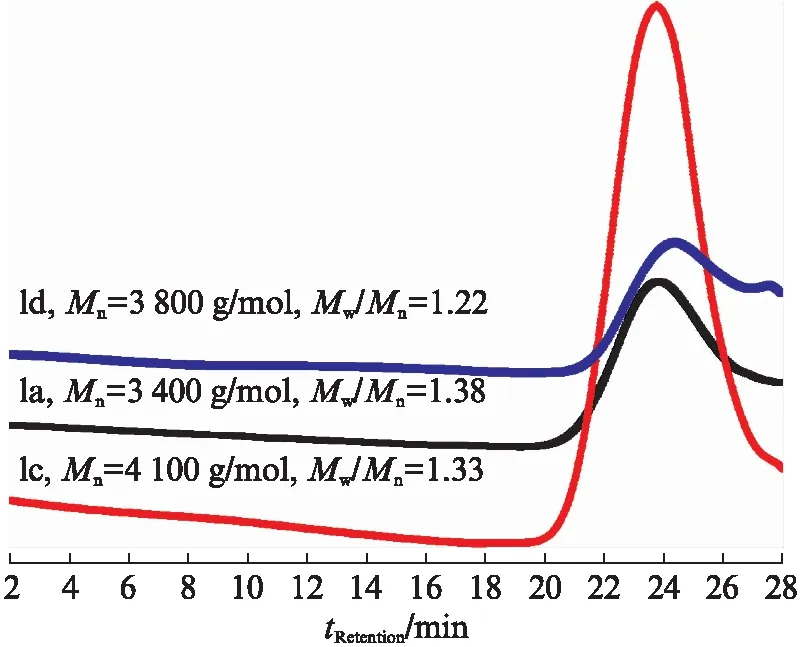
图3 THF中PCB-co-PPFMA-co-PEGMEMA 共聚物的GPC流出曲线Fig.3 GPC traces of PCB-co-PPFMA- co-PEGMEMA in THF
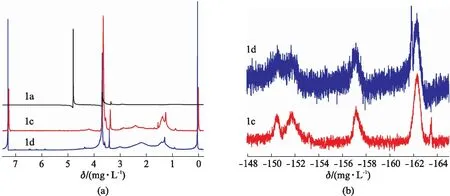
图4 D2O和DMSO中PCB-co-PPFMA-co-PEGMEMA共聚物的1H NMR和19F NMR谱图Fig.4 1H NMR and19F NMR spectrums of PCB-co-PPFMA-co-PEGMEMA in D2O and DMSO
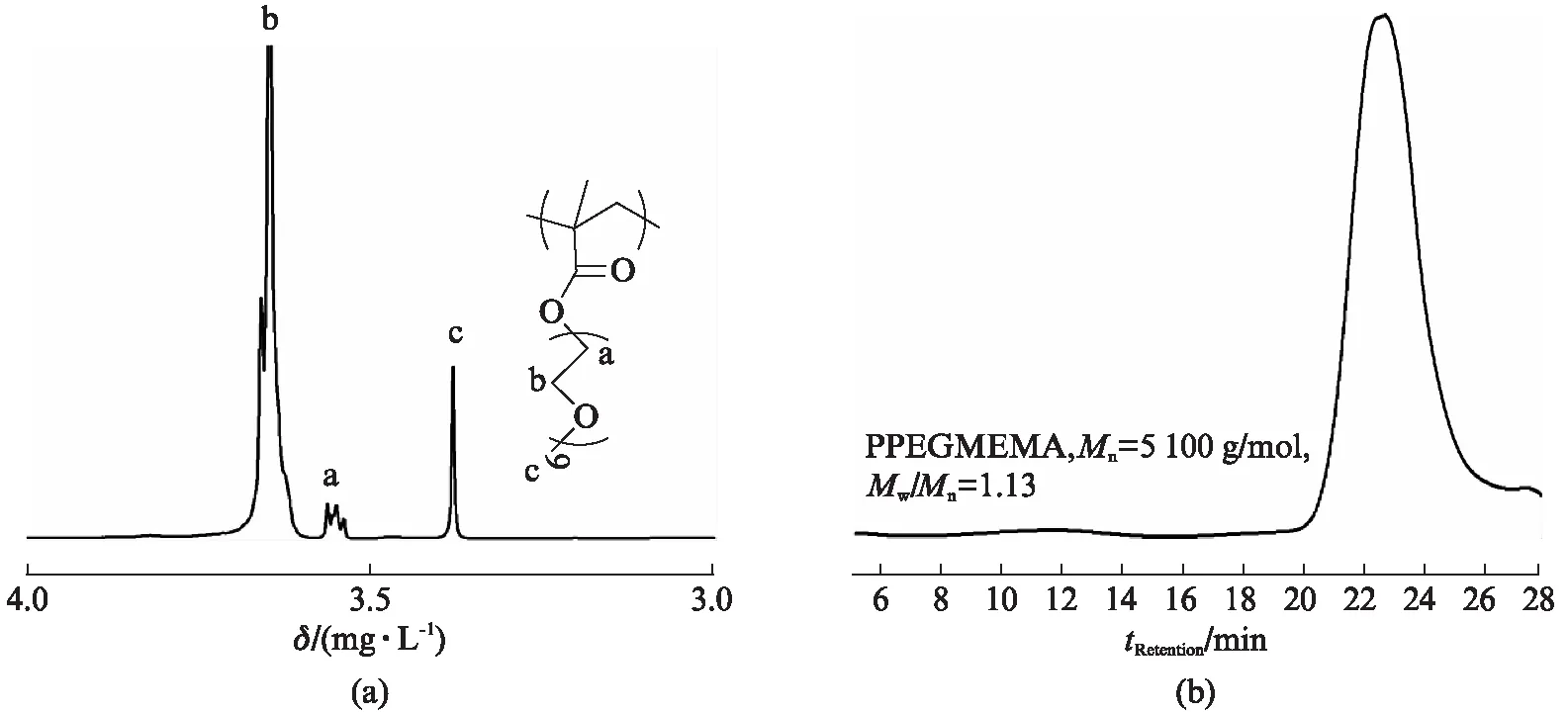
图5 CDCl3和THF中均聚物PPEGMEMA的1H NMR谱图和GPC流出曲线Fig.5 1H NMR spectrum and GPC trace of PPEGMEMA in CDCl3 and THF
2.4 氨基二茂铁对两性离子共聚物PCB-co-PPFMA-co-PEGMEMA修饰后的合成分析
我们尝试利用氨基二茂铁对带有甲基丙烯酸PFMA侧链的三元共聚物PCB-co-PPFMA-co-PEGMEMA进行取代反应,来探究PFMA结构的后修饰策略是否能够成功通过带有茂环的大位阻来实现。我们利用核磁对已经透析和后修饰的聚合物进行检测,图6分别为后修饰之后聚合物的1H NMR谱和19F NMR谱图。从氢谱图中可以明显看出,修饰透析之后的核磁信号峰有了明显的减少,但是在3.64处仍然能够观察到PEGMEMA单体的质子峰,但是其他单体峰的位置不明显。1H NMR(300 MHz,CDCl3): 5.30(s,1H),3.64(s,5H),3.38(s,2H),1.25(s,3H)。如图6中氟谱所示,反应后体系中不存在PFMA基团的19F NMR信号(-153,-158,-163 ppm),说明PFMA侧链结构完全被氨基二茂铁取代,形成了新的丙烯酰胺类侧链。实验结果说明,聚合物中的PFMA侧链可以通过加入氨基二茂铁实现侧链的后修饰和功能化。
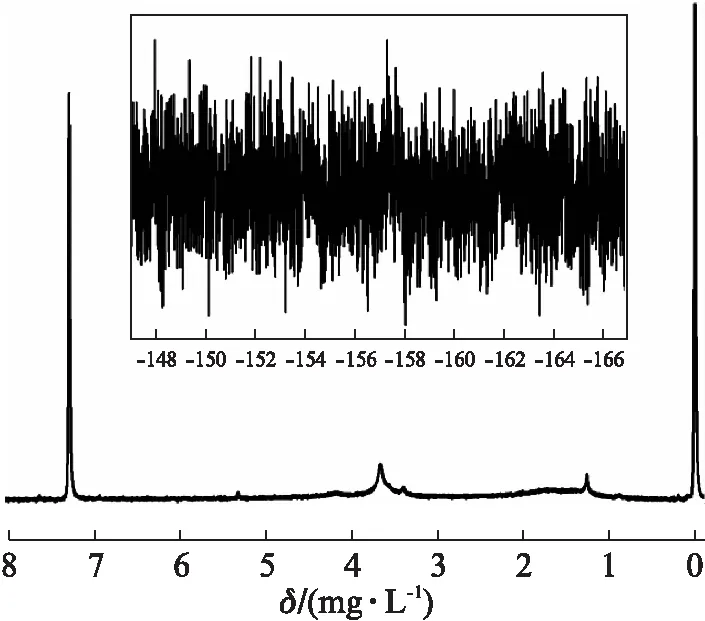
图6 CDCl3中修饰反应后PCB-co-PPFMA-co-PEGM- EMA的1H NMR和19F NMR谱图Fig.6 1H NMR and 19F NMR spectrum of PCB-co- PPFMA-co-PEGMEMA after reaction in CDCl3
2.5 两性离子共聚物PCB-co-PDMAEMA-co-PEGMEMA的合成分析
图7(a)为PCB-co-PDMAEMA-co-PEGMEMA的1H NMR谱分析图,从图中我们可以清楚地看到δ3.64,δ3.37和δ3.54位置处分别对应于PEGMEMA单体中的—(CH2)2O,—OCH3和—OCH2CH2链段,δ2.58和δ2.27分别对应于DMAEMA单体中的—NCH2和—(CH3)2链段[20]。1H NMR谱图结果说明合成的聚合物中出现了DMAEMA和PEGMEMA单体,但是却没有检测到两性离子的基团特征峰,核磁的分峰数据如下:1H NMR(CDCl3):δ3.63(s,19H),3.53(s,1H),3.36(s,3H),3.09(d,J=213.8 Hz,6H),2.42(d,J=118.1 Hz,20H)。1H NMR的结果中未检测到两性离子单体信号。图7(b)为聚合物2a的GPC流出曲线,沉降之后聚合物的GPC曲线没有完全的对称,说明聚合物中还有未反应的单体存在,且聚合物的分散度较高,说明聚合体系反应不具备可控/活性自由基聚合的典型特征。因此得出结论,CBMA单体与另外两种单体在RAFT聚合体系下无法进行反应。
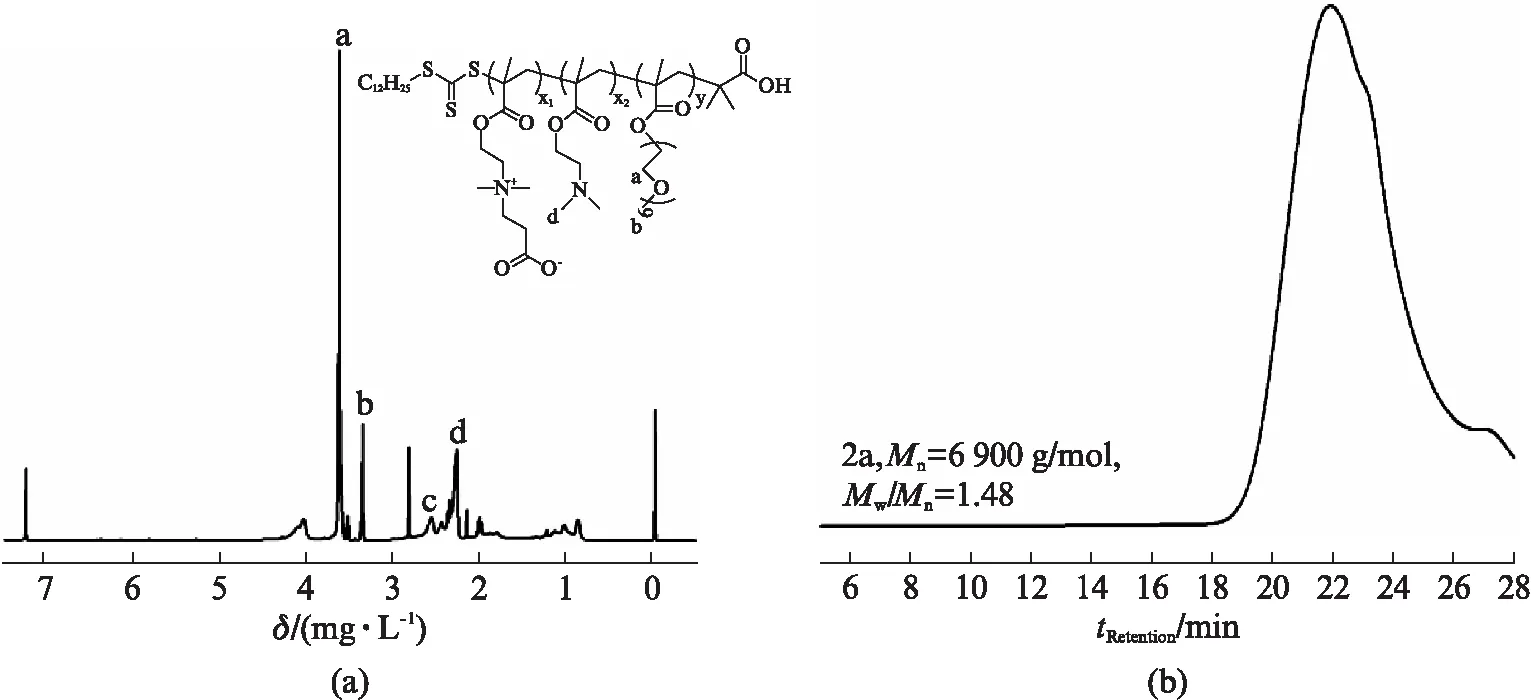
图7 CDCl3和THF中PCB-co-PDMAEMA-co-PEGMEMA的1H NMR谱图和GPC流出曲线Fig.7 1H NMR spectrum and GPC trace of PCB-co-PDMAEMA-co-PEGMEMA in CDCl3 and THF
3 结 论
本研究利用RAFT聚合方法研究CBMA与其他功能性单体的聚合反应条件和相关性能。以CBMA为两性离子模型,制备具有可替换的功能性单体和PEG基团的三元无规共聚物。在单因素实验基础上,对聚合反应体系的链转移剂(CTA)、溶剂、单体浓度、反应时间及反应温度进行筛选,以聚合反应的程度为考察依据筛选出最佳的反应条件。利用甲基丙烯酸五氟苯酯(PFMA)和聚乙二醇甲醚丙烯酸酯(Poly(ethylene glycol)methyl ether acrylate)与CBMA在不同条件下进行RAFT聚合尝试,以期制备出同时具有两性离子和PEG基团的双重抗生物污染的共聚物,同时也对三元共聚以及可替换的功能性单体进行了探索。

