经胆囊板入路与传统腹腔镜胆囊切除术治疗胆囊结石临床疗效对比研究
肖乐,江宗兴,罗皓,王涛,谭震,汪涛
全军普通外科中心,西部战区总医院,成都 610083
自1987 年Mouret 医生[1]开展首例腹腔镜胆囊切除手术(laparoscopic cholecystectomy,LC),由于其疼痛轻微、切口美观、恢复快的特点,迅速取代了开腹胆囊切除术成为国内外治疗胆囊结石病的标准手术方式[2]。三十多年来,胆管损伤依然是LC 无法回避的话题,也是最为严重的并发症之一,目前国内胆囊切除术中导致胆管损伤的发生率稳定于0.2%~0.5%[3]。在通过改进手术入路从而减少LC 医源性胆道损伤的策略方面,国内学者不断探索,已报道了沿胆囊管逆行追踪法[4]、胆囊后三角解剖入路[5]、Rouviere 沟引导的胆囊后三角入路[6],以及胆囊动脉入路[7]等方法。随着微创技术的发展,LC 朝着机器人外科、单孔腹腔镜、经自然腔道外科、日间手术、精准外科,以及快速康复等方向发展,降低并发症发生率、减少手术过程对患者日常工作生活的影响是外科医生努力追求的目标。结合胆道外科精细解剖技术发展,笔者近年来实践LC 过程中小结出一种新的手术策略,即经胆囊板(cystic plate)入路,可能兼具有规避术中胆道损伤风险与体现精准外科理念促进术后快速康复的优势,报告如下。
1 资料与方法
1.1 临床资料
收集西部战区总医院全军普通外科中心肝胆胰病区2016 年7 月~2019 年12 月期间完成的择期全麻下LC 的胆囊结石患者280 例,其中男110 例,女170例;年龄平均46.6 岁。入选条件:(1)年龄16~85 岁,患者均有症状且经本中心专科彩超证实胆囊结石,胆囊壁厚0.2~0.5 cm;(2)若发现胆总管扩张(大于0.6 cm)需进一步完成MRCP 排除胆总管梗阻可能;(3)入院心电图、胸片/胸部CT、心彩超,以及常规化验项目无手术禁忌证,60 岁以上患者经肺功能和动脉血气分析评估可耐受手术。排除条件:(1)合并胆总管结石或术后胆囊病检证实为恶性肿瘤;(2)既往上腹部开腹手术史;(3)急性胆囊炎疼痛超过72 h,或既往化脓性胆囊炎经过胆囊穿刺引流后。全部患者由一个治疗小组收治并完成手术。根据本治疗组2018 年2 月以后完全应用“胆囊板”入路技术完成LC 的时间点,之前的病例设置为对照组(170 例),时间点之后的病例为实验组(110 例)。所有病例的患者及家属取得参与本研究的书面同意书。
1.2 研究方法
1.2.1 “胆囊板”入路概念 肝大胆管和血管周围的结缔组织形成Glisson 鞘包绕肝门构成肝门板系统(hepatic hilar plate system),包括肝门板(hilar plate)、胆囊板与脐板[8],肝外部分由肝十二指肠韧带表面的浆膜覆盖。胆囊壁分为4 层,最外层浆膜与肝十二指肠韧带外侧浆膜相延续,而胆囊床侧胆囊壁缺乏浆膜层,对侧肝由Laennec 被膜覆盖,即位于包膜内侧覆盖肝实质表面的菲薄膜性结构(裸区无包膜,肝实质直接由Laennec 被膜覆盖),两者间存在潜在的间隙。胆囊板即胆囊壁4 层结构的第3 层-结缔组织层,与门板系统中的肝门板相延续(图1)。因此,理论上胆囊板与肝总管表面覆盖的肝门板之间存在解剖上的潜在间隙。“胆囊板”入路即在胆囊三角区域打开浆膜,使用电钩始终沿胆囊板逐步拓展、紧贴胆囊侧分离胆囊壶腹、胆囊管与肝总管,直至裸化胆囊管,显示胆囊与胆总管之间的唯一通道。
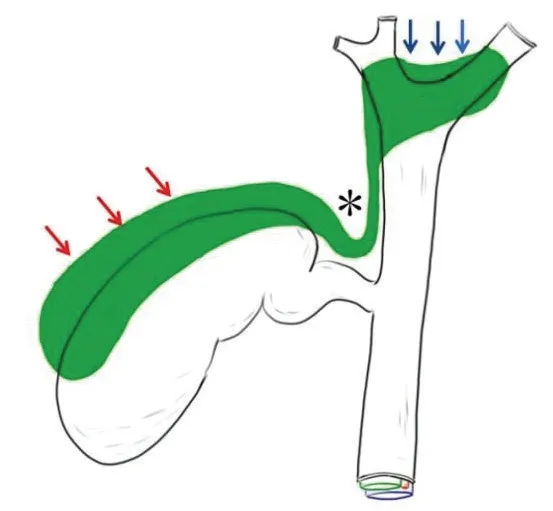
图1 胆囊板与肝门板示意图 绿色区域为概念区域,红色箭头指胆囊板,蓝色箭头指肝门板,*号为胆囊板与肝门板之间潜在的解剖间隙Fig.1 Schematic diagram of cystic plate and hepatic portal plate Cystic plate (red arrow) and hepatic portal plate(blue arrow) was marked in green,* potential space between the cystic plate and the hepatic portal plate
1.2.2 “胆囊板”入路LC 手术 全身静脉麻醉后,仰卧头高脚低左倾位,脐旁建立10 mm 观察孔,剑突与右侧肋骨夹角处建立12 mm 主操作孔,要利于右手器械向上挡住肝方叶,胆囊底腹壁投影位置下方3 cm建立5 mm 辅助孔,要利于胆囊床引流管低位引流。左手器械向右下方牵拉胆囊壶腹,右手持电钩杆向上挡住肝方叶,暴露胆囊三角区域,识别胆囊管淋巴结与胆囊三角“脂肪窗”,在靠近胆囊侧电钩打开胆囊浆膜(图2a),沿胆囊床前缘打开浆膜(图2b)。左手器械向左前方牵拉胆囊壶腹,暴露胆囊后三角,沿胆囊床后缘尽可能打开浆膜(图2c)。左手器械向右下方牵拉胆囊壶腹,预计胆囊动脉走形范围内,使用电钩勾起少量组织,靠近胆囊侧逐层打开胆囊三角区域,裸化管道结构,识别胆囊动脉(图2d)后使用生物夹夹毕后离断。继续向上沿胆囊床前缘(图2e)、向下围绕胆囊管拓展,分离胆囊板与肝总管之间的间隙(图2f)。左手器械向右前方牵拉胆囊壶腹,使胆囊壶腹向右下前方旋转,紧贴胆囊板进行解剖,所遇超过3 mm(含3 mm)管道结构均使用生物夹夹毕后离断,注意胆囊动脉后支及胆囊床回流静脉;由壶腹部与胆囊管结合处即“象鼻”处(图2g),向胆总管方向,紧贴胆囊管将胆囊板完全从肝门板分离。使用生物夹在距离胆总管0.5 cm 处夹闭胆囊管并离断(图2h),将胆囊完全从胆囊床分离(图2i),电凝棒处理胆囊床(图2j)。胆囊床留置16 号皱襞式负压引流管。

图2 “胆囊板”入路LC手术步骤a:*示脂肪窗 b:红色箭头示胆囊床前缘浆膜 c:红色箭头示胆囊床后缘浆膜d:白色箭头示胆囊动脉e:*示胆囊前缘浆膜打开后胆囊板与肝床的间隙f:*示胆囊板与胆总管之间的间隙 g:黄色箭头示“象鼻”处 h:*示生物夹i:*示完全切除的胆囊j:*示胆囊床Fig.2 Surgical procedure of cystic plate approacha: * indicated fat window;b: red arrow showed the ventral serous membrane of the gallbladder bed; c: red arrow showed the dorsal serous membrane of the gallbladder bed; d: the white arrow showed the cystic artery; e: * showed the space between the cystic plate and the hepatic portal after the ventral serous membrane was opened; f:*indicated the space between the cystic plate and the common bile duct; g:yellow arrow showed the Hartmann pouch (similar to an elephant’s trunk); h: *showed the clip; i:* showed the gallbladder; j:* showed the gallbladder bed
1.2.3 术后处理 术后第1 d 复查血常规、肝功能、电解质,第2 d 复查腹部彩超,48 h 内引流量小于150 mL、且性质无异常则拔除腹腔引流管。手术当日21点、术后第1 d 9 点记录疼痛视觉模拟评分(VAS)。
1.2.4 观察指标与统计学方法 对比实验组与对照组术前临床资料,结石大小数量(cm,n)、术中出血总量(mL)、手术时间(min)、生物夹使用个数(n)、中转开腹率(n%),以及术后VAS(n)、术后出院天数(d)、并发症发生率(n)、术后引流液体总量(mL)。采用SPSS 软件进行统计分析,两组间计量资料比较采用t检验,计数资料比较采用χ2检验,检验水准a=0.05。
2 结果
两组间年龄、性别、结石大小数量无差异,手术时间、中转开腹率、手术当日疼痛评分、并发症发生率、术后住院天数无差异;实验组术中出血量、生物夹使用数目、术后引流液总量较少,术后第1 天疼痛评分更低,有统计学差异(表1)。实验组2 例、对照组3 例出现术后一过性胆红素增高,最高58 mmol/L,保肝治疗后好转,考虑泥沙样胆总管结石排石,实验组2 例、对照组2 例切口感染,加强换药后康复出院。实验组1 例、对照组3 例中转开腹,主要原因为胆囊三角区域炎症重,术野渗血多。所有病例随访6 月无胆道结石发生。

表1 两组患者围手术期资料Tab.1 Baseline characteristics of all patients in each group
3 讨论
我国胆道外科之父黄志强院士曾将医源性胆道损伤称为“胆道外科永远的痛”。虽然LC 胆管损伤发生率不高,但由于手术基数巨大和其所造成的“灾难性”后果,LC 术中胆道损伤永远是需要充分重视的问题。1995 年Strasberg 等[9]提出胆囊三角解剖的“Critical View of Safety(CVS)”原则,即离断胆囊管前确认其为肝外胆管进入胆囊的唯一管道,并以此作为最终确认胆囊管的黄金准则。西南医院肝胆外科回顾分析LC 胆道损伤病例诊治过程发现:肝门部解剖变异确实可能增加LC 术中发生胆管损伤的风险,但绝大多数的LC 胆管损伤发生在解剖结构清晰、无肝门部解剖变异的手术中,特别是在手术医生试图显露“唯一管道”的过程中[10,11]。胆道变异、三角局部炎症、术野渗血不清晰、电外科器械使用错误等原因易致手术医生做出错误的判断。最常见的LC 术中胆道损伤是误将肝总管判断为胆囊管后离断,笔者认为可能与识别胆囊管入路方式有关。Hugh[12]将航空航海领域的风险规避原则引入LC,提出基于Rouviere 沟的解剖定向技术避免胆管损伤。国内学者也在此方面不断探索,进一步优化手术策略,规避胆管损伤风险。
传统腹腔镜胆囊切除术手术策略通常分为:“顺行”胆囊切除,即胆囊三角分离并离断胆囊动脉和胆囊管,夹闭后离断,由胆囊壶腹至胆囊底方向顺行剥离胆囊,是最经典的胆囊切除方式,其优势为利于三角区域暴露、分离胆囊快捷;“逆行”胆囊切除,即首先分离并离断胆囊动脉(或者不处理胆囊动脉),由胆囊底部至胆囊壶腹方向逆行剥离胆囊,由于最后离断胆囊管,完全确定“唯一管道”,较为可靠、放心,但手术暴露相对困难。对于胆囊三角区域使用分离方式多为钝性分离或钝性+锐性分离,留下管道结构后再夹闭离断,其优点在于分离速度快,不易损伤主要的管道结构。由于钝性分离具有一定盲目性,可能引起细小胆管、血管、淋巴管损伤导致渗血、渗液。
“胆囊板”入路的理论基础是胆囊壶腹以及胆囊管的纤维组织层与肝总管区域肝门板相延续并存在解剖上可分离的间隙,经胆囊板入路拓展裸化胆囊三角区域,确认“唯一管道”,可以理解为部分逆行切除,兼顾了传统“逆行”、“顺行”胆囊切除的安全性与高效性。变异的胆囊管汇入肝总管的形态分为汇入右肝管、右副肝管、或者低位和高位汇入胆管,以及极为罕见地汇入交通性副肝管等,高位汇入胆总管或者右肝管/右副肝管是需要警惕的情况。笔者应用“胆囊管”入路发现相当部分胆囊管“高位汇入”胆总管,胆囊管“增粗”的病例实际为胆囊管在肝门板区域迂曲,通过紧贴胆囊板往胆总管方向分离,类似于降低肝门板技术,将胆囊板与肝门板之间延续且折叠的间隙打开,使得胆囊管离断平面远离肝外胆管。同时胆囊三角区域精细的解剖可更清楚地识别管道结构,减少术中出血量与术后引流总量,从而减少患者术后疼痛,避免盲目使用生物夹,并未显著增加手术时间。
值得提出的是理解副肝管的变异方式有助于LC术中胆囊管离断平面的把握。副肝管的定义为除左、右肝管外,直接来自肝内,具有引流肝某区域胆汁并汇入肝外胆道,包括肝总管、胆总管或胆囊管的胆管称为副肝管。蔡德亨等[13]解剖学专家早在80 年代通过尸体解剖归纳出我国人群副肝管的7 种分型。从解剖上看(图3),I、II、VII 型副肝管离胆囊管相对较远,较不易被误伤;III、V 型副肝管的汇入部位离胆囊管较近,损伤几率显著增加;而IV 型和VI 型副肝管常直接汇入胆囊管或与之形成交叉走行,因此误伤的概率极大。高分辨率腹腔镜、3D 腹腔镜设备普及应用增强了外科医生裸眼的分辨能力,利于手术医生看到更清晰的结构、完成更精细解剖。过去认为的“迷走胆管”以及胆囊板的精细结构可能在高清腹腔镜下变得容易识别,经胆囊板入路的LC 手术策略充分利用这样的解剖学特点,可能缩短医生的学习曲线,提高LC 的安全性,并且利于患者快速康复。
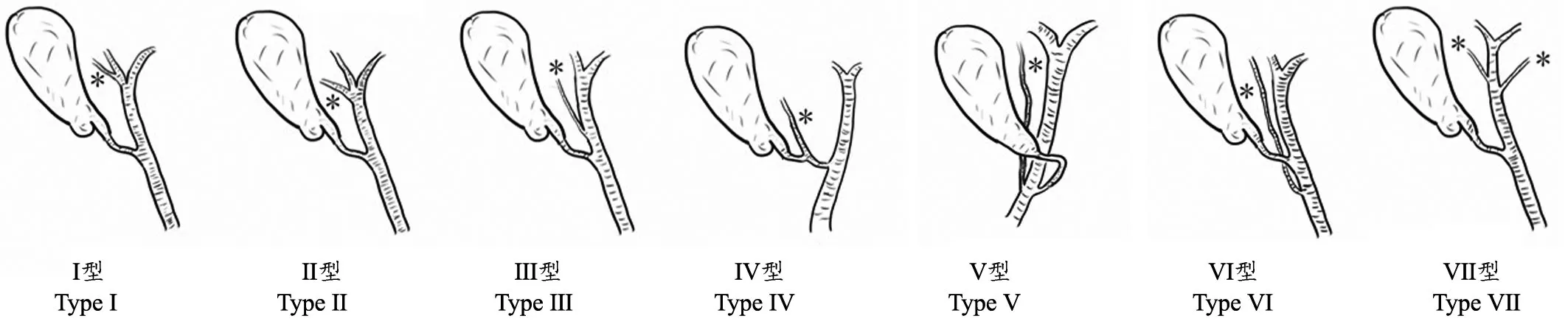
图3 副肝管的7 种分型特点Ⅰ型:副肝管汇入右/左肝管Ⅱ型:副肝管汇入左右肝管分叉Ⅲ型:副肝管汇入肝总管Ⅳ型:胆囊管汇入副肝管Ⅴ型:胆囊管左侧汇入胆总管,副肝管汇入右侧胆总管Ⅵ型:副肝管汇入胆总管Ⅶ型:双副肝管汇入肝总管*指示副肝管Fig.3 Characteristics of 7 types of accessory hepatic ductTypeⅠ:accessory hepatic duct drained into the right/left hepatic duct;Type Ⅱ:accessory hepatic duct drained into the bifurcation of left and right hepatic ducts;Type Ⅲ:accessory bile duct drained into the hepatic duct;Type Ⅳ:cystic duct drained into the accessory hepatic duct;Type Ⅴ:cystic duct drained into the left side of the common hepatic duct and the accessory hepatic duct drained into the right side of the common hepatic duct;TypeⅥ:accessory bile duct drained into the common hepatic duct;Type Ⅶ:double accessory hepatic ducts drained into the hepatic duct;(*Indicates the accessory bile duct)
对胆囊板解剖结构与变异副肝管类型的深入理解、应用高分辨率腹腔镜系统有助于更安全、精准地完成胆囊切除手术。经胆囊板入路LC 安全可行,理论上具有规避术中胆道损伤风险的优势。本研究病例数量较少,结论需要更长期、大量的实践进一步验证。

