云南金花茶叶不同极性提取物的抗氧化活性分析
何旭华,石志娇,彭小伟,阚 欢,赵 平,刘 云*
(1.西南林业大学 生命科学学院,云南 昆明 650224;2.西南林业大学 西南地区林业生物质资源高效利用国家林业局重点实验室,云南 昆明 650224)
云南金花茶,学名簇蕊金花茶(CamelliafascicularisH.T.Chang),又名云南显脉金花茶,为山茶科山茶属金花茶组植物,拥有独特的金黄色花瓣[1-3]。金花茶因其物种资源珍稀且具有较高的观赏价值,被称为“植物界大熊猫”和“茶族皇后”[4]。金花茶组植物在中国共有10个种和8个变种,主要分布于广西南部、贵州和云南[3]。云南的金花茶组植物资源主要分布在河口、个旧和马关,部分金花茶资源已遭到严重破坏,因此,进行科学研究对金花茶组植物的保护具有重要意义[5]。金花茶的叶和花均可作为药材,其含有丰富的矿质元素和生理活性成分,其中天然有机锗、硒和锌等微量元素达400多种,更有总黄酮、茶多酚、茶多糖、茶皂碱、茶黄酮和皂苷等诸多生理活性成分[1,6-7],使其成为一种很好的药食两用植物,有极高的研究价值[8]。金花茶有清热解毒、利尿消肿、止血止痛、延缓衰老、降血脂、抗肿瘤、抗过敏、增强机体免疫机能等药理作用[9-11]。金花茶的抗氧化活性与其含有的多酚类物质有关,如儿茶素、表儿茶素、牡荆素、异牡荆素、槲皮素-7-O-β-D-吡喃葡萄糖和山柰酚等,其中槲皮素-7-O-β-D-吡喃葡萄糖和儿茶素的抗氧化性较强[12]。农彩丽等[13]对金花茶总黄酮进行研究,发现金花茶总黄酮能抑制4种肿瘤细胞株体外增殖作用,有抗肿瘤功效。目前,对云南金花茶叶片不同极性提取物抗氧化活性的研究鲜有报道。因此,本研究采用不同极性溶剂对云南金花茶叶片进行提取,测定提取物中多酚和总黄酮的含量,并考察不同极性提取物的抗氧化活性,以期为云南金花茶叶片活性成分的分离和天然抗氧化剂的开发提供依据。
1 实 验
1.1 材料及仪器
云南金花茶(CamelliafascicularisH.T.Chang)的叶片,2019年10月29日采自云南省马关县八寨镇。将云南金花茶叶片于45 ℃干燥4 h,粉碎,取粒径<0.25 mm,备用。
芦丁标准品、没食子酸标准品,上海源叶科技有限公司;1,1-二苯基-2-三硝基苯肼(DPPH,纯度>97.0%)、2,2’-联氮-双-(3-乙基苯并噻唑-6-磺酸)(ABTS,纯度>98.0%),合肥博美生物科技有限责任公司。甲醇、石油醚、CHCl3、乙酸乙酯、正丁醇、NaNO2、NaOH、Al(NO3)3、Na2CO3、无水乙醇(纯度99.7%)、过硫酸钾、铁氰化钾、磷酸盐缓冲液、三氯乙酸(TCA)、6H2O·FeCl3,均为市售分析纯。
FD5-3型冷冻干燥机;HB 10 S96旋转蒸发仪;DK-98-Ⅱ电热恒温水浴锅;DHG-9240A电热恒温鼓风干燥机;YB-250A型高速多功能粉碎机;SHZ-DⅢ循环水式多用真空泵;UV-2600紫外可见分光光度计,岛津仪器(苏州)有限公司;SB25-12DTDS超声波清洗机,宁波新艺超声设备有限公司;5804 R多功能台式高速冷冻离心机,艾本德公司;SpectraMax190酶标仪,美谷分子仪器有限公司。
1.2 云南金花茶叶片提取物的制备
1.2.1粗提液 称250 g云南金花茶叶片粉末,按料液比1∶10(g∶mL)溶于甲醇,250 W、30 ℃超声波作用40 min,真空循环抽滤3次,合并滤液,旋转蒸发后得到云南金花茶粗提取物浸膏,用300 mL蒸馏水溶解成粗提液备用。
1.2.2不同极性溶剂提取物 参考文献[14]方法并略作调整制备不同极性提取物。取1.2.1节制备的粗提液300 mL于分液漏斗中,按体积比1∶1加入石油醚300 mL,摇匀、静置、分层,再取石油醚(体积比为1∶1)加入下层液,摇匀、分离。重复此步骤,直至下层液无色,收集合并上层液,为石油醚相萃取液。
取下层液依次加入氯仿、乙酸乙酯和正丁醇(体积比均为1∶1),重复上述过程,得不同极性萃取液。将各相萃取液旋转蒸发,冷冻干燥得云南金花茶石油醚相、氯仿相、乙酸乙酯相、正丁醇相、水相提取物,于4 ℃的冰箱避光存放,备用。
1.3 不同极性提取物成分的测定
1.3.1总酚的测定 选用福林酚法测定总酚含量[15],配制没食子酸标准品质量浓度为0.05 g/L的母液,母液稀释至不同质量浓度,通过测定不同质量浓度(x)的没食子酸溶液的吸光值(y)绘制标准曲线:y=0.039+82.371x,R2=0.999。将云南金花茶不同极性溶剂提取物配制成合适的质量浓度并测定吸光度值,依据没食子酸标准曲线算出云南金花茶不同极性溶剂提取物中多酚的含量。
1.3.2总黄酮的测定 参照文献[16]配制芦丁标准品质量浓度为0.05 g/L的母液,母液稀释至不同质量浓度,通过测定不同质量浓度的芦丁溶液的吸光值绘制标准曲线:y=0.019+13.186x,R2=0.999。将云南金花茶不同极性溶剂提取物配制成合适的质量浓度并测定吸光度,依据芦丁标准曲线算出云南金花茶不同极性溶剂提取物中总黄酮的含量。
1.4 提取物抗氧化能力的测定
1.4.1DPPH·清除能力 参考Hua等[17]的方法,配制质量浓度为0.05 g/L DPPH-无水乙醇溶液,将云南金花茶不同极性溶剂提取物配制成质量浓度为30、50、70、90、110、130和150 mg/L的样液,各取200 μL与DPPH-无水乙醇溶液置于0.5 mL的离心管中,混合均匀,在37 ℃的水浴中暗反应30 min,于96孔酶标板在517 nm处测定样品组吸光值(Ap)。用甲醇代替样液测定样品控制组吸光值(Aq),用无水乙醇代替DPPH-无水乙醇溶液测定空白组吸光值(Aw)。以Vc作阳性对照,比较云南金花茶不同极性溶剂提取物对DPPH·的清除率。
1.4.2·ABTS+清除能力 参考Li等[18]的方法,将7 mmol/L·ABTS+与5 mmol/L过硫酸钾溶液于棕色容量瓶中等体积混合,静置反应12 h,即得·ABTS+反应液。在734 nm处用蒸馏水稀释·ABTS+反应液至吸光值0.700(±0.02),避光现用。将云南金花茶不同极性溶剂提取物配制成质量浓度为250、500、750、1 000、1 250、1 500和1 750 mg/L的样液,取20 μL样液与380 μL·ABTS+反应液于96孔酶标板混合均匀,暗反应6 min,在734 nm测定Ap。用甲醇代替样液测定Aq,用蒸馏水代替·ABTS+溶液测定Aw。以Vc作阳性对照,比较云南金花茶不同极性溶剂提取物对·ABTS+的清除率。
1.4.3·OH清除能力 参照Mao等[19]的方法,将云南金花茶不同极性溶剂提取物配制成质量浓度为1 000、2 000、3 000、4 000、5 000、6 000和7 000 mg/L的样液,取云南金花茶不同极性溶剂提取物样液100 μL、9 mmoL/L FeSO4溶液100 μL、9 mmoL/L水杨酸-乙醇溶液100 μL和质量分数30% H2O2100 μL,于96孔酶标板混合均匀,避光反应1 h,在510 nm测定Ap。甲醇代替样液测定Aq,用乙醇溶液代替水杨酸-乙醇溶液测定Aw。以Vc作阳性对照,比较云南金花茶不同极性溶剂提取物对·OH的清除率。
1.4.4总还原能力 采用铁氰化钾法[20],将云南金花茶不同极性溶剂提取物配制成质量浓度为250、500、750、1 000、1 250、1 500和1 750 mg/L的样液,取样液、pH值6.6磷酸缓冲液、1%铁氰化钾各100 μL混合均匀,置于50 ℃的水浴中20 min,加入10% TCA溶液100 μL,混合均匀后离心(4 000 r/min)10 min。分别取100 μL上清液、蒸馏水和1%三氯化铁于96孔酶标板,混合均匀静置10 min,700 nm处测吸光值。以VC作阳性对照。
1.4.5自由基清除率和IC50值的计算 DPPH·、·ABTS+、·OH清除率计算公式如下:
式中:Ap—样品组的吸光值;Aq—样品控制组的吸光值;Aw—空白组的吸光值。
采用Origin 2018对数据进行拟合,得到清除率(Y)和质量浓度(X)的二元一次方程,求清除率(Y)为50%,对应的质量浓度(X)值,即为IC50值。
1.4.6数据分析 采用SPSS 20.0和GraphPad Prism 8软件对试验数据进行分析,利用Origin 2018对实验数据进行拟合,得到拟合方程,进行平行试验3次,以平均值±标准偏差为结果。
2 结果分析
2.1 提取物中多酚和总黄酮含量
云南金花茶叶片提取物中多酚和总黄酮含量见表1。水相提取物中多酚含量最高,为(140.259±5.989)mg/g;正丁醇相中多酚含量最低,为(62.866±2.278)mg/g;石油醚相和氯仿相的多酚含量无显著差异(P>0.05)。水相提取物总黄酮含量最高,为(102.324±1.095)mg/g,略高于乙酸乙酯相;正丁醇相总黄酮含量最低,为(26.484±3.047)mg/g,总黄酮含量均存在差异显著(P<0.05)。
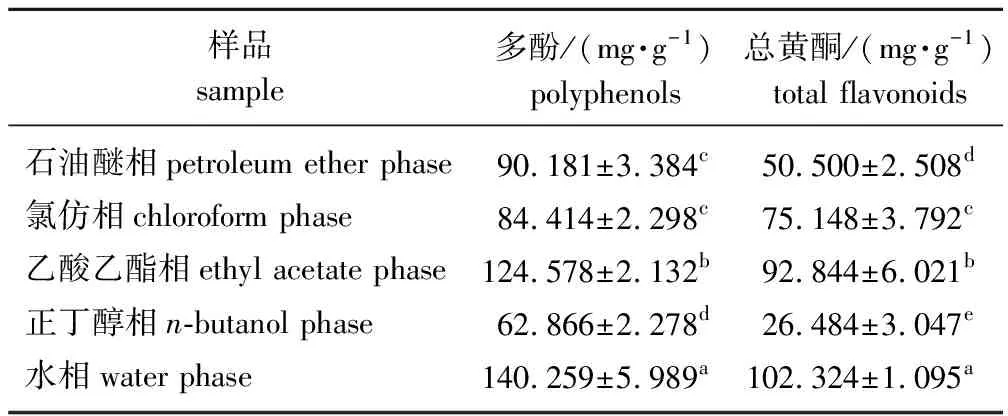
表1 云南金花茶不同极性提取物中多酚和总黄酮含量1)
2.2 不同极性提取物的抗氧化活性
2.2.1DPPH·清除能力 DPPH·无水乙醇溶液呈紫色,当加入有清除DPPH·能力的物质时,会使反应系统的颜色褪色,因而可以通过吸光值变化来定量分析[21-22]。云南金花茶叶片不同极性溶剂提取物对DPPH·清除能力见图1(a)。当Vc质量浓度为13 mg/L时,对DPPH·的清除率高达94.046%。云南金花茶不同极性提取物质量浓度在30~150 mg/L时,对DPPH·清除效果随样品浓度增大而增强,水相对DPPH·的清除率高于其他极性提取物。半数抑制质量浓度(IC50)可衡量各提取物对DPPH·的清除能力,IC50值越小,说明清除能力越强,反之越弱。云南金花茶不同极性溶剂提取物清除DPPH·的能力大小顺序为:水相((38.634±2.556)mg/L)>乙酸乙酯相((50.845±3.985)mg/L)>氯仿相((63.598±3.854)mg/L)>石油醚相((66.197±5.950)mg/L)>正丁醇相((119.810±8.207)mg/L)。
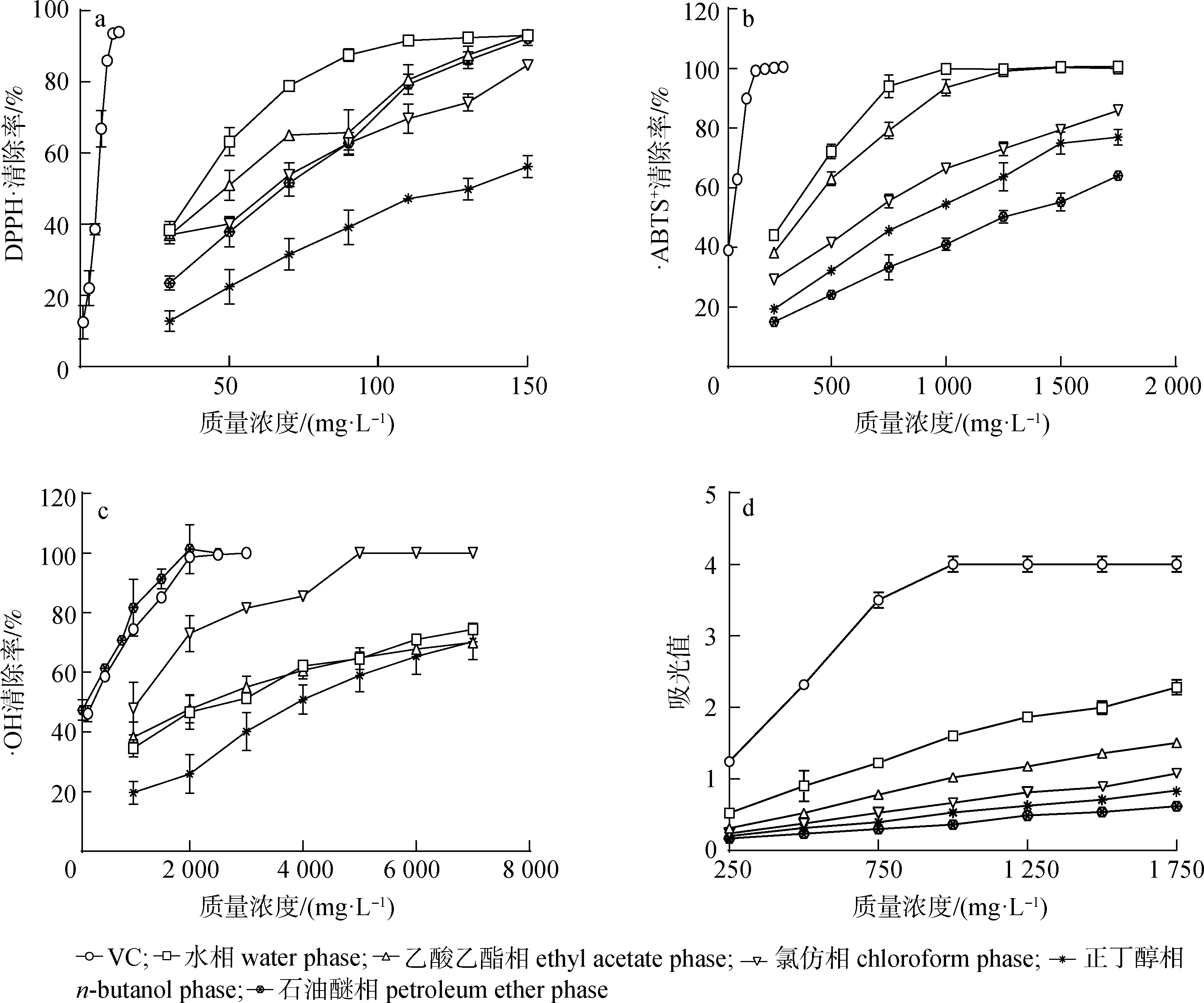
a.DPPH·;b.·ABTS+;c.·OH;d.总还原能力total reducing power
2.2.2·ABTS+清除能力 ·ABTS+清除能力主要是根据电子转移实现的,而且氢原子转移是边缘反应途径[23]。·ABTS+呈蓝绿色是由·ABTS+和过硫酸钾反应生成,当加入能清除·ABTS+的物质时,反应系统颜色会褪色[24]。云南金花茶叶片不同极性溶剂提取物对ABTS·清除能力见图1(b)。由图可知,不同提取物对·ABTS+均有较好的清除率。当提取物质量浓度在250~1 750 mg/L范围内,清除率随质量浓度增大而升高。Vc在质量浓度为250 mg/L时,对·ABTS+清除率高达100%,高于云南金花茶不同提取物的清除效果。云南金花茶不同极性溶剂提取物清除·ABTS+的能力大小顺序为:水相((276.610±8.416)mg/L)>乙酸乙酯相((362.754±22.555)mg/L)>氯仿相((643.692±29.651)mg/L)>正丁醇相((865.188±35.706)mg/L)>石油醚相((1 276.462±39.405)mg/L)。
2.2.3·OH清除能力 过氧化氢与二价的铁离子反应形成芬顿系统,产生·OH,在该系统中加入水杨酸溶液时,·OH与水杨酸形成羟基化合物即2,3-二羟基苯甲酸,当加入有清除·OH的物质时,有色化合物生成会减少,吸光值会降低[25]。云南金花茶叶片不同极性提取物对·OH清除能力见图1(c)。由图可知,提取物对·OH有明显的清除效果,提取物质量浓度在300~3 000 mg/L范围时,石油醚相对·OH的清除率高于Vc,当质量浓度为2 000 mg/L时,石油醚相和Vc对·OH的清除率均达到了100%,明显高于其他相。质量浓度在300~7 000 mg/L范围时,各极性提取物清除·OH的能力大小顺序为:石油醚相((180.880±49.568)mg/L)>氯仿相((1 130.630±157.932)mg/L)>乙酸乙酯相((2 472.160±826.007)mg/L)>水相((2 601.500±164.756)mg/L)>正丁醇相((3 936.230±621.700)mg/L)。
2.2.4总还原能力 以铁氰化钾法测不同提取物的总还原能力,还原生成的亚铁氰化钾与三氯化铁反应生成普鲁士蓝,吸光值越大反应样品的还原能力越强,即抗氧化能力也越强[26]。云南金花茶叶片不同极性溶剂提取物的总还原能力见图1(d)。由图可知,Vc的吸光值高于不同提取物,不同提取物均具有一定的还原力。当提取物质量浓度达到1 000 mg/L,反应体系中的三价铁离子已经被完全反应,故呈现平缓趋势。不同极性溶剂提取物总还原能力的吸光值大小为水相(2.281±0.103)>乙酸乙酯相(1.504±0.021)>氯仿相(1.077±0.056)>正丁醇相(0.838±0.021)>石油醚相(0.618±0.022)。
2.2.5抗氧化活性及相关性分析 云南金花茶叶片不同极性溶剂提取物对自由基清除率和总还原力的曲线方程及IC50值见表2。由表2可知,拟合方程的R2>0.95,R2越接近1,表明拟合方程的拟合程度较好。
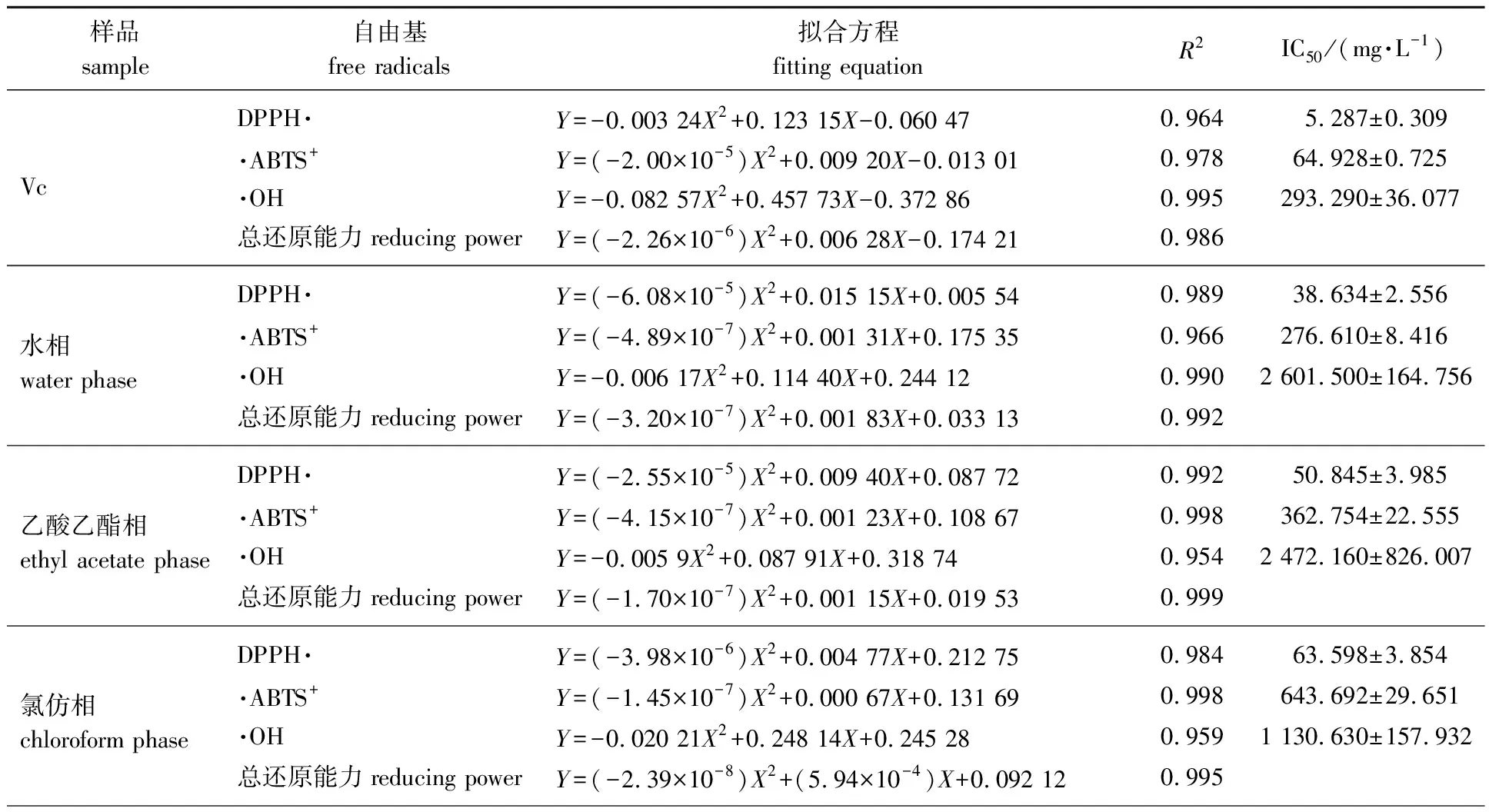
表2 云南金花茶不同极性提取物对自由基清除率和总还原力的曲线方程及IC50值
由表2的IC50值数据可以看出:水相对DPPH·、·ABTS+的清除能力最强,石油醚相对·OH清除能力最强;正丁醇相对DPPH·、·OH的清除能力最弱,石油醚相对·ABTS+清除能力最弱。不同极性溶剂提取物抗氧化活性能力的比较见图2。图2直观表明:云南金花茶叶片不同极性溶剂提取物的总还原能力均较强,对DPPH·清除能力强于对·ABTS+和·OH清除能力,而对·OH清除能力最弱。这是因为云南金花茶提取物的抗氧性能力不仅取决于其所含的黄酮类的极性,还取决于黄酮类化合物对自由基的选择性和作用机理,不同极性溶剂提取物中黄酮类化合物的不同化学结构导致了其对不同自由基的清除能力的差异。
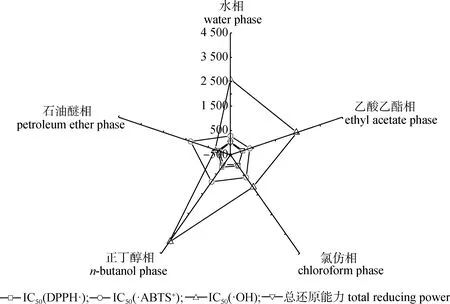
图2 云南金花茶不同极性提取物抗氧化活性雷达图
云南金花茶叶片不同极性溶剂提取物的抗氧化活性与多酚、总黄酮含量之间的相关性见表3。
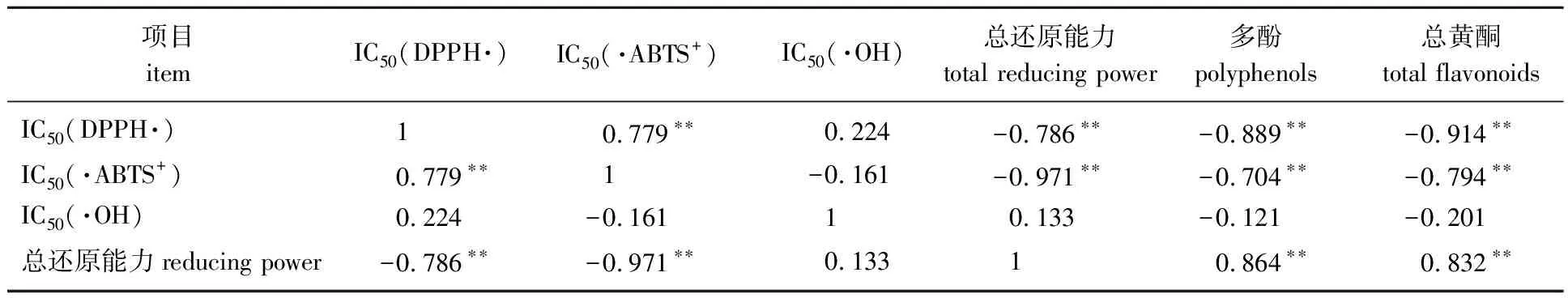
表3 云南金花茶不同极性提取物的抗氧化活性与多酚、总黄酮含量之间的相关性分析
由表3可知,不同提取物的4种抗氧化能力之间存在一定的相关性,其中DPPH·清除率的IC50、·ABTS+清除率的IC50及总还原能力之间存在极显著的相关性,三者间的相关系数分别为0.779、-0.786、-0.971(P<0.01);DPPH·、·ABTS+以及·OH清除率的IC50与多酚和总黄酮含量存在负相关,总还原能力与多酚和总黄酮的含量存在正相关,其中DPPH·、·ABTS+清除率的IC50以及总还原能力与多酚和总黄酮的含量存在极显著的相关性(P<0.01),表明云南金花茶叶片不同极性溶剂提取物的抗氧活性与多酚和总黄酮含量存在一定的剂量效应,多酚和总黄酮含量越高,抗氧化活性越强。
此外,水相和乙酸乙酯相中多酚和总黄酮的含量及其总体的抗氧化能力均高于氯仿相、正丁醇相和石油醚相。因此,云南金花茶叶片的抗氧化活性成分可能集中在水相和乙酸乙酯相,后期可进一步对其组分进行测定,分离单体化合物,确定具体的抗氧化物质,并基于体外抗氧化活性研究,利用细胞模型、动物模型分析不同极性提取物的抗癌活性。
3 结 论
3.1采用不同极性溶剂对云南金花茶叶片中的有效成分进行提取,其多酚提取能力依次为水>乙酸乙酯>石油醚>氯仿>正丁醇,总黄酮提取能力依次为水>乙酸乙酯>氯仿>石油醚>正丁醇。水相和乙酸乙酯相所含多酚为(140.259±5.989)和(124.578±2.132)mg/g,含总黄酮为(102.324±1.095)和(92.844±6.021)mg/g,均显著高于其他相(P<0.05)。
3.2云南金花茶叶片不同极性溶剂提取物的抗氧化活性测定结果表明:水相和乙酸乙酯相对DPPH·、·ABTS+的清除能力及总还原能力较强;石油醚相对·OH清除能力较强。DPPH·、·ABTS+的IC50值与总还原能力之间存在极显著的相关性,且与多酚和总黄酮的含量也存在极显著的相关性(P<0.01)。

