骨质疏松患者髋关节置换术的研究进展
孙长鲛 余鹏 许平平 李慧敏 谢兰兰 杨凯 蔡谞
一、背景
世界每年的关节置换术数量正趋于增加[1],髋部退行性疾病或外伤性疾病需要手术干预的比例在老年人群中较高。随着我国老龄化人群的增多,可以预见选择接受髋关节置换术 (hip arthroplasty,HA)改善生活质量的老年患者人数将会增加[2-3]。需要关节置换的骨关节炎患者同时也是发生骨质疏松症的高风险人群。我国卫健委发布的首个中国骨质疏松症流行病学调查结果显示,骨质疏松症已成为我国中老年人群的重要健康问题,50 岁以上人群骨质疏松症患病率为 19.2%,中老年女性骨质疏松问题尤甚,50 岁以上女性患病率达 32.1%,远高于同龄男性的 6.0%,而 65 岁以上女性骨质疏松症患病率更是达到了 51.6%。此外,我国男性骨质疏松症患病率与各国差异不大,但女性患病率显著高于欧美国家,与日韩等亚洲国家相近。因此,在未来的老龄化社会中,骨科医师会面对越来越多的骨质疏松患者进行 HA。
骨质疏松患者在进行 HA 时需要考虑几个重要的临床问题:髋关节骨关节炎和骨质疏松的关系,股骨解剖特点,假体的骨整合,假体选择,骨质疏松患者行 HA 的临床效果,骨质疏松增加并发症以及抗骨质疏松药物的 使用。
二、骨关节炎与骨质疏松的关系
骨关节炎和骨质疏松是老年患者常见的两种疾病,其患病率随着年龄的增长而增加。约 50年前,一项回顾性研究指出,发生股骨近端骨质疏松性骨折的患者其髋关节没有骨关节炎改变[4]。约 20年前,学者认为骨质疏松和骨关节炎具有相反的关系,骨关节炎可以保护人群免受骨质疏松的侵害,即如果患者发生了髋关节骨关节炎就很难发生骨质疏松性骨折,反之亦然[5]。但最近的一项研究发现,骨关节炎与骨质疏松似乎并不具有反比关系。在准备进行全髋关节置换术 (total hip arthroplasty,THA)平均年龄 > 70 岁的骨关节炎患者中,18% 的患者存在骨质疏松,41% 的患者存在骨量低下[6]。另一项研究对平均年龄 64.7 岁重度骨关节炎患者准备行非骨水泥 THA 的患者进行骨密度评估,发现 28% 的患者存在骨质疏松,45% 的患者存在骨量低下[7]。同时,与对侧髋关节相比,患有骨关节炎的髋关节在股骨颈处骨密度更高,而在大转子区域骨密度更低。其它研究也发现,准备接受 THA 和全膝关节置换术 (total knee arthroplasty,TKA)的骨关节炎患者人群中,同时存在骨质疏松的比例高达 26%,而这一比例与普通人群的骨质疏松患病率是相似的[8-9]。这提示过去医师可能低估了 THA 手术人群中骨质疏松患者的比例,建议在患者接受 THA 之前评估并改善骨骼质量,以确保获得最佳结果。可以在术前咨询患者本人钙和维生素 D 的摄入量,并建议患者戒烟及减少对骨骼质量有害的药物 (如可的松)剂量。测量高危患者的骨密度值可以帮助诊断骨质减少或骨质疏松。Chu 等[10]在 THA 术中获得了 39 例股骨头标本,其中骨关节炎组 19 例;同时伴有骨质疏松组 20 例,并使用 10 例健康尸体捐赠者的标本作为对照组。通过显微计算机断层扫描和显微有限元分析评估软骨下骨的显微结构和生物力学性能。通过组织学、组织形态学测量和免疫组织化学来评估软骨下骨重塑和软骨损伤情况。结果发现,与骨关节炎组相比,伴有骨质疏松组患者的软骨下骨畸形影响了骨微观结构,导致生物力学性能的恶化,可能会影响负荷应力从软骨到软骨下骨的传递,进而导致伴有骨质疏松患者的骨关节炎加重。该结果可能表明了骨关节炎和骨质疏松之间关系的作用机制,也说明软骨下骨的改变或骨质疏松可能会影响骨关节炎的发展,而骨代谢药物对软骨下骨的改善可能有助于减轻同时存在骨关节炎和骨质疏松患者骨关节炎病程的进展。
三、骨质疏松患者的股骨解剖特点
骨质疏松不仅会改变骨密度,也会随着年龄的增加改变骨的形态,骨质疏松会导致皮质骨厚度减少,皮质骨孔隙率的增加,因此骨质疏松患者往往存在与年龄相关的髓腔扩张[11]。这种骨髓扩张在绝经后女性中更为常见,因为绝经后期的特征就是骨质流失加速和髓腔扩张,因此骨质疏松患者进行 THA 时需要考虑到髓腔扩张的问题。Ahlborg 等[12]对 112 例绝经女性进行 19年的随访,发现在绝经后,受试者骨密度平均每年下降 1.7%,而髓腔宽度每年增加 0.9%。股骨髓腔扩张可能也是 THA 术后股骨假体松动的原因。Hofmann 等[13]将 30 例初次 THA 假体松动的病例与 30 例稳定 THA 患者进行对照研究,发现无菌性松动 THA 组其手术侧髓腔宽度增加程度是非手术侧的 2 倍,松动组的股骨髓腔宽度增大程度是稳定 THA 的 4 倍。而当松动组出现症状后,其手术侧髓腔宽度增加的速度会加倍。这说明当出现假体松动的症状后,需要尽早进行干预以避免过多骨丢失。
四、骨质疏松患者的假体骨整合
Brånemark 和他的同事创造了术语“骨整合”来描述钛与骨组织形成机械和功能互连而不插入结缔组织的能力[14]。骨整合表明假体与骨组织之间没有软组织,是直接接触的状态,其承受的负荷能通过这种直接接触持续不断地传递并分散到骨组织中。骨整合需要成骨细胞首先在植入体表面黏附、丛集,然后在假体表面分泌骨基质,使植入骨表面上的新骨直接生成,并从假体表面逐渐向骨创面生长、延伸。假体 - 骨界面骨整合被认为是人工关节置换术后的理想状态[15]。目前对骨整合的描述侧重于假体周围骨抵抗剪切力和拉力的能力,及在假体表面与宿主骨之间 50 μm 距离内防止纤维组织附着的能力[15]。传统观点认为,骨整合的速度主要与骨质量有关,骨质疏松患者转子间区域骨质量较差会导致骨整合失败,但目前的观点认为宿主骨质量并不是影响骨整合的惟一因素。Moritz 等[16]对平均年龄 64 岁进行 THA 手术患者的股骨粗隆部位进行骨活检,通过放射线立体分析 (radiostereometric analysis,RSA)测量,发现尽管转子间区域的松质骨质量差,但不会影响近端羟基磷灰石涂层的解剖型股骨假体早期骨整合。Nazari-Farsani 等[17]研究绝经后女性非骨水泥 THA 术后骨水泥柄移位的原因,前瞻性评估 65 例髋关节骨关节炎绝经后女性 (Dorr A 型或 B 型股骨解剖)的非骨水泥 THA,通过 RSA 评估股骨柄移位情况,结果表明人口统计学特征 (包括髋关节骨密度、年龄、股骨骨皮质厚度、髓腔闪烁指数)以及柄和髓腔的比例均与柄的下沉无关。其它研究也已证实,在解剖型非骨水泥型髋关节中,宿主骨质量不是维持假体主要稳定性或骨整合的惟一关键因素[18-19]。影响骨整合的因素较多,包括假体周围骨代谢情况、假体表面特性、假体设计、宿主骨质量、手术部位准备、假体初始稳定性、负荷条件、感染预防等。来自活化血细胞的生长和分化因子在界面释放并引发一系列生物事件,从而导致植入物周围的骨形成[20]。当假体发生适当的骨整合时,界面就几乎完全被骨填充[20]。假体表面形态也会直接影响成骨细胞和破骨细胞的附着和代谢[21],当使用表面粗糙的多孔植入物 (50~400 μm)时,可以获得最好的骨整合效果和骨骼固定。非骨水泥固定骨整合的一个挑战是在早期阶段防止微动,使骨骼和假体形成牢固的互相锁定,否则就可能形成纤维组织界面,影响骨整 合[22-23]。目前的文献表明如果采用合理的假体设计例如多孔涂层的椎形股骨柄,THA 术后即刻负重可以避免产生微动[24]。这些都为骨质疏松患者使用非骨水泥假体提供了理论依据。
五、骨质疏松患者的假体选择
骨水泥固定过去被认为是骨质疏松性患者行 HA 的金标准[25]。骨水泥固定可以提供即刻稳定性,患者可以在术后第 1 天就完全负重[25]。但是,一些骨质疏松患者的髓腔过宽,即使最大的骨水泥股骨柄也无法完全填充髓腔,这种情况下可能会导致骨水泥鞘的厚度增加 1~2 mm 以上,或股骨柄尺寸相对髓腔变小导致发生无菌性松动[26-27]。此外,在使用骨水泥的过程中患者病死率略有增加,并有发生脂肪栓塞、心血管、肺部疾病的风险[28-29]。因此,有更多医师使用非骨水泥柄并建议患者在术后早期部分负重,获得了良好的临床效果。但要注意的是,非骨水泥柄发生假体周围骨折的风险高于骨水泥柄,原因可能是骨水泥柄在打入假体过程中仅产生较低的环向应力。关节注册中心的数据也显示,非骨水泥型柄、高龄和骨骼质量差是假体周围骨折的主要诱因。来自 1995 - 2009年北欧人工关节注册中心 325 730 例骨水泥股骨柄和 111 899 非骨水泥柄的数据显示,非骨水泥柄发生假体周围骨折进行翻修的风险是骨水泥柄的 8.72 倍[30]。
在骨质疏松患者中使用非骨水泥柄时有一些注意事项。当使用带颈领的非骨水泥柄时,要注意这种柄的植入依赖于股骨近端的形态,在技术上具有一定挑战性。当使用羟基磷灰石涂层的非骨水泥柄以增强骨长入或使用双锥度柄时,要注意将假体打入骨质疏松患者的股骨时会增加环向应力及术中骨折的风险[31-32]。此外,如果髓腔较大需要使用大号非骨水泥柄可能会导致非骨水泥柄的打入困难,导致手术侧肢体变长,此时可以考虑采取适当的手术技巧,如股骨颈低位截骨,以避免下肢肢体不等长。在骨质疏松患者中使用大号非骨水泥柄的另一个担忧是应力遮挡。股骨柄较大时,应力遮挡更为突出。研究表明,26% 的全多孔涂层柄在 2年内会产生应力遮挡[33]。在近端涂层的股骨柄上也观察到了这种现象[34]。然而,应力遮挡的长期结果尚未知。
尽管无颈领非骨水泥柄 THA 在骨质疏松症患者中显示出良好的疗效,但对于骨质疏松性股骨颈骨折准备进行 THA 的创伤患者而言,可能需要谨慎使用无颈领非骨水泥柄。Pentlow 等[31]比较了普通患者和创伤患者两组人群,评估使用非骨水泥压配羟基磷灰石涂层柄的下沉情况。与普通人群相比,大多数创伤患者存在骨质减少或骨质疏松以及 Dorr C 型股骨形态。与普通人群相比,创伤患者人群在 6 个月时的翻修率和脱位率均更高 (均为 8.7%vs.0%)。4 例翻修中有 3 例是因为股骨假体下沉继发的脱位,作者得出结论,骨质疏松症发病率增加的创伤患者可能并不适合使用无颈领非骨水泥柄,因此,建议对于这类患者使用骨水泥柄或带颈领的非骨水泥柄。一项类似的研究中[35],作者将 Biomet Fracture Stem (BFX;Biomet UK Ltd.,Bridgend,UK)用于股骨颈骨折的 THA,平均随访期为 5年,通过 RSA 和双能 X 线骨密度仪 (dual-energy X-ray absorbtiometry,DEXA)扫描,结果发现,这种羟基磷灰石全涂层的双锥度非骨水泥柄用于股骨颈骨折术后发生晚期假体周围骨折的风险很高 (12%),虽然 RSA 显示 2年后假体固定稳定且无移位,但是 DEXA 显示在整个 5年研究期间,所有 Gruen 分区 (尤其是 1 区和 7 区)的骨质流失均增加,这可能解释了晚期发生假体周围骨折比例增加的原因。作者建议不要使用这种无颈领非骨水泥柄来治疗老年患者的骨质疏松性股骨颈骨折。
此外,一些长期随访数据对医师选择股骨柄具有一定借鉴意义。在常用的两款骨水泥柄 (Exeter 和 Lubinus SP Ⅱ)和 5 款非骨水泥柄 (Bi-Metric,Corail,CLS Spotorno,ABG Ⅰ 和 ABG Ⅱ)中,Exeter 柄发生假体周围骨折进行翻修的风险比比 Lubinus SP Ⅱ 柄高 5 倍,非骨水泥柄中,ABG Ⅱ 发生假体周围骨折进行翻修的风险比增加为 1.63,而 Corail 柄的风险比减少为 0.47[36]。
目前,尚无研究深入探讨骨质疏松对髋臼杯固定和长期生存的影响,也缺乏与对照组 (非骨质疏松患者)进行对比的研究。当医师选择使用非骨水泥杯时,必须考虑两个问题以避免术中发生骨折。首先,髋臼准备过程中磨挫髋臼的尺寸与髋臼假体的尺寸应该相差 1 mm 以内或与假体大小相同,以安全的打入臼杯。其次,为获得更好的初始稳定性,建议在骨质疏松患者中使用螺钉固定[37]。而一些臼杯设计例如椭圆形整体杯形设计会增加术中骨折的风险[38],应避免使在骨质疏松患者中使用这类臼杯设计。
六、骨质疏松患者行 THA 的临床效果
来自大型人群研究的数据表明,骨质疏松症患者行 THA 的临床效果并不差。来自丹麦关节注册中心的研究纳入 1995 - 2006年 16 145 例之前存在骨质疏松或骨质疏松性骨折的 THA 病例,这些 THA 病例中有 632 例进行翻修手术。该研究发现,16 145 例 THA 10年累计的假体翻修率为 8.3%,该比例与丹麦关节注册中心所有 THA 患者的翻修率 8.9% 相近[39]。然而,该文章的作者也指出,外科医师或骨质疏松症患者本身可能由于担心骨质疏松会增加发病率和病死率而不愿进行翻修手术,这可能会使骨质疏松患者的翻修率看起来没那么高。目前在骨质疏松患者中使用非骨水泥柄获得了良好的中长期临床结果 (表 1)。
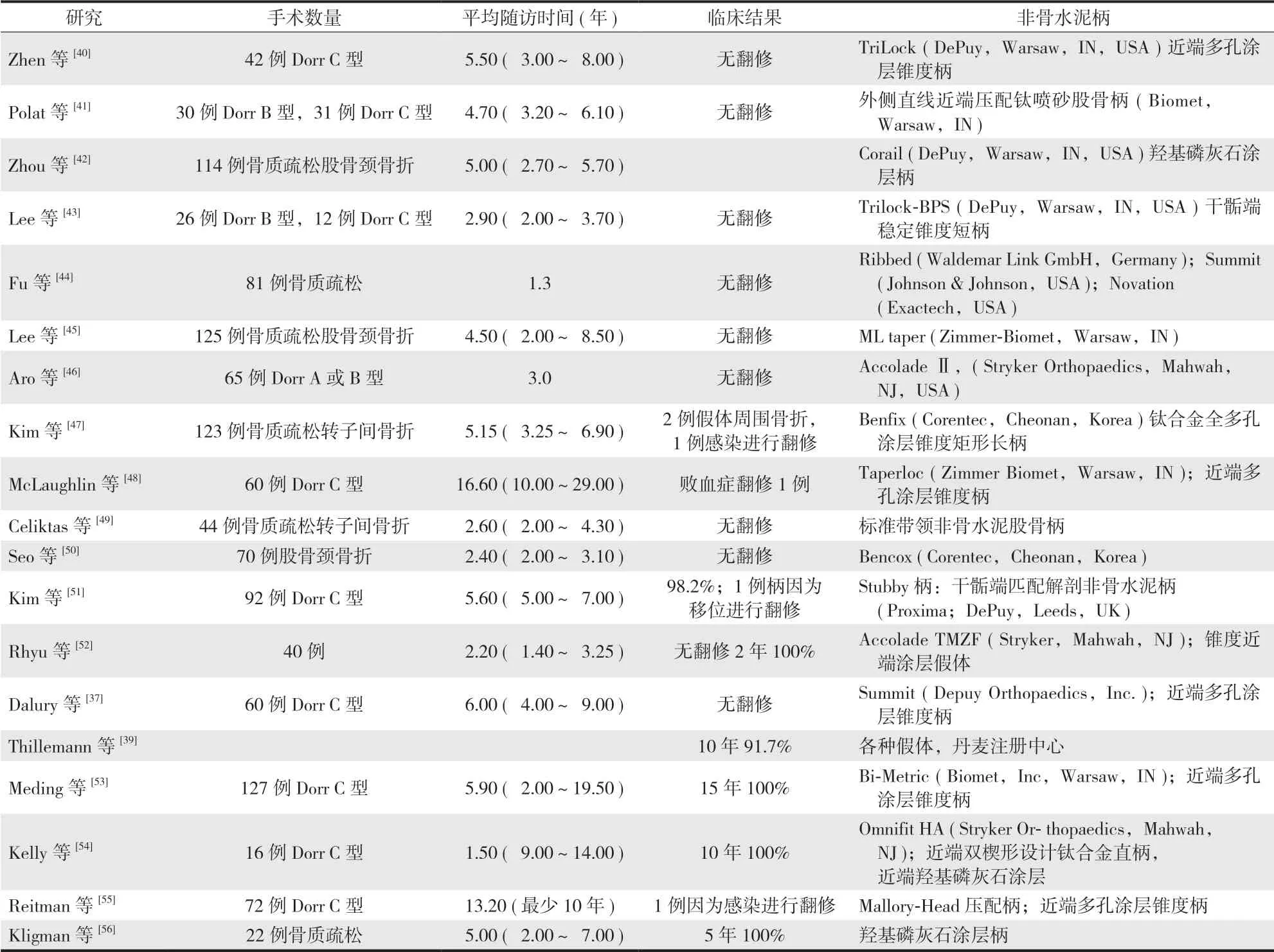
表1 骨质疏松症患者采用非骨水泥柄的临床效果Tab.1 Clinical effects of cementless stems in patients with osteoporosis
七、骨质疏松增加并发症风险
骨质疏松是术中假体周围骨折和非骨水泥性假体稳定性降低的主要原因之一[57-58]。 骨质疏松还增加了非骨水泥柄 THA 术后假体周围骨折的风险[58-61]。假体周围骨折不仅会影响 THA 的临床结果,也会增加病死率[59,62-63]。据报道,THA 术后发生假体周围骨折的比例为 0.07%~ 18.00%[64],其中高龄、肥胖、骨质疏松、非骨水泥柄、翻修手术均是危险因素[36,64-66]。术中假体周围骨折通常发生在将非骨水泥柄打入到骨质疏松性股骨时,且通常发生在股骨距区域。另一项研究中,Nixon 等[67]将平均随访 7.7年后骨水泥 THA 无菌性松动的患者与匹配的患者进行比较。结果发现,在排除失用性骨质疏松的因素下,无菌性松动患者的髋部和腰椎骨密度都更低。作者还提出,骨质疏松和无菌性松动的特点都是骨转换增加,提示骨质疏松患者有一个额外的假体松动危险因素,建议对这些骨质疏松患者在 THA 术后应进行更密切的随访,以发现任何松动的早期迹象。
八、抗骨质疏松药物治疗
对于骨质疏松和骨量低下的患者来说,THA 术后的骨质流失是一个问题[68]。在 THA 术后第 1年即会发生骨丢失,随后会恢复到一定程度。由于应力遮挡,某些骨质流失,尤其是在 Gruen 7 区的骨质流失会持续存在。已有研究证实,骨矿物质密度的改善可能有助于假体的长期固定和减少关节置换术后假体周围骨折的发生率[69]。抗骨质疏松药物的依从性和持久性在骨质疏松症的医学治疗中至关重要[70-71]。目前已经使用双膦酸盐作为防止骨丢失的一种药物方法[72]。最近的一项荟萃分析[73]纳入 9 项随机对照试验研究,共 359 例 THA 病例,发现应用双膦酸盐对维持早期假体周围骨量具有积极作用,在术后 6 个月、 12 个月、2年均可以有效维持假体周围 1、2、3、4、6、7 区的骨量,同时使用双膦酸盐的安全性高。一项基于英国全科医学研究数据库的回顾性队列研究对 1986 - 2006年间 18 726 例 TKA 和 23 269 例 THA 进行统计,其中使用双膦酸盐的患者有 1912 例,使用参数化生存模型并调整倾向评分来确定双膦酸盐对假体生存率的影响,发现使用双膦酸盐的患者术后 5年的翻修率低于未使用双膦酸盐者 (0.93vs.1.96),双膦酸盐类药物使用者的假体存活时间明显长于未使用双膦酸盐类药物者 (风险比为 0.54),使用双膦酸盐组的翻修时间也几乎翻倍 (时间比为 1.96)[74]。假设 5年内假体失败率为 2%,则估计有 107 例置换患者口服双膦酸盐类药物就可以避免一次翻修手术。基于美国关节注册中心的数据[75]也得出了类似的结论。共纳入 12 878 例 THA 患者,其中 17.8% 患者使用双膦酸盐。将双膦酸盐治疗组患者的年龄和性别校正后,发现双膦酸盐治疗组的全因翻修风险 (风险比 0.50)和因无菌性松动翻修的风险 (风险比 0.53)均要低于未使用双膦酸盐者。然而,丹麦 HA 注册中心的数据[39]值得引起重视,他们发现初次 THA 术后使用双膦酸盐可降低全因翻修风险,但使用双膦酸盐可能与深部假体周围感染导致翻修风险增加有关,为了阐明这种关联是否是真正的因果关系,有必要进行进一步的研究。
九、结论
骨科医师会面对越来越多的骨质疏松患者进行 THA,要重视行 THA 患者的骨质疏松人群比例。建议在患者接受 THA 之前,评估并改善骨骼质量,以确保获得最佳结果。骨质疏松由于股骨髓腔扩张的特点,要更加重视股骨柄的固定,选择非骨水泥柄和骨水泥柄均会获得良好结果。骨质疏松是假体周围骨折和假体松动的高危风险因素,使用抗骨质疏松药物如双膦酸盐可以改善植入物的骨整合并减少假体周围骨折的发生率。对骨质疏松患者在 THA 术后应进行更密切的随访,以发现任何松动的早期迹象。

