鸦胆子中苦木素类成分及其生物活性
吴佳辉, 何 潇, 熊紫微, 谭 婷, 冯育林,, 杨世林, 温 泉*, 陈道峰,3
(1.江西中医药大学,江西 南昌 330006;2.创新药物与高效节能降耗制药设备国家重点实验室,江西 南昌 330006;3.复旦大学药学院,上海 201203)
鸦胆子Bruceajavanica(L.)Merr.是鸦胆子属苦木科常绿灌木或者小乔木,广泛分布于我国广东、广西、云南及东南亚地区[1],其干燥成熟果实鸦胆子是传统中药,其性苦味寒,有小毒[2]。已有240多种化合物从鸦胆子的种子和果实中分离得到,其中大约120 种为苦木素类化合物[3],苦木素类化合物作为鸦胆子的主要成分,具有多种生物活性,如抗癌[4]、抗炎[5]、抗病毒[6]、抗原虫[7]等。
补体是经活化后具有生物活性,可介导免疫和炎症反应的蛋白。中药作用于传染病通常是通过抑制炎症和退热,其机制可能与抑制体内补体系统的过度激活有关[8-9],因此补体系统在中药抑制炎症过程中起重要作用。鸦胆子苦木素具有抗炎[5]和体外抗补体活性[10],并且补体系统还参与肿瘤细胞的杀伤和监视作用[11]。因此,本实验对具有抗补体活性的化合物3、8进行抗肿瘤活性筛选,结果显示对HepG2细胞具有良好的杀伤作用。
1 材料
HP20大孔吸附树脂(日本三菱公司);Sephadex LH-20凝胶(美国GE公司);100~200目硅胶柱、GF254型薄层色谱(青岛海洋化工厂);YMC-Pack ODS-A HPLC(250 mm×20 mm,5 μm;250 mm×10 mm,5 μm,日本YMC公司);Global Chromatography色谱柱(4.6 mm×250 mm,苏州环球色谱有限责任公司)。
小鼠单核巨噬细胞株(RAW264.7)、小鼠肺泡巨噬细胞株(MH-S)、人肝癌细胞株(HepG2)均购于大连美仑生物技术有限公司;胎牛血清(FBS)、Cell Counting kit-8 细胞计数试剂(CCK-8)、Annexin V-FITC/PI细胞凋亡检测试剂盒均购自上海翌圣生物科技有限公司;磷酸缓冲盐溶液(PBS)、EDTA-胰蛋白酶、DMEM高糖培养基、RPMI1640培养基均购自北京索莱宝科技有限公司;脂多糖(LPS)购自美国Sigma-Aldrich公司;一氧化碳(NO)检测试剂盒购自上海碧云天生物技术公司。
鸦胆子于2018年采自广西,经江西中医药大学钟国跃教授鉴定为正品,凭证标本(YDZ20181107)保存于江西中医药大学本草标本馆。
2 方法
2.1 提取分离 取鸦胆子20 kg,粉碎后石油醚脱脂3次,挥干石油醚后用95%乙醇提取3次,每次2 h,合并提取液,滤过,减压浓缩至无醇味,得粗浸膏,浸膏加适量甲醇溶解,硅胶拌样,上样硅胶柱,以二氯甲烷-甲醇(100∶1、20∶1、2∶1、0∶1)洗脱,得到4个流分Fr.A~Fr.D。Fr.B(260 g)用适量水溶解,上样HP-20大孔吸附树脂,依次以30%、60%、95%甲醇洗脱,得30%甲醇洗脱部位浸膏(Fr.B-1,98 g)、60%甲醇洗脱部位浸膏(Fr.B-2,77 g)、95%甲醇洗脱部位浸膏(Fr.B-3,108 g)。Fr.B-1加适量甲醇溶解,拌样,采用硅胶柱(100~200目)分离,以二氯甲烷-甲醇(50∶1、20∶1、10∶1、5∶1、0∶1)梯度洗脱,合并相似成分,得到5个流分Fr.B-1-1~ Fr.B-1-5,Fr.B-1-2经Sephadex LH-20凝胶柱分离,甲醇洗脱,合并相似成分,得到6个流分Fr.B-1-2-1~ Fr.B-1-2-6,在254 nm波长处,Fr.B-1-2-2经半制备HPLC分离(乙腈-0.1%甲酸,22∶78),得化合物7(24.1 mg)、3(41.6 mg);Fr.B-1-2-4经半制备HPLC分离(乙腈-0.1%甲酸,27∶73),得化合物5(22.9 mg)、8(43.2 mg)。Fr.B-2加适量甲醇溶解,拌样,采用硅胶柱(100~200目)分离,以二氯甲烷-甲醇(50∶1、20∶1、10∶1、5∶1、2∶1、0∶1)梯度洗脱,合并相似成分,得到6个流分Fr.B-2-1~Fr.B-2-6,Fr.B-2-4后经Sephadex LH-20凝胶柱分离,甲醇洗脱,合并相似成分,得到8个流分Fr.B-2-4-1~Fr.B-2-4-8,在254 nm波长处,Fr.B-2-4-3经半制备HPLC分离(乙腈-0.1%甲酸,35∶65),得化合物10(66.8 mg)、2(63.2 mg)、1(13.2 mg);Fr.B-2-4-6经半制备HPLC分离(乙腈-0.1%甲酸,38∶62),得化合物6(37.5 mg)、9(46.2 mg)、4(47.8 mg)。
2.2 细胞培养 RAW264.7、HepG2细胞在含10%胎牛血清、1%青霉素-链霉素(PS)、高糖DMEM完全培养基中培养,MH-S细胞在含10%FBS、1%PS的1640培养基中培养,条件均为37 ℃、5%CO2。
2.3 细胞存活率检测 在96孔板中接种对数生长的RAW264.7(每孔1×104/100 μL)、MH-S(每孔8×103/100 μL)、HepG2(每孔6×103/100 μL)细胞,培养24 h后,弃上清,加入化合物1~10(80、40、20、10、5 μmol/L)继续培养48 h,弃上清,每孔加入100 μL 10%CCK-8,孵育2 h至未处理对照组颜色变为橙色,在 450 nm波长处测定吸光度。
2.4 NO水平检测 取对数生长期RAW264.7细胞接种于96孔培养板中(每孔1×105/200 μL),培养24 h,设置对照组(DMEM)、LPS组(2 μg/mL LPS)、不同浓度给药组(40、20、10 μmol/L化合物1~10,预处理2 h,加入2 μg/mL LPS的培养基),每组设置3个重复孔。培养48 h后,收集上清液,采用Griess法检测NO水平。
2.5 补体经典途径实验 将化合物1~10与肝素钠(阳性对照)溶于二甲基亚砜(DMSO)中,PBS缓冲液稀释成不同浓度,加入临界浓度的补体(1∶10稀释的豚鼠血清)、溶血素、2%SRBC,在37 ℃下水浴30 min,离心后取上清液,在405 nm波长处测定吸光度,设置对照组和全溶血组,测定溶血抑制率。
2.6 HepG2细胞凋亡检测 采用Annexin V-FITC凋亡试剂盒,将对数生长期的HepG2细胞以每孔2×105个的密度接种于6孔板中,在37 ℃下孵育24 h,加入化合物3、8(20、10 μmol/L)继续培养48 h,胰酶消化后离心收集细胞,400 μL 1×buffer缓冲液重新混悬,加入5 μL Annexin V-FITC、10 μL碘化丙啶,室温避光孵育15 min,通过流式仪检测,FlowJo 7.6软件进行分析。
3 结果
3.1 结构鉴定 化合物1:无定型粉末(甲醇),ESI-MSm/z:705.2 [M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:3.33(1H,d,J=15.5 Hz,H-1α),2.57(1H,d,J=15.5 Hz,H-1β),3.01(1H,d,J=3.7 Hz,H-9),4.91(1H,brs,H-11),5.13(1H,brs,H-12),4.01(1H,brd,J=11.0 Hz,H-14),6.48(1H,brs,H-15),2.50(3H,s,H-18),1.80(3H,s,H-19),5.03(1H,d,J=7.5 Hz,H-20a),3.87(1H,d,J=7.5 Hz,H-20b),3.64(3H,s,OCH3),5.68(1H,s,H-2′),1.59(3H,s,H-4′),2.11(3H,s,H-5′),5.43(1H,d,J=7.7 Hz,H-1″),4.20(1H,dd,J=8.7,7.7 Hz,H-2″),4.30(1H,dd,J=9.2,8.7 Hz,H-3″),4.37(1H,t,J=9.2 Hz,H-4″),4.18(1H,m,H-5″),4.46(1H,dd,J=11.7,4.0 Hz,H-6″α),4.57(1H,dd,J=11.7,2.7 Hz,H-6″β),6.62(1H,brs,11-OH),8.25(1H,brs,12-OH);13C-NMR(DMSO-d6,150 MHz)δ:51.0(C-1),193.8(C-2),146.8(C-3),147.7(C-4),48.1(C-5),27.6(C-6),83.8(C-7),46.2(C-8),31.9(C-9),39.7(C-10),73.3(C-11),76.3(C-12),82.7(C-13),48.8(C-14),68.4(C-15),167.0(C-16),16.7(C-18),26.5(C-19),73.5(C-20),170.5(C-21),52.3(-OCH3),165.5(C-1′),116.4(C-2′),158.8(C-3′),26.5(C-4′),20.5(C-5′),104.9(C-1″),75.6(C-2″),78.1(C-3″),71.1(C-4″),77.9(C-5″),62.4(C-6″)。以上数据与文献[12]报道基本一致,鉴定为javanicoside A。
化合物2:无色粉末(甲醇),ESI-MSm/z:685.2 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:6.55(1H,s,H-1),2.48(1H,m,H-4),2.12(1H,d,J=7.1 Hz,H-5),1.92(1H,m,H-6α),1.74(1H,d,J=4.0 Hz,H-6β),4.92(1H,d,J=4.0 Hz,H-7),4.30(1H,brs,H-11),4.16(1H,brs,H-12),1.04(3H,d,J=6.7 Hz,H-18),1.48(3H,s,H-19),4.52(1H,d,J=7.2 Hz,H-20α),3.64(1H,d,J=7.2 Hz,H-20β),3.70(3H,s,-OCH3),2.17(2H,d,J=7.1 Hz,H-2′),1.98(1H,m,H-3′),0.91(6H,m,H-4′,5′);13C-NMR(DMSO-d6,150 MHz)δ:132.3(C-1),150.3(C-2),198.1(C-3),41.9(C-4),44.9(C-5),30.6(C-6),84.6(C-7),47.4(C-8),41.1(C-9),40.2(C-10),72.9(C-11),76.9(C-12),83.3(C-13),50.5(C-14),68.3(C-15),170.2(C-16),12.8(C-18),17.8(C-19),73.6(C-20),177.0(C-21),53.1(-OCH3),172.0(C-1′),43.9(C-2′),26.7(C-3′),22.8(C-4′),22.7(C-5′),102.9(C-1″),74.9(C-2″),78.4(C-3″),71.5(C-4″),77.6(C-5″),62.7(C-6″)。以上数据与文献[13]报道基本一致,鉴定为yadanzioside A。
化合物3:白色粉末(甲醇),ESI-MSm/z:769.3 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:6.54(1H,s,H-1),2.48(1H,m,H-4),2.01(1H,brd,J=5.0 Hz,H-5),1.93(1H,m,H-6α),1.77(1H,m,H-6β),4.30(1H,s,H-11),4.16(1H,s,H-12),6.81(1H,d,J=13.0 Hz,H-15),1.17(3H,d,J=6.0 Hz,H-18),1.64(1H,s,H-19),4.53(1H,d,J=7.3 Hz,H-20a),3.68(1H,d,J=7.3 Hz,H-20b),3.64(3H,s,-OCH3),6.06(1H,s,H-2′),2.26(3H,s,H-5′),1.42(3H,s,H-6′),1.46(3H,s,H-7′)1.95(3H,s,H-9′);13C-NMR(DMSO-d6,150 MHz)δ:130.3(C-1),149.3(C-2),198.1(C-3),41.9(C-4),44.9(C-5),30.6(C-6),84.6(C-7),47.4(C-8),41.1(C-9),40.2(C-10),72.9(C-11),76.9(C-12),83.3(C-13),49.5(C-14),71.3(C-15),167.2(C-16),12.8(C-18),17.8(C-19),74.6(C-20),172.0(C-21),53.1(-OCH3),166.0(C-1′),113.5(C-2′),169.4(C-3′),82.8(C-4′),14.5(C-5′),26.6(C-6′),26.5(C-7′),162.0(C-8′),21.6(C-9′),102.9(C-1″),74.9(C-2″),78.4(C-3″),71.5(C-4″),77.6(C-5″),62.7(C-6″)。以上数据与文献[13]报道基本一致,鉴定为yadanzioside G。
化合物4:白色粉末(甲醇),ESI-MSm/z:701.4 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:7.27(1H,s,H-1),2.01(1H,brd,J=15.0 Hz,H-5),5.18(1H,brs,H-7),2.52(1H,d,J=5.1 Hz,H-9),4.94(1H,brs,H-11),5.13(1H,brs,H-12),1.16(3H,d,J=6.6 Hz,H-18),1.64(3H,s,H-19),3.90(1H,d,J=7.7 Hz,H-20α),5.07(1H,d,J=7.8 Hz,H-20β),3.80(3H,s,-OCH3),2.88(1H,d,J=13.7 Hz,H-2′a),2.94(1H,d,J=13.7 Hz,H-2′b),1.61(6H,s,H-4′,5′),5.35(1H,d,J=7.3 Hz,H-1″),4.48(1H,brd,J=10.3 Hz,H-6″);13C-NMR(DMSO-d6,150 MHz)δ:130.3(C-1),148.3(C-2),195.1(C-3),43.9(C-4),40.9(C-5),30.6(C-6),83.6(C-7),46.4(C-8),41.1(C-9),40.2(C-10),73.9(C-11),76.3(C-12),82.3(C-13),50.5(C-14),68.3(C-15),168.2(C-16),12.8(C-18),17.8(C-19),73.6(C-20),171.2(C-21),52.1(-OCH3),170.3(C-1′),48.5(C-2′),69.4(C-3′),29.8(C-4′),29.5(C-5′),102.9(C-1″),74.9(C-2″),78.4(C-3″),71.5(C-4″),78.6(C-5″),62.7(C-6″)。以上数据与文献[14]报道基本一致,鉴定为yadanzioside J。
化合物5:白色无定型粉末(甲醇),ESI-MSm/z:434.5 [M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:4.20(1H,s,H-1),6.15(1H,s,H-3),3.15(1H,brd,H-5),2.16(1H,d,H-6a),1.54(1H,d,H-6b),2.75(1H,brs,H-9),6.01(1H,brs,H-11),4.43(1H,brs,H-12),6.13(1H,brs,H-15),1.75(3H,s,H-18),1.57(3H,s,H-19),2.09(3H,s,H-20),2.06(3H,s,H-21);13C-NMR(DMSO-d6,150 MHz)δ:85.3(C-1),199.3(C-2),125.1(C-3),164.9(C-4),42.9(C-5),25.6(C-6),79.6(C-7),43.4(C-8),44.7(C-9),49.2(C-10),75.9(C-11),78.9(C-12),78.3(C-13),78.5(C-14),68.9(C-15),174.2(C-16),22.8(C-18),11.8(C-19),20.6(C-20),25.8(C-21)。以上数据与文献[15]报道基本一致,鉴定为yadanziolide S。
化合物6:白色粉末状固体(甲醇),ESI-MSm/z:529.2 [M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:2.53(1H,d,J=16.0 Hz,H-1α),2.84(1H,d,J=16.0 Hz,H-1β),2.99 (1H,d,J=13.0 Hz,H-5),2.30(1H,dt,J=14.5,2.0 Hz,H-6α),1.88(1H,J=14.5,13.5,2.0 Hz,H-6β),4.91(1H,s,H-7),2.21(1H,s,H-9),4.17(1H,d,J=4.0 Hz,H-11),4.14(1H,s,H-12),3.24(1H,m,H-14),6.17(1H,brs,H-15),1.84(3H,d,J=1.5 Hz,H-18),1.37(3H,s,H-19),4.70(1H,d,J=7.5 Hz,H-20a),3.74(1H,brs,H-20b),5.68(1H,s,H-2′),1.92(3H,s,H-4′),2.15(3H,s,H-5′);13C-NMR(DMSO-d6,150 MHz)δ:51.4(C-1),194.4(C-2),145.8(C-3),130.4(C-4),43.1(C-5),30.1(C-6),84.8(C-7),46.2(C-8),42.7(C-9),42.2(C-10),70.9(C-11),78.6(C-12),83.4(C-13),49.8(C-14),66.9(C-15),169.7(C-16),13.4(C-18),16.0(C-19),71.5(C-20),174.5(C-21),166.5(C-1′),116.4(C-2′),159.8(C-3′),27.5(C-4′),20.5(C-5′)。以上数据与文献[16]报道基本一致,鉴定为desmethyl-brusatol。
化合物7:白色无定型粉末(甲醇),ESI-MSm/z:643.2 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:7.24(1H,s,H-1),2.40(1H,m,H-4),2.01(1H,brd,H-6α),1.63(1H,m,H-6β),2.49(1H,d,J=4.0 Hz,H-9),5.16(1H,m,H-11),6.53(1H,brs,H-15),1.15(3H,d,J=6.5 Hz,H-18),1.59(3H,s,H-19),5.02(1H,d,J=7.5 Hz,H-20a),3.87(1H,d,J=7.5 Hz,H-20b),3.73(3H,s,-OCH3),2.06(3H,s,H-2′),5.31(1H,d,J=7.5 Hz,H-1″);13C-NMR(DMSO-d6,150 MHz)δ:129.3(C-1),148.9(C-2),194.5(C-3),43.8(C-4),40.5(C-5),30.0(C-6),83.6(C-7),46.4(C-8),41.7(C-9),39.2(C-10),72.9(C-11),76.9(C-12),82.3(C-13),50.5(C-14),68.9(C-15),168.2(C-16),18.8(C-18),12.8(C-19),73.6(C-20),171.8(C-21),52.9(-OCH3),169.6(C-1′),20.6(C-2′),102.0(C-1″),74.9(C-2″),78.4(C-3″),71.5(C-4″),78.6(C-5″),62.7(C-6″)。以上数据与文献[13]报道基本一致,鉴定为yadanzioside F。
化合物8:无色粉末(甲醇),ESI-MSm/z:685.3 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:4.42(1H,m,H-2),5.69(1H,brs,H-3),6.76(1H,d,J=13.0 Hz,H-15),1.43(3H,brs,H-18),1.45(3H,s,H-19),3.72(3H,s,-OCH3),5.82(1H,brs,H-2′),1.67(3H,s,H-4′),2.14(3H,s,H-5′);13C-NMR(DMSO-d6,150 MHz)δ:84.8(C-1),84.3(C-2),124.1(C-3),135.9(C-4),43.2(C-5),28.6(C-6),81.6(C-7),46.4(C-8),42.9(C-9),44.4(C-10),75.9(C-11),75.9(C-12),82.3(C-13),50.5(C-14),68.3(C-15),168.2(C-16),20.8(C-18),12.1(C-19),73.6(C-20),171.4(C-21),52.1(-OCH3),165.3(C-1′),116.3(C-2′),158.7(C-3′),27.8(C-4′),20.7(C-5′),106.9(C-1″),75.9(C-2″),78.4(C-3″),71.5(C-4″),78.6(C-5″),62.7(C-6″)。以上数据与文献[13]报道基本一致,鉴定为yadanzioside E。
化合物9:无色粉末(甲醇),ESI-MSm/z:705.3 [M+H]+。1H-NMR(DMSO-d6,600 MHz)δ:2.51(1H,d,J=16.2 Hz,H-1a),3.27(1H,d,J=16.2 Hz,H-1b),3.06(1H,brd,J=12.0 Hz,H-5),2.28(1H,d,J=14.6 Hz,H-6α),1.74(1H,ddd,J=14.6,12.8,2.1 Hz,H-6β),5.11(1H,brs,H-7),2.62(1H,d,J=4.2 Hz,H-9),4.78(1H,brs,H-11),5.06(1H,brs,H-12),4.10(1H,brd,J=12.8 Hz,H-14),2.08(1H,s,H-18),1.75(1H,s,H-19),5.13(1H,d,J=7.5 Hz,H-20a),3.97(1H,d,J=7.5 Hz,H-20b),3.54(3H,s,-OCH3),8.23(1H,d,J=7.5 Hz,H-3′,7′),7.50(1H,d,J=7.7 Hz,H-4′,6′),7.37(1H,d,J=7.7 Hz,H-5′),5.46(1H,d,J=7.0 Hz,H-1″),3.89(1H,m,H-5″),4.46(1H,d,J=10.2 Hz,H-6″a),4.34(1H,m,H-6″b);13C-NMR(DMSO-d6,150 MHz)δ:51.0(C-1),193.6(C-2),146.6(C-3),147.9(C-4),43.3(C-5),29.3(C-6),83.8(C-7),46.2(C-8),42.2(C-9),40.8(C-10),73.0(C-11),75.7(C-12),82.7(C-13),50.8(C-14),69.4(C-15),168.0(C-16),15.3(C-18),15.8(C-19),73.5(C-20),171.5(C-21),52.3(-OCH3),165.5(C-1′),130.4(C-2′),130.1(C-3′),128.8(C-4′),133.6(C-5′),128.8(C-6′),130.1(C-7′),104.9(C-1″),76.1(C-2″),78.9(C-3″),71.1(C-4″),78.4(C-5″),62.4(C-6″)。以上数据与文献[17]报道基本一致,鉴定为javanicoside J。
化合物10:非晶形粉末(甲醇),ESI-MSm/z:707.4 [M+Na]+。1H-NMR(DMSO-d6,600 MHz)δ:6.08(1H,d,J=2.2 Hz,H-3),2.02(1H,dd,J=11.9,3.0 Hz,H-6α),1.54(1H,t,J=12.8 Hz,H-6β),4.84(1H,s,H-7),2.91(1H,d,J=4.2 Hz,H-9),6.16(1H,d,J=5.0 Hz,H-11),6.92(1H,brs,H-15),0.86(1H,d,J=6.8 Hz,H-18),1.83(1H,s,H-19),5.08(1H,d,J=7.4 Hz,H-20a),3.87(1H,d,J=7.4 Hz,H-20b),3.84(3H,s,-OCH3),2.36(1H,d,J=6.6 Hz,H-2′),0.99(3H,s,H-4′),0.96(3H,s,H-5′),5.44(1H,d,J=7.2 Hz,H-1″),3.98(1H,m,H-5″),4.54(2H,d,J=12.0 Hz,H-6″),6.32(1H,d,J=5.6 Hz,11-OH),7.88(1H,brs,12-OH);13C-NMR(DMSO-d6,150 MHz)δ:199.7(C-1),146.3(C-2),124.8(C-3),31.4(C-4),44.0(C-5),28.6(C-6),82.8(C-7),46.6(C-8),36.9(C-9),48.7(C-10),75.3(C-11),76.3(C-12),82.7(C-13),50.8(C-14),68.4(C-15),168.0(C-16),18.7(C-18),14.5(C-19),73.5(C-20),171.5(C-21),52.3(-OCH3),171.9(C-1′),43.4(C-2′),25.9(C-3′),22.5(C-4′),22.4(C-5′),100.9(C-1″),74.6(C-2″),78.9(C-3″),71.1(C-4″),78.9(C-5″),62.4(C-6″)。以上数据与文献[18]报道基本一致,鉴定为javanicoside B。
3.2 细胞毒性 由表1 可知,化合物1~10浓度在 50 μmol/L 时对RAW264.7、MH-S细胞的毒性较小,存活率高,但化合物3、8对HepG2细胞毒性较大。
3.3 抗炎活性 由图1可知,化合物3、8~10对NO生成有抑制作用,其他化合物活性较弱。
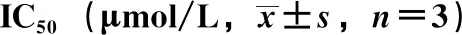
表1 化合物1~10 对RAW264.7、MH-S、HepG2细胞的
注:与对照组比较,##P<0.01;与模型组比较,*P<0.05,**P<0.01。
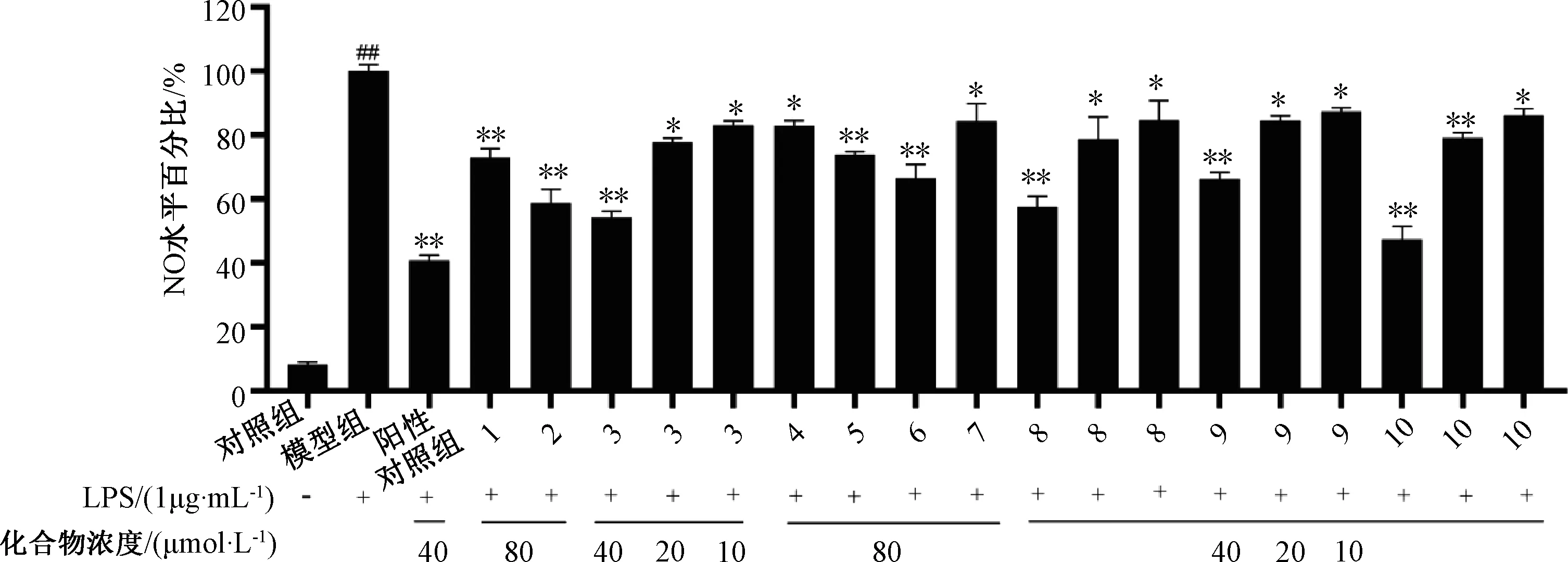
3.4 抗补体活性 由图2可知,化合物3、8对补体激活具有抑制作用,其他化合物无抑制作用。
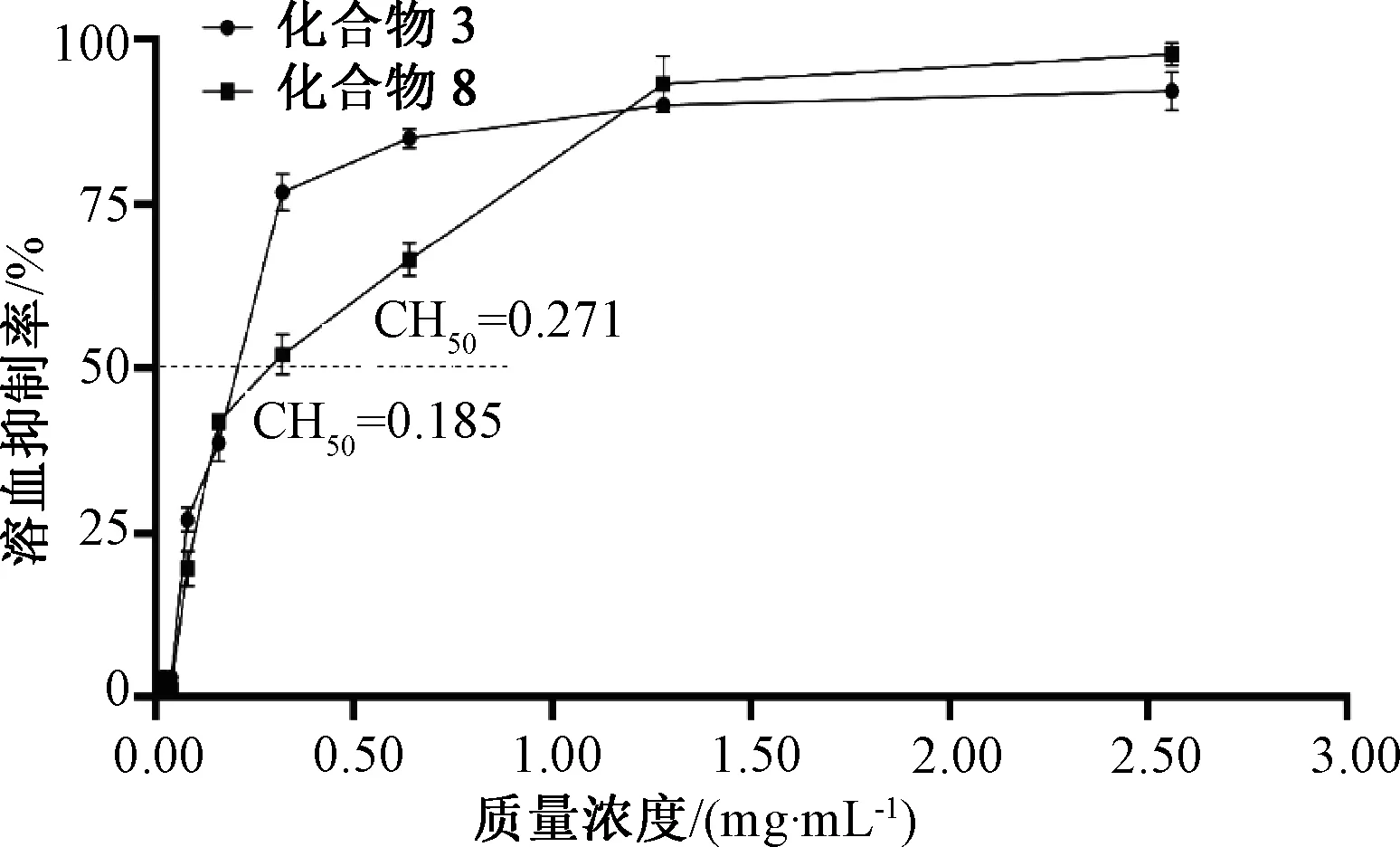
图2 化合物3、8抗补体活性
3.5 细胞凋亡 如图3所示,随着化合物3、8浓度增加,HepG2细胞凋亡率升高。
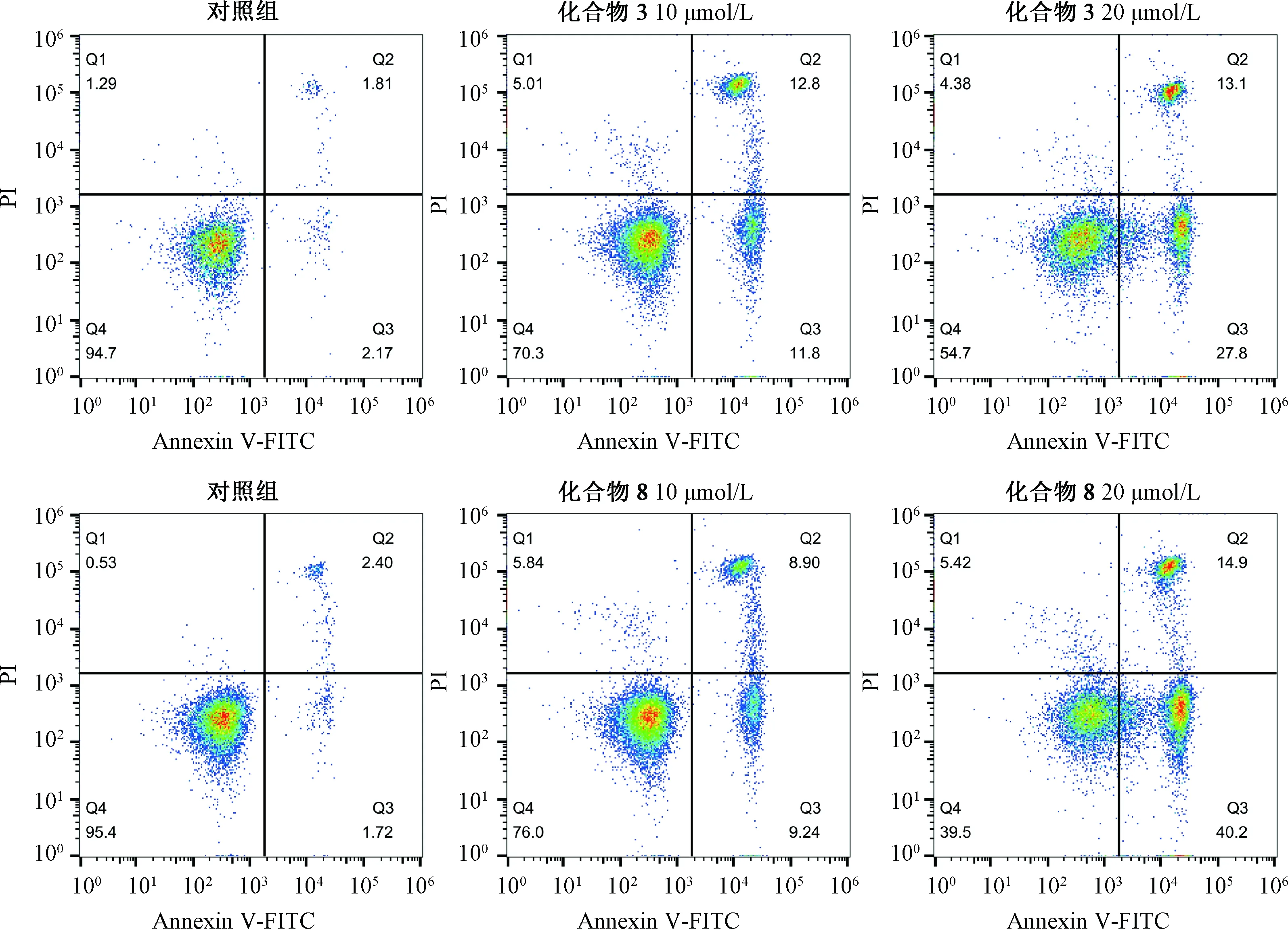
图3 化合物3、8对HepG2细胞凋亡的影响
4 讨论
中药鸦胆子化学成分的药理活性引起了国内外学者的普遍关注[19]。补体因子C5a 能激活ERK1/2、MEK1/2、p38MAPK和JNK使其磷酸化[20],并且补体系统激活会产生过量的TNF-α 、IL-1β、IL-6等炎症因子,造成局部增生损害[21],因此补体系统可能是炎症反应的上游路径,有抗补体活性的化合物具有抗炎活性。因此有文献导向分离鉴定具有抗补体活性的主要成分进行抗炎活性研究[22]。本研究通过对化合物1~10进行抗炎活性的筛选,用具有抗炎活性的化合物进行补体经典途径实验,证明化合物3和8具有良好的抗补体活性。鸦胆子苦木素广泛应用于多种癌症的治疗,但都通过细胞凋亡途径进行研究[23]。本研究初步证明具有良好抗补体活性的化合物3和8对人肝癌细胞具有杀伤作用,为鸦胆子苦木素抗肿瘤活性研究提供参考。

