酪氨酸激酶抑制剂治疗晚期甲状腺癌的最新研究进展
何紫燕,邱娴,萨日,陈立波
甲状腺癌是最常见的内分泌恶性肿瘤。2020年甲状腺癌发病率在世界范围内排名第9位,发病人数达58.6万[1]。甲状腺癌分为来源于甲状腺滤泡细胞的分化型甲状腺癌(differentiated thyroid cancer,DTC)和甲状腺未分化癌(又名间变性甲状腺癌)(anaplastic thyroid cancer,ATC)以及来源于滤泡旁细胞的甲状腺髓样癌(medullary thyroid cancer,MTC),其中DTC最为常见。鉴于DTC自身的惰性以及包括手术、131I治疗和促甲状腺激素(thyroid stimulating hormone,TSH)抑制在内的传统治疗,使得DTC患者的预后一般较好。然而,对于ATC、MTC和放射性碘难治性分化型甲状腺癌(radioiodine-refractory differentiated thyroid cancer,RR-DTC)而言,传统治疗方法的疗效果不佳,肿瘤复发和转移率较高。
近年来,由于对甲状腺癌分子病理学研究的深入,酪氨酸激酶抑制剂(tryosine kinase inhibitor,TKI)在晚期甲状腺癌治疗中取得突破性进展,凡德他尼、卡博替尼、索拉非尼、乐伐替尼、达拉非尼、曲美替尼和塞帕替尼先后被美国食品药品监督管理局批准用于甲状腺癌的治疗,其疗效和安全性已在临床试验中得到了证实。然而,在实际的临床工作中,许多患者并不符合临床试验的纳入标准,并且患者的特征、经历和治疗方案往往也不同于临床试验的控制环境[2],因此在临床试验的基础上进行真实世界研究十分必要。此外,TKI治疗的最佳启动时机仍不明确。为了更全面地认识TKI治疗晚期甲状腺癌的疗效和安全性,并且优化启动时机以改善患者结局,本文总结了TKI治疗晚期甲状腺癌的最新研究进展。
1 TKI治疗晚期甲状腺癌的作用机制
甲状腺癌的发生和发展涉及多种机制:受体酪氨酸激酶活性失调;血管内皮生长因子(vascular endothelial growth factor,VEGF)促进肿瘤血管生成[3];RAS、BRAF、RET和NTPK等基因改变导致RAS/MAPK和PI3K/AKT等信号通路的异常激活[4-6]等。靶向抑制肿瘤驱动蛋白和抗血管生成是当前TKI治疗晚期甲状腺癌的基本机制。
2 TKI治疗晚期甲状腺癌的疗效及安全性
2.1 RR-DTC
在进展性局部晚期或转移性DTC中,有25%~50%的病灶表现出失分化特点,患者因病灶摄碘功能不佳而无法从131I治疗中获益,10年生存率仅为10%[7]。近年来,在Ⅲ期临床试验[8-14](表1)的基础上,索拉非尼和乐伐替尼成为局部晚期或转移性进展性RR-DTC临床治疗的标准选择。近年来,TKI治疗晚期RR-DTC的真实世界研究的结果(表2)也陆续公布。
2.1.1 索拉非尼
索拉非尼是一种作用于血管内皮细胞生长因子受体(vascular endothelial growth factor receptor,VEGFR)-1、VEGFR-2、VEGFR-3和血小板衍生生长因子受体(platelet-derived growth factor receptor,PDGFR)-β以 及RET和RAF基因的口服激酶抑制剂[36-37],能够通过抑制RAF信号转导通路以及抑制VEGFR和PDGFR-β,直接或间接地抑制肿瘤生长[37]。虽然不同的研究得到的中位无进展生存期(progressionfree survival,PFS)存在差异,但是在Ⅲ期临床试验中的有效性在真实世界研究中得到了充分的验证(表2)。除一项研究的中位PFS为9.7个月以及另一项研究未获得PFS以外,其余研究的中位PFS均超过10.8个月。
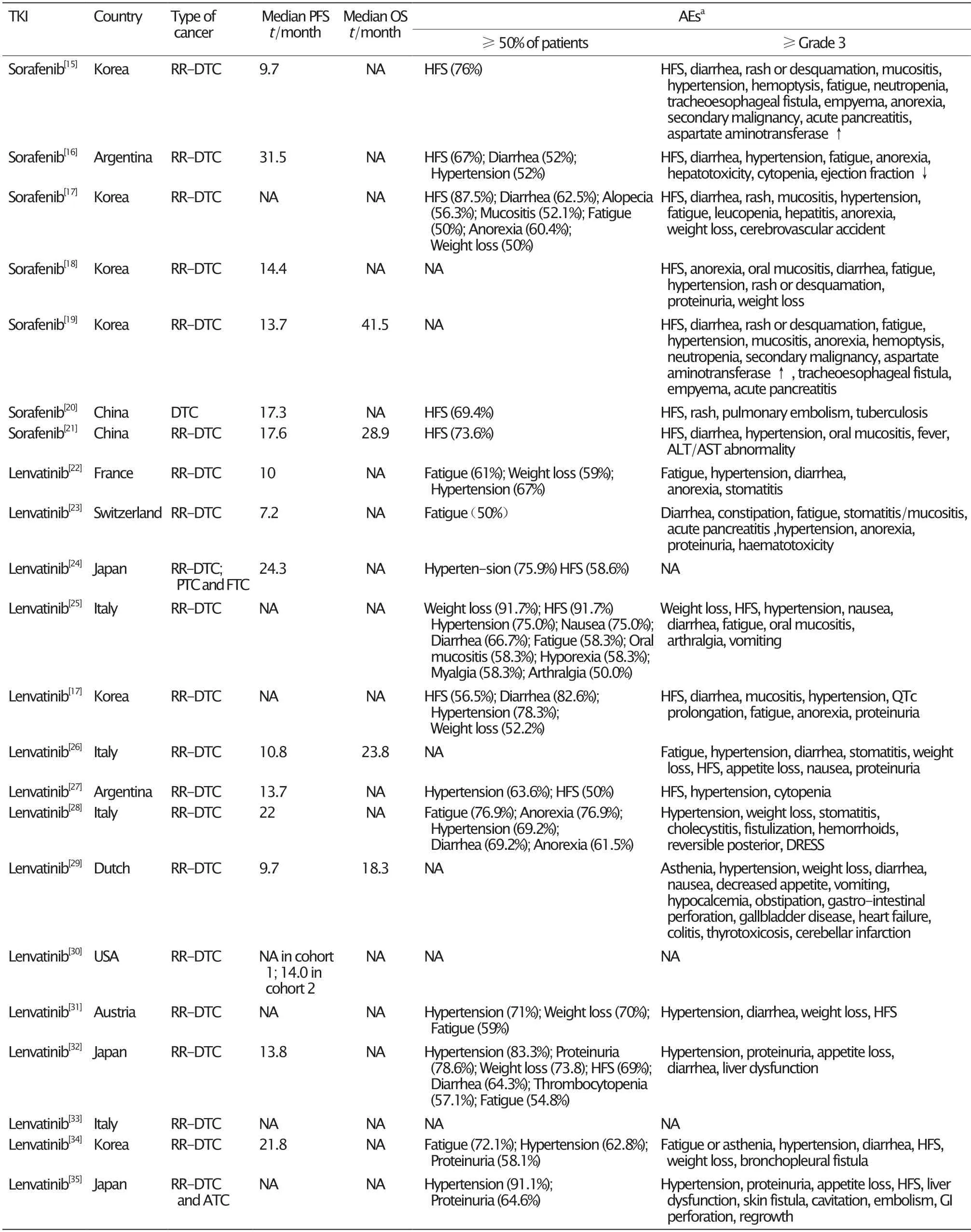
表2 TKI治疗RR-DTC的真实世界研究汇总Table 2 The real-world studies of TKIs treatment in RR-DTC
预后预测因素分析结果显示,无肿瘤相关症状和手足皮肤反应与较长的PFS和总生存期(overall survival,OS)相关,年龄和性别并不影响PFS,而肺转移、骨转移、肿瘤大小和肿瘤倍增时间是否与PFS和OS相关还存在争 议[15,18,21]。一项研究表明,更高的索拉非尼维持剂量(≥600 mg/dvs<600 mg/d)与更长的PFS相关[20];但是,另一项研究的结果却提示服用剂量为800 mg/d索拉非尼的患者的PFS较服用剂量低于800 mg/d索拉非尼的患者的短。此外,在服用索拉非尼超过6个月的患者中,不同的索拉非尼剂量组(<600 mg/d、600~799 mg/d和800 mg/d)患者的PFS无显著差异[18]。索拉非尼剂量对于疾病进展的影响,有待进一步研究。
在一项研究中,除了已知的手足皮肤反应、腹泻、皮疹或脱屑、高血压以及脱发等常见的不良反应以外,还观察到在DECISION试验中未观察到的咯血、中性粒细胞减少、气管食管瘘、脓胸和急性胰腺炎等严重不良反应[15]。此外,在另一项研究中,高血压患病率明显低于DECISION试验的结果(4%vs10%),这是因为当检测到患者血压有轻微升高时,即积极地进行抗高血压治疗[18]。由此表明,通过积极地监测和处理,可以减少或减轻索拉非尼相关不良反应。此外,大多数的不良反应都出现在索拉非尼治疗早期,不同的治疗组中均有因严重不良反应而导致的剂量减少、中断治疗和永久停药,这会在一定程度上影响索拉非尼治疗的长期疗效[24]。因此,早期监测和管理药物不良事件对疗效和安全性而言至关重要。
2.1.2 乐伐替尼
乐伐替尼是一种口服的多靶点TKI,可以抑制VEGFR-1、VEGFR-2、VEGFR-3、成纤维细胞生长因子受体(fibroblast growth factor receptor,FGFR)-1、FGFR-2、FGFR-3、FGFR-4、PDGFRα、RET和KIT信号通路[38-40]。自2015年获得批准以来,乐伐替尼已成为常用的RR-DTC一线治疗药物。SELECT试验[9]显示,乐伐替尼可以明显延长RR-DTC患者的PFS(中位PFS:18.3个月)。在3项研究中,患者的中位PFS分别为24.3、22和21.8个月;在真实世界研究中,乐伐替尼的疗效大多未达到临床试验的水平,这可能是因为入选患者的特征(一般健康状况和治疗经过等)存在差异[23,26-27]。疗效分析结果显示,高肿瘤负荷、肿瘤相关症状以及骨转移与疗效较差有关[41],药物维持剂量可能是影响疗效的因素之一。一项研究显示,乐伐替尼≤10 mg/d组和乐伐替尼≥14 mg/d组24个月后的总生存率分别为63%和82%[31]。虽然每日剂量较高组的疗效似乎更好,但较高的维持剂量可能会导致严重的不良反应,影响患者的生活质量,因此综合考虑选择合适的药物剂量是十分重要的。
除了作为一线治疗药物,乐伐替尼作为挽救用药应用于索拉非尼耐药的RR-DTC患者的研究[16,19]也已发表。
除了已报道的常见不良反应如疲劳、高血压、乏力和腹泻等,在真实世界研究中,也发现了可逆性后部白质脑病综合征、伴有嗜酸性粒细胞增多的药物皮疹和全身症状、外阴溃疡、出血性直肠炎以及药物相关胆囊和胆管疾病等罕见且严重的不良反应[27-28]。索拉非尼与乐伐替尼比较研究的结果显示,与索拉非尼组相比,乐伐替尼组的高血压、QT间期延长和蛋白尿发生率均显著升高[17]。既往研究的结果也显示,接受乐伐替尼治疗的患者罹患高血压和蛋白尿的风险增加[42-43]。因此,对高血压和蛋白尿等不良事件应进行密切监测。有趣的是,一项对乐伐替尼Ⅲ期临床试验数据进行探索性分析的研究发现,与乐伐替尼相关的高血压与RR-DTC患者预后的改善显著相关[44]。有时因为患者出现严重的不良反应,导致临床医师需要面对药物减量、暂停用药或永久停药的选择,但是部分会因为停药而导致肿瘤复发,从而对其生命造成严重威胁,甚至导致死亡[35]。因此,在发生严重的不良反应时,应尽可能选择减少药物剂量以维持治疗,而非选择停药。
2.2 ATC
ATC是一种罕见但极具侵袭性的恶性肿瘤,早期即可发生浸润和转移,预后差。ATC的常见突变基因包括PIK3CA、BRAF、RAS和TP53等[6]。在传统治疗方案疗效极差的情况下,针对MAPK信号通路,达拉非尼和曲美替尼联合治疗的Ⅱ期临床试验已获得了良好的结果,有望使这一治疗方案成为治疗ATC的新选择之一[13](表1)。此外,乐伐替尼也可以作为ATC的一种治疗选择,但是患者的生存获益情况仍需要通过长期的随访进行评估[45]。上述药物相关真实世界研究数据见表3。
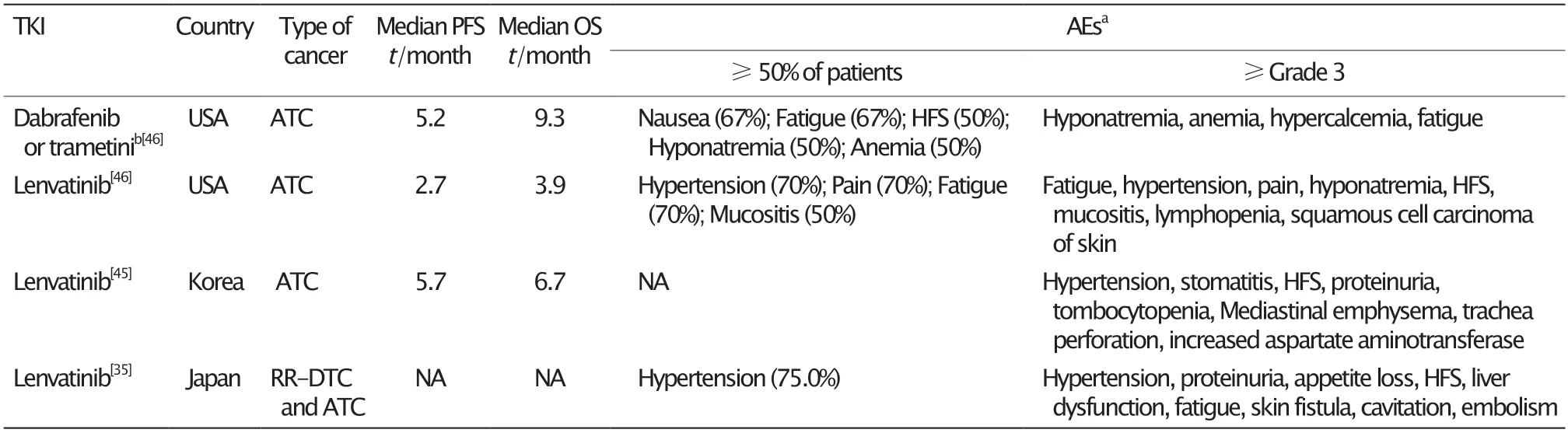
表3 TKI治疗ATC的真实世界研究Table 3 The real-world studies of TKIs treatment in ATC
2.2.1 达拉非尼和曲美替尼
达拉非尼和曲美替尼分别抑制BRAF和MEK基因,可以靶向抑制MAPK信号通路,从而抑制肿瘤细胞的生长。对于BRAFV600E突变的ATC患者,Ⅱ期临床试验显示达拉非尼联合曲美替尼的靶向治疗表现出了较高的总缓解率(总缓解率为69%),并且延长了缓解期和生存期[13]。一项真实世界研究[46]的结果显示,达拉非尼联合曲美替尼组中,50%的患者获得部分缓解,33%的患者病情稳定,患者的临床获益值得肯定。然而,这项研究中有1例BRAF突变患者经手术切除病灶后,在其复发病灶内未检测出BRAF突变,这可能会影响达拉非尼联合曲美替尼的疗效。因此,对于肿瘤复发的患者而言,即使初次诊断时已接受过基因检测,在开始靶向治疗之前,也仍应接受基因检测。一项临床试验指出,达拉非尼联合曲美替尼的新辅助治疗策略可能改善BRAFV600E突变的ATC患者的预后[47];但是,这项研究仅纳入6例患者,因此其结论的可靠性仍需通过开展大样本的临床试验予以验证。
达拉非尼和曲美替尼的常见不良反应包括恶心、疲劳、手足皮肤反应、低钠血症、贫血和体质量减轻等。在真实世界研究中,未发现患者发生既往Ⅱ期临床试验中出现的发热和高血糖症,推测可能与样本量较小有关[46]。
2.2.2 乐伐替尼
相较于达拉非尼和曲美替尼,乐伐替尼治疗ATC的严重不良反应发生率较高[46],可发生与治疗相关的肿瘤迅速收缩和瘘形成,由此导致皮肤瘘、气管穿孔、气胸和纵隔气肿等严重的不良反应,其他的致命性不良反应还包括大出血和肺炎等[35,45]。据悉,在使用乐伐替尼治疗时,ATC患者较DTC患者更易发生给药后肿瘤迅速收缩等不良反应[34,48]。鉴于乐伐替尼对ATC患者的生存获益存疑[45],以及其严重的不良反应发生率较高,乐伐替尼似乎更适合作为解救治疗。同时,必须对患者进行严格的不良反应监测以及合理的处置。
2.3 MTC
MTC侵袭性强,易发生淋巴结和远处转移,预后欠佳。RET突变在MTC的发生和发展中具有重要作用,在60%的散发性MTC患者以及几乎所有的遗传性MTC患者中均发现RET突变,其中RETM918T最常见[5]。凡德他尼和卡博替尼均可靶向抑制RET,其疗效已在临床试验(表1)和真实世界研究(表4)中得到了证实。
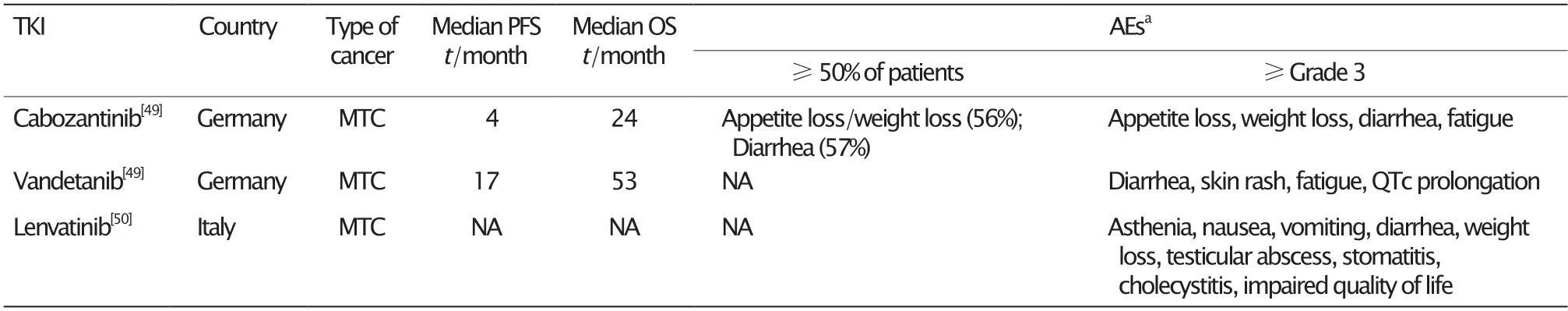
表4 TKI治疗MTC的真实世界研究Table 4 The real-world studies of TKIs treatment in MTC
2.3.1 凡德他尼
凡德他尼是一种口服的多靶点TKI,可以选择性靶向抑制RET、VEGFR和EGFR[51-52]。一项Ⅲ期临床试验[12]发现,在凡德他尼治疗组中,散发性MTC患者中的RETM918T阴性患者的客观缓解率低于RETM918T阳性患者(30.9%vs54.5%)。然而,一项真实世界研究[49]的结果却显示,RET突变状态与PFS和OS无明显相关性。因此,RET突变状态对凡德他尼治疗MTC患者的生存获益的影响,尚存在争议。凡德他尼开始治疗时,患者年龄大于60岁及有骨转移与较差的预后相关[49,53]。在真实世界的研究中,未观察到影响生命的严重不良事件,常见的不良反应包括腹泻、皮疹和乏力等。
2.3.2 卡博替尼
卡博替尼是口服的小分子多激酶抑制剂,可以抑制MET、VEGFR-2和RET[54]。一项研究发现,卡博替尼组患者的部分缓解率、疾病稳定率和无进展生存期均劣于凡德他尼组,这与Ⅲ期临床试验的结果一致,但这可能是由于卡博替尼组的样本量较少,并且接受卡博替尼治疗的患者的肿瘤侵袭性更强所致[11-12,49]。因此,尚无法确定二者谁更适合一线治疗。另外,在接受卡博替尼的患者中,骨转移的存在与预后没有显著相关性,这表明卡博替尼在骨转移患者中可能优于凡德他尼[49]。
真实世界研究中,卡博替尼的常见不良反应包括食欲减退、体质量减轻、腹泻和疲劳,这些均在临床试验中有所报道,未发现其他罕见的不良反应。与凡德他尼组相比,卡博替尼组的患者似乎更容易发生血细胞计数改变、电解质改变以及促甲状腺激素升高等情况[49]。
2.3.3 乐伐替尼
已有Ⅱ期临床试验[55]对乐伐替尼治疗晚期MTC的有效性和安全性进行了研究,但未检索到其作为一线治疗的真实世界研究。一项关于乐伐替尼解救治疗晚期MTC的研究显示,乐伐替尼可能在没有其他任何治疗选择的患者中是有效的,尤其是对于RET突变状态为阴性、无法获得新的高选择性靶向治疗的患者而言[50]。
2.3.4 塞帕替尼
塞帕替尼是抑制RET的单靶点TKI。最新的一项Ⅰ/Ⅱ期临床试验结果显示,接受过卡博替尼和(或)凡德他尼治疗的RET突变MTC患者的总缓解率为63%,未接受过卡博替尼或凡德他尼治疗的RET突变MTC患者的客观缓解率为73%,RET融合MTC患者的客观缓解率为79%[56]。已经获得批准的一线治疗药物卡博替尼和凡德他尼的Ⅲ期临床试验的客观缓解率分别为28%和45%[11-12]。基于目前的数据,在RET突变或融合的MTC患者中,塞帕替尼的疗效似乎优于卡博替尼和凡德他尼。然而,需要注意的是,卡博替尼和凡德他尼临床试验的纳入对象存在非RET突变或融合MTC患者的可能;在这些患者中,可能更倾向于选择卡博替尼和凡德他尼。
塞帕替尼的常见不良反应包括口干、高血压、疲劳和血清天冬氨酸转氨酶水平升高等。相较于卡博替尼和凡德他尼,塞帕替尼高选择性抑制RET,对VEGFR-2的影响极小,其在临床试验中因药物不良反应而导致暂停用药和永久停药的概率更低[11-12,56],其安全性更具优势。由于塞帕替尼具有高效低毒的优势,因此有望成为晚期MTC的一线治疗选择。此外,为确保塞帕替尼的疗效,在进行治疗之前开展分子筛选是必要的。
3 TKI治疗的启动时间
鉴于TKI引起的降低患者生活质量的不良反应发生率较高,因此对TKI治疗启动时间的选择十分困难。对于甲状腺癌患者来说,当发生转移灶较局限的远处转移时,可以首先采取局灶治疗;在局灶治疗效果不佳时,或是由于某些原因不能进行局灶治疗时,应考虑包括多激酶抑制剂治疗在内的系统治疗[57]。
美国甲状腺协会指南指出,TKI治疗应用于转移性、快速进展性和病情危重的甲状腺癌患者[57]。修订的MTC管理指南指出,对于有明显肿瘤负荷、有症状或进展性及转移性MTC患者,考虑给予以RET和VEGFR为靶点的TKI治疗[5]。有研究认为,高肿瘤负荷和肿瘤相关症状与不良预后相关,建议TKI治疗应在肿瘤负荷过大以及肿瘤相关症状占主导地位之前开始[41]。随着不同时间启用TKI治疗的疗效及预后相关数据的增多,上述共识可能会发生改变。
目前,TKI治疗晚期甲状腺癌的最佳启用时间尚无定论,特别是在无症状患者中。一项研究指出,将肿瘤直径与肿瘤倍增时间相结合,可能有助于临床医师确定在无症状个体中最早开始多激酶抑制剂治疗的时间[58]。此外,一项旨在评估多激酶抑制剂在无症状的进展性RR-DTC患者中的作用的研究(RIFTOS MKI)[59]正在进行之中,该研究有望解决无症状患者的TKI治疗最佳启动时间问题。由于存在个体差异,TKI治疗的启动时间应根据患者的病理特征、一般健康状况以及其他因素以制定个体化的方案,从而使患者取得最大的获益,以及尽可能减少药物的不良反应。
4 总结
通过对临床试验以及真实世界研究进行综合分析,发现虽然不同的研究得到的PFS和OS存在差异,但是临床试验中TKI治疗的有效性在真实世界中也得到了充分的验证。对于RR-DTC患者而言,咯血、中性粒细胞减少、气管食管瘘、脓胸和急性胰腺炎等在Ⅲ期临床试验中未出现的严重不良反应,都在真实世界研究中有所发现。此外,关于乐伐替尼和索拉非尼的剂量选择,尚待开展更多的研究进行探索。对于ATC患者来说,乐伐替尼相较于达拉菲尼和曲美替尼可能更适合于ATC的解救治疗。对于MTC患者而言,凡德他尼在RETM918T阳性和阴性的MTC患者中的疗效是否存在差异,仍待进一步验证。塞帕替尼由于具有高效低毒的特性,而有望成为RET突变阳性MTC患者的一线治疗选择。
目前对于TKI治疗晚期甲状腺癌的最佳启动时间尚无定论,特别是在无症状患者中。目前,对于时间选择,有研究建议在肿瘤负荷过大和肿瘤相关症状占主导地位之前开始。此外,肿瘤直径和肿瘤倍增时间相结合或许也能够为其提供帮助。同时,有助于确定治疗启动时间的预后预测因素也在不断探索之中。使用TKI治疗甲状腺癌时,需要平衡药物剂量与疗效和不良反应之间的利弊,积极监测不良反应,并且予以合理的处置,以使患者取得最大的生存获益。

