多核巨细胞在结核分枝杆菌感染过程中的作用研究
于有利,黎玉琼,*,王建东,梁小军,郭亚男,薛 峰
(1.宁夏农林科学院动物科学研究所,宁夏 银川 750002;2.南京农业大学动物医学院)
结核分枝杆菌是结核病的病原体,可导致无症状的潜伏性慢性感染,也可引发人和动物的活动性结核。在结核分枝杆菌感染的潜伏阶段,分枝杆菌可以感染不同器官和组织,导致免疫激活和肉芽肿的形成。肉芽肿(又名结节)是结核分枝杆菌感染的标志,是应对持续性炎症反应而形成的免疫细胞聚集体。肉芽肿可在某些病原体的感染中观察到,如分枝杆菌和隐球菌感染中,在免疫缺陷的情况下也会发现肉芽肿,如慢性肉芽肿。此外,肉芽肿也是非传染性特发性炎症性疾病的病理标志,如在系统性结节病和Blau综合征/早发性结节病。其中研究最多是由结核分枝杆菌感染导致的结核样肉芽肿,其组成和结构特征较为明确。典型的结构为干酪样坏死的中心,中心周边围绕大量炎症细胞如巨噬细胞、多核巨细胞、中性粒细胞、以及坏死或凋亡的巨噬细胞,最外层是T、B细胞和自然杀伤细胞,这样的结构被认为是分枝杆菌与宿主免疫系统的“主战场”,可阻止细菌向外扩散。然而最新的研究表明了相反的观点,Fenhalls等人通过分析肉芽肿大小和肉芽肿外围浸润的炎症细胞面积与干酪样坏死面积的比值时发现肉芽肿越大该比值越小,提示干酪样坏死区的扩大是以牺牲外周浸润细胞为代价,而不是通过从外周血中趋化炎症细胞来逐渐扩大的。在坏死区和外周细胞浸润处的交接处是分枝杆菌与免疫反应直接作用的地方,不会发生细胞的增殖和细胞因子分泌。这些发现表明,肉芽肿可能是分枝杆菌与宿主发生免疫反应后废弃的“战场”。因此了解肉芽肿独特的组织反应及组成的细胞成分对于了解结核病进展过程是至关重要的。
早在1868年,朗汉斯首次描述了多核巨细胞(MGC),并将其视为包括分枝杆菌、寄生虫等感染性疾病和结节病、克罗恩病等非感染性疾病的一种病理特征。mgc一般含有3个以上的细胞核,不同的疾病中mgc的形态不同,由此分为几种类型,如在分枝杆菌感染中MGC主要是Langhans mgc(LGCs),LGCs的细胞核呈花环状或马蹄状有序排列在细胞边缘,而异物巨细胞(Foreign-body-type giant cells,FGC)细胞核呈无序排列。由于肉芽肿中MGC的数量通常很少,很难分离和纯化。并且MGC很难进行表征和分类,因为它们的表型取决于它们所在环境、融合刺激的性质以及它们的功能。目前关于结核性肉芽肿中mgc细胞的生理学和功能的信息知之甚少。
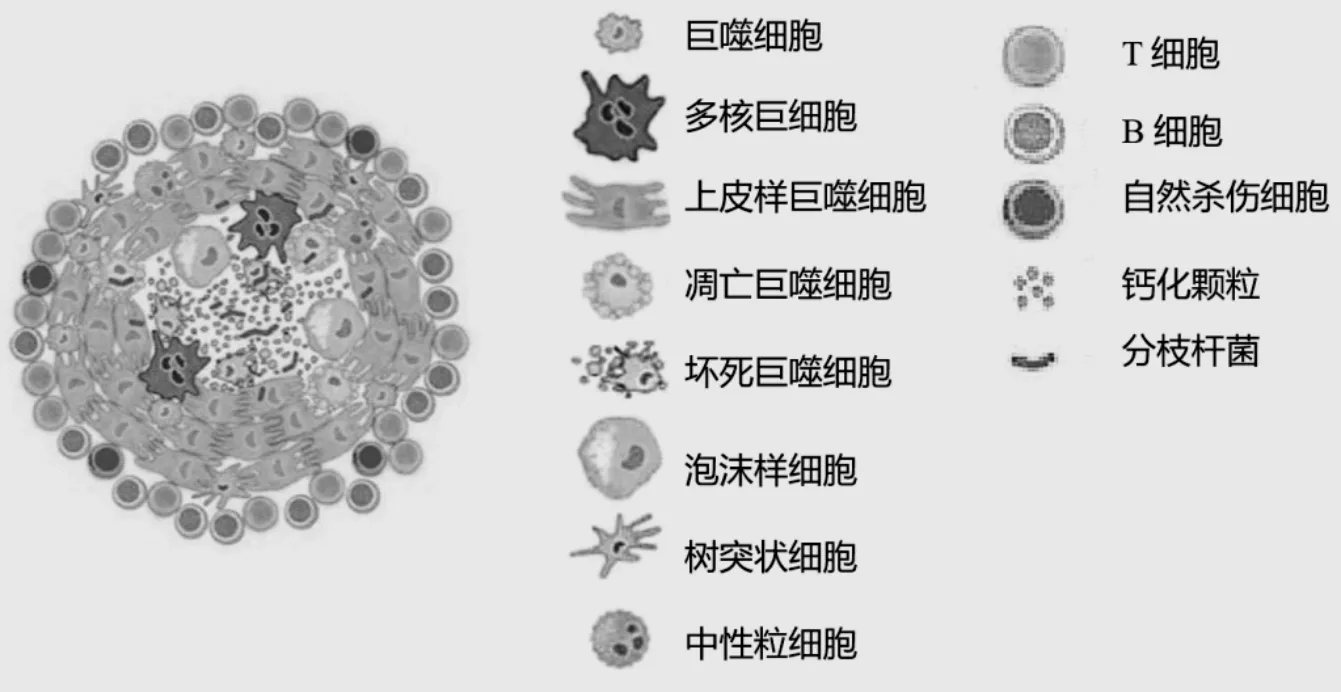
图1 结核样肉芽肿结构示意图
1 多核巨细胞(MGC)的形成
基于一些已有的疾病模型研究报道,在肉芽肿性炎症中巨噬细胞吞噬异物或病原体后,将其中一部分递呈给T淋巴细胞,并活化其他细胞。随后由这些细胞产生细胞因子,如白细胞介素(IL)-2激活其他T细胞;干扰素(IFN-γ)激活其他巨噬细胞,这种连锁反应导致巨噬细胞不断的转化为上皮样细胞和多核巨细胞。同样在体外一些细胞因子和分子可诱导不同类型的mgc,例如粒细胞-巨噬细胞集落刺激因子(GM-CSF)、巨噬细胞集落刺激因子(MCSF)和IL-3可以诱导LGCs的形成;IL-4、IL-13、DAP12和a-生育酚等可诱导FGCs。除了这些已被广泛证明的细胞因子,最近王洪生等人报道IL-15也可通过激活的T细胞和髓系细胞之间的相互作用来诱导LGC的形成。除了此类炎症介质外,一些病原体衍生的因子也可以诱导MGC的形成。胞壁酰二肽(MDP)是细菌细胞壁的肽聚糖成分,其可以在体外MGC形成过程中优先诱导LGC。同样Mizuno等人在体外单独或添加MDP的条件培养基培养CD14++/CD16-单核细胞的同时加入抗IFN-γ、抗IL-3或抗GM-CSF单克隆抗体(mAb)时,发现抗-IFN-γ mAb完全抑制了MGC的形成,而抗GM-CSF和抗IL-3 mAb显著抑制了LGC的形成。这些发现表明单核细胞可通过源自肉芽肿性疾病病原体的MDP与炎症介质(如IFN-γ、IL-3和GM-CSF)相互作用后促进LGCs的形成。Puissegur等人在体外建立结核分枝杆菌感染模型时发现分枝杆菌包膜糖脂通过TLR2和b1整合素ADAM9介导细胞融合机制诱导肉芽肿中mgc形成。另外,Sakai等人通过将人单核细胞与自体T细胞共同培养在含有ConA的培养液中用于体外诱导LGCs时发现CD41T细胞比CD81T细胞能诱导更多LGC形成,并且CD40和CD40配体(CD40L)之间的相互作用是诱导LGC形成所必需的。树突状细胞特异性跨膜蛋白(DC-STAMP)作为一种单核细胞融合相关分子,是促进LGC的形成的有效分子,其在LGC形成过程中表达上调,并通过siRNA下调DC-STAMP可抑制LGC的形成。

A.皮肤结核病例的代表性病理图像显示肉芽肿中的LGC(箭头)。苏木精和伊红染色。比例尺,100μm。B.rhGM-CSF联合rhIFN-γ诱导体外肉芽肿模型(箭头)
经典的理论认为mgc是巨噬细胞在细胞因子或细菌成分的刺激下融合而形成,类似于破骨细胞的形成。髓系细胞融合形成mgc是一个时空调控的多步骤过程。首先,细胞需要获得融合能力,这是由外源刺激和内源信号通路共同激活的,激活后触发具有融合能力细胞与底物发生黏附、细胞运动、细胞与细胞之间相互作用等,最后是膜融合。但是最新研究却发现了完全不一样的机制,与传统观念相反,该研究认为mgc 形成是由于细胞分裂失败导致的。据报道分别通过MCSF联合TNF或病原微生物刺激原(如BCG感染、TLR配体作用等)持续刺激用于诱导巨噬细胞分化成mgc时,发现巨噬细胞核发生了复制和分裂,但是细胞质却未分化成相应数目,胞质分裂失败与巨噬细胞产生的一氧化氮诱导的DNA 损伤修复有关。另外,mgc形成过程也可能与巨噬细胞的上皮样化过程有关有研究者认为上皮细胞样化过程与mgc融合过程调控着相同的信号通路,在上皮样化过程中具有增强粘附相关的基因如E-cadherin、DCSTAMP、OC-STAMP等表达上调,而粘附又是融合的基础。陈延庆等人通过激光捕获显微切割肉芽肿组织中LGCs联合 RNA测序研究LGCs分子特征时,发现LGCs中调控细胞形状和细胞骨架的肌动蛋白基因表达水平显著升高。肌动蛋白是维持细胞形状、细胞运动和细胞间粘附的关键因素,肌动蛋白也对细胞器运输过程也至关重要,因此猜测LGCs可能是来源于具有活跃的细胞变形和移动特性的巨噬细胞亚群。
作者认为,尽管上述研究已经部分揭示了调控MGC形成的分子信号机制,但是,由于结核肉芽肿存在不同核型、不同形态的MGC,提示结核肉芽肿微环境中各种细胞因子、趋化因子、结核分枝杆菌分泌蛋白、细胞壁脂质等可能共同诱导了不同类型MGC的产生,还有待进一步研究。
2 多核巨细胞(MGC)在结核分枝杆菌中的作用
mgc作为巨噬细胞发展的最终阶段,其功能的研究相对较少。目前MGC对宿主是有益的还是有害的仍然没有定论,因为肉芽肿中mgc虽抑制了结核分枝杆菌的传播,但不能有效的消灭所有的分枝杆菌,并促进了分枝杆菌存在的持久性。以响应细胞内病原体形成的MGC是宿主防御机制中的重要组成部分,缺乏MGC表明宿主免疫反应无效。Lay等人利用牛分枝杆菌BCG体外诱导LGCs时,比较了LGCs和巨噬细胞的吞噬能力,发现LGCs比巨噬细胞能够更多吞噬分枝杆菌,但LGC相较巨噬细胞杀菌能力较弱甚至无法杀灭细菌。这一结果同陈延庆等人报道一致的是通过比较LGCs和巨噬细胞的转录组学数据发现与巨噬细胞相比,LGCs中与免疫应答相关的许多基因和信号通路均下调表达。在体外,IL-4诱导的MGC比未诱导的巨噬细胞前体能更有效地吞噬大量异物。在麻风病患者肉芽肿中,LGCs主要存在于结核样皮损中,而在麻风瘤样皮损中较少,表明LGCs与宿主限制病原体的能力有关。免疫抑制药物特别是针对TNF-α的药物,可破坏肉芽肿的稳定性,减少MGC的数量导致细菌的扩散。MGC能够促进吞噬分枝杆菌的细胞发生凋亡,从而发挥抗分枝杆菌能力。另外,在结核分枝杆菌感染过程中,MGC是趋化因子的重要来源之一,在MGC分化过程中可分泌CXCL8、CCL2和CCL3,其中CCL2在单核细胞分化为mgc过程中发挥关键作用,对于肉芽肿的形成是必需的。然而,相反的观点表明mgc是有害的,据报道在结核患者肉芽肿中通过比较mgc和巨噬细胞基质金属蛋白酶-9(MMP-9)和基质金属蛋白酶-1(TIMP-1)的分泌能力时,发现mgc比巨噬细胞分泌更多的MMP-9和更少的TIMP-1。MMP-9通过上调表达一氧化氮合酶(iNOS)和环氧合酶-2(COX-2)介导了炎症反应损伤组织。巨噬细胞在感染分枝杆菌可分泌高水平一氧化氮(NO),NO可促进巨噬细胞向MGC分化,但矛盾的是mgc又促进了分枝杆菌持续存在。上皮样细胞可能是巨噬细胞和MGC之间的一种中间表型,增加了细菌负担,减少了宿主细胞的存活时间对宿主造成潜在的危害。
结核肉芽肿中存在多种MGC的诱导因素,诱导的MGC的表型不同,其功能很可能也不相同,不同MGC与结核病进展、抗结核治疗效果之间的关系,仍有待进一步研究。
3 多核巨细胞对提升免疫系统水平和持续性上将发挥重要作用
结核分枝杆菌作为一种成功且可持久感染的病原体,已经建立了一系列广泛的策略来逃避和颠覆免疫反应以助其在宿主体内持续存在。肉芽肿是结核分枝杆菌感染后的主要病变,目前尚不清楚肉芽肿是对宿主具有保护性还是破坏性。在肉芽肿形成发展过程中,免疫细胞、分枝杆菌的有关成分以及在病变部位存在的细胞因子都发挥着关键作用。MGC作为肉芽肿的特征性细胞,目前对MGC形成的机制及其在分枝杆菌感染中的作用研究,缺乏一个操作简单可靠的实验模型。已有动物模型如小鼠、家兔等与人体的免疫反应有差异,而且操作复杂,分离纯化困难,不能产生大量MGC,不利于系统深入的研究。因此进一步建立、完善接近体内病理条件下肉芽肿和MGC形成的体内外实验模型对于全面了解MGC的在分枝杆菌感染过程中发挥的作用其在以及分枝杆菌和宿主免疫之间复杂的相互作用机制具有重要意义。

