典型稀土元素修饰的二氧化钛光催化性能研究进展
高健 邹彬妮 陈佳琪 宋慧瑾
摘 要:TiO2的禁带宽度较宽,其带隙值一般为3.0~3.2 eV,将其光激发区域限制在紫外光区域,大范围的可见光甚至近红外光区的光子都没有被利用起来.此外,TiO2较高的电子—空穴对重组率也导致了其具有活性的光生载流子寿命降低,限制了TiO2作为光催化剂的效率.为了使这些问题得到妥善解决,可采用稀土元素(镧系元素)改善TiO2表面形貌、晶体类型、光学特性和光催化性能.综述了近年来被用作TiO2修饰改性的热门镧系元素的研究,重点阐述了镧系元素如何修饰改性TiO2,使其性能提升远超过纯TiO2,并介绍了镧系元素-TiO2在光催化和电子电器方面的应用.稀土元素的修饰可通过减小带隙,将TiO2工作波长从紫外光区移到可见光区域,抑制锐钛矿相到金红石相的转变,以及减弱光生电子对的重组效率等方式提高TiO2的光催化效率.
关键词:二氧化钛;稀土元素;光催化
中图分类号:O621.259.2;O643.36
文献标志码:A
0 引 言
纳米科学与纳米技术在近几十年内得到了飞速的发展,促进了对能源与光催化材料的深入研究.大量的半导体光催化材料已经被开发应用到各种领域之中[1],比如吸收二氧化碳、裂解水分子、固定氮气,以及降解废水中的有色染料和抗生素等[2].一般而言,光催化的过程主要体现在以下几个步骤:1)催化剂通过被光照产生光生载流子;2)光生载流子的分离与转移;3)通过消耗光生载流子将反应物转化为目标产物.当光照时催化剂吸收的光子能量大于或者等于其带隙值,价带(VB)中的电子就会被激发到导带(CB)之中,在VB中形成空穴,进而形成了电子—空穴对,然后电子和空穴分别在催化剂表面进行还原和氧化反应[3].
二氧化钛(TiO2)是一种半导体光催化剂,具有较高的化学稳定性,较低的毒性,更好的耐化学性等,并遵循具有低成本效益的大规模生产制备策略[4].TiO2由于其独特的回收能力和高能量转换效率,是最高效的金属氧化物半导体[5],在涂料、化妆品、电子电器与环境治理领域得到了重要的应用.光催化被认为是一种治理环境污染的友好方法,可以将有机污染物氧化为二氧化碳和水,从而除去水和空气中的污染物[6].
一般情况下,TiO2纳米颗粒以锐钛矿、金红石和板钛矿3种晶相存在[7].在这3种晶相中,锐钛矿相对于其他2种晶相而言,由于其自身的开放性结构,具有更稳定与更高效的光催化活性[8].金红石是TiO23种晶相中最稳定的结构,同时也表现出一定的光催化活性,但是活性程度相对锐钛矿低了很多;板钛矿相由于自身的不稳定性,较低的光催化活性应用较少[9].锐钛矿具有较强的光催化活性通常归因于表面吸附氧形成O-2或O-[10].然而,锐钛矿此类光催化剂具有3.20 eV的寬带隙能量,这限制了其在紫外光区域(波长为 387 nm)的应用,只有大约5%的太阳辐射可以被TiO2光激发[11].
各种修饰TiO2的策略,如将金属和非金属掺杂到TiO2的改性中,以减少电子—空穴复合并将吸收波长移到所需的可见光区域(波长大于400 nm),降低带隙值[12].一般来说,TiO2的应用分为能源应用和环境应用2种,这些应用不仅取决于纯TiO2本身的性质,还依赖于修饰剂和掺杂剂对TiO2表面的修饰[13].据报道,金属氧化物如氧化锌(ZnO)、硫化镉(CdS)和三氧化钨(WO3)掺杂TiO2半导体的性能较纯TiO2有了较大的提升,但由于这些半导体对光腐蚀的敏感性,使其实际应用范围受到了限制.除此之外,ZnO在水介质中不稳定,CdS和铁氧化物易受到阳极腐蚀,WO3的光照活性相对较低[8].也有研究人员通过改变TiO2的形貌进而改进其催化性能,例如,常见的TiO2纳米颗粒与TiO2纳米线等[14],通过增大比表面积和增加孔隙率来提升性能,然而形貌的控制通常需要较为复杂的制备工艺,因此制备难度较大.用稀土金属修饰制备TiO2是一种调节半导体对可见光区响应并增强其光催化性能的高效方法.
本文综述了近年来稀土(镧系元素)掺杂TiO2的研究,介绍了镧系元素-TiO2在光催化和电子电器方面的应用,并阐述了几种典型镧系元素如何修饰改性TiO2,使其催化性能远超纯TiO2.
1 镧系元素特征
镧系元素-TiO2具有优异的光催化性能可以吸收边缘的红移,也能提高锐钛矿向金红石相转变的温度和与各种路易斯物质形成复合物的能力,如醇、醛、酸、胺和硫醇[15].此外,由三价镧系离子修饰的材料通常具有发光特性.具有阶梯状能级的三价镧系离子嵌入在适当的无机材料晶格中,可以通过连续吸收多个近红外光子发射紫外光或可见光,这一过程可以导致光从近红外光和可见光谱范围转变为紫外光,从而提升宽带隙半导体的性能[16].镧系元素总共由15种元素组成,原子序数为57(镧)到71(镥).稀土离子的发光来自于其4f轨道内的f-f电子跃迁.由于5s和5p轨道与周围的微环境进行了空间屏蔽,使得电子跃迁几乎没有扰动,这些特定的狭窄带隙发射带发射的镧系离子导致了这些跃迁现象.这一现象使镧系元素在光催化应用中具有独特的化学性质[17].
2 纯TiO2与改性TiO2的光催化机制
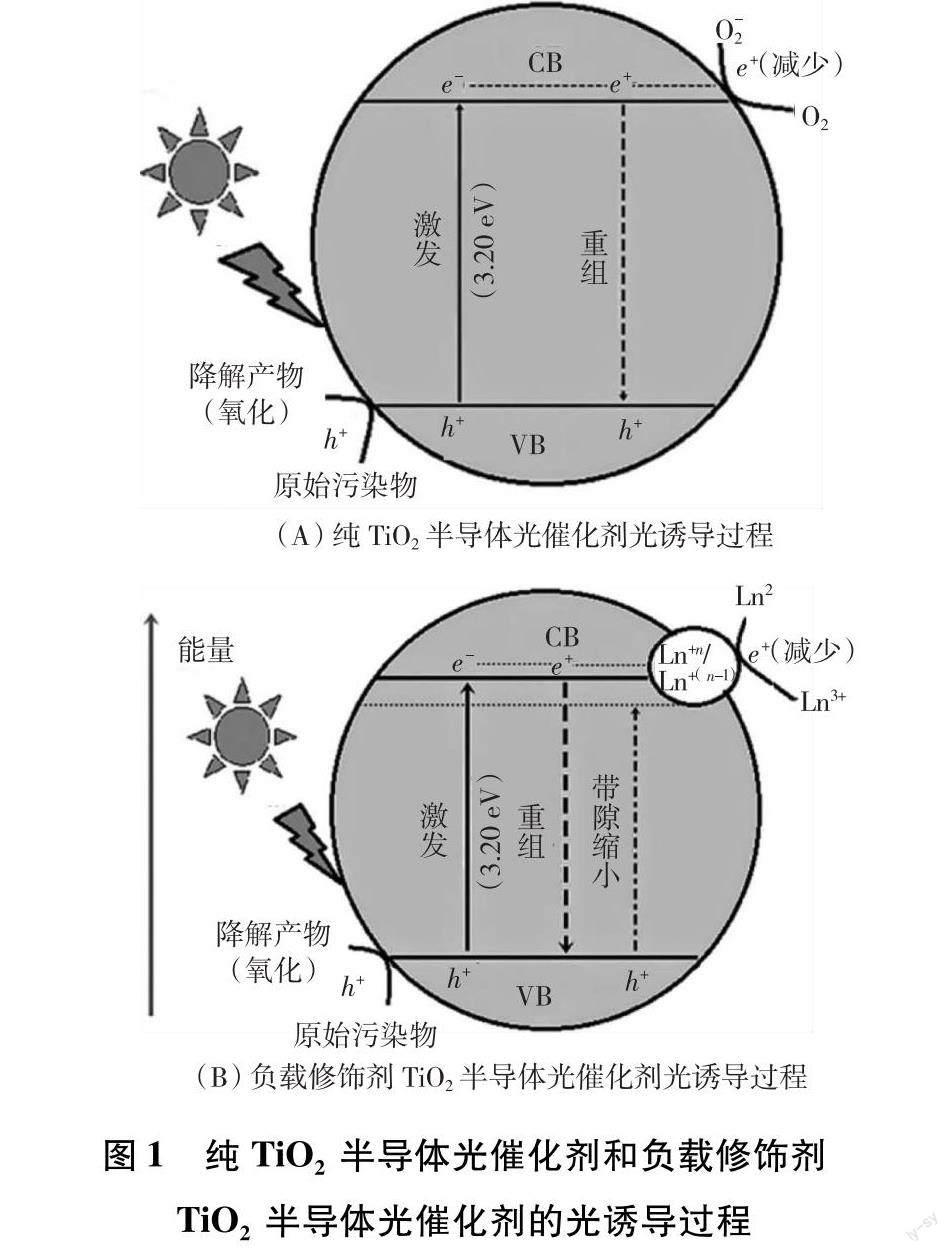
初级半导体光催化机制涉及吸收光能应该要大于材料的带隙能量阈值,导致光生电子(e-,CB)和正空穴(h+,VB)产生.通常,纯TiO2光催化性能的缺陷被简单地描述为TiO2的锐钛矿相带隙能(3.20 eV),意味着其光诱导激活仅发生在紫外光区域.其次,TiO2半导体通常存在光生电子—空穴对的重组的现象.金属改性剂的修饰不仅可以降低带隙值,也可以作为光生电子的捕获器.最终,这些光产生的电子将留在金属掺杂剂中,这限制了电子—空穴对的重组,最终导致光活性的增强.在没有合适的电子诱捕的情况下,电子—空穴对的重组率很高.这导致存储的能量在几纳秒内耗散,从而极大地降低了光催化效率[18].
研究表明,半导体如TiO2、ZnO、硫化锌(ZnS)和氧化铈(CeO2)被金属/非金属氧化物纳米颗粒修饰后,如金(Au)、银(Ag)、汞(Hg)和铈(Ce)等,通过将吸收边缘转移到更长的波长,以及降低光催化剂的电子—空穴对重组速率来提高光催化活性[19].纯TiO2半导体光催化剂和负载修饰剂TiO2半导体光催化剂的光诱导过程如图1所示.
通过在纯TiO2晶格中引入过渡金属离子,可以调整TiO2的费米能级、带隙能量和带分布及d-电子结构.由于部分占据的d轨道,产生了各种低于CB的新能级,这意味着红移,将产生更低的带隙,以及可见光吸收增强[20].TiO2晶格中过渡金属离子的存在改变了光生载流子密度,抑制了电子—空穴对的重组过程,提高了降解率.过渡金属离子改性的TiO2材料的性质与掺杂剂的浓度和分布、掺杂剂在半导体晶格中的能级、电子结构、电子供体量和光照射的强度有关.通过添加过渡金属掺杂剂,可以更好地提高TiO2的光催化活性[21].与传统金属相比,镧(La)、Ce和铒(Er)等稀土金属具有4f、5d和6s的構型,是调节TiO2特性的最佳掺杂剂.当三价镧系离子进入目标载体(TiO2)的晶格后,将会替代Ti4+而存在,这个变化使得TiO2的内部出现一定程度的畸变,例如,La3+的半径大于Ti4+,在晶格内部替换后会引起不平衡的电荷变化,为了使电荷重新达到平衡,将会在邻近位置产生氧空位,因此Ti4+被还原成Ti3+,形成以Ti3+为核心的还原中心,产生的氧空位和还原中心即可作为光催化反应的活性中心,进而提高催化性能[21].稀土金属的掺杂将改变光催化剂材料的晶体结构、电子态和光学特性.稀土离子掺杂抑制了TiO2光诱导电子—空穴对的重组,扩大了TiO2的光响应域,提高了其光催化活性.稀土金属将通过官能团与其f轨道的相互作用,与各种有机化合物生成配合物,以这种方式增强光活性响应.光催化剂中稀土离子的加入为更有效地利用太阳能分解污染物提供了可能[22].
3 镧系元素修饰改性TiO2
3.1 Ce修饰改性TiO2
Jin等[23]采用溶胶—凝胶法制备了Ce和锰(Mn)掺杂纳米TiO2,发现掺杂Ce的Mn/TiO2在低温选择性催化还原法(SCR)过程中,其对二氧化硫(SO2)的耐性显著提升,同时,硫酸铵((NH4)2SO4)的积累和活性得到了极大的抑制.其原理是SO2存在的情况下,在SCR过程中,Ce-TiO2催化剂促使SO2优先形成硫酸盐.Ce的掺杂明显降低NH+4与SO2-4的结合能,从而使得(NH4)2SO4的分解更加容易,(NH4)2SO4在Ce-Mn/TiO2催化剂的作用下,比Mn/TiO2时的分解温度降低大约70℃,说明了Ce掺杂可以有效地延缓表面硫酸化物质的形成,从而提高了催化剂的耐硫性.Liang等[24]在室温条件下采用溶胶法制备纳米结构的TiO2、Ag-TiO2和Ce-TiO2用于光催化降解甲醛,结果表明,掺杂Ag或Ce可以显著提高TiO2的光催化性能,湿度35%是最佳的实验条件,并且氧的浓度越高,去除甲醛效果越好.Tong等[25]利用乙醇和乙酸的醇化反应控制钛酸丁酯水解,进行水热反应来制备Ce-TiO2催化剂,发现掺杂Ce的TiO2能够有效提高催化剂在紫外光和可见光下的光催化活性,在紫外光和可见光的条件下最佳的掺杂浓度为0.2%和0.4%.光催化活性的提高可能与Ce4+/Ce3+特殊的4f电子构型有关.在紫外光照射下,Ce 4f电子能级对界面电荷转移,以及抑制电子—空穴重组起着重要作用.在可见光照射下,Ce 4f能级可以接收Ce-TiO2VB和三氧化二铈(Ce2O3)基态激发的电子,并进一步将电子转移到吸附氧中,进而产生超氧阴离子自由基.此外,Ce4+/Ce3+也可以提高光敏反应的效率.Ce-TiO2的吸收边缘红移用以下方程表示.
Ce-TiO2+hv→e-+h+(1)
Ce2O3+hv→e++h+(2)
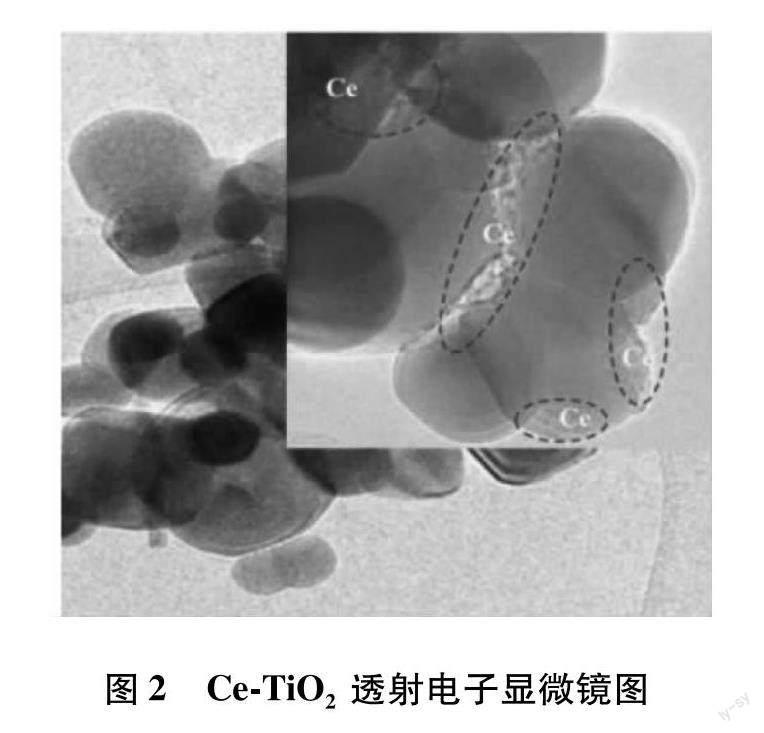
Behera等[26]采用水热法制备均匀的0.2%Ce-还原氧化石墨烯(RGO)/TiO2,对复合材料中的Ce4+浓度和RGO的调节,催化剂在可见光照射下的带隙调节起着至关重要的作用,通过光电流测试发现,0.2%Ce和10%RGO掺杂显著提高了催化剂的光电流密度,对杀虫剂吡虫啉具有良好的光催化降解性能,同时,该催化剂在可见光照射下对大肠杆菌和金黄色葡萄球菌具有良好的抗菌性能.在Ce-TiO2中,Ce4+掺杂在TiO2中引入了一种新的电子态,这个电子态使带隙值从紫外光降低到可见光的范围,在可见光的照射下TiO2的VB电子被激发到CexTi(1-x)O2的陷阱位点,光电子被氧捕获,在催化剂表面产生超氧离子,而且掺杂Ce可以增强催化剂表面的氧空位,增加对氧气(O2)的吸附,如图2所示.
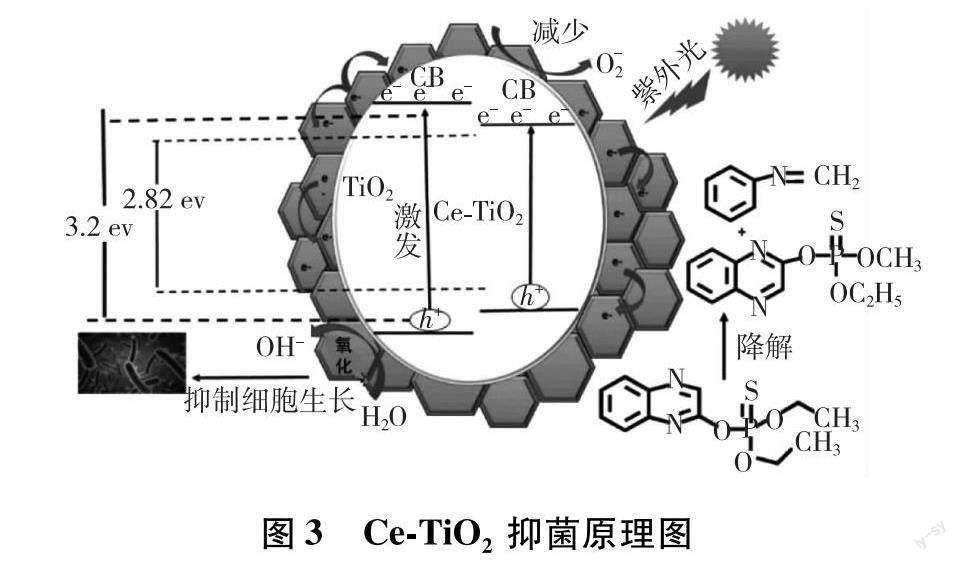
Lee等[27]通过浸渍法在不同煅烧温度下制备10 wt%Ce-TiO2催化剂,发现在氨气(NH3)被选择性催化氧化成N2的过程中,催化剂的性能主要取决于Ce的氧化态种类和催化剂中氧的行为.在350℃下表现出最高的NH3转化率(96%),这是由于在催化剂中具有分散良好的Ce4+,并且在CeO2和TiO2之间较弱的相互作用导致了高晶格—氧迁移率.Behera等[26]通过水基溶胶—凝胶法和喷雾技术合成了带隙较小的多孔微球型的0~1.0 wt% Ce-TiO2,通过实验发现,Ce-TiO2催化剂在可见光下比纯TiO2更有活性,Ce-TiO2的稀土离子(Ce3+/Ce4+)、Ti还原态(Ti3+/Ti2+)和氧空位降低了光诱导电子—空穴对的重组.因此,0.8 wt%Ce-TiO2对NOx的降解率是原始TiO2的2.8倍.Ce加入TiO2导致Ce4+/Ce3+的形成,不仅减少了带隙,还作为电子捕获器(Ce4++e-→Ce3+;Ce3++O2→O-2+Ce4+)来延缓电荷的重组.Ti3+、Ti2+(Ti还原态)和氧空位也促进了可见光区域的电荷转移和光子吸收.Khan等[28]采用溶胶—凝胶法制备Ce-TiO2的锐钛矿型薄膜,发现掺杂元素后的催化剂能带发生红移,如图3所示,因此证明Ce的掺杂有效地改变了截止波长,使得催化剂的带隙降低到3.09 eV,并且随着Ce的掺杂,由于结合磁极化子的增强,TiO2薄膜的磁性也随之增强.
3.2 Er修饰改性TiO2
王晓东等[29]采用浸渍—旋转法在石英玻璃片上制备了一系列的Er-TiO2多孔薄膜,并且发现当涂膜层数为3层,煅烧温度为550℃,煅烧时间为1 h时,催化剂的催化性能最为优越,在可见光照模拟实验中,薄膜对7.8 mg/L的甲基橙(MO)溶液用时6 h,催化降解率达到64.6%.梁春华[30]应用溶胶—凝胶法,制备了不同含量的Er-TiO2催化剂,发现所制备的催化剂均为锐钛矿型,在Er3+的掺杂用量为1.2%,催化剂的用量为0.6 g/L时,对甲胺磷的降解效果最佳,随着催化剂的用量提升,催化效率也会随之提升,但当用量继续提升效率却随之下降,这是由于在一定范围内,催化剂的增加使得反应表面积增大,光的可利用性也就随之增大,电子—空穴对也增多,所以降解率提升,但是当用量过多后,催化剂会对照射入反应溶液的光起到遮挡和散射作用,从而降解率会降低,如图4示.
Mazierski等[31]通过水热法制备一系列比例的Er-TiO2,此类催化剂既含有掺杂的Er,又含有表面吸附的Er,发现在相同的条件下,0.25 wt%Er-TiO2对苯酚的降解效率是最好的,Er在修饰改性过程中导致TiO2激活Vis反应,并且Er的4f的子带隙态引起轻微的带隙变窄,导致O-2产生,进一步加强了光催化降解能力.Zhang等[32]采用简单温和的水热法制备Er-TiO2纳米棒,可以通过红外光谱激发可见光,使得催化剂获得更多的激发能,产生更多的电子和空穴,从而导致电子浓度的增加.此外,Er-TiO2纳米棒的平带边缘发生正位移,相应地提高了向TiO2VB的电子注入驱动力,从而导致电流密度的增加.与未掺杂Er的TiO2相比,光电流密度为22.97 mA/cm2,功率转换效率为10.6%,性能的提高归因于扩展了光吸收的范围,提高了电子转移效率,减少了电子—空穴复合.Boikanyo等[33]通过溶胶—凝胶法制备Er掺杂的TiO2,得到的催化剂是一种单相晶体半导体氧化物,晶体尺寸变小,表面积和中孔度增加,且载流子重组率显著降低,其中纯TiO2的晶粒为13.93 nm,掺杂Er后的催化剂结构性能得到极大增强,晶粒为5.6 nm,比表面积为103.14 m2/g,孔隙体积为0.446 4 cm3/g.Lahiri等[34]采用电子束蒸发法制备了Er-Au/TiO2,采用电容电压(C-V)迟滞法研究了器件的记忆性能,在Er-TiO2的薄膜扫描电压为±10 V时,从滞后中提取的最大记忆窗口为3.068.在1MHz时,得到了Er-TiO2的电子和空穴捕获密度分别为9.9×1010/cm2和2.58×1010 /cm2.Mondal等[35]利用基于热蒸法的光栅角沉积技术(GLAD)制备了Er-Ag/TiO2,該类催化剂为锐钛矿/金红石的混合晶型,带隙能为3.14 eV,在530 nm处有光致发光(PL)发射,这与氧缺陷有关,且在380 nm光照下,比纯TiO2的光响应率高4.5倍.Talane等[36]通过溶胶—凝胶法制备出掺杂Er的纯锐钛矿相的TiO2催化剂,Er3+的掺杂使得催化剂颗粒粒径变小,导致带边发生红移,当Er3+的浓度达到1% mol时,表现出最低的PL发射强度,因此该催化剂具有最好的催化性能.Lahiri等[37]利用GLAD制备了掺杂Er的TiO2催化剂,与纯TiO2相比,由于Er的掺杂和取代,催化剂的带隙变低,同时紫外区的吸收有所增强,电测量中,在350 nm处,Er-TiO2在上升时间Tr=1.23 s和下降时间Tf=0.6 s时表现出更好的开关特性,性能优于纯TiO2,因此更适合应用于紫外检测器.Mondal等[38]应用溶胶—凝胶法合成了掺杂Er3+的TiO2,Er3+浓度的增加导致了晶粒尺寸的减小,0.75 wt% Er和0.98 wt% Er掺杂的TiO2粒径大小分别为22 nm和16 nm,在PL测试中,掺杂的TiO2(0.98 wt% Er)在1.537 μm的PL强度增加到约4倍.未掺杂的TiO2的屏障高度计算为0.87 eV,中等掺杂的TiO2(0.75 wt% Er)降低到0.77 eV,较高掺杂的TiO2(0.98 wt% Er)增加到0.99 eV.随着Er掺杂量的增加,同时由于去氧,理想因子和反向饱和电流逐渐降低,在370 nm处,基于Er掺杂的TiO2(0.98 wt% Er)的器件的响应率比未掺杂的器件提高了13倍.基于Er掺杂的TiO2(0.98 wt% Er)的器件在370 nm的波长下显示出最大内部增益,因此随着Er掺杂浓度的增加,开关性能有所提高.Singh等[39]采用溶剂热法成功合成掺杂Er介孔TiO2,TiO2(1mM Er)的光催化活性最好,在28 min内罗丹明B的降解率为98.78%.Er对O2的吸附增强,并且TiO2的表面积增大,导致了光催化活性的增强,可作为可见光照明下工业废水处理的光催化剂.
3.3 La修饰改性TiO2
Kocˇí等[40]采用普通的溶胶—凝胶法制备了0.2~1.5 wt% La-TiO2催化剂,发现当La的含量为0.2 wt%时,催化剂的产氢效率是纯TiO2的2倍,低La负载材料的光催化活性的增强可以解释为La-TiO2异质结的协同效应,显示出较低的電子—空穴重组,以及更好的电荷传输和转移.Tahir[41]通过溶胶—凝胶法成功合成了La改性的碳纳米管(CNTs)/TiO2复合材料,并测试了在可见光照射下,光催化甘油—水(H2O)混合物促进H2的生成.催化剂的结构大大提高了H2的产量,La-TiO2 纳米棒(NRs)/CNTs产量最高,比La-TiO2纳米颗粒(NPs)/CNTs复合样品高1.14倍.La-TiO2的性能优于纯TiO2,显然是由于较大的表面积,能有效地捕获和运输光产生的电荷,如图5所示.
Armakovi?等[42]采用改良的溶胶—凝胶法,并在450~750℃的煅烧温度下,制备了1 wt%La-TiO2,当煅烧温度为450℃时表现出最佳的光催化性能,在降解盐酸普萘洛尔(PRO)和美托洛尔酒石酸盐(MET)中表现最好,原因是该温度下的掺杂催化剂拥有最大的比表面积和最小的晶粒.Tahir等[43]应用溶胶—凝胶法制备La修饰的纳米TiO2催化剂,发现由于氧化镧(La2O3)的存在,使催化剂的晶粒尺寸减小,而比表面积(BET)和碱度增加,在光诱导二氧化碳—甲烷(CO2-CH4)反应体系中,La-TiO2催化剂检测到的主要产物为一氧化碳(CO)、氢气(H2)和乙烷.超过5 wt%La-TiO2产生的CO量是纯TiO2产生的CO量的9.6倍.当将H2O加入CO2-CH4反应体系时,CO的产率比纯TiO2提高了37倍.Nguyen等[44]制备了La-TiO2和活性炭纤维(ACF)的组合,并用于双酚A(BPA)和2-氯苯酚(2-CP)的光催化分解,结果发现,在TiO2中引入La可以缩小带隙能量,延长可见光吸附范围,从而提高有机污染物的降解性能.与商业TiO2相比,La-TiO2/ACF对BPA和2-CP具有更明显的光催化降解效果.对BPA和2-CP的降解产物进行了研究,结果表明,在60 min后,有机污染物几乎被降解为CO2和H2O.Zhang等[45]采用溶胶—凝胶法结合真空退火处理制备了TiO2纳米颗粒,发现少量的La3+被掺杂到TiO2晶格中,而大部分La原子以La2O3的形式均匀分布到TiO2基质中.Ti1-xLaxO2纳米颗粒表面氧空位的浓度是通过将La3+与TiO2基质的结合来控制的.Pascariu等[46]采用静电纺丝法在400~700℃下煅烧,合成纯TiO2和La3+掺杂的TiO2纳米纤维,发现当La3+的掺杂量为0.1 wt%,煅烧温度为600℃,在可见光照时间为300 min时,光催化降解亚甲基蓝效率最佳为91%,降解速率为2.179×10-2 /min,降解环丙沙星的效率为99.5%,降解速率为1.981×10-2 /min.其原因是TiO2晶格中引入La3+,可以调整TiO2的费米能级、带分布及d-电子结构,导致红移、更低的带隙和增强的可见光收获,同时带隙从3.21 eV减少到2.86 eV,抑制电子—空穴对的重组,提高降解速率.
4 结 语
TiO2的性能可通过添加部分镧系元素进行改性,具体是通过控制光催化剂的宽禁带、激发光范围和锐钛矿到金红石的相变,以及电子—空穴对的重组过程,使得催化效率得到明显改善.尽管镧系元素掺杂TiO2在制备方法和性能改进上已经取得了较大的进步,但仍然存在着较多的难题:
1)目前稀土离子修饰的TiO2光催化剂依旧是粉末状,在水中进行光催化反应后依旧处于难以回收的状态,很难做到重复利用.
2)由于测试实验往往需要耗费大量的时间,需要比较苛刻的测试条件和精密的测试仪器,以及大量可能存在的镧系元素-TiO2结构组合,导致了镧系元素-TiO2光催化剂很难得到正确的表征.
3)在复合TiO2的合成过程,一般都采用溶胶—凝胶法,需要大量的烷烃前体和溶剂,产品最终的制成率相当低,产出的废料比率相当高.
參考文献:
[1]Linsebigler A L,Lu G,Yates J.Photocatalysis on TiO2surfaces:principles,mechanisms,and selected results[J].Chem Rev,1995,95(3):735-758.
[2]Wang X,Jing D,Ni M.Solar photocatalytic energy conversion[J].Sci Bull,2017,62:597-598.
[3]Tong H,Ouyang S,Bi Y,et al.Nano-photocatalytic materials:possibilities and challenges[J].Adv Mater,2012,24(2):229-251.
[4]Asemi M,Ghanaatshoar M.Hydrothermal growth of one-dimensional Ce-doped TiO2nanostructures for solid-state DSSCs comprising Mg-doped CuCrO2[J].J Master Sci,2017,52(1):489-503.
[5]Li R,Li T,Zhou Q.Impact of titanium dioxide (TiO2) modification on its application to pollution treatment:A review[J].Catalysts,2020,10(7):804.
[6]Wang G,Wang H,Ling Y,et al.Hydrogen-treated TiO2nanowire arrays for photoelectrochemical water splitting[J].Nano Lett,2011,11(7):3026-3033.
[7]Chen H,Zhao L,Xiang Y,et al.A novel Zn-TiO2/C@SiO2nanoporous material on rice husk for photocatalytic applications under visible light[J].Desalin Water Treat,2015,57(21):9660-9670.
[8]Zhang X,Chen J,Jiang S,et al.Enhanced photocatalytic degradation of gaseous toluene and liquidus tetracycline by anatase/rutile titanium dioxide with heterophase junction derived from materials of Institut Lavoisier-125(Ti):Degradation pathway and mechanism studies[J].J Colloid Interface Sci,2021,588:122-137.
[9]Li S,Shi W,Liu W,et al.A duodecennial national synthesis of antibiotics in China's major rivers and seas (2005—2016)[J].Sci Total Environ,2018,615:906-917.
[10]Daghrir R,Drogui P,Robert D,et al.Modified TiO2for environmental photocatalytic applications:A review[J].Ind Eng Chem Res,2013,52(10):3581-3599.
[11]Cacciotti I,Bianco A,Pezzotti G,et al.Synthesis,thermal behaviour and luminescence properties of rare earth-doped titania nanofibers[J].Chem Eng,2011,166(2):751-764.
[12]Chen X,Mao Y.Titanium dioxide nanomaterials:Synthesis,properties,modifications,and applications[J].Chem Rev,2007,107(7):2891-2959.
[13]Chowdhury P,Moreira J,Gomaa H,et al.Visible-solar-light-driven photocatalytic degradation of phenol with dye-sensitized TiO2:Parametric and kinetic study[J].Ind Eng Chem Res,2012,51(12):4523-4532.
[14]Wang G,Wang H,Ling Y,et al.Hydrogen-Treated TiO2Nanowire Arrays for Photoelectrochemical Water Splitting[J].Nano Lett,2011,11(7):3026-3033.
[15]Reszczyńska J,Grzyb T,Sobczak J W,et al.Visible light activity of rare earth metal doped (Er3+,Yb3+or Er3+/Yb3+) titania photocatalysts[J].Appl Catal B,2015,163:40-49.
[16]Yu L,Yang X,He J,et al.One-step hydrothermal method to prepare nitrogen and lanthanum Co-doped TiO2nanocrystals with exposed {0 0 1} facets and study on their photocatalytic activities in visible light[J].J Alloys Compd,2015,637:308-314.
[17]Zhan W,Guo Y,Gong X,et al.Current status and perspectives of rare earth catalytic materials and catalysis[J].Chinese J Catal,2014,35(8):1238-1250.
[18]Barka N,Qourzal S,Assabbane A,et al.Kinetic modeling of the photocatalytic degradation of methyl orange by supported TiO2[J].J Environ Sci,2010,4(5):1-4.
[19]Ashkarran A A,Aghigh S M,Farahani N.Visible light photo-and bioactivity of Ag/TiO2nanocomposite with various silver contents[J].Cur Appl Dhys,2011,11(4):1048-1055.
[20]Zhang Y,Kilin D S.Computational modeling of wet TiO2(001) anatase surfaces functionalized by transition metal doping[J].Int Quanturn Chem,2012,112(24):3867-3873.
[21]Mazinani B,Masrom A K,Beitollahi A,et al.Photocatalytic activity,surface area and phase modification of mesoporous SiO2-TiO2prepared by a one-step hydrothermal procedure[J].Ceram Int,2014,40(8):11525-11532.
[22]Ma Y T,Li S D.Photocatalytic activity of TiO2nanofibers with doped La prepared by electrospinning method[J].J Chin Chem Soc-Taip,2015,62(4):380-384.
[23]Jin R,Liu Y,Wang Y,et al.The role of cerium in the improved SO2tolerance for NO reduction with NH3over Mn-Ce/TiO2catalyst at low temperature[J].Appl Catal,2014,148/149:582-588.
[24]Liang W,Li J,Jin Y.Photo-catalytic degradation of gaseous formaldehyde by TiO2/UV,Ag/TiO2/UV and Ce/TiO2/UV[J].Building Environ,2012,51:345-350.
[25]Tong T,Zhang J,Tian B,et al.Preparation of Ce-TiO2catalysts by controlled hydrolysis of titanium alkoxide based on esterification reaction and study on its photocatalytic activity[J].J Colloid Interface Sci,2007,315(1):382-388.
[26]Behera L,Barik B,Mohapatra S.Improved photodegradation and antimicrobial activity of hydrothermally synthesized 0.2Ce-TiO2/RGO under visible light[J].Colloid surf A Physicochem Eng Asp,2021,620:126553-1-126553-12.
[27]Lee S M,Lee H H,Hong S C.Influence of calcination temperature on Ce/TiO2catalysis of selective catalytic oxidation of NH3to N2[J].Appl Catal A-Gen,2014,470:189-198.
[28]Khan H,Gar Alalm M,Lalonde-Lavoie M,et al.Photocatalytic degradation of NOxand ethanol in the gas phase by spray dried Ce-TiO2[J].J Environ Chem Eng,2021,9(6):106813-1-106813-9.
[29]王曉东,黄玉娇,李少妮,等.多孔Er-TiO2薄膜的制备及其光催化性能[J].中国有色金属学报,2017,27(8):1621-1631.
[30]梁春华.铒掺杂二氧化钛光催化降解甲胺磷农药的研究[J].吉林农业大学学报,2012,34(5):536-539.
[31]Mazierski P,Mikolajczyk A,Grzyb T,et al.On the excitation mechanism of visible responsible Er-TiO2system proved by experimental and theoretical investigations for boosting photocatalytic activity[J].Appl Surf Sci,2020,527:146815-1-146815-11.
[32]Zhang H,Zhang Q,Lv Y,et al.Upconversion Er-doped TiO2nanorod arrays for perovskite solar cells and the performance improvement[J].Mater Res Bull,2018,106:346-352.
[33]Boikanyo D,Mishra S B,Ray S,et al.Structure-activity relationships of Er3+and MWCNT-modified TiO2:Enhancing the textural and optoelectronic properties of TiO2[J].J Phys Chem,2019,123(51):31246-31261.
[34]Lahiri R,Mondal A.Improved capacitive memory of Er:TiO2TF based MOS device[J].J Alloys Compd,2019,792:679-683.
[35]Mondal S,Ghosh C,Dhar Dwivedi S M M,et al.An experimental and theoretical understanding of a UV photodetector based on Ag nanoparticles decorated Er-doped TiO2thin film[J].Ceram Int,2021,47(10):14879-14891.
[36]Talane T E,Mbule P S,Noto L L,et al.Sol-gel preparation and characterization of Er3+doped TiO2luminescent nanoparticles[J].Mater Res Bull,2018,108:234-241.
[37]Lahiri R,Ghosh A,Choudhuri B,et al.Investigation on improved performance of Erbium doped TiO2nanowire based UV detector[J].Mater Res Bull,2018,103:259-267.
[38]Mondal S,Ghosh A,Piton M R,et al.Investigation of optical and electrical properties of erbium-doped TiO2thin films for photodetector applications[J].J Mater Sci Mater Electron,2018,29(22):19588-19600.
[39]Singh K,Harish S,Kristy A P,et al.Erbium doped TiO2interconnected mesoporous spheres as an efficient visible light catalyst for photocatalytic applications[J].Environ Sci Pollut Res,2018,449:755-763.
[40]Kocˇí K,Troppova I,Edelmannova M,et al.Photocatalytic decomposition of methanol over La/TiO2materials[J].Int J Hydrog Energy,2018,25(35):34818-34825.
[41]Tahir M.La-modified TiO2/carbon nanotubes assembly nanocomposite for efficient photocatalytic hydrogen evolution from glycerol-water mixture[J].Arab J Chem,2019,44(7):3711-3725.
[42]Armakovi? S J,Gruji?-Broj?in M,??epanovi? M,et al.Efficiency of La-doped TiO2calcined at different temperatures in photocatalytic degradation of β-blockers[J].Arabian Journal of Chemistry,2019,12(8):5355-5369.
[43]Tahir B,Tahir M,Amin N A S.Tailoring performance of La-modified TiO2nanocatalyst for continuous photocatalytic CO2reforming of CH4to fuels in the presence of H2O[J].Energ Convers Manage,2018,159:284-298.
[44]Nguyen T D,Jitae K,Viet N M,et al.Combination of La-TiO2and activated carbon fiber for degradation of toxic organic pollutants under the visible light[J].J Environ Chem Eng,2019,7(3):103180-1-103180-9.
[45]Zhang H,Wang Y,Zhong W,et al.Tailoring the room temperature ferromagnetism in TiO2nanoparticles by modulating the concentration of surface oxygen vacancy via La incorporating[J].Ceram Int,2019,45(10):12949-12956.
[46]Pascariu P,Cojocaru C,Homocianu M,et al.New La3+doped TiO2nanofibers for photocatalytic degradation of organic pollutants:Effects of thermal treatment and doping loadings[J].Ceram Int,2022,48(4):4953-4964.
(實习编辑:罗 媛)
Research Progress on Photocatalytic Properties of TiO2Modified with Typical Rare Earth Elements
GAO Jian,ZOU Binni,CHEN Jiaqi,SONG Huijin
(School of Mechanical Engineering,Chengdu University,Chengdu 610106,China)
Abstract:TiO2has a wide band gap,and its band gap value is generally 3.0~3.2 eV,which limits its photoexcitation region to the ultraviolet region,and a large range of visible light and even near-infrared photons are not used.In addition,the high electron-hole pair recombination rate of TiO2also leads to the reduced lifetime of its active photogenerated carriers,which limits the efficiency of TiO2as a photocatalyst.In order to solve these problems properly,the use of rare earth elements (lanthanides) to improve the surface morphology,crystal type,optical properties and photocatalytic performance of TiO2have been studied.This paper reviews the recent studies on the hot lanthanide elements used as TiO2modification.It focuses on how Ln elements modify TiO2to improve its performance far beyond that of pure TiO2,and focuses on the application of Ln-TiO2in photocatalysis,electronics and electrical appliances.The modification of rare earth elements can improve the photocatalytic efficiency of TiO2by reducing the band gap,shifting the working wavelength of TiO2from ultraviolet to visible region,inhibiting the transition from anatase phase to rutile phase,and weakening the recombination efficiency of photogenerated electron pairs.
Key words:TiO2;rare earth elements;photocatalysis

