牛羊毛发中3种β-受体激动剂药物残留测定的EMR-Lipid方法研究
李文辉,于寒冰,倪香艳,张晶晶,魏紫嫣,王乐宜,赵雅妮,赵莹,方芳,孙志文
(北京市农产品质量安全中心,北京 102600)
克伦特罗、沙丁胺醇、莱克多巴胺等是最常见的β-受体激动剂类药物,具有促进动物快速生长、降低脂肪含量、提高瘦肉率的作用[1-2],在我国常被违规作为促生长添加剂使用而被广泛关注。政府多次发布牛羊养殖过程非法使用β-受体激动剂类药物的情况,药物在动物体内残留通过食物链进入人体后会使人产生肌肉震颤、心悸、恶心等中毒症状,危害人类健康[1-3]。欧盟和国际食品法典委员会(CAC)制定了药物的限制使用规定,我国早在1997年明令禁止克伦特罗作饲料添加剂,农业农村部250号公告[4]已经对克伦特罗等β-受体激动剂类药物在所有可食用动物组织中做出明确的禁用规定,但现实养殖过程中,为了缩短上市周期,获得高回报收益,特别是在牛羊等长养殖周期动物上的使用仍然存在。
目前通常选用可食性组织或者血液和尿液作为监测目标,动物可食性组织的采集需在屠宰之后,存在时滞性和局限性,即使检出不合格,对于已流入市场的不合格样品因追溯困难也难以做到及时有效的管控;同时药物在血液和尿液中代谢速度快,停药一段时间后已检测不到药物残留,此时动物组织中仍可能有药物残留,容易造成漏检,严重威胁着动物性食品安全,使监管面临巨大挑战[1-2]。多项研究表明动物毛发中可以蓄积多种兽药,包括兴奋剂类、激素类等药物[3,5-8],同时,β-受体激动剂药物在动物毛发中代谢活性低,动物毛发消除规律研究表明药物在毛发中可以稳定存在,因此可作为β-受体激动剂药物在畜禽养殖环节违法添加监测监管的靶标,也成为评价动物性产品中药物残留量的重要参考组织[1-2]。为了解决上述问题,本研究提供了一种牛羊毛发样品中β-受体激动剂类药物残留检测方法,利用动物毛发实现无需宰杀动物检测β-受体激动剂类药物并可以对牛羊养殖屠宰整个周期持续监测,结合高效的强化基质去除技术(EMR-Lipid)获取出色的待测药物回收率,提高多种药物同时定量分析的效率,满足高效率测定的需求,准确度、灵敏度和精密度高,为动物性产品中β-受体激动剂类药物残留量测定提供参考依据。
1 材料与方法
1.1 主要仪器设备和耗材
Waters Xevo TQ-S超高效液相色谱串联质谱仪(配有MassLynx V4.1软件处理系统,美国沃特世公司);TTL-DCII氮吹仪(美国Jnc公司);Vortex 3000 Elite旋涡振荡器(德国艾卡公司);JM-03D-80超声波清洗器(洁盟清洗设备公司);A11球磨机(德国艾卡公司);Captiva EMR-Lipid净化柱、QuEChERS净化柱和萃取盐包(美国安捷伦公司);HLB和MCX固相萃取柱(美国沃特世公司);GCB石墨化炭黑(美国赛默飞公司);溶剂过滤器(孔径 0.22 μm,美国颇尔公司)。
1.2 主要试剂和标准品
试剂:乙腈、甲醇和甲酸(色谱级和质谱级,美国赛默飞公司);十二烷基磺酸钠和盐酸(分析纯,国药集团化学试剂有限公司)。
标准品:克伦特罗(C11668560),莱克多巴胺(C16805000),沙丁胺醇(C16903000),含量均≥98.0% (美国Dr.E公司)。克伦特罗-D9同位素标记物(C11668561),莱克多巴胺-D6同位素标记物(A16805010),沙丁胺醇-D3同位素标记物(XA16903001),含量均≥98.0%(美国Dr.E公司)。
1.3 溶液和标准溶液的配制
0.01 g/mL十二烷基磺酸钠溶液:称取十二烷基磺酸钠10 g,加水溶解并稀释至1 000 mL,混匀。0.1 mol/L盐酸溶液:取盐酸8.3 mL,加水稀释至1 000 mL,混匀。5%氨化乙腈溶液:取氨水5 mL,加入乙腈95 mL,混匀。0.1%甲酸溶液:取甲酸1 mL,加水稀释至1 000 mL,混匀。
标准储备液:取约10 mg标准品(精密称定),分别置于10 mL棕色容量瓶中,用甲醇溶解并稀释至刻度,配成浓度为1 mg/mL的标准储备液,-18 ℃以下保存,有效期12个月。混合标准工作液:吸取混合标准中间液0.1 mL,置于10 mL棕色容量瓶中,用0.1%甲酸溶液溶解并稀释至刻度,配成浓度为100 ng/mL混合标准工作液,现配现用。
1.4 试样的制备与保存
1.4.1 样品采集
选取牛羊皮肤毛发,毛发从根部剪断,保存备用,单只动物采集毛发的量应不少于4 g。
1.4.2 样品制备和保存
取2 g毛发加入50 mL烧杯中,加入20 mL 0.01 g/mL的十二烷基磺酸钠溶液[2],超声清洗30 min,后用水洗净毛发,放在40 ℃的干燥箱中烘干,用球磨机将其粉碎至粉末,置于干燥器中保存备用。
1.5 试样的提取和净化
1.5.1 提取
取试样(0.50±0.02)g(精确至0.01 g)置于离心管内,样品中添加适量同位素标记物标准工作液(100 ng/mL)25 μL,取5 mL 0.1 mol/L盐酸溶液于离心管中,涡旋混匀。于60 ℃水浴中水解4 h,7 000 r/min离心10 min,取上清液加入10 mL 5%氨化乙腈,加萃取盐包,涡旋混匀5 min,8 000 r/min离心10 min,上清液取5 mL氮气吹至2.5 mL左右备用。
1.5.2 净化
将提取后的上清液和0.5 mL超纯水加入到Captiva EMR-Lipid净化柱中,收集滤液后,加入50 mg GCB,用涡旋混合器混匀1 min,然后在4 ℃,9 000 r/min离心10 min,得到的净化溶液过0.22 μm的微孔滤膜,得到待测样品溶液供仪器测定分析。
1.6 测定方法条件
1.6.1 液相色谱参考条件
色谱柱:Waters UPLC BEH C18柱,规格50 mm×2.1 mm,填料粒径1.7 μm;柱温:40 ℃;进样量:2 μL;流动相A:乙腈;流动相B:0.1%甲酸水;流速:0.3 mL/min,梯度洗脱。具体程序见表1。
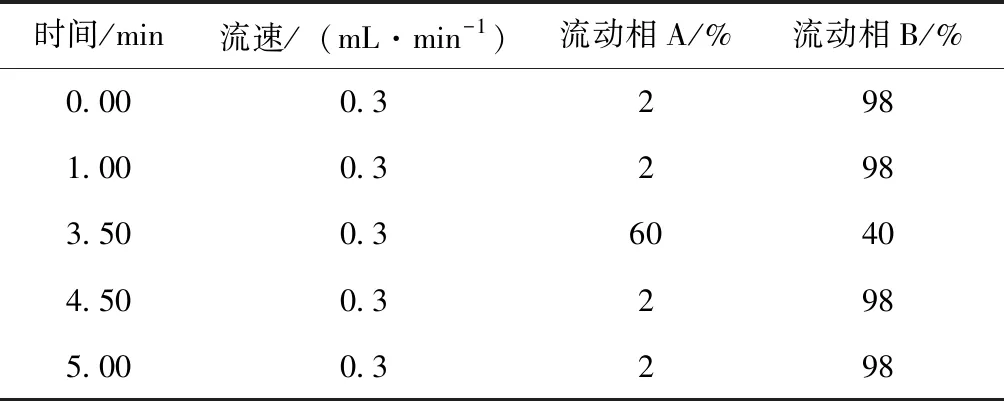
表1 梯度洗脱程序
1.6.2 质谱参考条件
离子源:电喷雾ESI+离子源;检测方式:MRM质谱多反应监测信号采集;毛细管电离电压:3.00 kV;离子源温度:150 ℃;雾化温度;450 ℃;锥孔气流速:150 L/h;雾化气流速:800 L/h。待测药物及同位素内标定性/定量离子对、锥孔电压及碰撞能量的参考值见表2。
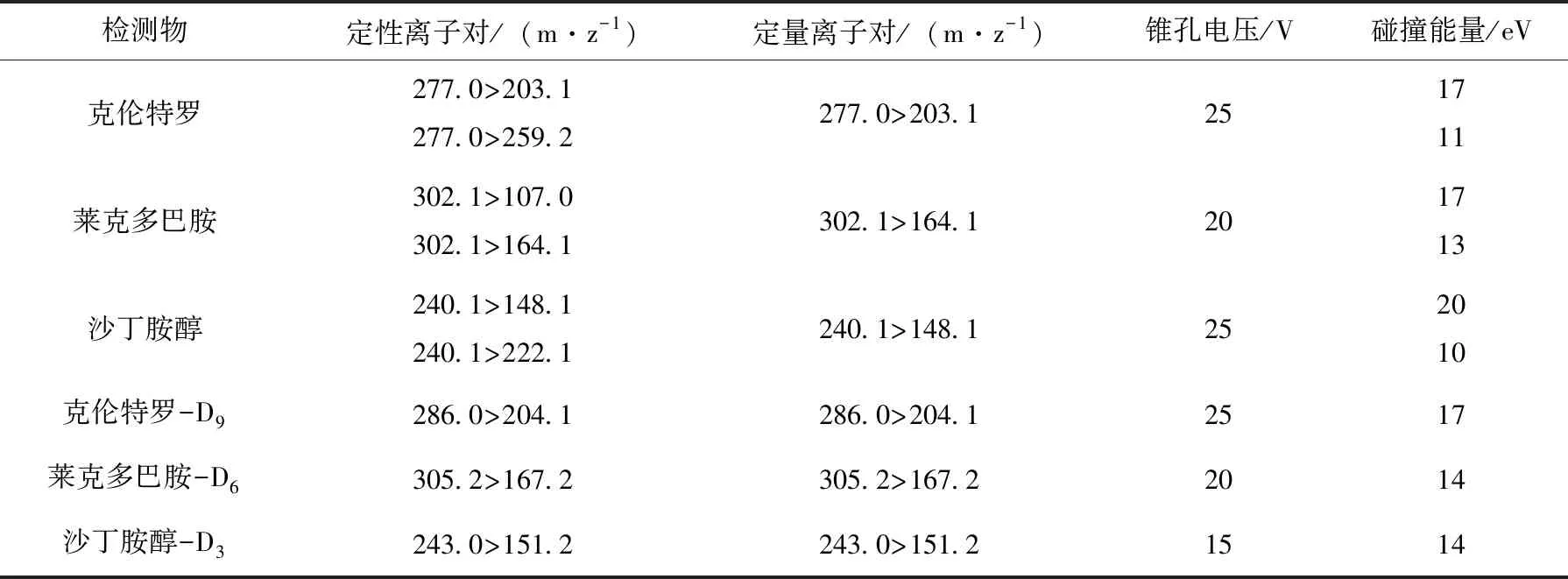
表2 药物及同位素内标定性定量离子对、锥孔电压及碰撞能量
1.7 标准曲线的制备
精密量取混合标准工作液、混合内标工作液适量,用流动相稀释成浓度为0.1、1、5、10、50和100 ng/mL的系列标准工作液(含内标溶液均为5.00 ng/mL),供液相色谱-串联质谱仪测定。以待测分析物特征离子质量色谱峰的峰面积与内标物特征离子质量色谱峰的峰面积比值为纵坐标,相应的浓度为横坐标,绘制标准曲线,求回归方程和相关系数。
1.8 灵敏度
参照文献[9-11]中关于方法学考察的操作,采用空白基质中添加目标化合物的方法,依据特征离子质量色谱峰信噪比S/N≥3的浓度为方法的检出限,S/N≥10的浓度为方法的定量限,在0.5 g空白试样中添加适量标准混合溶液,制备得到添加样品,经前处理过程后上机检测,在相应的保留时间,空白试样对所测的药物无干扰,以评价方法的灵敏度。
1.9 准确度和精密度
参照文献[9-10],采用标准添加法,分别准确称取空白样品0.5 g,添加一定体积的标准工作溶液,使牛羊毛中β-受体激动剂类药物浓度分别为1、20和100 μg/kg,按上述样品前处理方法处理后进行测定,每个添加浓度设6个平行,重复测定3 d,内标法定量,计算待测药物的回收率和计算批内、批间相对标准偏差以评价方法的准确度和精密度。
1.10 基质效应
基质(样品组织)对待测分析物的检测过程一般都会有干扰,会对待测分析物的离子化有很大的影响,并在一定程度上影响结果的准确性。采用基质(牛羊毛发)添加标准品方法添加,用目标物的相对响应值来考察基质效应(ME),计算公式:ME=(空白样品基质中添加同等含量目标分析物的响应值/在纯溶剂中目标分析物的响应值)×100%。若ME<100%,则基质呈现抑制效应;若ME>100%,则基质呈现增强效应[11];若ME=100%,则不存在基质效应。参照“1.5”方法进行试样制备操作,配制1、10、100 μg/L 3个添加浓度的空白样品标准溶液与对应浓度的溶剂标准溶液,通过目标分析物响应值的比较,计算ME值。
2 结果与分析
2.1 标准曲线
由表3可以看出,在0.1~100 ng/mL的浓度范围内3种待测药物呈现出良好的线性相关性,且相关系数R2均大于0.995。
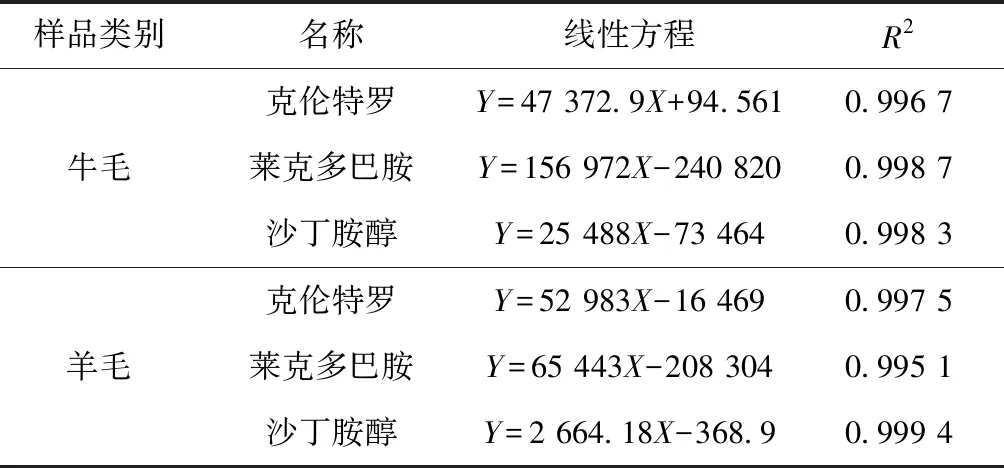
表3 牛羊毛发基质线性标准曲线方程及相关系数
2.2 方法的灵敏度
在对应的保留时间内,空白试样中基质对待测药物无明显干扰,响应强,峰型好,母离子和子离子完全匹配。当牛羊毛发中3种药物添加量为0.2 μg/kg时,信噪比S/N大于3;添加量为0.5 μg/kg时,信噪比S/N大于10。3种药物的检测限(LOD)为0.2 μg/kg,定量限(LOQ)为0.5 μg/kg。10 μg/kg的3种β-受体激动剂的标准溶液离子色谱见图1。牛毛空白样品和加标样品(添加量为10 μg/kg)离子色谱见图2。羊毛空白样品和加标样品(添加量为10 μg/kg)离子色谱见图3。

图1 10 μg/kg的3种β-受体激动剂的标准溶液离子色谱
2.3 方法的准确度和精密度
由表4可见,在3个添加浓度下,牛毛中3种药物的批内和批间回收率范围为 80.2%~110.0%;批内变异系数为1.23%~8.00%,批间变异系数为2.13%~10.10%。羊毛中3种药物的批内和批间回收率范围为79.3%~105.0%;批内变异系数为2.04%~7.80%,批间变异系数为3.31%~12.60%。该方法稳定性和重现性好,回收率高,精密度符合残留检测的基本要求。
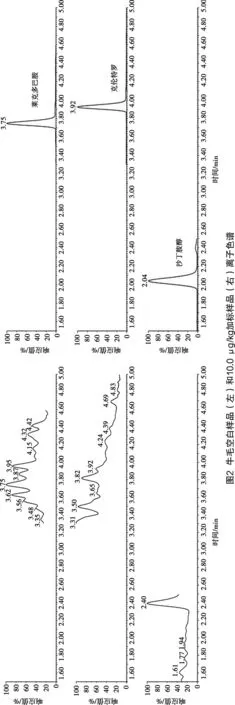
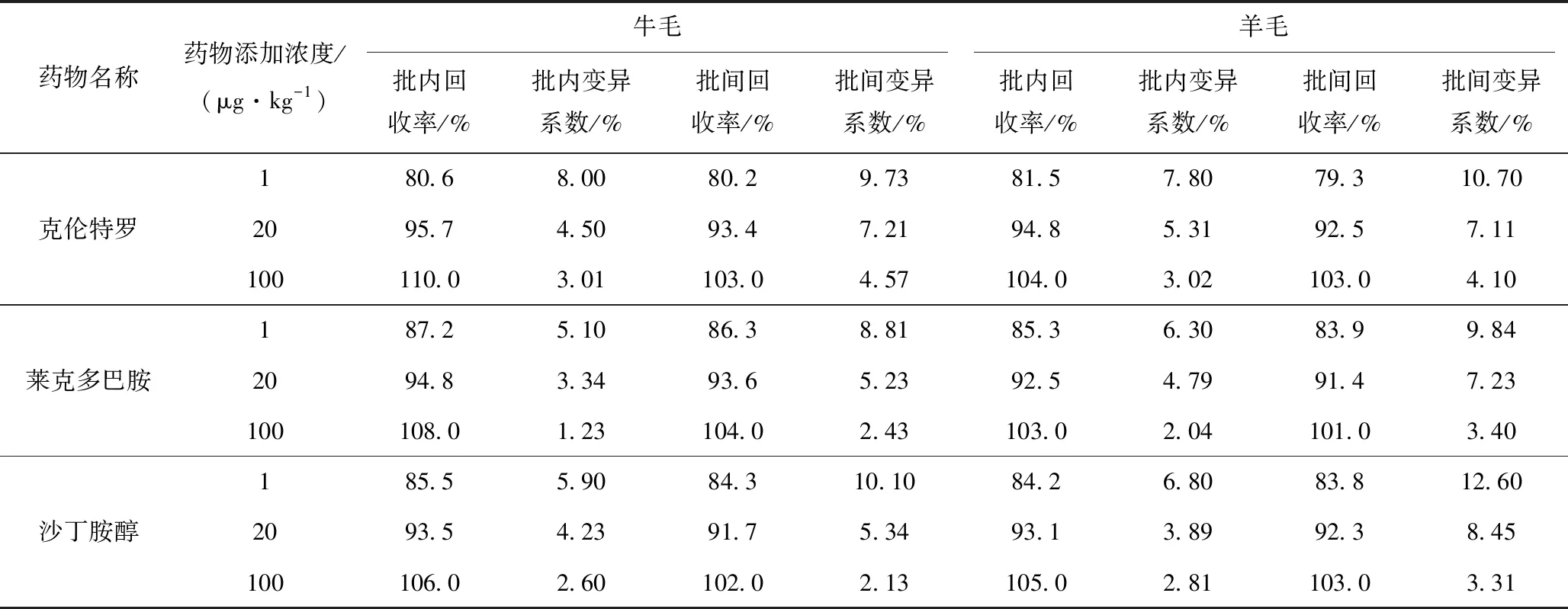
表4 牛羊毛发基质添加回收率和变异系数试验结果
2.4 基质效应
按公式计算,克伦特罗、莱克多巴胺、沙丁胺醇的ME平均值分别为 74.8%、65.7%、71.2%,证明牛羊毛发对3种β-受体激动剂存在基质抑制效应。基质抑制效应很强,选则添加内标物消除基质抑制效应,有助于提高检测的回收率。
3 讨论
本研究中牛羊毛发样品的处理,使用十二烷基磺酸钠清洗剂可以在保证毛发清理彻底的前提下,去除毛发表面的杂质[2];采用酸水解方式,可以使毛发中的药物充分释放进而提高药物检测的准确性和回收率。使用酸溶液和碱溶液水解对比,结果发现碱溶液水解后,测得药物回收率低,经查阅文献发现,碱溶液虽然能够充分水解毛发,但极易造成药物降解损失,需要调节pH值[12]。本研究采用盐酸溶液提取后回收率明显高,准确度高。
对比了Captiva EMR-Lipid净化柱、QuEChERS净化柱、HLB和MCX固相萃取柱4种快速高效净化方式和常规固相萃取柱方法,结果发现,MCX固相萃取柱回收率稳定,但同等处理条件下,需要试剂种类多,过程繁琐,过柱时间长,回收率明显偏低;使用Captiva EMR-Lipid净化柱和QuEChERS净化柱明显对脂质类物质作用效果明显,无需活化和平衡直接过滤样品,目标药物的准确度和灵敏度高,线性关系好。因此本方法选用Captiva EMR-Lipid作为主要净化物质,该吸附剂技术可以通过尺寸排阻和吸附剂化学两种机制有效捕获脂质,较好地去除脂肪、磷脂和蛋白,获得良好的方法稳定性[13]。针对毛发多是深色的属性,加入石墨化炭黑可以较好地清除毛发颜色,便于观察,同时有利于保护仪器。
待测分析物的成分影响离子化的效率容易导致质谱分析中出现基质效应,因此,对色谱分离条件进行合理的优化,使待测目标物和干扰物有效分离,可以在一定程度上有效改善基质效应对测定结果的影响[14]。流动相的pH值变化可影响物质的保留时间,而且影响电离程度,本研究发现延长梯度时长,可改善基质效应的影响,待测物分离度好,保留时间居中,灵敏度高。
色谱柱的选择也会对分离效果产生影响,同样会产生不同的基质效应,本研究对比使用BEH C18100 mm的长色谱柱与50 mm的短色谱柱,结果发现100 mm的长色谱柱可以有效延长待测药物的保留时间,峰型尖锐,但实验室应用短色谱柱也可以收获足够稳定的回收率和高灵敏度,同时极大程度上节省了检测时间,因此选用BEH C1850 mm的短色谱柱。
质谱条件的设置会影响方法的灵敏度。在仪器条件和方法合理的情况下,选择合适的离子源,也可以消除基质效应的影响。本研究选择ESI离子源模式,优化质谱参数,结合分子式结构和电喷雾信号强度,最终选择ESI+扫描模式。
关于牛羊毛发中β-受体激动剂类的检测方法鲜有报道,仅有部分应用于法医学检测人毛发中药物残留的方法[15-16]。闵佳玲等[3]的方法中,前处理采用常规的固相萃取柱操作复杂,耗时长,灵敏度不够;Zhang 等[17]的方法中,适用组织和检测药物种类范围有限,灵敏度低;Font等[18]的方法中,采用碱水解方式易造成药物损失,检测结果准确性不高。无论是尿液、血液还是可食性组织,在动物停药一段时间后,由于新陈代谢,兽药残留量会低于检测方法的检出限,导致无法检出,成为了不法养殖逃避监管的漏洞[19]。本研究中的方法与现有的检测动物产品的国家标准方法进行对比[20],前处理过程操作简单、回收率高,灵敏度相当,完全满足检测需求,重要的是牛羊毛发是易于采集、转运、贮存和提取的样本,采集毛发样品是非破坏性的,不会引起动物的任何伤害和疼痛,监测期长,可有效控制养殖屠宰上市全过程的药物残留状况,而且本研究中应用的Captiva EMR-Lipid吸附技术可以通过尺寸排阻和吸附剂化学两种机制有效捕获脂质,较好地去除脂肪、磷脂和蛋白,获得良好的方法回收率和稳定性[21]。
同位素内标法和基质匹配标准曲线法是基质效应消除的常见方法,因此本方法研究选择这两种方法进行对比。选择样品中一定量的纯物质作为对照物加入待测的样品中,然后对比待测物和标准对照物的色谱信号响应值,对待测物含量进行测定的方法称为内标法[22]。内标法能够在很大程度上消除试验条件变化而产生的误差,确保方法精密度和准确度[23]。当样品的基质复杂时,可以采用此方法,但内标物价格比较高且不容易获得,不适合大批量操作,但能收获高而稳定的回收率。基质标准溶液校正也可以消除基质效应的干扰,通过比较本研究中内标法收到了满意的结果。
4 结论
本研究建立了一种以牛羊毛发为靶组织结合EMR-Lipid技术检测β-受体激动剂药物残留的高效检测方法。该方法打破了传统以动物可食用组织作为残留检测靶组织的常规思路,选取更能稳定长期存在并不需要破坏活体的毛发作为靶组织,前处理方法操作简便,无需经过液-液萃取,采用强化除杂质技术,回收率稳定,灵敏度和准确度高。本方法对牛和羊毛发中兴奋剂类药物的检测限为0.2 μg/kg,定量限为0.5 μg/kg,在0.1~100 ng/mL添加浓度范围有良好的线性拟合关系,R2≥0.995。综上,该方法具有样品易获取、灵敏度高、精密度好等特点,为牛羊毛发中β-受体激动剂类药物的筛查与定量检测提供了参考,便于开展日常检测和保障监测。

