流行性乙型脑炎高免阳性血清的制备与应用
李 翠,王 兆,2,王德丽,高月异,沈青春,高金源
(1.中国兽医药品监察所,北京 100081;2.山东第一医科大学,山东济南 250117)
流行性乙型脑炎(Japanese encephalitis,JE)简称乙脑,是由黄病毒科黄病毒属的乙型脑炎病毒(Japanese encephalitis virus,JEV)感染引起的一种以蚊虫为传播媒介的人兽共患传染病,对人类危害极大。猪是JEV 传播的中间宿主,为该病的主要传染源。JEV 可引起猪的严重繁殖障碍,给养猪业带来了严重威胁[1]。精准高效的JE 诊断技术[2]及疫苗免疫等是该病防治的关键。JEV 仅有1 个血清型,但在使用血清学方法进行检测时,与其同属的西尼罗病毒会出现交叉反应,对诊断结果判定造成了干扰[3-4]。JE 诊断技术研发和疫苗质量控制都需要标准阳性血清[5-6]。目前,已报道制备的JEV阳性血清多为鼠源、人源[7],血清效价偏低,制备数量也受到限制,无法满足相关疫苗检验、研究的需求。综合考虑阳性血清的纯净性和特异性要求,JE 活疫苗对不同动物的安全性及免疫效力[8-9]以及前人经验[7,10],本研究选用SPF 鸡作为试验动物,以JE 活疫苗和灭活疫苗为免疫原,制备了纯净性、特异性好,中和效价较高的JE 阳性血清,可满足JE 活疫苗的鉴别检验和外源病毒检验[11]需求。
1 材料与方法
1.1 材料
1.1.1 试验动物 30~35日龄SPF 鸡15 只,购自北京维通利华实验动物技术有限公司。
1.1.2 免疫原及相关材料 JE 灭活疫苗(P3 株),购自上海生物制品研究所;猪JE 活疫苗(SA14-14-2株),购自武汉科前生物股份有限公司;BHK21细胞和地鼠肾原代细胞,由中国兽医药品监察所提供;安瓿瓶,购自中海生物科技有限公司。
1.1.3 特异性试验所需病毒 口蹄疫病毒(FMDV)、猪圆环病毒(PCV)、伪狂犬病病毒(PRV)、猪瘟病毒(CSFV)、猪繁殖与呼吸综合征病毒(PRRSV)、猪细小病毒(PPV)和牛病毒性腹泻病毒(BVDV),均来自中国兽医药品监察所。
1.2 免疫程序
选取30~35日龄SPF 鸡15 只,以猪JE 活疫苗(SA14-14-2 株)和JE 灭活疫苗(P3 株)分别作为免疫原对其进行免疫。免疫程序:使用稀释为1 mL/头份的猪JE 活疫苗(SA14-14-2 株)进行肌肉注射1 mL/只,首次免疫后14 d 以相同剂量进行第2 次免疫;第2 次免疫后7 d,使用稀释为1 mL/头份的JE 灭活疫苗(P3 株)进行肌肉注射1 mL/只(第3 次免疫),间隔7 d 后以相同剂量再次免疫1 次,共免疫4 次,全免疫周期35 d。本试验重复2 次,第1 次使用SPF 鸡8 只,编号分别为1-1—1-8,第2 次使用SPF 鸡7 只,编号分别为2-1—2-7。
1.3 血清抗体检测
首次免疫后,每隔7 d 对SPF 鸡进行翅静脉采血(1 mL/只),将采集的血液以3 000 r/min 离心15 min 收集上层血清。使用噬斑减少中和试验(PRNT)进行血清抗体效价检测。将10 倍系列稀释的被检血清与100 PFU/0.1 mL 的JEV(SA14-14-2 株)等体积混合,然后置于37 ℃水浴中和90 min,间隔30 min 振荡混匀;将中和后的病毒液接种于长满单层BHK21 细胞的24 孔板中,各稀释度接种4 孔,每孔0.1 mL,同时以浓度分别为100 和0.1 PFU/0.1 mL 的病毒液各设置4 个重复作为病毒回归试验;以4 孔不作处理的细胞作为空白对照。将24 孔板置于37 ℃、5% CO2培养箱中吸附90 min,弃去病毒液,以PBS 清洗3 次,然后加入0.5 mL RPMI 1640 培养基(含4%胎牛血清)与2%低熔点琼脂糖等体积混合的培养液,在室温下等待其自然凝固。将凝固后的24 孔板置于37 ℃、5% CO2培养箱中培养3~5 d,加入1%结晶紫染色。对蚀斑进行计数,计算每个血清稀释度的蚀斑减少率,50%蚀斑减少的最大血清稀释度为噬斑减少中和抗体滴度,即为被检血清的抗体效价。
1.4 血液采集与血清分离
免疫程序结束后,当血清抗体效价达到1:1 000以上时,以心脏采血法对试验鸡采集血液至其死亡。将采集的血液以3 000 r/min离心15 min,收集血清。将血清置于-20 ℃及以下冷冻保存备用。
1.5 高免血清检验
免疫结束后,将15 只SPF 鸡的血清样品各取200 µL,每5 份混合共获得3 份混合样品,随后进行纯净性检验、效价测定和特异性检验。若某只试验动物不符合要求,可按照少于5 份混合。混合样品检验后若出现不符合标准结果,需将5 份样品进行单独检验。
1.5.1 纯净性检验 按照《中华人民共和国兽药典》(以下简称《兽药典》)[12]附录3306、3308和3305 进行无菌、支原体及外源病毒检验。上述检验均为阴性表明纯净性检验符合标准。
1.5.2 效价测定 以PRNT 进行检测,结果不低于1:1 000 表明符合效价测定标准。
1.5.3 特异性检验 以《兽药典》附录3406 中和试验分别检测FMDV、PCV、PRV、CSFV、PRRSV、PPV 和BVDV 抗体。上述检验均为阴性表明特异性检验符合标准。
1.6 分装冻干
将检验合格的高免血清混合均匀,在无菌条件下以瓶顶分装器定量分装至安瓿瓶中,每支装量1 mL,共200 只。冷冻干燥后抽真空熔封。
1.7 冻干高免血清检验
1.7.1 真空度测定和剩余水分测定 按《兽药典》附录3103 和3204 进行,结果应符合规定。
1.7.2 纯净性检验、特异性检验和效价测定 按《兽药典》附录3306、3308、3305 和3406 进行无菌、支原体、外源病毒检验和特异性检验;以PRNT 进行效价检测,所有检测应符合规定。
1.7.3 均匀性检验 随机选取10 支冻干血清,采用PRNT 进行效价测定,然后以方差分析法分析样品均匀性[13]。通过比较组间和组内方差来判断各组测量值之间是否存在系统性差异,如果两者的比值小于统计检验的临界值,则认为样品均匀。
1.8 应用
按照《兽药典》附录猪JE 活疫苗中鉴别检验项和外源病毒检验项,以本研究制备的阳性血清进行猪JE 活疫苗(SA14-14-2 株)的鉴别检验和外源病毒检验。
2 结果
2.1 血清制备及抗体检测
对两次试验每次免疫后采集的SPF 鸡血液分离血清,使用PRNT 检测不同免疫时期抗体效价。结果(表1~2)显示,免疫周期结束后,仅编号为1-2 的鸡血清效价低于1:1 000,其余鸡血清效价均满足试验要求。
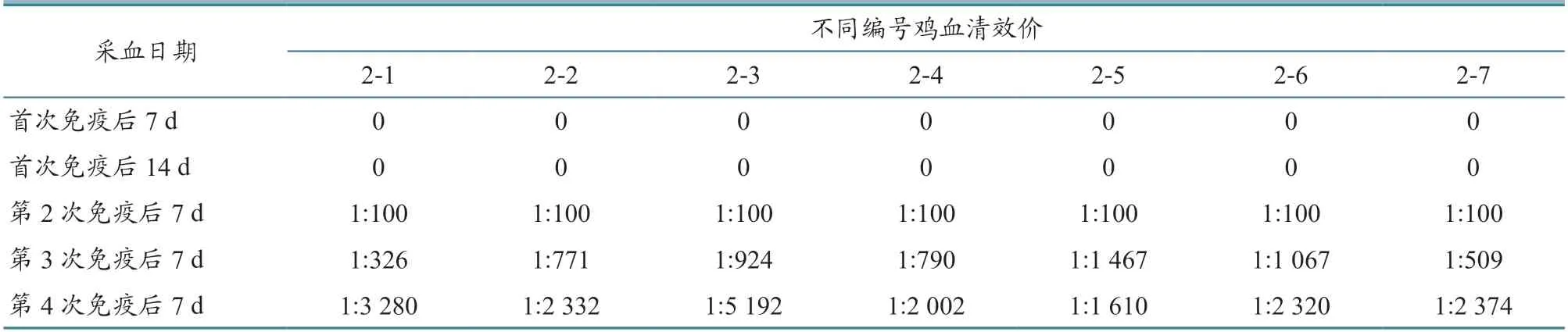
表2 第2 次试验血清抗体水平检测结果
2.2 高免血清检验
2.2.1 纯净性检验 将准备的3 份血清混合样品进行无菌、支原体及外源病毒检验,结果均为阴性,符合规定。
2.2.2 特异性检验 将准备的3 份血清混合样品进行FMDV、PCV、PRV、CSFV、PRRSV、PPV和BVDV 抗体检测,结果均为阴性,符合规定。
2.2.3 效价测定 将准备的3 份血清混合样品分别进行PRNT,发现其血清效价分别为1:3 320、1:5 192、1:2 309,符合规定。
2.3 冻干血清检验
2.3.1 纯净性检验 随机选取5 支冻干血清进行无菌、支原体以及外源病毒检验,结果均为阴性,符合规定。
2.3.2 效价测定 随机抽取10 支冻干血清,以1 mL 灭菌生理盐水复溶后,测定噬斑减少中和效价,发现所有结果均大于1:1 000(表3)。
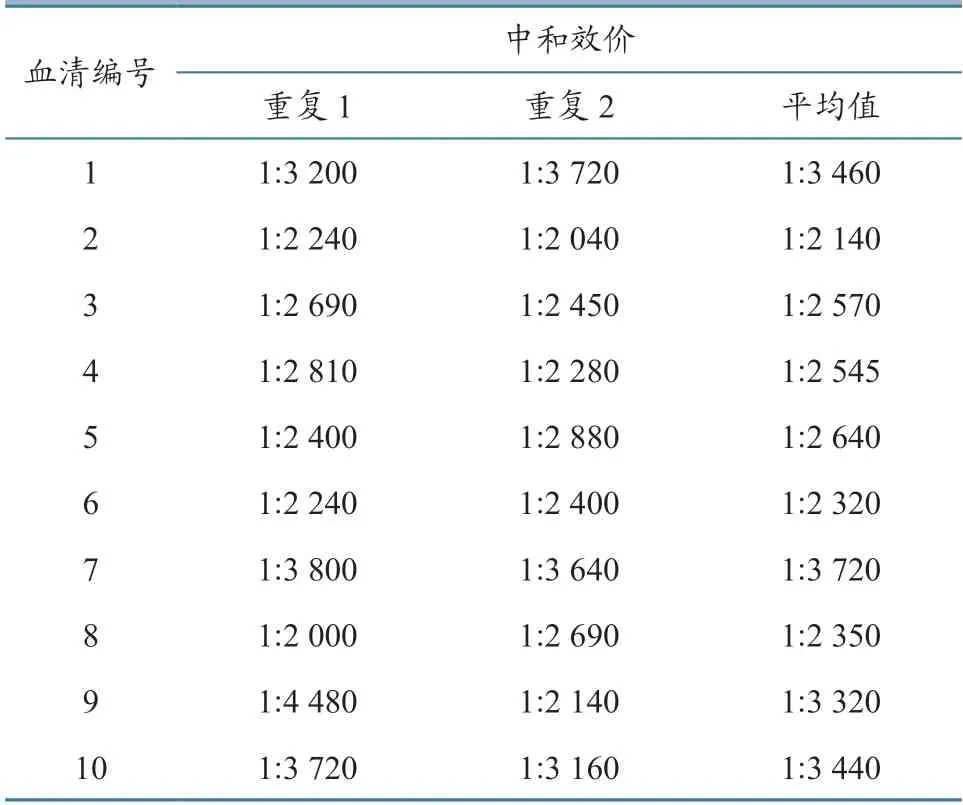
表3 冻干阳性血清噬斑减少中和效价测定结果
2.3.3 特异性检验 随机抽取10 支冻干血清,以1 mL 灭菌生理盐水复溶后,进行FMDV、PCV、PRV、CSFV、PRRSV、PPV 和BVDV 抗体检测,所有结果均为阴性,符合规定。
2.3.4 剩余水分测定 按《兽药典》附录3204剩余水分测定法进行,发现剩余水分含量分别为0.9%、1.2%、0.9%、0.8%,均<3%,结果符合规定。
2.3.5 真空度测定 按《兽药典》附录3103 真空度测定法进行,结果均符合规定。
2.3.6 均匀性检验 采用方差分析法统计2.3.2 中10 个样品的效价测定结果。经检验,10 个样品组内、组间均无明显差异(P<0.05),样品是均匀的。
2.4 应用
2.4.1 鉴别检验 结果显示,本研究制备的JEV特异性阳性血清按1:100 稀释后,能够完全中和500 PFU/mL 的JEV(SA14-14-2 株)。
2.4.2 外源病毒检验 将冻干血清应用于3 批JE活疫苗(SA14-14-2 株)的外源病毒检验,检测结果见表4。结果显示,1 mL 血清能完全中和10 头份病毒含量为107.0TCID50/头份的疫苗样品。

表4 3 批JE 活疫苗外源病毒检验结果
3 讨论
按照《兽药典》猪JE 活疫苗标准,鉴别检验项和外源病毒检验项需要纯净性好、中和效价高的JEV 特异性血清。本研究以SPF 鸡作为免疫动物,优化了免疫程序,以JE 活疫苗进行基础免疫后,再以JE 灭活疫苗协同免疫,最终获得了中和效价大于1:1 000 的JEV 阳性血清。SPF 鸡不含猪源病原体,将其用于制备猪用活疫苗外源病毒检验用的阳性血清,在纯净性上容易控制,可更好地保证阳性血清具有良好的特异性。此外,本研究中免疫原为商品化JE 灭活疫苗和活疫苗,没有使用JEV 强毒,降低了生物安全风险;免疫程序共为4 次,简便易行,适合大规模血清制备。特异性好且中和效价高的JEV 阳性血清的制备,完善了JE 活疫苗的检验工作。
按《兽药典》附录3305 外源病毒检验法,非禽源活疫苗按瓶签注明头份稀释至每1.0 mL 至少含10 头份,再用等体积的特异性血清中和后作为检品进行外源病毒检验。参照《兽药典》猪JE 活疫苗标准,每头份病毒含量应不低于105.7TCID50。在实际生产中,猪JE 活疫苗的病毒含量可达到107.0TCID50/头份,这对用于外源病毒检验的阳性血清中和效价要求更高。为确保外源病毒检验可操作,在实际生产检验中需考虑阳性血清效价能否满足活疫苗中病毒的完全中和。本研究中,制备的JEV 血清能等体积完全中和10 头份病毒含量为107.0TCID50/头份的疫苗样品,表明制备的血清中和效价高,应用性良好,可满足JE 活疫苗的检验需求。

