魔芋葡甘聚糖-尼莫地平药膜体外释放性能的初步探讨
江贵林,陈文平,汪 超,2*,吕文平,陈士勇,姜发堂,2
1湖北工业大学生物工程学院,武汉 430068;2武汉力诚生物科技有限公司,武汉 430068
魔芋葡甘聚糖-尼莫地平药膜体外释放性能的初步探讨
江贵林1,陈文平1,汪 超1,2*,吕文平1,陈士勇1,姜发堂1,2
1湖北工业大学生物工程学院,武汉 430068;2武汉力诚生物科技有限公司,武汉 430068
本文选用尼莫地平(nimodipine,NMP)作为模型药物,以魔芋葡甘聚糖 (Konjac glucomannan,KG M)为材料制备 KG M-NMP药膜,对其在体外不同介质和不同温度下的释药特性进行考察,初步探讨魔芋葡甘聚糖-尼莫地平药膜的体外释放性能。采用扫描电子显微镜观察药膜各个释放阶段的形态及表面结构,药膜呈胶束状,表面平整光滑,个别表面有凹凸状;用药物释放动力学方程拟合药物释放数据曲线,推导建立数学模型,同时结合电镜扫描结果分析,KG M-NMP药膜的溶蚀特性更符合零级动力学方程,释放机制为扩散和骨架溶蚀的协同作用。该药膜在体外具有明显的缓控释作用,24 h内释药稳定。
魔芋葡甘聚糖;尼莫地平;体外药物释放
随着安全、环保意识的提高,天然高分子材料中又因特殊宗教信仰和素食饮食原则需回避动物性的蛋白质(如明胶),多糖现已逐渐成为重要的研究对象。魔芋葡甘聚糖(konjac glucomannan,KG M)作为一种优良的食用亲水胶体,是由D-葡萄糖和D-甘露糖以 1:1.6通过β-1,4糖苷键连接的杂多糖,其水合能力强,不带电荷,易于成膜和凝胶[1]。近年来,在药物制剂中利用 KG M-硼凝胶体[2]和 KG M-其它多糖共混体系作为释放载体的研究逐年递增,KG M已成为开发新型高分子辅料的重要成员之一[3-5]。
尼莫地平是第二代二氢吡啶类钙拮抗剂,临床上广泛应用于脑血管疾病的预防和治疗。NMP水溶性差,体内生物利用度低,半衰期短 (约为 1.5~2 h),1 d内需给药 3~4次,而且光稳定性差[6]。口服制剂首过效应大,生物利用度低,血药浓度波动大[7]。将NMP制成固体分散体可以提高生物利用度,但不能减少服用次数和血药浓度波动[8]。制成注射剂,由于NMP的水不溶性需添加大量乙醇 (>20%),存在给药不方便的缺点[9]。
本实验根据尼莫地平的特点,以魔芋葡甘聚糖为释放基材,研制了 KG M-NMP药膜,并对其体外释放特性进行了初步研究,以期为该药膜的完善提供依据。
1 仪器与材料
1.1 原料与试剂
魔芋精粉,花魔芋 (特级),湖北星宇魔芋产业发展有限公司;尼莫地平,批号 H19999225,武汉远程生物科技有限公司;其余试剂均为国产分析纯。
1.2 仪器设备
紫外分光光度计,UV-3010(日本 H ITACH I);实验室悬臂式搅拌器,EUROSTAR(德国 IKA);溶出度仪 (Dissolution),2100C(美国 D ITEK);扫描电子显微镜(SEM),JS M-6390LV(日本 JEOL)。
2 实验方法
2.1 方法可行性实验
精密称取干燥至恒重的尼莫地平 50 mg,乙醇溶解定容 1000 mL配制尼莫地平溶液 (a)。同时按照药膜制备中的添加比例配制不含 NMP的辅料KG M-DMSO-乙醇溶液(b)。以蒸馏水为空白在 200~400 nm波长范围内扫描。结果,尼莫地平在波长237 nm处有最大吸收峰,但辅料在此处有干扰;尼莫地平在波长 358 nm处有次吸收峰,且辅料在此处无干扰,故选择 358 nm作为尼莫地平含量的测定波长。
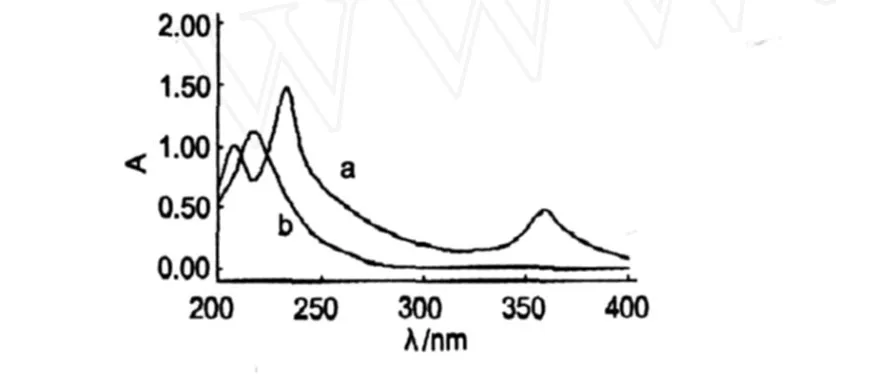
图 1 尼莫地平与辅料在乙醇中的紫外吸收Fig.1 UV absorption spectra of nimodipine and adjuvant in ethanol
2.2 KG M-NMP药膜的制备
参照李斌的方法制备 KG M[10]。准确称取定量魔芋精粉于固定蒸馏水中,在 70℃水浴条件下搅拌使之充分溶胀,形成 3.0%(w/v)凝胶。精确称取50.0 mg NMP溶于定量的DMSO,混入溶胀的水溶胶中充分搅拌混合。取出后在 4℃恒温恒湿箱中静置设定时间,脱气,干燥成膜保存于干燥器中。
2.3 含量测定实验
2.3.1 含量标准曲线
精确称取尼莫地平 100 mg,乙醇溶解定容至1000 mL。分别精密吸取适量用以乙醇稀释成浓度为 l0、20、30、40、50、60、70μg/mL的系列标准溶液,以乙醇作空白对照,在 358 nm波长处测定吸收值。将吸收度A对浓度 C(μg/mL)进行线性回归,得标准曲线方程:
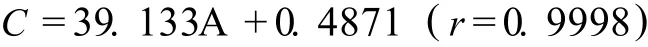
2.3.2 含量测定
取 KG M-NMP药膜 10片,精密称重并研细,置1000 mL容量瓶中,加乙醇溶解定容、摇匀、过滤,于波长 358 nm处测紫外吸收值,代入回归方程计算NMP浓度。药膜的NMP含量可由下式计算:

2.4 体外释放实验
2.4.1 缓冲溶液的配制
模拟胃液:Ph 1.2盐酸液,0.1 mol/L盐酸 9 mL,蒸馏水稀释至 1000 mL,摇匀即得。模拟小肠液:pH 6.8磷酸盐缓冲液,0.2 mol/L磷酸二氢钾溶液 250 mL,加 0.2 mol/L氢氧化钠溶液 118 mL,蒸馏水稀释至 1000 mL,摇匀即得。模拟结肠液:pH 7.4磷酸盐缓冲液,磷酸二氢钾 6.8 g,加 0.1 mol/L氢氧化钠溶液 395 mL,蒸馏水稀释至 1000 mL,摇匀即得[11]。
2.4.2 释放度标准曲线
精密称取尼莫地平 50 mg,乙醇溶解,然后用模拟胃液(小肠液/结肠液),定容至 500 mL棕色容量瓶中,分别精密吸取适量,以模拟胃液 (小肠液/结肠液)稀释成浓度为 l0、20、30、40、50、60、70μg/mL的系列标准溶液,以模拟胃液 (小肠液/结肠液)作空白对照,在 358 nm波长处测定吸收值。将吸收度(A)对浓度 C(μg/mL)进行线性回归,得标准曲线方程:

2.4.3 体外释放
取 KG M-NMP药膜,按照《中国药典》2005第二版的方法,采用桨法进行体外释放实验,搅拌速度(50±1)r/min,介质体积 900 mL。通过更换介质模拟人体胃肠道中 pH值的连续变化,药膜在模拟胃液中释药 2 h,模拟小肠液中释药 10 h,模拟结肠液中释药 12 h。在规定时间取样 5 mL,并及时补充所消耗的介质。样液在 358 nm下测定紫外吸收值,然后根据释放度标准曲线方程计算释放的NMP浓度。
2.5 体外溶蚀实验
取 KG M-NMP药膜3片,称重后在 37℃下进行体外释放,每间隔一段时间,将膜片取出,用蒸馏水清洗,然后放入干燥器中室温下干燥称重。质量损失百分比是通过比较间隔一定时间后的样品质量和初始样品质量的比率计算出来的。用导电胶将聚合物膜片的断面固定在铜片上,真空喷金后在扫描电子显微镜下观察不同释放阶段膜片表面结构的变化。
3 实验结果与分析
3.1 物理特性
该膜为白色半透明状,均匀有韧性,厚度约 1 mm,呈弱酸性(pH≈5),具有较好的吸湿性、柔韧性和抗拉性。
3.2 NMP含量测定结果
KG M-NMP药膜 10片,测定并计算,结果分别为 98.46%、97.30%、98.64%、99.32%、98.62%、97.95%、98.77%、97.26%、98.56%、98.23%。平均含药量为为 98.31%,表明按此工艺制得的 KG MNMP药膜含量均匀性较好。
3.3 KG M-NMP药膜体外释放结果
3.3.1 不同释放阶段的释放度考察
由于尼莫地平的水溶性差,在释放介质中加入0.55%的十二烷基硫酸钠溶液[12],可改善 NMP在释放介质中的浸润状态,增加其溶解度,从而更好地模拟NMP在体内的真实情况。
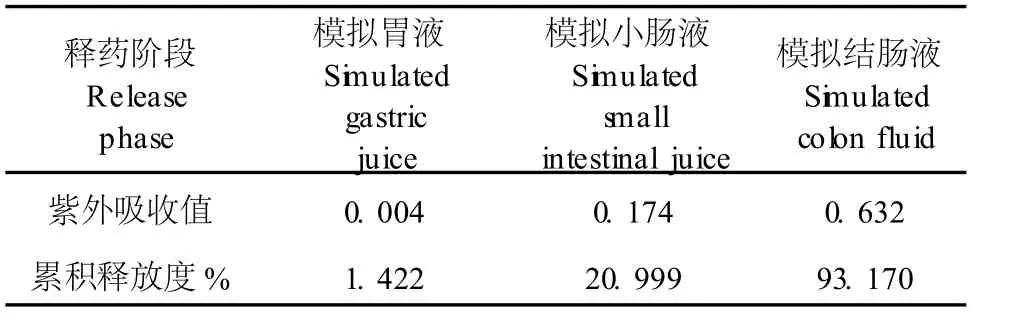
表1 KG M-NMP药膜在不同pH条件下的释放Table 1 Release of KG M-NMP membrane in differentmedia at 37℃
由表可知,NMP在模拟胃液中几乎不释放,减轻了药物释放导致的恶心反应,同时还起到了掩味和增强患者顺应性的作用;在模拟小肠液中有一部分释放,而在模拟结肠液中几乎完全释放。KG M是一种 pH敏感性多糖,3种释放介质的 pH存在差异,直接影响了 KG M在释放系统中的溶胀促发时间和溶蚀程度,因而在 pH值更高的模拟结肠液中其溶蚀度也更高。KG M作为天然多糖,人体内胃、小肠缺乏相应的酶而不能将其降解,而结肠有许多独特的细菌,产生的β-糖苷酶可将 KG M降解,从而达到结肠定位释放的目的,因而此药膜将会有更好的体内释放效果。
3.3.2 不同释放温度的累积释放度考察
人体的正常体温是 35.5~37.7℃,但人体存在低温或发热的情况,下图是人体自身温度极限范围内NMP的释放情况。通过考察不同温度下NMP在pH连续变化介质中的释放情况,可以作为临床上对不同年龄阶段和身体状况的患者采取相应给药方式的依据,从而使病患得到更加有效的控制及治疗;同时对治疗患者低温或发热的给药也提供了依据。
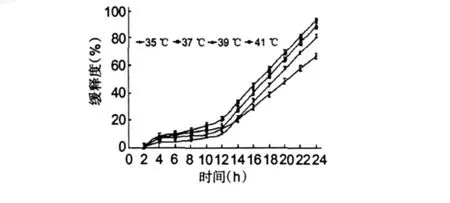
图 2 KG M-NMP药膜在不同温度条件下的累积释放曲线Fig.2 Release of KG M-NMP membrane at different temperature
采用不同药物释放模型方程对以上曲线进行拟合,结果显示NMP在不同温度的各阶段药物释放接近零级释放,在每个阶段内药物的释放不受时间的影响。口服后将以零级释药速率释药至少 24 h以上,体内血药浓度相对稳定,这使药物的治疗效应最大化,同时也使超过治疗的药物浓度产生的毒副作用减小。
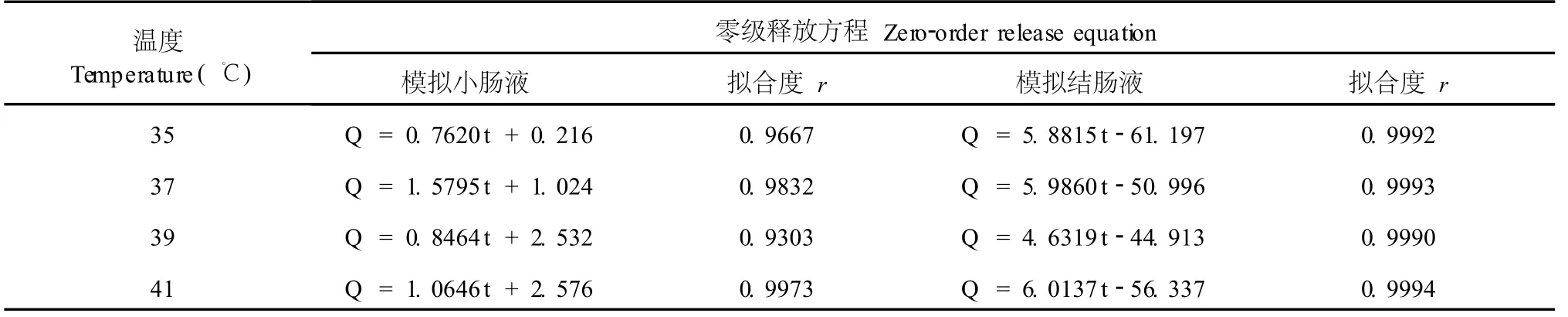
表 2 KG M-NMP药膜不同释放阶段的零级释药模型拟合方程Table 2 Zero-order release kinetics of KG M-NMP membrane

图 3 扫描电镜结果Fig.3 Membrane were characterized by scanning electron microscopy
3.4 体外溶蚀状态
由上图可知,①为制备的干燥 KG M-NMP药膜,呈胶束状,表面平整光滑,个别表面有凹凸,NMP微粒均匀分散在其中;②为在模拟胃液中释放 2 h后的药膜,在此过程中 KG M表面润湿形成凝胶层,表面NMP向模拟胃液扩散;③为在模拟小肠液中释放10h后的药膜,在此过程中 KG M凝胶层继续水化溶胀,凝胶层增厚延缓NMP释放,溶胀到一定阶段开始溶蚀;④KG M凝胶层继续溶蚀,直到NMP完全扩散到模拟结肠液中,更进一步说明了其结肠定位释放特性。
4 结论
本实验通过更换介质模拟人体胃肠道中的 pH值连续变化,考察 KG M-NMP药膜在不同温度下的释放特性,结果表明 KG M作为释放载体具有良好的控制释放作用,取得了在结肠中定位释放的效果。KG M-NMP药膜的释药依赖 pH和时滞性也存在一定的缺点,将其制成靶向性更高的释放系统,提高释放的确定性和稳定性,这有待进一步研究。
1 Liu HX(刘红霞).Application of biodegradable polymeric materials in medicine.Heilongjiang M ed J(黑龙江医药), 2004,17:371-373.
2 Gao YX(高玉香),Yan YH(阎玉华),et al.Application of biodegradable polymeric materials as release carriers.Sci Tech Overseas Building M at(国外建材科技),2005,26 (5):20-23.
3 Wang YP(王玉鹏),Zhao LH(赵丽华).Application of the matrix materials in pharmaceutics.China Phar m(中国药房),2007,18:1987-1988.
4 Karim AA,Chang YP,Norziah MH,et al.Exothermic events on heating of semi-dilu.te konjac glucomannan-water systems.Carbohydrate Polymers,2005,61:368-373.
5 LiB(李斌),Wang C(汪超),Sun HC(孙寒潮).Investigation of sustained release property of KG M-Borate composite gel to salicylic acid.Southwest Agric Univ(西南农业大学学报),2003,(6):487-490.
6 Brooks SP,CroftAP,Norman G,et al.Little.Nimodipine prior to alcoholwithdrawal prevents memory deficits during the abstinence phase.Neuroscience,2008,157:376-384.
7 Qiu F,Chen XY,Li XY,et al.Determination of nimodipine in human plas ma by a sensitive and selective liquid chromatography– tandem mass spectrometry method.Journal of Chromatography B,2004,802:291-297.
8 Sun YZ,Yang R,ZhouWL,et al.N imodipine semi-solid capsules containing solid dispersion for improving dissolution international.Journal of Phar maceutics,2008,359(1-2):144-149.
9 Laslo AM,Eastwood JD,UrquhartB,et al.Subcutaneous administration of nimodipine improves bioavailability in rabbits.Journal of NeuroscienceM ethods,2004,139:195-201.
10 LiB(李斌),Wang C(汪超),Wu LZ(吴良志).Investigation of swelling-dissolving property of KG M-borate composite gel.Food Sci Tech(食品科技),2003,7:3-6.
11 Ch P(section 1),2005(《中国药典》(第一部)05年版). 2005,Appendix(附录):99-100.
12 HossainMM,Suzuki T,Unno T,et al.Differentialpresynaptic actions of pyrethroid insecticides on glutamatergic and GABAergic neurons in the hippocampus.Toxicology,2008, 243:155-163.
In vitroRelease Properties of Konjac Glucomannan-n imodipine M embrane
J IANG Gui-lin1,CHEN Wen-ping1,WANG Chao1,2*,LV Wen-ping1,CHEN Shi-yong1,J IANG Fa-tang1,2
1School of B iological Enginerring,Hubei University of Technology,W uhan 430068,China; 2W uhan Licheng B iotechnology Co.,Ltd.,W uhan 430068,China
Thein vitrorelease propertiesofNMPwere analysised by konjac glucomannanmembrane.In vitrodrug release and erosion condition of themembranewere studied respectively in releasemediawith differentpH and temperature.And the shape and surface of the membrane were characterized by scanning electron microscopy(SEM),which showed that the membrane were s mooth except few membrane with accidented surface.Mathematic models were used to imitate the drug release,which showed that dissolution process ofNMP from hydrophilic matrix confor med to zero-order release kinetics.The cumulative drug release was explained by the co-operation of diffusion and erosion.The KG M-NMP membran possessed sustained release characteristic,and the drugwas released constantly during 24 h.
konjac glucomannan;nimodipine;in vitrorelease profile
R282;Q946.91
A
1001-6880(2010)05-0761-04
2009-05-25 接受日期:2009-07-20
国家高技术研究发展计划(863计划)(批准号:2002AA 2Z4181);武汉市科技局晨光计划(20065004116-52)
*通讯作者 Tel:86-532-88963253;E-mail:wangchao5412@163.com

