高效液相色谱法测定散结止痛颗粒中芍药苷含量
袁继承 沙启营 吕伟斌 袁继鲁
散结止痛颗粒(批准文号:鲁药制字再Z17080034)是菏泽市中医医院一种主治各种乳腺增生的中药制剂,具有理气活血、散结止痛的功效,适用于治疗气滞血瘀痰凝而致的乳房胀痛、乳肿结块等各种类型的乳腺增生疾病。该医院制剂已使用多年,临床疗效好,具有开发上市前景。
散结止痛颗粒全方由香附、赤芍、当归、柴胡等共十六味中药组成,赤芍为本制剂的君药,具有清热凉血、散瘀止痛功效。赤芍总苷具有较强的清除自由基和抗凝血活性[1];其中芍药苷(paeoniflorin)是赤芍总苷的主要活性成分,在总苷中含量占75%以上[2],具有多种生物作用,如抗菌抗炎、调节免疫功能[3-4],所以测定芍药苷含量可以控制该制剂的内在质量。由此建立了测定散结止痛颗粒中芍药苷含量的高效液相色谱法(High Performance Liquid Chromatography,HPLC)。
1 仪器与试药
日本岛津LC-10ATVP液相色谱仪,SPD-10Avp紫外检测器;KQ-250E型医用超声波清洗器(昆山市超声仪器有限公司);Sartorius BP211D电子天平。
芍药苷(批号:110736-200525)购于中国药品生物制品检定所;乙腈为色谱纯;水为纯净水;散结止痛颗粒样品均为菏泽市中医医院制剂科自制。
2 方法与结果
2.1 色谱条件与系统适应性试验[5]
色谱柱:依利特Hypersil ODS2 高效液相色谱柱(4.6×250 mm,5 μm);流动相:乙睛—水(17:83);流速:1.0 ml/min;柱温:室温;检测波长:230 nm;芍药苷的理论塔板数不低于3000。经过多种芍药苷的测定方法实验比较,本方法对芍药苷分离效果好,同时阴性样品无干扰,且洗脱时间短,因此,最终采用上述芍药苷的高效液相色谱条件。
2.2 对照品溶液及标准曲线制备
精密称取芍药苷对照品5.24 mg,置于10 ml容量瓶中,用甲醇溶解并稀释至刻度,即得浓度为0.524 mg/ml的芍药苷对照品储备溶液。取对照品储备溶液2.5 ml,置于5 ml容量瓶中,用甲醇稀释至刻度,摇匀,即得浓度为262.0 mg/ml的芍药苷对照品溶液。
芍药苷标准曲线制备:精密吸取配制的芍药苷对照品储备溶液0.2、0.4、0.6、0.8、1.0、1.5、2 ml,分别置于2 ml容量瓶中,用甲醇稀释至刻度,摇匀,即得系列浓度为52.4、104.8、157.2、209.6、262.0、393.0、524.0 μg/ml的芍药苷对照品溶液,用0.45 μm微孔滤膜滤过,进样10 μl于色谱仪中测定。结果芍药苷浓度在52.4~524 μg/ml范围内与峰面积有良好的线性关系,以峰面积(Y)为纵坐标,浓度(X)为横坐标,进行线性回归,得回归方程:Y=6341.9X+76190,r=0.9999。
2.3 供试品溶液制备
精密称定2.0 g散结止痛颗粒(批号:20100503),用50 ml甲醇为溶剂分两次进行超声提取,每次超声15分钟,放冷,称重,滤过,得续滤液于蒸发皿中水浴蒸干,定量转移至10 ml容量瓶中,用流动相定容至刻度即得供试品溶液。
2.4 专属性试验
根据处方中各药味的比例,按照散结止痛颗粒制备工艺制备不含赤芍的颗粒,按照供试品提取条件及制备方法配制空白溶液,用高效液相色谱法测定,结果该空白溶液与散结止痛颗粒溶液的HPLC色谱图在相应的保留时间无吸收,表明该方法对散结止痛颗粒中芍药苷的测定具有专属性,可以用于散结止痛颗粒的芍药苷含量测定(见图1)。
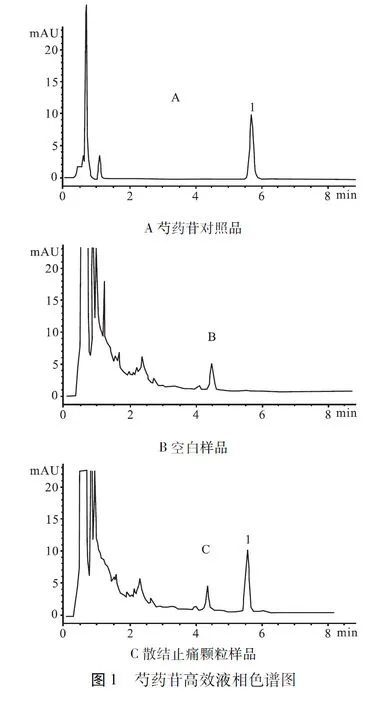
2.5 对照品和样品稳定性试验
取芍药苷对照品溶液和供试品溶液分别于配制后1小时、24小时、48小时分别连续3次依法测定峰面积,结果表明,对照品溶液和供试品溶液在48小时内稳定。
2.6 精密度试验
精密吸取浓度为262.0 μg/ml的对照品溶液10 μl于色谱仪中,重复进样5次,计算其峰面积的RSD为0.44%,表明精密度较好。
2.7 重现性试验
取同一批散结止痛颗粒5份,按照2.2方法测定样品中芍药苷含量,计算样品RSD为2.80%,表明重现性良好。
2.8 回收率试验
精密称取己知含量的同一批散结止痛颗粒6份,分别精密加入一定量的芍药苷储备液,用供试品溶液方法提取浓缩,定量转移至5 ml容量瓶中,用流动相定容至刻度。依法测定,并计算回收率, 平均回收率为99.76%,RSD为4.68%。表明本法具有良好的回收率。
2.9 样品测定结果
取5批次散结止痛颗粒样品,按照所述方法进行芍药苷测定含量,每批3次,结果见表1。
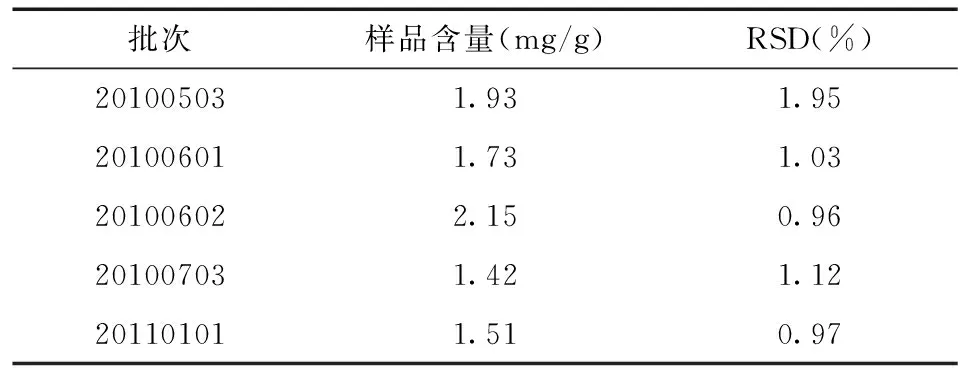
表1 5批样品中芍药苷含量测定结果
根据中国药典2010年版一部对赤芍药材中芍药苷不得少于1.8 %的规定,结合制备的5批样品中芍药苷的含量测定结果,最低含量1.42 mg/g,最高含量2.15 mg/g,故初步暂定散结止痛颗粒中芍药苷(C23H28O11)的含量不得小于1.5 mg/g。每袋装量12 g,则本品含芍药苷的量每袋不小于18.0 mg。
3 讨论
本实验流动相系统的确定时,分别考察了甲醇—水、甲醇—0.1%磷酸溶液两种流动相[6],结果芍药苷分离不完全,受到其他成分一定的干扰,且峰型不好,故选择乙腈—水系统,确定乙腈—水溶液(17∶83)为流动相时,芍药苷的分离度、峰型均较好,符合测定含量的要求。
在制备供试品溶液的提取方法中,分别考察了提取方法和时间、提取次数、提取溶剂及其使用量对芍药苷的影响。首先参考相关文献[7]初步采用甲醇提取芍药苷,在提取方法选择上,结果超声提取比回流提取简单易操作,并可以达到提取完全的
目的,故采用超声提取方法;在超声时间和溶媒用量上,通过多次试验,结果50 ml甲醇分两次提取,每次超声15分钟即可将芍药苷提取完全。
该医院制剂成分复杂,多年临床应用证明其安全、有效,但其质量标准仅对成品进行两味药材定性鉴别,未建立中间产品及成品定量检测控制标准。为保证药品质量,本试验建立的散结止痛颗粒中芍药苷含量测定方法简便、准确、结果可靠,能有效地控制散结止痛颗粒的质量,保证了临床疗效的稳定,并可为进一步申报中药新药做好准备。
[1]朴田,莫晓燕,林瑞峥.赤芍总苷提取液体外清除自由基和抗凝血活性的研究[J].中国药房,2007,19(9),643-646.
[2]马双成,邓少伟.赤芍总苷的生产工艺条件研究[J].中草药,1998,29(10):664.
[3]华东,吴明媛,于晓红,等.赤芍总苷对荷瘤鼠细胞免疫功能的影响[J].中医药学报,2004,32(1):47.
[4]王晓玉,魏伟,唐丽琴,等.芍药苷对佐剂性关节炎大鼠腹腔巨噬细胞吞噬功能及其产生细胞因子的影响[J].安徽医科大学学报,2007,42(2):191-192.
[5]吴洪文,李明艳.高效液相色谱法测定蝎龙酒中芍药苷的含量[J].中国医院药学杂志,2010,30(17):1486.
[6]侯林中,裴玉书,张熙洁,等.HPLC法测定宽心口服液中芍药苷的含量[J].中国药房,2011,22(31),2933-2934.
[7]李文博,韩建平,倪倩,等.SPE-UPLC法测定养血清脑颗粒中的芍药苷含量[J].药物分析杂志,2011,31(7):1385-1388.

