补骨脂中异戊烯基黄酮类化合物及其药理作用研究进展
耿革霞,黄又五,郭夫江
1河北省食品药品监督管理局药品审评认证中心,石家庄 050000;2上海中医药大学,中药化学教研室,上海 201203
异戊烯基黄酮是黄酮中一类重要的烷基化产物,是自然界中一大类天然产物,但是其分布并不广泛。研究显示,约有10科37属的植物含有异戊烯基黄酮类化合物,主要分布于豆科、芸香科、桑科、山竹子科、小檗科、萝藦科和大戟科等科的部分属的植物中[1]。因其在某些植物中含量较高,且结构独特、多样并具有一定的药理活性而受到重视,如抗菌作用、抗肿瘤活性、心血管活性、抗HIV活性、抗免疫活性、抗疟、抗氧化、治疗肝硬化和高血压,以及对一些酶的抑制作用等[2-4]。同时,黄酮被异戊烯基取代之后,增加了它的脂溶性和对生物膜的亲和力,以及靶蛋白的相互作用,从而影响了很多它的生理活性[5]。正是由于异戊烯基黄酮在生物活性研究中所表现出来的显著活性,使得对该类化合物的研究日益加深。
补骨脂是我国传统中药,为豆科植物补骨脂Psoralea corylifolia L.的干燥成熟果实,其功能是温肾助阳,纳气平喘,温脾止泻,消风祛斑,用于肾阳不足,阳痿遗精,遗尿尿频,腰膝冷痛,肾虚作喘,五更泄泻,外用治疗白癜风和秃斑[6]。到目前为止,已经从该植物中提取分离得到许多成分,其中香豆素类、黄酮类及单萜酚类化合物是其主要特征成分[7]。近年来,在补骨脂中异戊烯基黄酮类化合物的研究上有了诸多研究成果,现将补骨脂中异戊烯基黄酮类化合物的化学和药理作用综述如下。
1 异戊烯基黄酮类化合物的化学研究
现有的实验研究显示,已经从补骨脂中提取、分离、纯化出28个异戊烯基黄酮类化合物,此外,还有学者通过液质联用技术表征了更多的该类化合物[5]。现在根据黄酮类化合物的结构特征进行如下分类。
1.1 黄酮类
补骨脂中的异戊烯基黄酮类化合物有2个,分别是corylifol C[8](1)和补骨脂色烯黄酮coryfolia D(corylifol D)[9](2)。
1.2 二氢黄酮类
该类化合物有5个,分别是补骨脂甲素或名补骨脂二氢黄酮 bavachin(corylifolin)[10](3),补骨脂二氢黄酮甲醚bavachinin[11](4),异补骨脂黄酮亦称异补骨脂二氢黄酮 isobavachin[12](5),7,8-Dihydro-8-(4-hydroxyphenyl)-2,2-dimethyl-2H,6H-[1,2-b:5,4-b]dipyran-6'-one[8](6),6-prenylnaringenin[13](7)。
1.3 异黄酮
补骨脂中异戊烯基异黄酮类化合物较多,有11个,它们是补骨脂宁亦称补骨脂异黄酮corylin[14](8),erythrinin A[8](9),新补骨脂异黄酮 neobavaisoflavone[13](10),8-prenyldaidzein[8](11),corylifol A[8](12),isoneobavaisoflavone[8](13),补骨脂新异黄酮 5-(2-Hydroxy-1-methylethyl)-4,5-dihydrofurano[2,3-h](4'-hydroxy-3',5'-dimethoxy)isoflavone/bavarigenin[9](14),补骨脂醇 psoralenol[16](15),2',3'-dihydro-2',2'-dimethyl-,diacetate[16](16),2',3'-dihydro-3'-hydroxy-7-methoxy-2',2'-dimethyl[16](17),3'-(acetyloxy)-2',3'-dihydro-7-methoxy-2',2'-dimethyl[16](18)。
1.4 查尔酮
补骨脂中异戊烯基查尔酮类化合物有10个,是补骨脂查耳酮 bavachalcone(broussochalcone B)[17](19),补骨脂乙素亦称异补骨脂查尔酮isobavachalcone(corylifolinin)[18](20),补骨脂色烯素 psorachromene(bavachromene)[19](21),4'-O-methylbavachalcone[20](22),补骨脂色酚酮 bavachromanol[21](23),isobavachromene[22](24),骨脂色烯查耳酮亦称巴库查耳酮 bakuchalcone[23](25),Psorachalcone A[8](26),brosimacutin G[8](27),corylifol B[8](28)。
补骨脂中异戊烯基黄酮类化合物的结构见Figure 1。
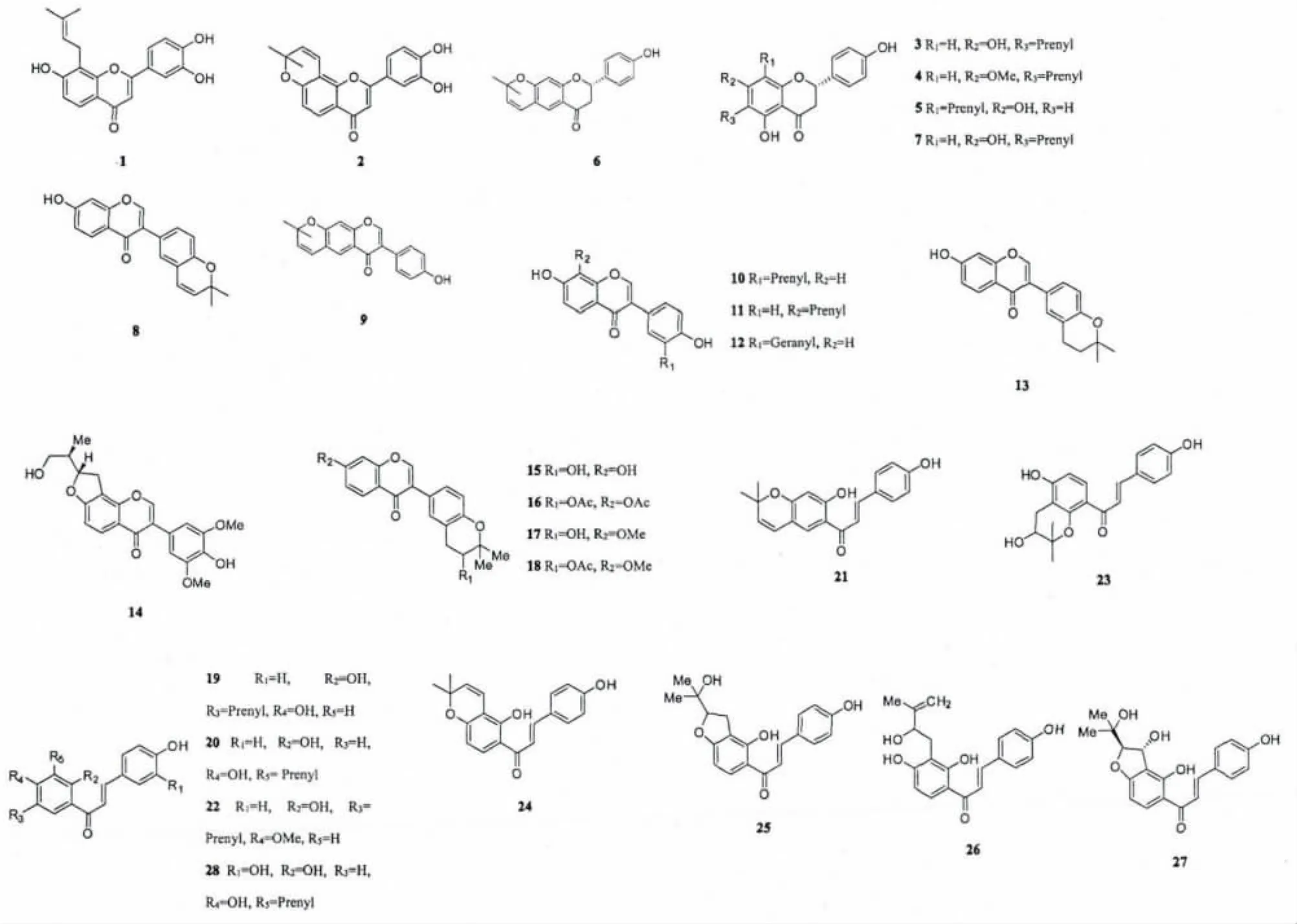
图1 补骨脂中的异戊烯基黄酮类化合物Fig.1 Prenylated flavonoids from Psoralea corylifolia Linn.
2 异戊烯基黄酮类化合物的药理作用
2.1 抗菌作用
Yin Sheng 等学者[8]对化合物 1,3,4,6,8,9,10,11,12,13,19,20,25,26,27,28 做两种葡萄球菌staphylococcus aureus和staphylococcus epidermidis进行了抗菌活性研究,结果显示,化合物3,4,6,9,10,13,19,20和28显示出明显的抗菌作用,MICs水平在0.009 ~0.073 mM。尤其是化合物 28,10,6,19,3显示出与阳性药bakuchiol和magnolol相当的抗菌活性,20,4和9甚至比阳性药效果更强。从构效关系分析,查耳酮衍生物,在A环有异戊烯基的化合物28,20和19显示更强的活性,而当异戊烯基被氧化或是环化,比如26,25和27则是不活跃的。在B环C-3'和C-4'带有羟基的化合物28与只有C-4'位有羟基的化合物20相比,28的抗菌作用显著减弱。异戊烯基黄酮衍生物1,6,3和4中,二氢黄酮衍生物6,3,4显示出更强的抗菌作用。带有7-甲氧基的化合物4比带有7-羟基的化合物3显示出更强的作用。
ElSohly HN等人研究显示,化合物20显示出抗AIDS相关的条件致病菌Candida albicans和Cryptococcus neoformans的作用[24]。
Nkengfack Augustin E等人研究显示,化合物13表现出显著的体外抗金黄色葡萄球菌作用[25]。
2.2 在骨质疏松上的作用
Wang D W等人的研究显示,补骨脂提取物,化合物8、3可能刺激骨形成或是有潜在的活性以抗骨质酥松症[26]。
Park CK等人的研究显示,化合物19抑制破骨细胞形成,是通过干扰ERK和Akt信号通路,和c-Fos与NFATc1变异引发的。他们的实验表明,化合物19可能对治疗骨吸收疾病有用[27]。
Don MJ等人的实验研究显示,化合物10能通过p38调节转录因子的上调和MC3T3-E1细胞中类骨质基因的表达刺激骨生长其机制可能是激活p38依赖的信号通路来上调Runx2和Osx的mRNA水平,来刺激骨基质蛋白的表达[28]。
2.3 对胚胎干细胞作用
Wang DY等人研究显示,化合物5可以促进老鼠的胚胎干细胞分化成为神经细胞[29]。
2.4 治疗哮喘作用
Yin ZN等人的专利显示,在体外通过IL-4-GFP转基因报告小鼠高通量筛选模型,采用IL-4-GFP转基因报告小鼠全脾脏细胞,用刀豆蛋白A、白细胞介素-2和白细胞介素-4因子刺激,再与梯度稀释的不同浓度的化合物4共同培养48 h,后收细胞,用anti-CD4-APC对培养的细胞分别染色,最后进行流式分析化合物4对IL-4-GFP+量的影响。实验证实化合物4可以在细胞水平显著抑制IL-4的分泌,同时,通过构建小鼠哮喘模型,在体内实验证实,化合物4具有很好的抗哮喘和抗炎作用[30]。
2.5 抗炎作用
Szliszka E等人的研究显示,化合物10能显著的抑制 ROS,RNS的功能,和在 LPS+IFN-γ或是PMA刺激的RAW264.7巨噬细胞中抑制细胞因子IL-1β,IL-6,IL-12p40,IL-12p70,TNF-α[31]。
Lee SW 等人的研究显示,化合物 3、4、8、10、12和20能抑制Hep3B细胞中IL-6诱导的STAT3促进作用,IC50为4.57 ±0.45,3.02 ±0.53,2.77 ±0.02,0.81 ±0.15,1.37 ±0.45,2.45 ±0.13,and 4.89 ±0.05 μM,同时,它们也能抑制 Hep3B细胞中 IL-6诱导的STAT3磷酸化作用[10]。
2.6 对心血管系统的作用
Chen CC等人研究表明,化合物10、20具有抑制花生四烯酸、血小板活化因子和胶原诱导的血小板凝集作用[32]。
2.7 抗肿瘤作用
Sun N J等人的研究表明,采用SV40生物测定法发现化合物3有抑制复制型DNA聚合酶的活性,同时高浓度的化合物10可抑制复制型DNA聚合酶的活性[33]。
Bronikowska J等人的研究显示,化合物10在Hela细胞会增强TRAIL诱导的细胞凋亡[34]。
Zhu D Y等人的实验研究显示,化合物20在体外有抑制 Hela细胞作用[35]。
Szliszka E等人的研究显示,化合物10和psoralidin在前列腺癌细胞中能致敏TRAIL拮抗细胞和显著增强TRAIL调节的细胞凋亡和细胞毒性[36]。
Waetjen W等人的研究显示,在代谢活跃的H4IIE肝癌细胞和代谢较弱的C6胶质瘤细胞中,当研究化合物licoflavone C和化合物5的内在效应时,显示出显著的毒性,在H4IIE中IC50分别是42±5 and 96 ±19 μmol/L,在 C6 细胞中 IC50分别是 37 ±6 and 69±3 μmol/L,与之对比的未异戊烯化的糖基化衍生物牡荆苷vitexin在高达250 μmol/L是也几乎没有毒性[37]。
2.8 对神经系统的作用
Lee MH等人的研究显示,在激活的小胶质细胞中,化合物6可以通过抑制I-κB-α的退化抑制一氧化氮合酶的表达,从而可能作为先导化合物开发神经保护药[38]。
2.9 对视网膜作用
Chiou GCY等人的实验研究显示,化合物20能促进视网膜功能恢复,可以用来治疗视网膜缺血症[39]。
2.10 抗氧化作用
Guo J N博士的实验研究表明,化合物3、8具有较强的抗氧化活性[40]。
Chen J W等人讨论了在清除羟自由基作用上的构效关系,其中,化合物3、20能有效的清除羟基自由基而且抑制了系统的化学发光,IC50为66.8(63.2 ~74.4)g/L、262(190 ~346)g/L。同时得出如下5个结论;(1)黄酮类化合物的酚羟基是够清除羟基自由基的主要活性成分;(2)在A环和B环上的羟基是清除羟基自由基的重要活性基团;(3)在A环和、或B环上的邻位二羟基能显著的增强清除作用;(4)对比化合物quercetin,heliosin,hyperoside,baicalin,lysionotin 和 matteucinol的 IC50,可知羟基在3',4'位置能显示极大的清除作用,而且羟基在B环比在A环效果要好。就以上6个化合物而言,羟基或是葡萄糖苷在C环的3位与清除作用也相关;(5)黄酮类化合物的结构类型也能影响羟基自由基清除作用[41]。
2.11 酪氨酸酶抑制作用
Kim J Y 等人的研究表明,化合物3、4、20、4'-O-methylbavachalcone和 isobavachromene具有抑制酪氨酸酶的作用,实验研究了这些多酚类化合物对蘑菇酪氨酸酶的酪氨酸酶活动抑制效能,IC50为12.3,48.8,15.8,23.6,and 143.9 μM,其中,在对 Lineweaver-Burks和Dixon-plot的分析中,化合物3、20、4'-O-methylbavachalcone和 isobavachromene的强效抑制作用显示出特征性竞争抑制作用[42]。
2.12 对脂多糖活跃的巨噬细胞的影响
Matsuda H等人的研究显示,在产生一氧化氮NO的脂多糖活跃的巨噬细胞中,化合物4、10、12、20和psoralidin显著的抑制亚硝酸盐积累,其中,化合物 4(IC50=26 um),20(17 μm),10(ca.29 μm),12(ca.21 μm),和 psoralidin(ca.23 μm)[43]。
3 结语
目前,对于异戊烯基黄酮的研究发现,它们具有广泛的生物活性,而具有较高药用价值的常用植物药补骨脂中,通过对其异戊烯基黄酮类化合物的成分和药理作用的研究显示,该类成分也具有较高的抗菌、抑制骨质疏松、治疗哮喘、抗炎、抗癌、抗氧化等作用。同时,通过构效关系研究发现,异戊烯基黄酮的抗菌活性与异戊烯基黄酮中酚羟基和异戊烯基有关,并且,黄酮被异戊烯基取代之后,其脂溶性和对生物膜的亲和力增加,靶蛋白的相互作用增加,很多生理活性被影响。然而,对于补骨脂中异戊烯基黄酮类化合物的构效关系的研究依然不多,没有系统的、更加深入的研究报道。相信随着进一步的研究,在现有的研究基础之上,可以取得更加深入和系统的研究结果,在补骨脂药物作用与其中的异戊烯基类黄酮的构效关系上获得突破性成果,为提高人们的健康水平做贡献。
1 Yu DQ(于德泉),Wu YL(吴毓林).Advances in Natural Product Chemistry(天然产物化学进展),Beijing:Chemical Industry Press,2005,134-167.
2 Donnelly DMX,Boland GM.Isoflavonoids and neoflavonoids:naturally occurring O-heterocycles.Natural Product Reports,1995,12(3):321-338.
3 Huang CH(黄朝辉),et al.呫吨酮类化合物及其药理活性.Foreign Med Sci(国外医药植物药分册),2003,18:93-100.
4 Harborne JB,Willianms CA.Advances in flavonoid research since 1992.Phytochemistry,2000,55:481-504.
5 Xu MJ,et al.Simultaneous characterization of prenylated flavonoids and isoflavonoids in Psoralea corylifolia L.by liquid chromatography with diode-array detection and quadrupole time-of-flight mass spectrometry.Rapid Commun.Mass Spectrom,2012,26:2343-2358.
6 Chinese Pharmacopoeia Commission(国家药典委员会).Pharmacopoeia of the People’s Republic of China(中华人民共和国药典).Beijing:China Medical Science Press,2010.VolⅠ,174.
7 Ji L(吉力),Xu ZL(徐植灵).Review of Constituents in Fruits of Psoralea corylifolia L..Chin J Chin Mater Med(中国中药杂志),1995,20:120-128.
8 Yin S,et al.Antibacterial prenylflavone derivatives from Psoralea corylifolia,and their structure-activity relationship study.Bioorg Med Chem,2004,12:4387-4392.
9 Yang TT(杨彤彤),et al.Two new compounds from Psoralea corylifolia L..Acta Pharm Sinica(药学学报),2009,44:1387-1390.
10 Lee SW,et al.Phenolic compounds isolated from Psoralea corylifolia inhibit IL-6-induced STAT3 activation.Planta Med,2012,78:903-906.
11 Choi YH,et al.In vitro BACE-1 inhibitory phenolic components from the seeds of Psoralea corylifolia.Planta Med,2008,74:1405-1408.
12 Haraguchi H,et al.Antioxidative components of Psoralea corylifolia(leguminosae).Phytother Res,2002,16:539-544.
13 Matsuda H,et al.Bioactive constituents from Chinese natural medicines.XX.Inhibitors of antigen-induced degranulation in RBL-2H3 cells from the seeds of Psoralea corylifolia.Chem Pharm Bull,2007,55:106-110.
14 Guo JN(郭江宁),et al.Antioxidants from a Chinese medicinal herb-Psoralea corylifolia L..Food Chem,2005,91(2):287-292.
15 Gupta GK,et al.Corylinal:a new isoflavone from seeds of Psoralea corylifolia.Phytochemistry,1978,17:164.
16 Suri JL,et al.Psoralenol:a new isoflavone from the seeds of Psoralea corylifolia.Phytochemistry,1978,17:2046.
17 Qiu RL(邱蓉丽),et al.Chemical constituents of Psoralea corylifolia.J Chin Med Mater(中药材),2011,34:1211-1213.
18 Zhang YL(张玉林),Chen ZL(陈子林).Separation of isomeric bavachin and isobavachalcone in the Fructus Psoraleae by capillary electrophoresis-mass spectrometry.J Separation Sci,2012,35:1644-1650.
19 Tewari A,Bhakuni RS.New constituents from Psoralea corylifolia.India J Chem,2010,49B:256-259.
20 Oh KY,et al.Glycosidase inhibitory phenolic compounds from the seed of Psoralea corylifolia.Food Chem,2010,121:940-945.
21 Suri JL,et al.Bavachromanol:a new chalcone from the seeds of Psoralea corylifolia.Phytochem,1980,19:336-337.
22 Kim YJ,et al.Inhibition of Human 20S Proteasome by Compounds from Seeds of Psoralea corylifolia.Bull Korean Chem Soc,2009,30:1867-1879.
23 Gupta GK,et al.Bakuchalcone,a dihydrofuranochalcone from the seeds of Psoralea corylifolia.Phytochem,1982,21:2149-2151.
24 ElSohly HN,et al.Antifungal chalcones from Maclura tinctoria.Planta Med,2001,67:87-89.
25 Nkengfack AE,et al.An isoflavanone and a coumestan from Erythrina sigmoidea.Phytochem,1994,35:521-526.
26 Wang DW,et al.Osteoblastic proliferation-stimulating activity of Psoralea corylifolia extracts and two of its flavonoids.Planta Med,2001,67:748-749.
27 Park CK,et al.Bavachalcone inhibits osteoclast differentiation through suppression of NFATc1 induction by RANKL.Bioch Pharm,2008,75:2175-2182.
28 Don MJ,et al.Neobavaisoflavone stimulates osteogenesis via p38-mediated up-regulation of transcription factors and osteoid genes expression in MC3T3-E1 cells.Phytomedicine,2012,19:551-561.
29 Wang DY,et al.Promoting effects of isobavachin on neurogenesis of mouse embryonic stem cells were associated with protein prenylation.Acta Pharm Sin(中国药理学报),2011,32:425-432.
30 Yin ZN(尹芝南),et al.Application of bavachinin for treating asthma(补骨脂二氢黄酮甲醚抗哮喘病的应用).CN201110065703.9,2012-09-19.
31 Szliszka E,et al.Inhibition of inflammatory mediators by neobavaisoflavone in activated RAW264.7 macrophages.Molecules,2011,16:3701-3712.
32 Chen CC,et al.Antiplatelet Flavonoids from Seeds of Psoralea corylifolia.J Nat Prod,1996,59:671-672.
33 Sun NJ,et al.DNA polymerase and topoisomerase II inhibitors from Psoralea corylifolia.J Nat Prod,1998,61:362-366.
34 Bronikowska J,et al.The combination of TRAIL and isoflavones enhances apoptosis in cancer cells.Molecules,2010,15:2000-2015.
35 Zhu DY(朱大元),et al.Studies on the chemical constituents of Bu-Gu-Zhi,the seeds of Psoralea corylifolia L.Acta Pharm Sin(药学学报),1979,14:605-611.
36 Szliszka E,et al.Enhanced TRAIL-mediated apoptosis in prostate cancer cells by the bioactive compounds neobavaisoflavone and psoralidin isolated from Psoralea corylifolia.Pharm Rep,2011,63:139-148.
37 Waetjen W,et al.Prenylation enhances cytotoxicity of apigenin and liquiritigenin in rat H4IIE hepatoma and C6 glioma cells.Food Chem Toxicol,2007,45:119-124.
38 Lee MH,et al.Prenylflavones from Psoralea corylifolia Inhibit Nitric Oxide Synthase Expression through the Inhibition of I-κB-α Degradation in Activated Microglial Cells.Biol Pharm Bull,2005,28:2253-2257.
39 Chiou GC,et al.Facilitation of retinal function recovery by natural products after temporary ischemic occlusion of central retinal artery.J Ocul Pharmacol,1994,10:493-498.
40 Guo JN(郭江宁).Study on the antioxidant and antitumour of active constituents of Psoralea corylifolia L.Shenyang:Shenyang Pharmaceutical University(沈阳药科大学),PhD.2000.
41 Chen JW(陈季武),et al.Structure-activity relationship of natural flavonoids in hydroxyl radical-scavenging effects.Acta Pharm Sin(中国药理学报),2002,23:667-672.
42 Kim JY,et al.Polyphenols displaying tyrosinase inhibition from the seed of Psoralea corylifolia.J Korean Society for Appl Biol Chem,2010,53:427-432.
43 Matsuda H,et al.Bioactive constituents from Chinese natural medicines.XXXIII.Inhibitors from the seeds of Psoralea corylifolia on production of nitric oxide in lipopolysaccharideactivated macrophages.Biol Pharm Bull,2009,32:147-149.

