氧化铌掺杂PbO2电极的制备及降解分散蓝B
唐文伟,陈晓颖,张 旻,苏兴治,肖耀明,曾新平
1)同济大学化学系,上海200092;2)同济大学生命科学与技术学院,上海200092
染料废水是一种排放量大、污染严重的难降解有机废水[1].分散染料可生化性差,常规处理的效果不理想.而电化学氧化法反应条件温和,能有效降解各种污染物,是处理分散染料的不错选择[2].
电化学氧化应用的关键在于制备高性能电极[3].PbO2电极因具备可耐多种强酸与氧化剂、价廉易得、析氧电势高及电催化活性强等优点而受到广泛关注,但PbO2电极还存在电流效率不高、镀层易溶解 (不耐腐蚀)[5]和寿命不长[6]等问题.稀土金属元素具有f电子轨道,掺杂到电极的镀层后,有助于形成便于电子传输的通道,提高电极的催化活性[7].Kong 等[8]用共沉积法制备 Er2O3、Gd2O3和La2O3掺杂的PbO2电极,对4-氯酚的降解效果良好.用十二烷基苯磺酸钠和碳纳米管修饰PbO2电极,电极寿命延长[9].Aravind 等[10]制备了Nb+5掺杂TiO2电极,能有效提高电极的透明度和电子效率.氧化铌具有较高的化学稳定性,在催化和光学等领域应用广泛[11-13],但氧化铌掺杂改性PbO2电极用于降解染料却很少见报道.
本研究采用电沉积法制备了氧化铌掺杂的钛基PbO2电极,并用 X射线衍射 (X-ray diffraction,XRD)、扫描电镜 (scanning electron microscope,SEM)和电化学工作站进行表征,优化了电极制备条件.将制得的电极用于分散蓝B降解,考察了溶液pH值、电解质和电流密度等对脱色的影响,并进行了动力学分析.
1 实验
1.1 药品和材料
电极材料为陕西宝鸡某公司的钛板,裁剪成30 mm×20 mm×1 mm规格.实验所用药品均为分析纯,溶液采用去离子水配制.降解实验所用的分散蓝B由上海市染料研究所提供.
1.2 电极的制备
电极预处理.喷砂→洗洁精超声15 min→丙酮超声15 min→体积比为1∶1的HNO3和H2SO4混合液常温处理2 h.
电沉积制备.在水浴加热条件下,电沉积制备β-PbO2镀层.镀液组成为0.5 mol/L Pb(NO3)2、0.05 mol/L NaF和0.1 mol/L HNO3.沉积条件:以钛基体为阳极,商业钛电极为阴极,pH=1.5,温度70℃,电流密度5 mA/cm2,沉积90 min.
电极掺杂改性.将固体Nb2O5研磨后,分别以0.5,1.5,2.5和3.5 g/L掺杂到镀液中,在400 r/min搅拌下与β-PbO2共同沉积到钛基体上.
1.3 电极性能测试
采用XRD(D8 Advance型)分析电极的相结构,用Cu靶、Ka射线,工作电压40 kV,电流30 mA,扫描速度 10(°)/min,扫描范围 10°~70°.采用扫描电镜 (TESCAN 5136 MM)分析电极表面形貌,扫描电压为20 kV.采用电化学工作站 (Autolab model PGSTAT30)测试电极的电化学性能.以制备电极为工作电极,铂电极为对电极,饱和甘汞电极为参比电极.线性伏安扫描 (linear sweep voltammetry,LSV),扫速取100 mV/s,支持电解质分别为0.5 mg/L的Na2SO4与100 mg/L的分散蓝B混合溶液,及0.5 mg/L的Na2SO4溶液.通过阶跃分析考察电极对污染物的降解能力[14].设两段电压,第1段1.0 V,第2段2.5 V,时间均为100 s.强化寿命实验以制备的电极为阳极,商业钛电极为阴极,极板间距为1.5 cm,溶液为1.0 mol/L的H2SO4,电解温度控制在25℃,在恒电流密度为2 A/cm2下电解.规定槽电压比电解开始时电压增加10 V时的电解时间为电极强化寿命[15].通过紫外分光光度计 (Agilent 8453)测定染料脱色程度,初始浓度下和紫外照射后的光密度分别记为D0(575 nm)和D(575 nm),其脱色率
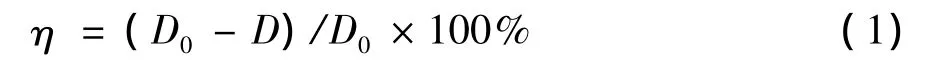
2 结果与讨论
2.1 电极的性能测试
2.1.1 XRD测试
Nb2O5掺杂前后PbO2电极的XRD见图1.从图1可知,Nb2O5的掺杂改变了PbO2沉积的晶型分布,掺杂后以α-PbO2晶型为主,这可能是由于Nb2O5的掺杂提高了电流效率,形成了只有在较高电流密度下才能形成的 α-PbO2晶型.在 2θ为22.94°和27.8°处的衍射峰分别对应标准的Nb2O5,说明Nb2O5已经掺杂在PbO2电极上,且以氧化物的形式存在[16].推测 α-PbO2填充在 β-PbO2晶体的缝隙中,形成了阻挡层,使得活性层与钛基体不易剥离,进而提高电极的寿命.根据Scherrer公式,计算未掺杂时β-PbO2晶粒尺寸为30.0 nm,掺杂后晶粒尺寸为33.8 nm.
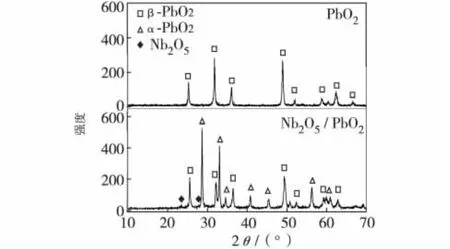
图1 掺杂3.5 g/L Nb2O5前后电极的XRD图Fig.1 XRD patterns of electrode undoped and doped with 3.5 g/LNb2O5
2.1.2 SEM分析
掺杂Nb2O5前后PbO2电极的SEM见图2.由图2(c)可见,掺杂Nb2O5的电极表面PbO2晶体排列规整均匀,Nb2O5具有促进PbO2分散的作用.在图2(d)中,电极表面的PbO2晶体非常明显,粒径大,且出现了一些空隙,表面不平整,这可能是由于Nb2O5填充在PbO2晶体的空隙中,阻碍晶体的连续生长,起到引导PbO2晶体生长的作用.对照图1可知,掺杂Nb2O5颗粒改性时,能促使PbO2重结晶,晶体粒径增大,且排列规整均匀.

图2 掺杂3.5 g/L Nb2O5前后电极的SEM图Fig.2 SEM image of electrode undoped and doped with 3.5 g/L Nb2O5
2.1.3 强化寿命分析
Nb2O5掺杂改性电极的强化寿命见表1.

表1 Nb2O5掺杂改性电极的强化寿命Table 1 Strengthen lifetime of Nb2O5doped electrode
如表1所示,Nb2O5的掺杂改性对β-PbO2电极的强化寿命有显著提高.当掺杂质量浓度为0.5 g/L时,强化寿命明显延长,随着掺杂质量浓度增大,强化寿命显著提高,掺杂质量浓度为3.5 g/L时,强化寿命达到702 min.
2.1.4 LSV和阶跃分析
Nb2O5掺杂改性电极的LSV和阶跃分析见图3和图4.
从图3可知,随着掺杂量的增加,掺杂改性电极的析氧电位不断提高,掺杂量为3.5 g/L时,达到最高析氧电位1.523 V,略高于未掺杂时的1.516 V,明显高于0.5,1.5和2.5 g/L Nb2O5掺杂电极的析氧电位 (分别为1.443,1.462和1.470 V).析氧电位越高,析氧反应就越难发生,电极对有机物的氧化能力越强.
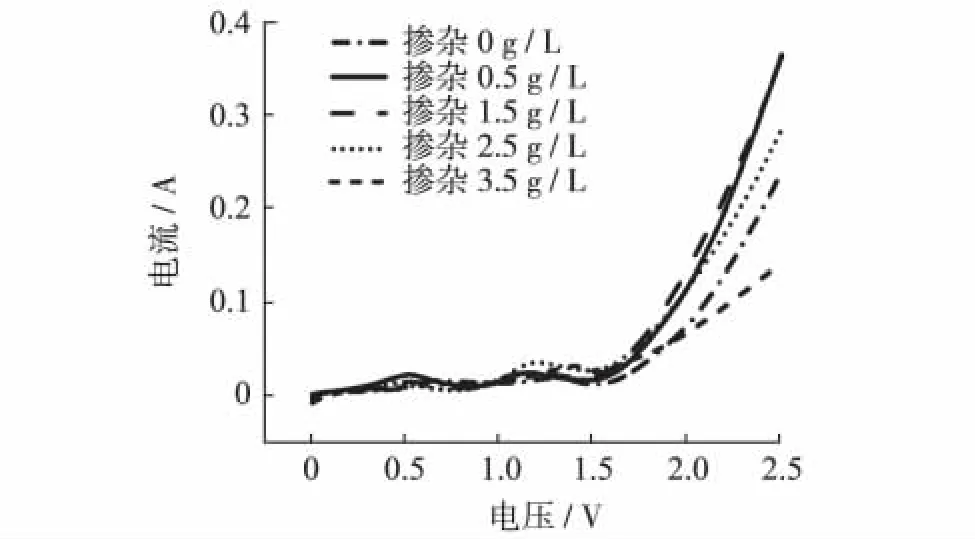
图3 Nb2O5掺杂改性电极的LSV图Fig.3 LSV curves of Nb2O5doped electrode
图4显示,先施加低于电极析氧电位的电压(1.0 V),100 s之后将电位阶跃至2.5 V(高于析氧电位),背景电流急剧增大,这是由于水的电解,发生析氧反应.两条曲线之间的差值即电极对污染物的阶跃氧化电流.
阶跃氧化电流反映了在施加电压高于析氧电位时,电极的氧化能力和氧化电流效率.掺杂质量浓度为3.5 g/L时,阶跃氧化电流为0.155 9 A,相对未掺杂时的0.103 3 A有明显提高,此时电极具有良好的氧化性能.
综合考虑析氧电位、阶跃氧化电流和强化寿命,以掺杂3.5 g/L Nb2O5的改性电极性能最优.
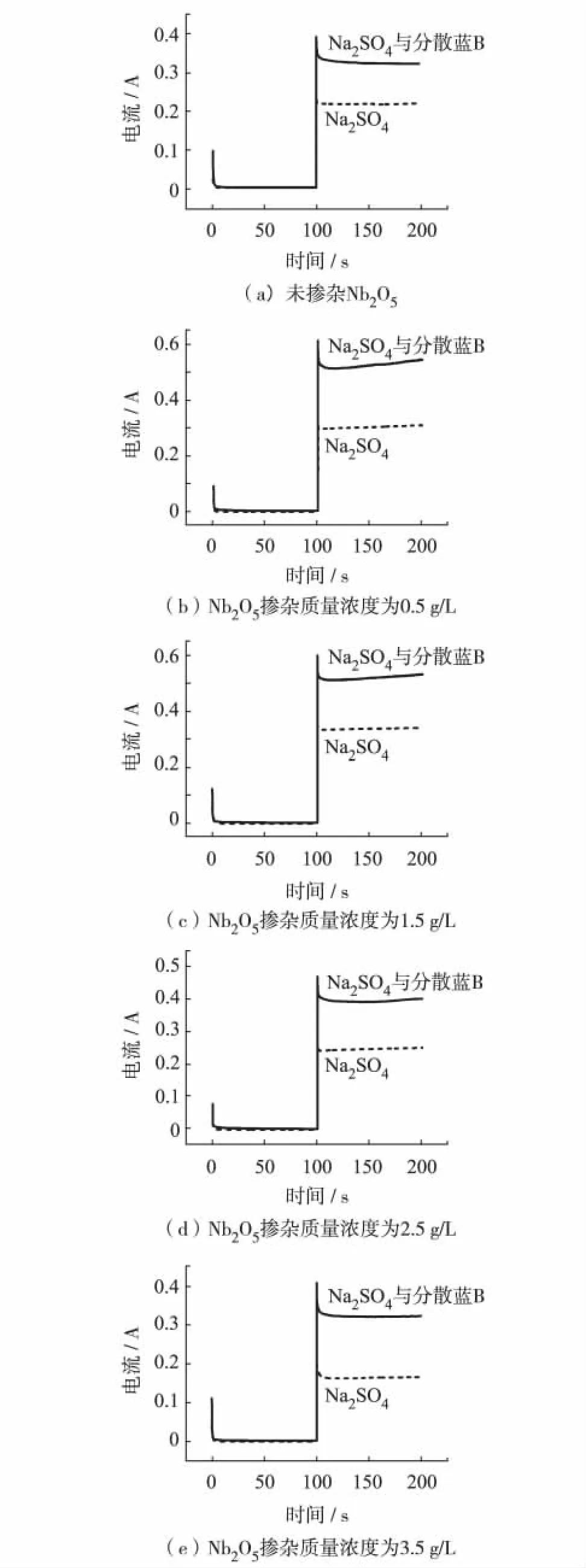
图4 氧化铌掺杂改性电极的阶跃图Fig.4 Stepcurrent curves of Nb2O5doped electrode
2.2 染料的降解研究
以掺杂3.5 g/L Nb2O5的改性电极为工作电极进行染料降解.
2.2.1 pH值的影响
在NaCl为0.5 mol/L,电流密度为40 mA/cm2时,用NaOH和HCl溶液调节电解液pH值,其对染料脱色的影响如图5.图5表明,pH=2时,脱色效果最佳,其后依次是pH值为6、8和12时.说明在酸性条件下染料分子发色基团易被打断,碱性条件下形态稳定,脱色效果较差.这是由于在酸性条件下·OH的氧化电位 (·OH+H++e-=H2O,E0=+2.85 V)高于碱性条件 (OH+e-=OH-,E0=+2.02 V),·OH在酸性条件下有更强的氧化性.同时,酸性条件下生成的活性氯主要以次氯酸的形式存在,而随着pH值上升,次氯酸逐渐转化为次氯酸盐,降低了氧化能力.
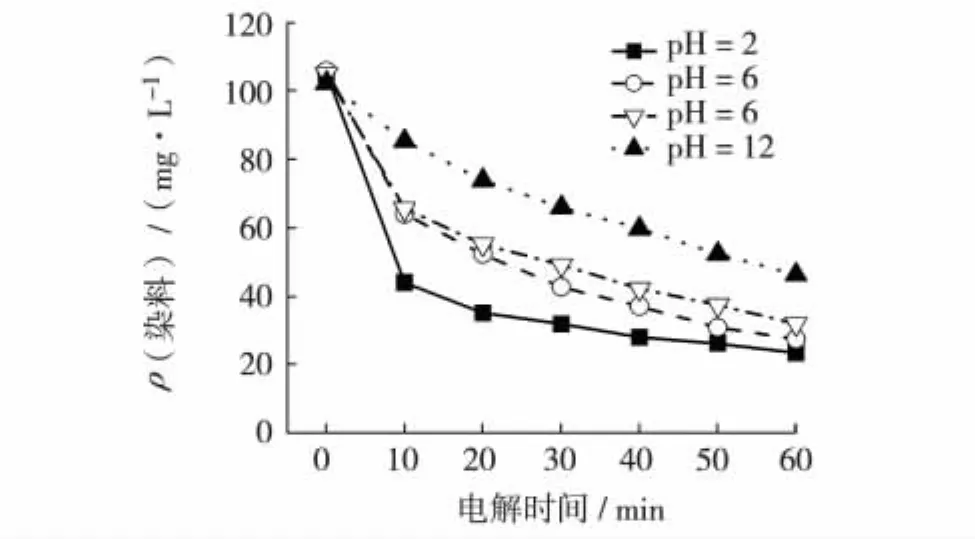
图5 pH对染料脱色的影响Fig.5 Influence of pH on decoloration of dye
2.2.2 支持电解质浓度的影响
NaCl作为常见的电解质普遍用于染料降解,随着NaCl浓度的增加,一方面溶液中自由离子数量增加,提高了溶液的导电性,利于电子在溶液和电极间传递;另一方面也增大了电解产生的活性氯浓度,提高了废水的脱色率.在溶液pH值为2,电流密度为40 mA/cm2时,NaCl浓度对染料脱色的影响如图6,表明在NaCl浓度为0.7 mol/L,电解60 min时,染料脱色率达89%,明显高于其他浓度.
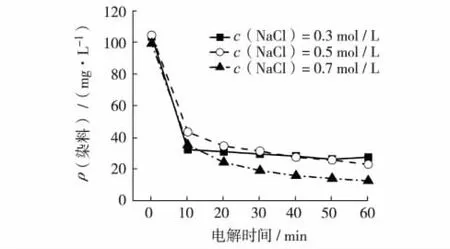
图6 支持电解质浓度对染料脱色的影响Fig.6 Influence of support electrolyte concentratin on decoloration of dye
2.2.3 电流密度的影响
在电解液pH=2,c(NaCl)=0.7 mol/L时,电流密度对染料脱色的影响如图7.
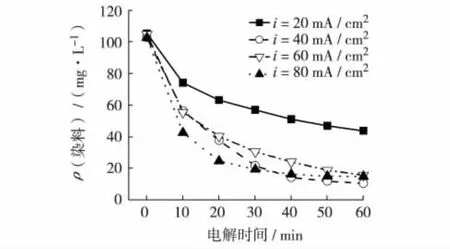
图7 电流密度对染料脱色的影响Fig.7 Influence of current density on decoloration of dye
电流密度表征了电化学降解体系的电子传递速度,也是电极反应的速度.电流密度越大,污染物在电极表面的反应速度就越快,污染物的直接降解作用越强.同时,降解体系产生了更多的·OH和·ClO等氧化性物质,促进了污染物的间接降解.但电流密度提高,析氧副反应也增加,导致电流效率下降.电流密度为40、60和80 mA/cm2时,分散蓝B脱色率变化不大的原因就在于此.图7显示,降解电流密度以40 mA/cm2为宜.
2.2.4 动力学分析
Fleszar等[17]认为,在阳极极化,PbO2电极晶格中的电子空穴受到激发,与吸附在电极表面的水分子发生如下反应,生成羟基自由基.
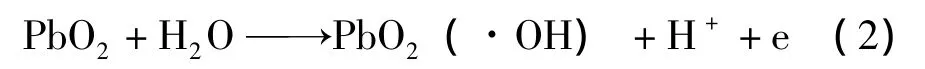
电化学降解污染物的过程主要是·OH作用的结果,其速率方程为
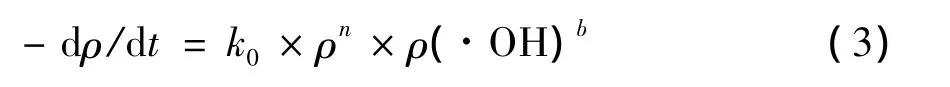
其中,ρ为污染物质量浓度;k0为反应动力学常数;ρ(·OH)为羟基自由基质量浓度;n和b分别为污染物和羟基自由基的反应级数.
·OH存在时间一般小于10-4s,可认为其处于假稳态,即dρ(·OH)/dt=0,由此可得

脱色反应体系具有均相反应特征,如用1级和2级反应动力学表达时,式(4)可表示为

其中,ρ0为污染物初始质量浓度;ρt为t时刻污染物质量浓度.
用式(5)和式(6)分别拟合图7数据,结果如表2.

表2 不同电流密度下分散蓝B降解的动力学参数Table 2 kinetic parameters of the influence of current densities on the decoloration of dye
表2显示,拟2级反应模型的R2(0.933 1~0.991 1)明显好于拟1级的R2(0.806 9~0.958 6),该掺杂改性电极对分散蓝B的脱色过程用拟2级反应来描述更合适.当电流密度为40 mA/cm2时,反应速率常数k最大,为0.001 6.
结 语
本研究采用电沉积法成功制备了掺杂氧化铌的钛基PbO2电极,其电化学性能、强化寿命和降解性能均明显提升.掺杂后电极活性组分以α-PbO2晶型为主,提高了镀层与基体的结合力.电极的晶粒粒径增加到33.8 nm,其表面更加规整均匀,析氧电位提高到1.523 V,强化寿命达到702 min,阶跃电流由未掺杂的0.103 3 A提升到0.155 9 A,提高了电极的氧化能力.氧化铌的最佳掺杂质量浓度为3.5 g/L.改性电极对难降解的分散蓝B有良好的脱色效果.最佳脱色条件为:镀液 pH=2,c(NaCl)=0.7 mol/L,电流密度i=40 mA/cm2.降解100 mg/L的分散蓝B溶液,1 h脱色率达89%,该电极对染料的脱色可用拟2级反应动力学描述.
/References:
[1] Aquino J M,Pereira G F,Rocha R C,et al.Electrochemical degradation of a real textile effluent using borondoped diamond or beta-PbO2as anode[J].Journal of Hazardous Materials,2011,192(3):1275-1282.
[2] Leonardo S A,Thiago T T,Diogo L S,et al.On the performances of lead dioxide and boron-doped diamond electrodes in the anodic oxidation of simulated wastewater containing the reactive orange 16 dye[J].Electrochimica Acta,2009,54(7):2024-2030.
[3] Wang Y,Shen Z,Li Y,et al.Electrochemical properties of the erbium-chitosan-fluorine-modified PbO2electrode for the degradation of 2,4-dichlorophenol in aqueous solution[J].Chemosphere,2010,79(10):987-996.
[4] Zhao G H,Zhang Y G,Lei Y Z,et al.Fabrication and electrochemical treatment application of a novel lead dioxide anode with superhydrophobic surfaces,high oxygen evolution potential,and oxidation capability [J].Environment Science and Technology,2010,44(5):1754-1759.
[5] Yeo I H,Wen S,Mho S I.Effect of interfacial oxides on the electrochemical activity of lead dioxide film electrodes on a Ti substrate [J].Analytical Science,2010,26(1):39-44.
[6] Zhou M H,Dai Q Z,Lei L C,et al.Long life modified lead dioxide anode for organic wastewater treatment:electrochemical characteristics and degradation mechanism[J].Environmental Science and Technology,2005,39(1):363-370.
[7] Gong Xiaozhong,Tian Peng,Zhou Zhi,et al.Electrodeposition and characterization of rare-earth element filled thermoelectric material CoSb3Smxand CoSb3Prx[J].Journal of Shenzhen University Science and Engineering,2010,27(2):217-223.(in Chinese)龚晓钟,田 鹏,周 智,等.稀土填充热电材料CoSb3Smx和CoSb3Prx的制备及表征 [J].深圳大学学报理工版,2010,27(2):217-223.
[8] Kong J T,Shi S Y,Kong L C,et al.Preparation and characterization of PbO2electrodes doped with different rare earth oxides [J].Electrochimica Acta,2007,53(7):2048-2054.
[9] Duan X Y,Ma F,Yuan Z X,et al.Lauryl benzene sulfonic acid sodium-carbon nanotube-modified PbO2electrode for the degradation of 4-chlorophenol[J].Electrochimica Acta,2012,76(1):333-343.
[10] Aravind K C,Frederic S,Montse C C,et al.Doping a TiO2photoanode with Nb5+to enhanced transparency and charge collection efficiency in dye-sensitized solar cells[J].Journal of Physical Chemistry C,2010,114(37):15849-15856.
[11] Bharat N P,Naik D B,Shrivastava V S.Photocatalytic degradation of hazardous Ponceau-S dye from industrial wastewater using nanosized niobium pentoxide with carbon[J].Desalination,2011,269(1/2/3):276-283.
[12] Ladera R,Finocchio E,Rojas S,et a1.Supported niobium catalysts for methanol dehydration to dimethyl ether:FTIR studies of acid properties [J].Catalysis Today,2012,192(1):136-143.
[13] Stosic D,Bennici S,Rakic V,et a1.CeO2-Nb2O5mixed oxide catalysts:preparation,characterization and catalytic activity in fructose dehydration reaction[J].Catalysis Today,2012,192(1):160-168.
[14] Zhao G H,Cui X,Liu M C,et a1.Electrochemical degradation of refractory pollutant using a novel microstructured TiO2nanotubes/Sb-doped SnO2electrode[J].Environmental Science and Technology,2009,43(5):1480-1486.
[15] Zhang Zhaoxian.Itanium Electrode Engineering[M].Beijing:Metallurgical Industry Press,2000:172-194.(in Chinese)张招贤.钛电极工学 [M].北京:冶金工业出版社,2000:172-194.
[16] He Jie,Fan Yining,Qiu Jinheng,et al.Dispersion state and catalytic properties of niobia species on the surface of Nb2O5/TiO2catalysts Nb2O5/TiO2[J].Acta Chimica Sinica,2004,62(14):1311-1317.(in Chinese)何 杰,范以宁,邱金恒,等.Nb2O5/TiO2催化剂表面铌氧物种的分散状态和催化性能 [J].化学学报,2004,62(14):1311-1317.
[17] Fleszar B,Ploszynska J.An attempt to define benzene and phenol electrochemical oxidation mechanism [J].Electrochimica Acta,1985,30(1):31-42.

