酮洛芬醇质体的制备、表征及其体外经皮渗透研究
王小宁,冯锁民,张存劳
(西安医学院 药学院,陕西 西安 710021)
酮洛芬属苯丙酸类非甾体抗炎药,在临床上主要用于治疗各种关节炎、术后疼痛及慢性癌痛等。但酮洛芬难溶于水,口服会对胃肠道有刺激作用,表现为消化道的溃疡、恶心、呕吐等不良反应。为避免上述不良反应,对酮洛芬的非口服剂型研究已经受到越来越多的关注[1-3]。其中,经皮给药制剂可以避免胃肠道副作用和首过效应,提高局部药物浓度,具有使用方便、可随时中断给药及缓控释等诸多优点而受到了广泛关注。醇质体是一种新型经皮给药制剂,由磷脂、高比例乙醇、水组成,具有脂质体双分子层结构,易于变形,流动性较高,可促进药物穿透皮肤吸收[4]。本论文制备酮洛芬醇质体,对其体外经皮渗透特性进行考察,为研制酮洛芬较好的经皮吸收制剂奠定基础。
1 实验部分
1.1 材料与仪器
酮洛芬原料药、卵磷脂、胆固醇均为医药级;甲醇,色谱级。
HJ-2 双头磁力加热搅拌器;S-450D 型探针式超声仪;ALC-210.4 型电子天平;KQ3200E 型超声波清洗器;PYJ-6B 型透皮扩散试验仪;Delsa Nano C Zeta 电位分析仪型;Agilent1260 型高效液相色谱仪。
1.2 实验方法
1.2.1 酮洛芬醇质体的制备 称取酮洛芬于80 mL烧杯中,加无水乙醇使其完全溶解,称取卵磷脂于烧杯中,密封,超声,使卵磷脂溶解,在密封条件下,将其置于磁力搅拌器上,缓缓加入pH=7.0 的磷酸盐缓冲液,继续搅拌30 min,过0.22 μm 滤膜,即得。
1.2.2 酮洛芬脂质体的制备 称取卵磷脂与胆固醇(2∶1)置茄形瓶中,加入适量氯仿溶解,再加入以甲醇溶解的酮洛芬溶液,混合均匀,45 ℃恒温水浴中旋转蒸发溶剂至形成薄膜后,取PBS(pH 7.0)加入薄膜中,振摇直至将膜全部洗下,再置于25 ℃水浴中旋转水化30 min,即得。
1.2.3 酮洛芬乙醇溶液的制备 精密称取酮洛芬0.12 g,加30 mL 无水乙醇使其溶解,置于100 mL容量瓶中,纯化水定容至刻度,即得。
2 结果与讨论
2.1 酮洛芬含量测定方法
2.1.1 色谱条件 Agilent HC-C18(2)(4.6 mm ×150 mm,5 μm),流动相:甲醇-0.05 mol/L 磷酸二氢钾(55 ∶45),柱温25 ℃,检测波长258 nm,流速1.0 mL/min,进样量20 μL。
2.1.2 标准曲线的绘制 精密称取酮洛芬0.05 g,加甲醇使其溶解并定容至100 mL。精密吸取供试液0.1,0.3,0.6,1.2,1.8,2.4 mL 分别于100 mL 容量瓶中,甲醇定容至刻度,即得浓度分别为0.50,1.50,3.00,6.00,9.00,12.00 μg/mL 的对照液,按2.1.1 节下的色谱条件测其峰面积。以浓度C 为横坐标,峰面积A 为纵坐标绘制标准曲线。标准曲线方程为:Y=59.858X+15.556,R2=0.999 9,表明酮洛芬在0.50 ~12.00 μg/mL 浓度范围内线性关系良好。
2.1.3 精密度实验 取2.1.2 节下的同一浓度的酮洛芬溶液(9.00 μg/mL),按照2.1.1 节色谱条件测定,连续进样6 次,计算RSD 值为1.8%,表明精密度良好。
2.1.4 稳定性实验 取2.1.2 节下的同一浓度的酮洛芬溶液(9.00 μg/mL),分别在0,1,2,3,6,12 h,按照2.1.1 节下的色谱条件进样测定,计算RSD 值为3.1%,表明在12 h 内稳定性良好。
2.1.5 加样回收率实验 ①空白醇质体的制备:量取无水乙醇于烧杯中,称取卵磷脂,密闭条件下在超声清洗器中超声溶解后将其置于磁力搅拌器上,密封条件下缓缓加入pH=7.0 的磷酸盐缓冲液,继续搅拌30 min,过0.22 μm 滤膜,即得。②加样回收率的测定:精密吸取2.1.2 节下的对照液0.3,1,2 mL 分别于100 mL 容量瓶中,分别加0.5 mL 空白醇质体,甲醇稀释至刻度,按2.1.1 节下给定的色谱条件测定,结果见表1。
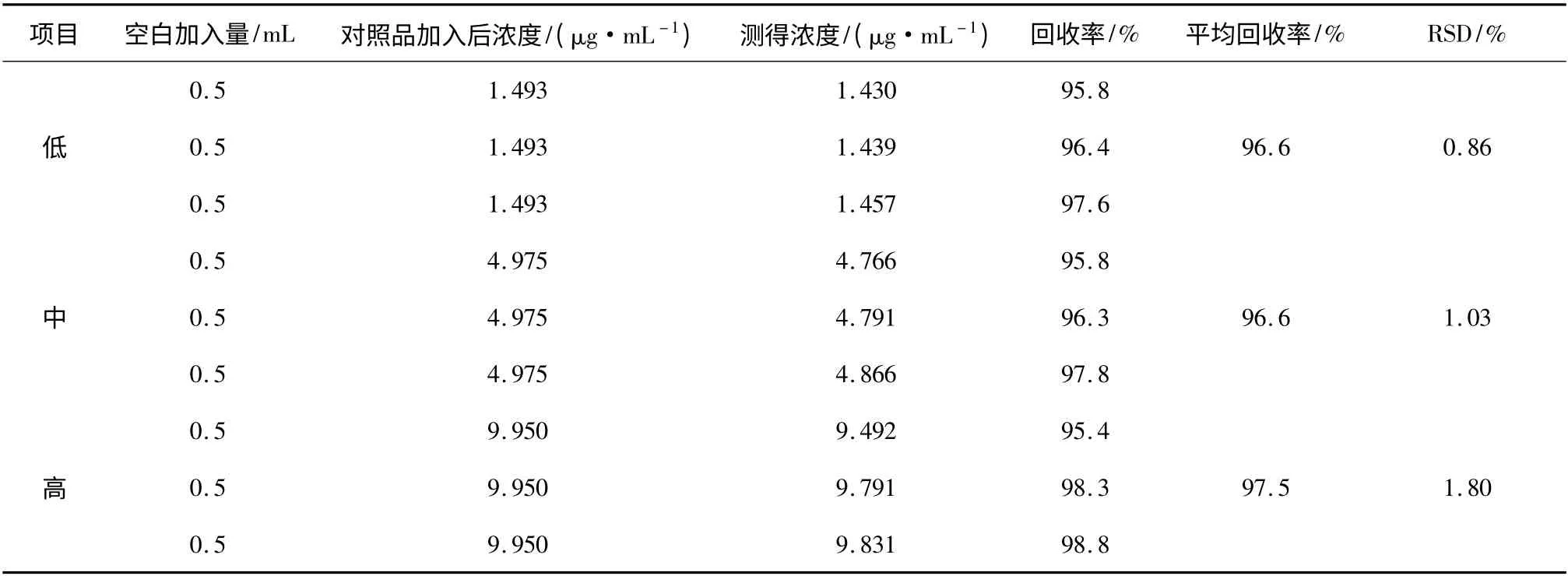
表1 加样回收率实验Table 1 Results of the sample recovery tests
由表1 可知,在低、中、高浓度测得的回收率分别为(96. 6 ± 0. 86)%,(96. 6 ± 1. 03)%,(97. 5 ±1.8)%。表明回收率良好。
2.2 粒径、Zeta 电位值及包封率的测定
酮洛芬醇质体和脂质体的粒径及Zeta 电位值由激光散射粒径分析仪测得,粒径分布见图1。包封率采用透析法测定:分别移取酮洛芬醇质体,酮洛芬脂质体2 mL 于透析袋中,将其放入含200 mL 的磷酸盐缓冲液(pH =7.0)的烧杯中,于磁力搅拌器上,20 h后取样,按照2.1.1 节下的色谱条件测定游离药物,按照下列公式计算其包封率。
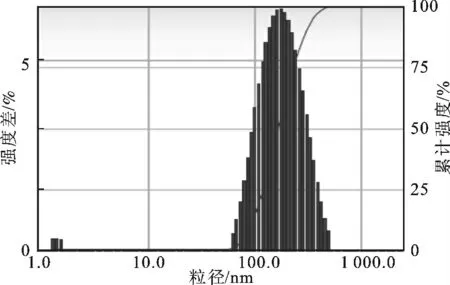
图1 酮洛芬醇质体的粒径及粒径分布图Fig.1 Particle size and size distribution of ketoprofen ethosomes

式中,W游为游离药物浓度,W总为药物总浓度。
醇质体与脂质体的Zeta 电位值、包封率结果见表2。由表2 可知,酮洛芬醇质体的粒径分布窄(PDI=0.17),粒径[(166.03 ±0.24)nm]显著小于脂质体(218.70±0.36),这可能是由于高比例的乙醇引起,乙醇可以改变体系表面电荷,增加醇质体的空间稳定性,从而使粒径减少。醇质体粒径小的特点有助于其进行深层经皮渗透。酮洛芬醇质体和脂质体的包封率由透析法测定,分别为(67.87 ±0.95)%和(94.50±0.26)%,这可能是由于醇质体中加入乙醇使膜的流动性和渗透性增加,从而使包封率下降。

表2 酮洛芬不同载体粒径、PDI、Zeta 电位值与包封率Table 2 Particle size,PDI,Zeta potential and encapsulation efficiency of different carrier
2.3 体外透皮实验
2.3.1 离体小鼠皮的准备 断颈法处死小白鼠,由背底部开始,沿背部纵向用手术剪剪开小鼠背部皮肤,并环绕剪开,剥离小鼠皮肤后,剪去多余皮毛,除去其皮下组织,用刀片将剥离下的皮肤皮毛刮干净,清水冲洗后再用少量生理盐水清洗,并将处理好的小鼠皮放于生理盐水中,4 ℃冰箱保存,24 h 内使用。
2.3.2 体外透皮实验 吸取6.5 mL 接受液于接受池中,用手术剪将已处理好的小鼠皮剪成适量大小,固定于供给室和接受池之间(注意使皮肤表层面向供给室,皮肤内侧面向接受室);分别量取酮洛芬乙醇溶液,酮洛芬脂质体、酮洛芬醇质体各2.5 mL 于供给室,将接受池置于恒温水浴(32 ℃)中,开启磁力搅拌器(200 r/min)。分别于0,0.5,1,2,3,5,7,9,12 h 取出0.2 mL 接收液,并及时补充等量恒温的接收液。12 h 后,将皮肤取出并用纯化水擦拭干净,滤纸吸干皮肤多余水分,剪碎皮肤,用适量甲醇超声,将取得的样品分别对应放入标记好的弹头试管中,经处理后,按照2.1.1 节下的色谱条件测其药物浓度,并根据下列公式计算累计渗透量(Q)。
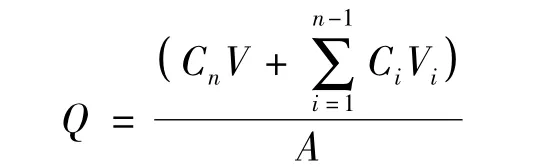
Cn:不同取样点时的接收液浓度;Ci:取样点时取样液浓度;V:接受池体积(mL);Vi:取样体积(mL);A:扩散面积(cm2)。
经皮渗透12 h 后,酮洛芬脂质体、醇质体和乙醇溶液的累计渗透量结果见图2 和表3。
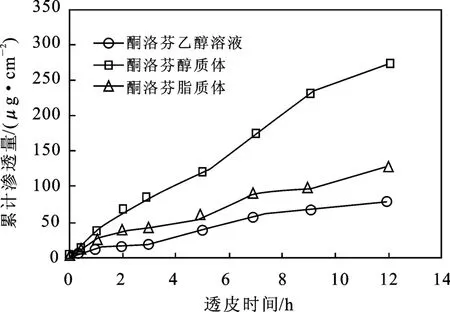
图2 体外透皮实验Fig.2 Results of in-vitro percutaneous experiment
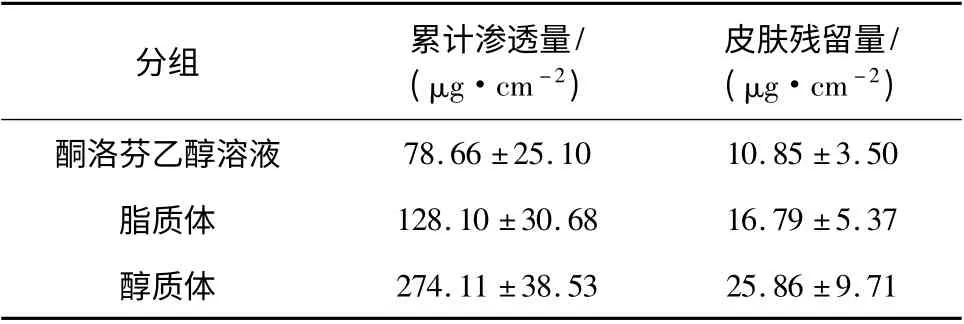
表3 12 h 后三种制剂的累计渗透量和皮肤滞留量Table 3 The cumulative permeation amount and skin retention of three formulations after 12 h
由图2 和表3 可知,经皮渗透12 h 后,皮肤累计渗透量由高到低依次为:酮洛芬醇质体>酮洛芬脂质体>酮洛芬乙醇溶液。醇质体组的累计渗透量[(274.11 ±38.53)μg/cm2]显著高于脂质体和乙醇溶液组[(78.66±25.10)μg/cm2](P <0.05),但是脂质体组[(128.10 ±30.68)μg/cm2]和乙醇溶液组间并无显著性差异(P >0.05)。醇质体组的皮肤滞留量也高于脂质体组和乙醇溶液组,说明酮洛芬醇质体与脂质体相比,表现出了更好的经皮渗透效果。
3 结论
醇质体的促进皮肤吸收机理目前仍不是很明确,但普遍认为与乙醇的加入有关。可能是因为乙醇改变了角质层的排列而增加了脂质分子的流动性,也可能是因为醇质体在经皮传递过程中发生了变形,从而通过紊乱的角质层[5]。与普通脂质体相比,醇质体具有更好的包封率,穿透皮肤角质层也显著提升,但是乙醇浓度过高会破坏醇质体的囊泡结构,对醇质体的形成不利,研究表明,当醇质体中乙醇的含量为30%时,制备的药物包封率最高[6]。
醇质体的粒径对其在体内的行为有很大的影响,通常认为粒径小于300 nm 的载体才能更容易地将药物输送到皮肤深部[7]。Zeta 电位值也可以衡量醇质体的稳定性,已有文献表明,醇质体因为乙醇的加入而带负电荷,故醇质体对阳离子型药物的包封率较高[8]。
醇质体包封率的测定方法一般有透析法和超速离心法。本论文采用透析法,避免了超速离心过程中因强大的能量引起的脂质变形破裂造成的药物流失[9]。醇质体在贮存期间,包封率可能发生变化,这与醇质体的稳定性有关,时间过长可能因乙醇的挥发导致卵磷脂的析出致使药物泄露。因此可以进一步制成凝胶制剂来改善醇质体的稳定性,同时可加入适量的胆固醇增加膜的硬度,从而增加醇质体的稳定性,减低药物的泄漏率[10]。关于酮洛芬醇质体的稳定性影响因素及透皮吸收的机制还需进一步的研究。
[1] 陈琰,胡晋红,范国荣,等. 酮洛芬的制剂研究[J]. 药学进展,2001,15(4):219-223.
[2] 孙华君,胡晋红,朱全刚.脂质体对酮洛芬体外透皮特性的影响[J]. 第二军医大学学报,1999,20(6):371-373.
[3] 胡晋红,钱俊,全山从,等. 酮基布洛芬片退热栓的试制与临床应用[J].现代应用药学,1991,8(6):28-31.
[4] 李欣蔚,林华庆,卜水. 经皮给药新型脂质体-醇质体[J].中国药师,2009,12(12):1726-1728.
[5] Dayan N,Touitou E.Carriers for skin delivery of trihexyphenidyl HCL:ethosomes vs liposomes[J]. Biomaterials,2000,21(18):1879-1885.
[6] 施晓琴,赵继会,王志东,等. 醇质体在经皮给药方面的应用[J]. 中国实验方剂学杂志,2013,19(12):352-355.
[7] Verma D D,Verma S,Blume G,et al.Particle size of liposomes influences dermal delivery of substances into skin[J].Int J Pharm,2003,258:141-151.
[8] 安珂瑶,孙勇. 醇质体的研究进展[J]. 中国药房,2011,22(5):463-465.
[9] 祝伟伟,翟光喜,赵军.醇质体的研究进展[J].食品与药品,2007,9(01A):46-49.
[10]杨飞,李芳,焦海胜,等. 秋水仙碱醇质体凝胶的制备及质量控制[J].中国药房,2009,20(1):50-52.
——有效的抗弓形虫药物靶标

