新型油酸基咪唑啉酰胺对A3碳钢的缓蚀性能研究
张 磊,项玉芝,周玉路,夏道宏
(1.中国石油大学(华东)理学院,山东 青岛 266580; 2.中国石油大学(华东)重质油国家重点实验室)
新型油酸基咪唑啉酰胺对A3碳钢的缓蚀性能研究
张 磊1,2,项玉芝1,2,周玉路1,2,夏道宏2
(1.中国石油大学(华东)理学院,山东 青岛 266580; 2.中国石油大学(华东)重质油国家重点实验室)
针对高酸原油加工中分馏塔顶循环回流(简称顶循)系统腐蚀加剧的现状,对自合成的新型油酸基咪唑啉酰胺(EYP)的缓蚀性能进行了研究。采用失重法评价缓蚀剂EYP在模拟顶循油体系中的缓蚀性能,考察了EYP的添加量和腐蚀体系温度对其缓蚀效率的影响,并采用电化学方法对缓蚀机理进行了探讨,采用SEM对碳钢表面的腐蚀形貌进行了分析。结果表明:EYP在顶循油模拟体系中对A3碳钢具有优良的缓蚀性能;随着腐蚀体系中EYP添加量的增大,缓蚀效率先增大然后略有降低;温度对EYP的缓蚀效率影响较小,随着温度升高,EYP的缓蚀效率略有降低; EYP在金属表面的吸附包括化学吸附和物理吸附,呈一种有序化的状态;EYP是一种能同时抑制阴极和阳极反应的高效“混合型缓蚀剂”。
油酸基咪唑啉酰胺 缓蚀性能 A3碳钢 分馏塔 顶循环回流

图1 油酸基咪唑啉酰胺的分子结构
1 实 验
1.1 主要仪器及试剂
仪器:美国Gamry公司生产的Gamry Reference-600电化学工作站;日立S-4800型冷场发射扫描电镜;上海雷磁PHS-3C型pH计;常压静态腐蚀试验装置。
试剂:盐酸、苯酚(phOH)、氨水、无水乙醇、丙酮等,均为分析纯。
1.2 腐蚀速率测定
采用失重法测定腐蚀速率。试验用钢片为A3碳钢,尺寸为50 mm×13 mm×1.5 mm,化学组成(质量分数)为:C 0.14%~0.22%,Mn 0.30%~0.65%,P低于0.045%,Si低于0.03%,余量为Fe。试片采用400#~800#的砂纸逐级打磨,经丙酮、无水乙醇清洗后用冷风吹干,放在干燥器中恒重30 min后称重(精确到0.000 1 g);将试片悬挂在空白及含有缓蚀剂的腐蚀介质中,在一定温度下浸泡一定时间。取出试片,立即用自来水洗净,用软毛刷刷洗;再用丙酮、无水乙醇冲洗,然后用冷风吹干,放入干燥器中约30 min后称量(准确到0.000 1 g),记录钢片表面的腐蚀情况。根据试片的失重量计算试片的腐蚀速率和缓蚀剂的缓蚀效率(IE)。IE的计算式如下:
(1)
式中,Vcor和Vinh分别表示空白和加有缓蚀剂的腐蚀介质中钢片的腐蚀速率,g/(m2·h)。
1.3 腐蚀机理分析
采用电化学法研究腐蚀机理。电化学测试采用三电极体系,工作电极采用A3碳钢,用环氧树脂封住,余横截面1 cm2为研究表面;辅助电极为铂电极;参比电极为Ag/AgCl电极。工作液为0.1 mol/L HCl-0.02 mol/L phOH-H2O溶液,测试温度为25 ℃。极化曲线测试的扫描速率为10 mV/s,扫描电位为-2 000~1 000 mV;交流阻抗施加的交流信号幅度为±10 mV,从高频到低频扫描,扫描频率为0.1~105Hz,采用对数扫频。
1.4 腐蚀形貌分析
采用冷场发射扫描电镜对碳钢表面的腐蚀形貌进行分析,加速电压为25 kV。
2 结果与讨论
2.1 EYP的缓蚀性能评价
为了建立与分馏塔顶循系统相一致的腐蚀环境,首先对分馏塔顶循系统腐蚀的原因进行了考察,发现氯化氢、硫化氢、氨及酚类化合物等是造成分馏塔顶循系统腐蚀严重的主要原因;分馏塔顶循油品的水溶性酸碱分析结果一般为pH 5.0~6.8[6-7]。
2.1.1 EYP添加量对缓蚀效率的影响 选取0.1 mol/L HCl-0.02 mol/L phOH-H2O体系作为腐蚀环境,用氨水将其pH调节至5.65,以醇类化合物将EYP溶解加入到上述腐蚀体系中,在腐蚀温度为90 ℃、腐蚀时间为8 h的条件下,考察缓蚀剂EYP添加量对缓蚀效率的影响,结果见图2。由图2可以看出,随着EYP含量的增大,缓蚀效率呈先升高后降低的变化趋势,当EYP质量分数为100 μg/g时,缓蚀效率达到最大值(79.04%)。推测产生该现象的原因为EYP分子吸附模式的改变[8],当EYP质量分数为0~100 μg/g时,带有长的烃基支链的EYP分子在碳钢表面的吸附为平行吸附模式[9],取代了碳钢表面的水分子,并且使碳钢表面的活性位点减少;EYP的含量越高,吸附在碳钢表面的EYP分子就越多,碳钢表面被保护的面积越大,因此缓蚀效率越高。然而,当EYP质量分数大于100 μg/g时,EYP分子间的相互排斥力更加明显,此时带有长的烃基支链的EYP分子的吸附方式倾向于垂直吸附,相比于平行吸附,垂直吸附的覆盖面积小[10],使碳钢表面受保护的面积变小,因此缓蚀效率略有降低。

图2 EYP添加量对缓蚀效率的影响
2.1.2 温度对缓蚀效率的影响 在EYP质量分数为100 μg/g、腐蚀时间为8 h的条件下,考察0.1 mol/L HCl-0.02 mol/L phOH-H2O腐蚀体系温度对EYP缓蚀效率的影响,结果见图3。 由图3可以看出,随着温度的升高,EYP的缓蚀效率逐渐降低,这与大多数缓蚀剂受温度影响的规律一致,这主要是由于温度升高时,腐蚀介质对碳钢的腐蚀速率加快,缓蚀剂在碳钢表面的脱附速率也加快[11],因此,缓蚀效率会有一定程度的下降。但EYP的缓蚀效率受温度的影响相对较小,在温度升至100 ℃时,缓蚀效率仍可达到74.86%。
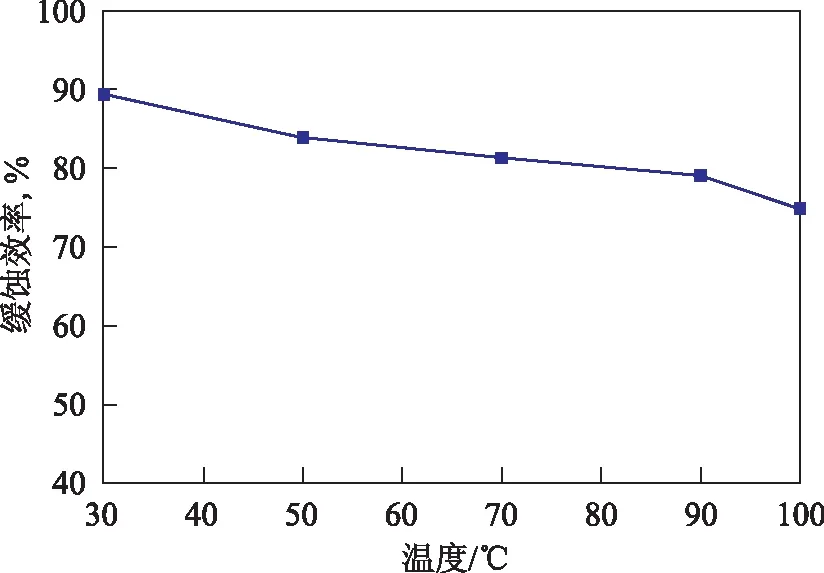
图3 腐蚀体系温度对缓蚀效率的影响
2.1.3 不同缓蚀剂在顶循油模拟体系中的缓蚀效果 选取200 μg/g HCl-100 μg/g phOH-100 μg/g (NH4)2S-白油体系模拟顶循油的腐蚀环境,采用醇类将不同缓蚀剂溶解后加入其中,加入量(w)为100 μg/g,腐蚀温度为90 ℃,腐蚀时间为8 h,并加以搅拌(转速为500 r/min),不同缓蚀剂的评价结果见表1,其中EYM为引入酰基前EYP合成的中间产物,NJZ为一种常用的效果较好的中和缓蚀剂。由表1可知,EYP的缓蚀效率高于EYM和NJZ,在顶循油模拟体系中具有良好的缓蚀效果。
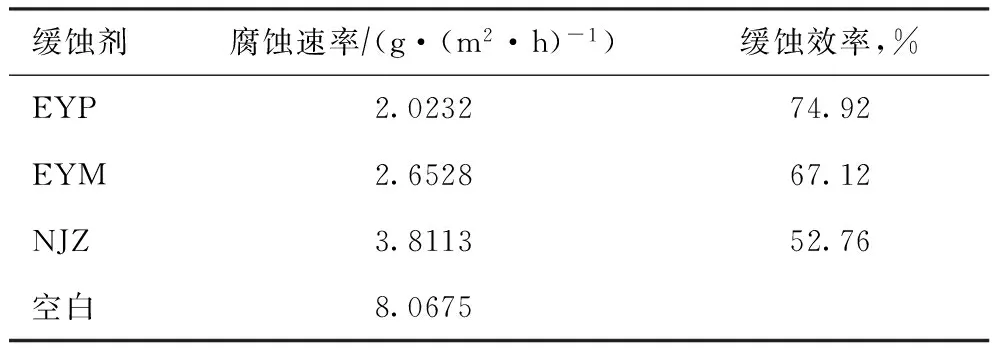
表1 不同缓蚀剂的缓蚀性能比较
2.2 EYP的缓蚀机理研究
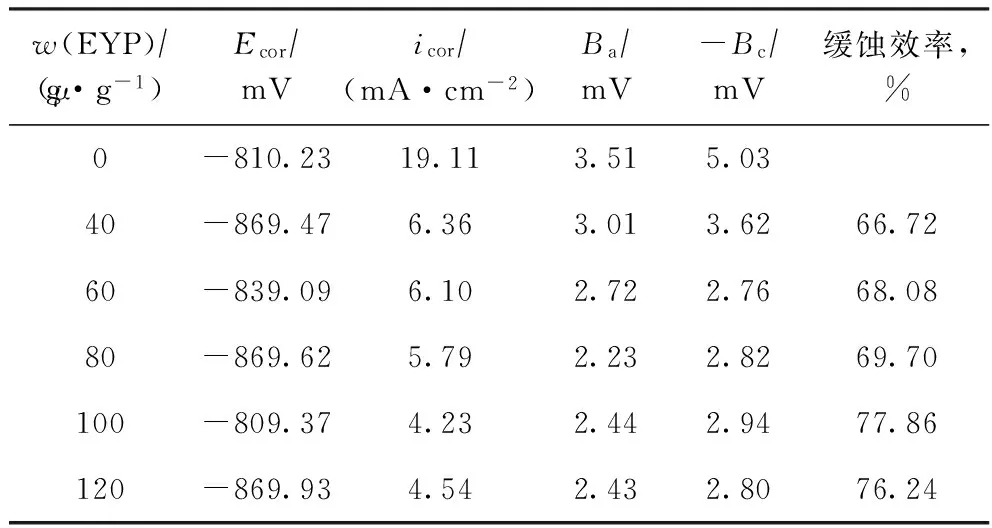
2.2.1 极化曲线法 图4是A3碳钢在不同浓度EYP的HCl/Cl-1-phOH-H2O体系(pH为5.65)中的极化曲线,表2是根据极化曲线拟合得到的电化学参数,其中,Ecor为自腐蚀电位,icor为自腐蚀电流密度,Ba为阳极塔菲尔斜率,Bc为阴极塔菲尔斜率。

图4 A3碳钢在HCl/Cl-1-phOH-H2O体系中的极化曲线w(EYP),%:■—0; ●—40; ▲—60; ; ◆—100; 图5同
表2 A3碳钢在HCl/Cl-1-phOH-H2O体系中的极化曲线参数
w(EYP)∕(μg·g-1)Ecor∕mVicor∕(mA·cm-2)Ba∕mV-Bc∕mV缓蚀效率,%0-810.2319.113.515.0340-869.476.363.013.6266.7260-839.096.102.722.7668.0880-869.625.792.232.8269.70100-809.374.232.442.9477.86120-869.934.542.432.8076.24
由图4和表2可知,腐蚀体系中加入EYP缓蚀剂后,自腐蚀电位变化不大,变化量小于85 mV[12],说明缓蚀剂同时抑制阳极以金属溶解为主的氧化反应和阴极以析氢为主的还原反应,因此该缓蚀剂属于混合型缓蚀剂。加入EYP后,阴、阳两极极化曲线均向低电流方向移动,腐蚀电流密度明显降低。在EYP的质量分数为0~100 μg/g时,随着EYP含量的增加,腐蚀电流密度逐渐减小,缓蚀能力增强;当EYP质量分数增大到100 μg/g时,腐蚀电流密度最小,缓蚀效率达到最大值;EYP含量继续增大时腐蚀电流密度会略有增大,缓蚀效率略有降低。加入EYP后,腐蚀电位变化较小,说明该缓蚀剂的作用机理为“几何覆盖效应”,即EYP或其反应产物吸附在试片表面上,在吸附粒子覆盖的表面区域,吸附粒子起着阻挡层的作用,阻碍了腐蚀过程的阳极反应和阴极反应,这就使得钢片表面上的实际反应面积缩小,腐蚀速率降低[13-16]。
从动电位扫描极化曲线得到的结论与腐蚀失重实验的结论是相吻合的,两者的微小差别可能是因为用失重法评价缓蚀效率是基于静态的平均腐蚀速率值,而用极化曲线评价缓蚀效率是基于动态的瞬时腐蚀速率值,另外,两种方法评价时的温度不同。


图5 A3碳钢在HCl/Cl-1-phOH-H2O体系中的交流阻抗谱图
采用Zview软件对该体系的交流阻抗谱以图6所示的等效电路进行拟合,解析结果见表3,其中Rs为电解质溶液电阻,Rt为电荷传递电阻,Cd为吸附电层电容。

图6 交流阻抗谱等效电路图
表3 A3碳钢在HCl/Cl-1-phOH-H2O体系中的交流阻抗谱参数

w(EYP)∕(μg·g-1)Rs∕(Ω·cm2)Cd∕(mF·cm-2)Rt∕(Ω·cm2)缓蚀效率,%016.461.342.134017.150.927.7472.486016.840.878.1473.838015.790.808.3274.4010016.100.7010.1679.0412013.710.618.5975.20
交流阻抗谱中容抗弧的半圆直径对应于电极反应电荷的传递电阻Rt,它可反映缓蚀效率的大小。由图5和表3可以看出,容抗弧呈现一定的不规则性,这种不规则与腐蚀过程中的电荷转移有关,说明在电腐蚀行为中固液两相的接触面处不平整[17-18]。在EYP质量分数为0~100 μg/g时,随着EYP含量的增加,容抗弧逐渐增大,对应的Rt增大,说明A3碳钢的腐蚀反应受到抑制,腐蚀速率减小,缓蚀效率升高;当EYP质量分数为100 μg/g时,容抗弧达到最大值,对应的Rt最大,此时的缓蚀效率最高;而当EYP质量分数继续增大到120 μg/g时,容抗弧略有减小,对应的Rt略有减小,说明此时缓蚀效率略有降低,这与失重法得到的规律一致。吸附电层电容Cd相比空白时则有不同程度的减小,这是因为该缓蚀剂分子在钢片表面发生了特性吸附,代替了尺寸小和介电常数高的水分子,使得界面电容减小[19]。
2.3 腐蚀动力学参数的计算
为了进一步探讨温度对EYP缓蚀效果的影响,根据Arrhenius方程[20]和过渡态方程计算相关的腐蚀动力学参数。Arrhenius方程为:
v=Ae-Ea/RT
(2)
式中:v为腐蚀速率;A为指前因子(也称频率因子);Ea为表观活化能;R为气体常数;T为温度。由式(2)可知,lgv对1/T作图可得一条直线,由该直线的斜率(-Ea/2.303R)可计算出表观活化能。
过渡态方程[21]为:
v=(RT/Nh)eΔS/Re-ΔH/RT
(3)
式中:N为Avogadro常量;h为Planck常量;ΔS和ΔH分别为金属溶解过程中的熵变和焓变。由式(3)可知,lgv/T对1/T作图可得一条直线,从该直线的斜率(-ΔH/2.303R)和截距[lg(R/Nh)+ΔS/2.303R]可分别计算出A3碳钢腐蚀过程中的焓变及熵变。
根据由失重法得到的数据计算腐蚀动力学参数,结果见表4。由表4可知,加入缓蚀剂EYP后,表观活化能Ea增大,说明金属腐蚀过程需要的能量更高了,金属溶解反应变得更加困难[22]。这可能是由于缓蚀剂EYP分子吸附在碳钢的表面,减少了碳钢表面和腐蚀介质间的相互作用,同时,Ea的增大也证明碳钢与缓蚀剂EYP之间存在着物理吸附作用[23-25],这与温度升高缓蚀效率降低得到的结论相吻合。焓变ΔH反映了金属溶解过程中所吸收的热量,ΔH>0说明金属溶解过程是吸热过程,据相关文献报道[26],ΔH<40 kJ/mol时为化学吸附,ΔH>40 kJ/mol时为物理吸附,表4中数据说明EYP在金属表面的吸附包含化学吸附,该化学吸附是通过EYP分子上的N原子和碳碳双键提供孤对电子与Fe原子提供空的d轨道形成共价键而产生的[27-29]。因此,EYP在碳钢表面的吸附包括物理吸附和化学吸附两种吸附类型。添加EYP前后ΔS均为较大的负值,表明金属在溶解的过程中,体系的混乱度呈降低的趋势,缓蚀剂EYP在A3碳钢表面的吸附呈一种有序化的状态。

表4 A3碳钢在HCl/Cl-1-phOH-H2O体系中的腐蚀动力学参数
2.4 碳钢表面腐蚀形貌分析

图7 A3碳钢在添加EYP前后的HCl-(NH4)2S-phOH-模拟油体系中的腐蚀形貌
3 结 论
(1) 随着腐蚀体系中EYP添加量的增大,缓蚀效率先增大然后略有降低;温度对EYP的缓蚀效率影响较小,随着温度升高,EYP的缓蚀效率略有降低。EYP在顶循油模拟体系中对A3碳钢具有较好的缓蚀效果。
(2) 采用电化学法对EYP的缓蚀机理进行研究可知,EYP为一种可以同时抑制阳极反应和阴极反应的“混合型缓蚀剂”。由碳钢表面的腐蚀形貌可知,加入EYP后能有效地抑制碳钢表面的腐蚀。
(3) 通过对腐蚀动力学参数进行计算可知,金属的溶解过程中焓变ΔH>0,EYP在金属表面的吸附包括化学吸附和物理吸附,呈一种有序化的状态。
[1] Foroulis Z A.Corrosion and corrosion inhibition in the petroleum industry[J].Materials and Corrosion,2004,33(3):121-131
[2] 黄本生,尹文锋,王小红,等.常减压蒸馏装置常用钢材在高温原油馏分中的腐蚀研究[J].中国腐蚀与防护学报,2013,33(5):377-382
[3] Zhang Kegui,Xu Bin,Yang Wenzhong,et al.Halogen-substituted imidazoline derivatives as corrosion inhibitors for mild steel in hydrochloric acid solution[J].Corrosion Science,2015,90(1):284-295
[4] Jevremovic I,Singer M,Nešic S,et al.Inhibition properties of self-assembled corrosion inhibitor tall oil diethylenetriamine imidazoline for mild steel corrosion in chloride solution saturated with carbon dioxide[J].Corrosion Science,2013,77(1):265-272
[5] Bilkova K,Gulbrandsena E.Kinetic and mechanistic study of CO2corrosion inhibition by cetyl trimethyl ammonium bromide[J].Electrochim Acta,2008,53(16):5423-5433
[6] 王玉洁.加工高酸原油常顶循系统腐蚀原因及缓蚀剂合成与筛选[D].青岛:中国石油大学(华东),2014
[7] 王雪.分馏塔顶循环回流油品腐蚀介质分析及缓蚀剂的筛选[D].青岛:中国石油大学(华东),2015
[8] Hackerman N,Justice D D,Mecafferty E. Homopiperazine as a corrosion inhibitor[J].Corrosion,1975,31(7):240-242
[9] 刘福国.油田钻具、管道系统腐蚀规律及缓蚀剂缓蚀性能和机制研究[D].青岛:中国海洋大学,2008
[10]Jiang Xiu,Zheng Yugui,Ke Wei.Effect of flow velocity and entrained sand on inhibition performances of two inhibitors for CO2corrosion of N80 steel in 3% NaCl solution[J].Corrosion Science,2005,47(11):2636-2658
[11]傅献彩,沈文霞,姚天扬,等.物理化学(下册)[M].北京:高等教育出版社,2006:368-369
[12]Ashassi-Sorkhabi H,Majidi M R,Seyyedi K.Investigation of inhibition effect of some amino acids against steel corrosion in HCl solution[J].Applied Surface Science,2004,225(4):176-185
[13]Ahmed A F,Hegazy M A.Synergistic inhibition effect of potassium iodide and novel Schiff bases on X65 steel corrosion in 0.5 mol/L H2SO4[J].Corrosion Science,2013,74(4):168-177
[14]Qian Bei,Wang Jing,Zheng Meng,et al.Synergistic effect of polyaspartic acid and iodide ion on corrosion inhibition of mild steel in H2SO4[J].Corrosion Science,2013,75(7):184-192
[15]Hu Junying,Zeng Dezhi,Zhang Zhi,et al.2-Hydroxy-4-methoxy-acetophenone as an environment-friendly corrosion inhibitor for AZ91D magnesium alloy[J].Corrosion Science,2013,74(4):35-43
[16]曹楚南.电化学阻抗谱导论[M].北京:科学出版社,2002:134-138
[17]Lebrini M,Lagrenée M,Vezin H,et al.Experimental and theoretical study for corrosion inhibition of mild steel in normal hydrochloric acid solution by some new macrocyclic polyether compounds[J].Corrosion Science,2007,49(5):2254-2269
[18]Najoua L,Mounim L,Fouad B,et al.Corrosion inhibition of carbon steel and antibacterial properties of aminotris-(methylenephosphonic) acid[J].Materials Chemistry and Physics,2010,119(3):330-336
[19]Noor E A.Potential of aqueous extract of hibiscus sabdariffa leaves for inhibiting the corrosion of aluminum in alkaline solutions[J].Journal of Applied Electrochemistry,2009,39(9):1465-1475
[20]Bentiss F,Lebrini M,Lagrenée M.Thermodynamic characterization of metal dissolution and inhibitor adsorption processes in mild steel/2,5-bis(n-thienyl)-1,3,4-thiadiazoles/hydrochloric acid system[J].Corrosion Science,2005,47(12):2915-2931
[21]Noor E A,Al-Moubaraki A H.Thermodynamic study of metal corrosion and inhibitor adsorption processes in mild steel/1-methyl-4[4’(-X)-styryl pyridinium iodides/hydrochloric acid systems[J].Materials Chemistry and Physics,2008,110(1):145-154
[22]Negm N A,Sabagh A M A,Migahed M A,et al.Effectiveness of some diquaternary ammonium surfactants as corrosion inhibitors for carbon steel in 0.5 mol/L HCl solution[J].Corrosion Science,2010,52(6):2122-2132
[23]Zhang Fan,Tan Yongming,Cao Ziyi,et al.Performance and theoretical study on corrosion inhibition of 2-(4-pyridyl)-benzimidazole for mild steel in hydrochloric acid[J].Corrosion Science,2012,61(8):1-9
[24]Ishtiaque A,Ragendra P,Quraishi M A.Thermodynamic,electrochemical and quantum chemical investigation of some Schiff bases as corrosion inhibitors for mild steel in hydrochloric acid solutions[J].Corrosion Science,2010,52(3):933-942
[25]Sanja M,Ivica S.Thermodynamic characterization of metal dissolution and inhibitor adsorption processes in the low carbon steel/mimosa tannin/sulfuric acid system[J].Applied Surfurce Science,2002,199(1/2/3/4):83-88
[26]印永嘉.物理化学简明教程[M].北京:高等教育出版社,2007:32-34
[27]Abdallah M.Rhodanine azosulpha drugs as corrosion inhibitors for corrosion of 304 stainless steel in hydrochloric acid solution[J].Corrosion Science,2002,44(4):717-728
[28]Liu Fang,Lü Yucui,Zhong Huiyun,et al.Laccase immobilized on mesoporous silica materials and its corrosion inhibition performance in circulating cooling water system[J].China Petroleum Processing and Petrochemical Technology,2015,17(4):8-19
[29]Xiong Sang,Sun Jianlin,Jiang Wei,et al.Study on surface adsorption and inhibition behavior of corrosion inhibitors contained in copper foil rolling oil[J].China Petroleum Processing and Petrochemical Technology,2015,17(1):96-107
INHIBITION PROPERTY OF OLEIC IMIDAZOLINE AMIDE FOR A3 MILD STEEL CORROSION
Zhang Lei1,2, Xiang Yuzhi1,2, Zhou Yulu1,2, Xia Daohong2
(1.CollegeofScience,ChinaUniversityofPetroleum(EastChina),Qingdao,Shandong266580;2.StateKeyLaboratoryofHeavyOilProcessing,ChinaUniversityofPetroleum(EastChina))
The corrosion inhibition performance of a newly synthesized oleic acid imidazoline amide (EYP) for the mild steel in overhead circulating reflux system of fractionation tower at different amount of EYP and system temperature was investigated by weight loss method. The surface morphologies of mild steel specimens were observed by scanning electron microscope (SEM). The electrochemical impedance spectroscopy (EIS) was used to study the corrosion mechanism. The results demonstrate that EYP can effectively protect A3 mild steel from corrosion in simulative top cycle oil. The inhibition efficiency of EYP increases firstly and then decreases mildly with the increase of EYP concentration, and the temperature changes only have slightly influence on the corrosion efficiency. EIS results and the calculated kinetic parameters reveal that the adsorption of EYP on the steel surface includes physical adsorption and chemical adsorption, showing an ordering state, and that EYP is a mixed-type inhibitor retarding reactions on anodic or cathodic electrode.
oleic acid imidazoline amide; corrosion inhibition property; A3 mild steel; fractionation tower; overhead circulating reflux system
2015-09-23; 修改稿收到日期:2016-01-20。
张磊,硕士研究生,主要研究方向为石油精细化工、腐蚀与防护。
项玉芝,E-mail:xiangyzh@163.com。

