SDP法制备碳纳米管-TiO2纳米复合光催化剂及降解喹啉
崔佳丽, 高永华, 高利珍
(太原理工大学 环境科学与工程学院,山西 太原030024)
SDP法制备碳纳米管-TiO2纳米复合光催化剂及降解喹啉
崔佳丽,高永华,高利珍
(太原理工大学 环境科学与工程学院,山西 太原030024)
针对溶胶凝胶法制备光催化剂过程中颗粒分散不均匀、易团聚的问题,采用SDP(Spinning disk process)联合溶胶凝胶法制备不同焙烧温度的多壁碳纳米管(MWCNTs)-TiO2光催化剂。通过XRD、FTIR、SEM、TEM表征样品的微观结构和形貌,利用UV-vis DRS(Ultraviolet visible diffuse reflectance spectra)表征其可见光响应性,并考察样品在可见光下降解喹啉的性能。结果表明,SDP联合溶胶凝胶法能够以连续流形式制备更微小的、分散更均匀的光催化纳米颗粒(晶粒尺寸约为10 nm);MWCNTs以光敏化剂的形式使样品具有可见光响应, 450 ℃下焙烧得到的光催化剂MCT3有最强的可见光吸收和最佳的催化活性,反应时间为180 min时,喹啉降解率为86.6%。
SDP; 可见光; 光催化剂; 喹啉
1 前言
光催化作为高级氧化技术(Advanced oxidation processes(AOPs))的一种,因其可产生羟基自由基,将有机物矿化为CO2和H2O[1],在环境、化学、材料等交叉学科引起了研究热潮[2]。TiO2光催化剂一直以来存在的问题是,TiO2通常对紫外光才具有响应,而这部分只占到太阳总发射能量的5%左右,因此使TiO2光催化剂向可见光方向拓展是目前的研究热点。已有不少研究表明,碳的掺杂[3-6]对于TiO2的可见光响应起到了一定的作用,但存在TiO2分布不均匀,可见光活性不高,制备过程复杂,不易于批量化生产等问题。众多碳质材料当中,碳纳米管的特殊电子结构,良好的吸附能力,较强的机械稳定性及热稳定性,使其成为研究热点之一。TiO2是n型半导体,其光催化过程主要是由光子的吸收,电子-空穴产生,而碳纳米管表面的原子配位不全,导致表面的活性点增加,因此TiO2的光催化作用可以通过引入碳纳米管得以提高[7]。
TiO2复合纳米光催化剂的制备方法有多种,包括溶胶-凝胶法、CVD法、喷雾热解法,但存在着耗时、反应时间长及蒸发等问题。目前报道的碳纳米管和TiO2复合催化剂最常用的制备方法是用溶胶-凝胶法,其优点是反应条件温和,产物纯度高。而此法在制备过程中,可能出现多种问题,包括纳米TiO2颗粒不易附着到碳管壁表面而自身团聚;高温处理带来不可避免的颗粒团聚,从而不利于CNTs和TiO2之间的电子传递;TiO2过度包覆CNTs,使其对于外界光源的响应率低下;反应过程通常要求1滴/s的缓慢速率滴加,反应耗时长等。
此外,热处理温度对催化剂活性也有较大影响,如焙烧会影响晶粒的大小,焙烧温度过高则会使碳被氧化形成CO2,CO等脱离样品,因此适宜的温度对于复合光催化剂的形成至关重要。Xu等[3]发现焙烧温度较低,产物的含碳量增多,主要以不定型炭形式存在,碳阻碍了TiO2对光的吸收,而在高温下碳进入TiO2晶格内部增强了催化剂产生的光电流,但温度过高存在着碳被氧化分解的可能,不能起到掺碳的作用。Xiao等[8]以 C2H6O2和 C6H8O7为碳源,利用溶胶凝胶自燃烧方法,研究了不同的焙烧温度对表明羟基自由基·OH以及C-TiO2光催化活性的影响,发现600 ℃焙烧时,样品单位面积的·OH含量更多,活性最佳。
为了克服制备过程中TiO2分布不均匀,可见光活性不高,制备过程耗时长等不足,笔者利用SDP(Spinning disc process)联合溶胶凝胶法,使MWCNTs(MWCNTs)与TiO2前驱物快速、均匀混合,以连续流的方式制备不同焙烧温度下MWCNT-TiO2复合光催化剂,对其性能进行表征分析,并考察其在可见光下降解喹啉的活性。
2 实验
2.1试剂
MWCNTs,外径约为20~40 nm,管长<2 μm; 钛酸四丁酯,成都市科龙化工试剂厂;浓硝酸,天津市科密欧化学试剂开发中心;乙醇,天津市富宇精细化工有限公司;乙酸,天津市化学试剂一厂;喹啉,南京化学试剂有限公司。
2.2MWCNT-TiO2纳米复合光催化剂的制备
MWCNTs预处理:为了去除不定型炭以及避免纳米颗粒之间相互团聚,首先将MWCNTs进行纯化。用质量浓度为69%的浓硝酸与去离子水通过离心的方法反复洗涤至pH为中性,之后置于干燥箱于80 ℃下烘干2 h。
MWCNT-TiO2纳米复合材料的制备:根据Raston[9]方法自制了旋转圆盘反应器(SDP),主要组成部分为(图1):直径为100 mm的可控速旋转圆盘(最大为3 000 r/min);进料口离转盘中心距离为5 mm。液体被注入至圆盘中心,在离心力的作用下,使液体分散形成液体薄膜。该法能够增加液体的传热和传质特性,加快反应速率,增加组分间的接触,使得反应停留时间缩短至数秒,有利于粒径更小的纳米颗粒的形成。这一方法可代替传统的化学批处理制备方法,为催化剂制备提供了连续流动态体系。该体系可以达到快速质传递的作用,并且转盘的快速旋转能产生薄膜(1~200 μm),有利于形成纳米颗粒。
将一定量纯化后的MWCNTs加入至40 mL的钛酸四丁酯中,之后分别加入100 mL乙醇,10 mL醋酸,超声振荡60 min,形成溶液A;烧杯中加入30 mL的乙醇,20 mL的无水乙酸以及8 mL去离子水,形成溶液B。将溶液A注入到进料管1,溶液B注入到进料管2,保持温度为30 ℃,3 000 r/min的旋转速度,使反应液形成薄膜,发生反应。注入完成后,停止转盘,生成的混合溶液通过排出口排出并收集至烧杯,室温下陈化24 h后形成凝胶。后在80 ℃烘干4 h,形成灰白色的粉末。得到的粉末分为3份,分别于350、400、450 ℃的温度在马福炉里焙烧4 h,得到MWCNT-TiO2复合材料,之后经过玛瑙研钵研磨,待测。3种样品分别记为MCT1,MCT2和MCT3(碳的质量分数为5%)。为了对比,纯TiO2亦通过相同方法制备,制备过程仅比上述MWCNT-TiO2的制备少了MWCNTs的加入。

图 1 旋转圆盘法(SDP)示意图
2.3MWCNT-TiO2复合光催化剂的表征
XRD测试: D/max 2500型X-射线粉末衍射仪测定样品的晶相组成(日本理学(Rigaku)公司),CuKα射线位为0.154 06 nm为射线源。FT-IR测试:将样品用溴化钾压片法在FTS-165-CDS-2000热解红外联用仪型(美国Bio-rad公司)上测试其红外光谱。SEM测试:在Philips XL30 SFEG型扫描电子显微镜上检测样品的形貌和微观结构。TEM测试: JEM2100F透射电镜(日本电子株式会社)。BET测试:TRISTAR II3020全自动比表面和孔隙分析仪(美国麦克默瑞提克公司)。UV-vis DRS: CARY-300紫外-可见分光光度计,测定固定催化剂的光吸收度(美国瓦里安)。
2.4MWCNT-TiO2复合光催化剂的活性测试
考察不同焙烧温度制备的MWCNT-TiO2纳米复合材料在可见光下降解喹啉的性能。反应器(图2)为双层中空圆筒,外层利用泵通入循环水以稳定由于光照引起的反应液温度的变化,用于模拟可见光的光源为镝灯(300 W),并经紫外线阻止滤膜过滤(滤掉390 nm以下的光)。喹啉初始质量浓度为50 mg·L-1,MWCNT-TiO2纳米复合材料投加量为0.2 g,反应温度为室温,在磁力搅拌和鼓风曝气双重作用下进行。反应开始前,遮光搅拌120 min,喹啉在催化剂表面达到吸附-脱附平衡;然后打开光源,每20 min取样,经8 000 r·min-1转速下离心分离,取上清液,利用紫外-可见分光光度计(UV-vis)在喹啉最大吸收波长313 nm处测定其吸光度变化,利用(1)式计算喹啉相对质量浓度ρ的变化率(Y):
(1)
式中:ρ0为喹啉初始浓度;ρ为每个取样点喹啉溶液的浓度。

图 2 光催化反应器示意图
3 结果与讨论
3.1MWCNT-TiO2纳米复合光催化剂的表征结果分析
图3为MWCNTS在空气气氛下的热重结果,由图可见,温度在350、400和450 ℃时,MWCNTs的失重率分别为0.08%、2.01%和9.20%,而当温度达到498.7 ℃时,MWCNTS出现明显的失重(失重率为54%),当温度达到540 ℃附近时,MWCNTs质量保持基本不变,说明MWCNTs已完全被氧化。因此,本实验对于MCT样品的焙烧温度保持在500 ℃以下,以保证MWCNTs在热过程中的稳定性。

图 3 MWCNTs在空气气氛中TG/DTG结果
图4、图5分别是纯TiO2,MCT1,MCT2和MCT3的SEM和TEM照片。从中可以看出MWCNTs的管状形貌,直径约为30 nm,纯TiO2的粒径范围为10~15 nm(图4(a),图5(a)),MCT2以及MCT3的粒径大约为5~10 nm(图5(c,d)。而MCT1中TiO2的负载量非常少(图4(b),5(b)),TEM能观察到的负载颗粒也明显比其他MCT2以及MCT3的粒径大(图5(b)。MCT2以及MCT3中MWCNTs表面包覆了大量分布均匀的TiO2颗粒层,外壁直径约由20~40 nm增粗至40~60 nm左右。利用扫描电镜在较大范围内观察,相比MCT1(如图4(b)和图5(b)),可以明显看出,MCT2和MCT3上TiO2纳米颗粒与MWCNTs表面的结合更为紧密(如图4(c,d)和图5(c,d)),说明适合的焙烧温度对于表明颗粒的分布有关键作用。MCT3的粒径分布图见图6,可以看出TiO2颗粒粒径主要集中分布在5~10 nm,分布均匀的TiO2颗粒层更有助于提高催化剂对有机物的降解率。
图7为TiO2,MCT1,MCT2和MCT3的XRD谱图。通过比对XRD谱图库(PDF Number: 73-1764),除了MCT1,纯TiO2,MCT2和MCT3都显示出较强的锐钛矿衍射峰,且样品中未发现金红石相。已有研究表明,温度高于600 ℃时,在2θ=27.4°处会出现金红石相TiO2的特征衍射峰,表明部分TiO2开始由锐钛矿相转变成金红石相[10]。相比而言,锐钛矿的畸变程度大,缺陷、位错较多,易于氧空位的产生,而金红石相经热处理过程后晶粒迅速长大,比表面积较小,TiO2对氧的吸附能力较差,光生电子和空穴对比较容易复合,导致催化活性降低;另外,它的导带位置比锐钛矿的低,使其氧化还原能力稍弱[11]。在350 ℃焙烧时的样品MCT1中,TiO2仍然是无定型态。根据锐钛矿在(101)晶面(2θ=25.46°)的半宽峰,通过Scherrer公式,计算得出晶粒尺寸。Scherrer方程如下:
d=Kλ/βcosθ
式中:d为晶粒的大小,K为晶粒的形状因子,一般取0.89,λ为X-射线波长,β为衍射峰的半高宽,θ为布拉格衍射角。

图 4 纯TiO2和MWCNT-TiO2的SEM照片((a)纯TiO2, (b)MCT1, (c)MCT2, (d)MCT3)

图 5 纯TiO2和MWCNT-TiO2的TEM照片((a)纯TiO2, (b)MCT1, (c)MCT2, (d)MCT3)

图 6 MCT3中TiO2颗粒的粒径分布图
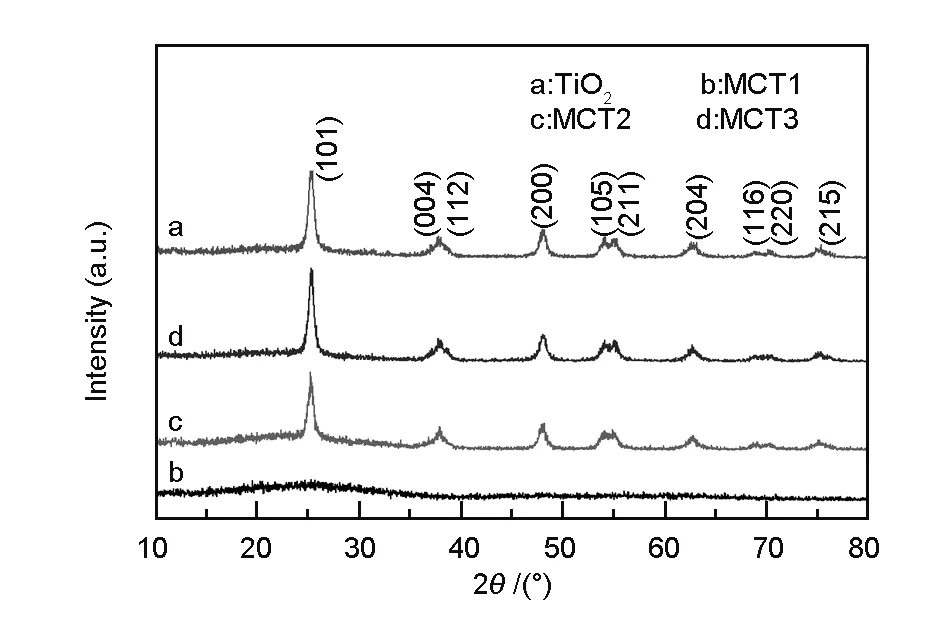
图7 MWCNT-TiO2复合光催化剂的XRD谱图
纯 TiO2,MCT2和MCT3复合物的晶粒尺寸分别约为8.20、10.26、10.41 nm。Wang等[12]研究了传统溶胶-凝胶法制得的不同MWCNTs复合量样品的晶粒参数,晶粒尺寸约为20 nm,比纯TiO2粒径(约30 nm)稍小。相比之下,笔者用SDP联合溶胶凝胶法制备的样品晶粒尺寸更小,更有利于光催化性能的发挥。此外,碳在2θ=26.7°的衍射峰由于与TiO2(101)峰交叠、掺杂量小低于仪器的检测限等原因并未显现,这一结论在其它文献中也得以证实[12, 13]。根据XRD表征结果得知,MWCNT-TiO2系列光催化剂的晶相组成与焙烧温度有很大关系。350 ℃焙烧后的MCT1为无定型态,说明样品中含有大量未水解的基团阻碍了催化剂的结晶化;MCT2和MCT3呈现锐钛矿相,且峰强度随着焙烧温度升高而加强。

图 8 (a)纯TiO2, (b)MCT1, (c)MCT2和(d)MCT3
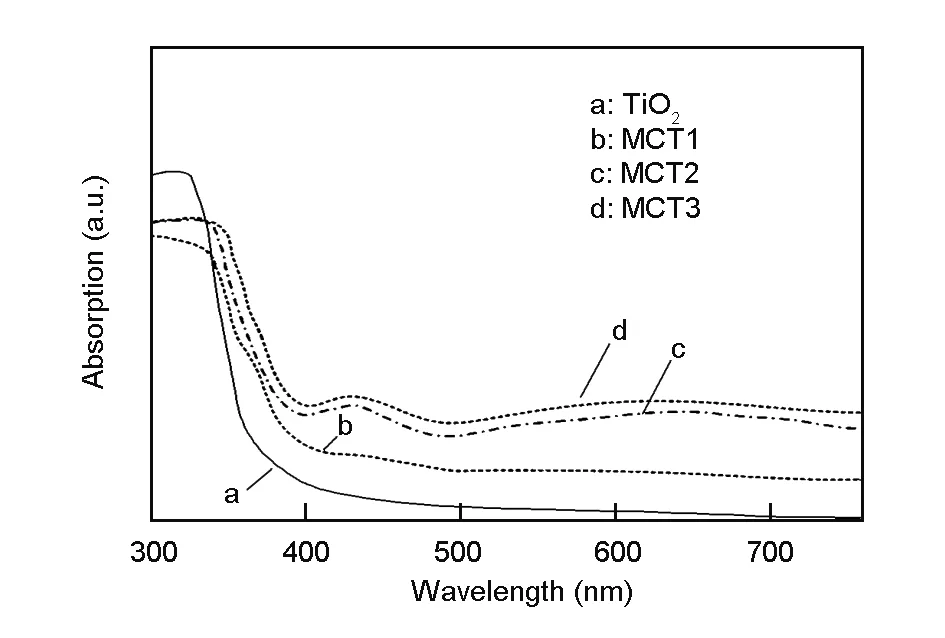
图 9 TiO2和MWCNT-TiO2样品的UV-vis DRS图谱
各样品的紫外-可见吸收光谱(UV-Vis DRS)见图9。所制备的TiO2和MWCNTs-TiO2复合催化剂在波长为300~750 nm区间均有一定的光吸收。TiO2在紫外光区(λ<400 nm)的吸收很明显。在350<λ<700 nm的光吸收范围内MWCNT-TiO2吸收强度明显大于TiO2样品,吸收边产生了红移,光谱响应范围向可见光区拓展,随着MWCNTs掺杂,MCT2和MCT3在可见光(λ>400 nm)的吸收比纯TiO2明显增强,且在420 nm附近处有最强吸收峰,这是由于MWCNTs的带隙较窄,能够在可见光照射下产生激发,掺杂了MWCNTs的复合催化剂,光谱吸收范围因其中MWCNTs的窄禁带吸收作用而拓宽到了可见光区而产生更高的光催化活性[19]。
3.2MWCNT-TiO2复合光催化剂的活性
图10和图11为MWCNT-TiO2复合光催化剂可在见光照射下降解喹啉和TOC的转化率。反应进行180 min,空白试验同时进行以作对照。从图10可以看出,喹啉浓度在不投加催化剂时,对于光照的影响基本可以忽略不计。MCT2和MCT3在前100 min降解迅速,降解率达到60%左右,直至反应180 min时,降解率分别为81.5%和86.6%;而MCT1降解缓慢,降解率最终为58%。MCT3显示出最高的可见光催化活性,其次为MCT2,MCT1和TiO2。TiO2在可见光下的降解率最低,主要由于纯TiO2对可见光的吸收很少(图9)。许多研究者也得出了类似的结论,Momeni等[20]制备了Co、WO3与TiO2复合光催化剂,在可见光照射下,未掺杂的TiO2对亚甲基蓝的降解率几乎为0,而WO3-TiO2, Co/TiO2及Co/WO3-TiO2均显示出不同程度的可见光活性;Wu等[21]研究了g-C3N4/C-TiO2复合光催化剂在可见光下的活性,反应150 min后,不同掺杂量的g-C3N4/C-TiO2复合材料对亚甲基蓝降解率均在95%以上,而纯TiO2的降解率非常低,约为2%;Momeni等[22]通过化学浴沉积法制备了TiO2纳米管及Pb/WO3-TiO2纳米管,纯TiO2纳米管在可见光下几乎无活性,而Pb/WO3-TiO2纳米管在照射60 min后,对亚甲基蓝降解率可达96%。

图 10 可见光下MWCNT-TiO2降解喹啉转化率
所制备样品MCT3,MCT2,MCT1和TiO2对于TOC的降解率在前120 min,与喹啉的降解率基本一致,但120 min之后,TOC去除率较喹啉降解率低,溶液中可能包括未被光催化的喹啉分子和中间产物,部分中间产物没有被进一步矿化。朱遂一等[23]采用P25薄膜光催化水中的喹啉时,TOC的降解率低于喹啉降解率,在转化过程中,产生比喹啉和异喹啉等中间产物,喹啉的降解率在氙灯照射2 h后达到97%。Jing等[24]利用静电吸引改性溶胶凝胶法制备了TiO2/氧化石墨烯复合材料 (TGO),结果表明,该材料在可见光下喹啉的降解率为75.56%。

图 11 喹啉溶液光催化降解TOC转化率
3.3机理分析
光催化活性的发挥取决于纳米颗粒的分散度,如颗粒-溶液的界面中表面活性位点,而这些会受催化剂形貌、粒径大小和及其颗粒间的相互作用所影响。经BET测试,TiO2、MCT1,MCT2和MCT3样品的比表面积分别为39.35、84.4、112.32、112.21 m2·g-1。MWCNTs大的比表面积,独特的中空结构使得负载TiO2后的复合颗粒的比表面积增大,可利用的活性位点增加,且提高了TiO2与有机物的接触,颗粒吸附有机物的可能性增大。


(2)
(3)
(4)
MWCNTs/TiO2+·OH+H+
(5)
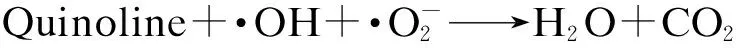
(6)
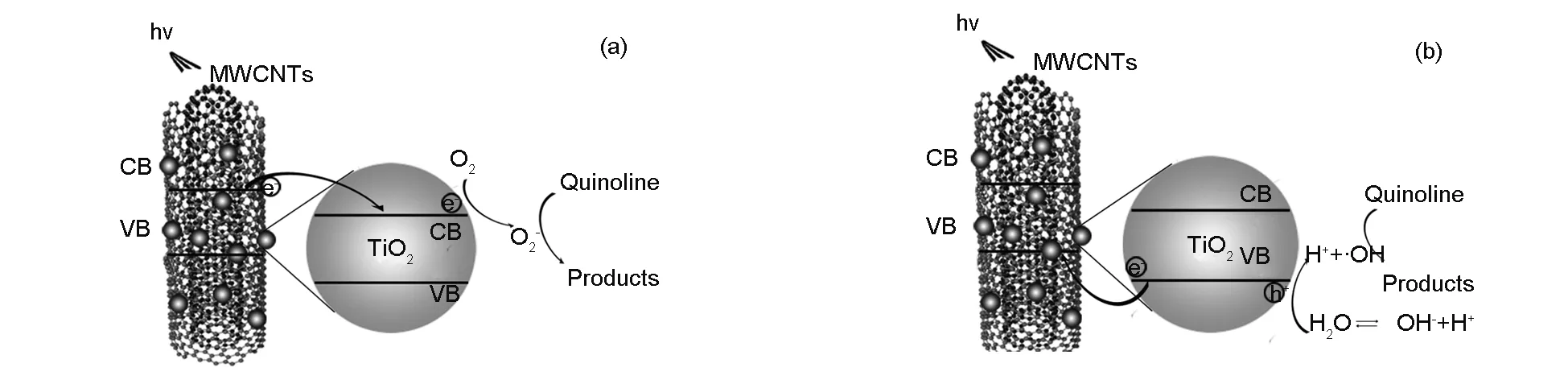
图 12 MWCNT-TiO2复合光催化剂的可见光降解喹啉机理示意图
4 结论
利用SDP联合溶胶凝胶法制备了不同焙烧温度形成的MWCNT-TiO2光催化剂。结果表明,相比传统的溶胶凝胶法,在良好的传质传热作用下,SDP能够使光催化剂形成分散更均匀的TiO2纳米颗粒。焙烧温度对复合光催化剂的可见光响应也有较大的影响。350 ℃焙烧形成的MCT1样品是无定形的,而400 ℃和450 ℃焙烧温度产生的催化剂活性更高。MWCNT-TiO2催化剂在可见光区域有明显的吸收,制得的MCT3有最强的可见光吸收和最佳的光催化活性,喹啉降解率为86.6%。碳的引入使得催化剂在可见光下具有光催化活性,且碳以光敏化剂的形式起作用。
[1]Hoffmann M R, Martin S T, Choi W, et al. Environmental applications of semiconductor photocatalysis[J]. Chem Rev, 1995, 95(1): 69-96.
[2]Forgacs E, Cserháti T, Oros G. Removal of synthetic dyes from wastewaters: a review[J]. Environ Int, 2004, 30(7): 953-971.
[3]Xu C K, Killmeyer R, Gray M L, et al. Enhanced carbon doping of n-TiO2thin films for photoelectrochemical water splitting[J]. Electrochem Commun, 2006, 8(10): 1650-1654.
[4]Dong F, Wang H, Wu Z. One-step “green” synthetic approach for mesoporous C-doped titanium dioxide with efficient visible light photocatalytic activity[J]. The Journal of Physical Chemistry C, 2009, 113(38): 16717-16723.
[5]Noworyta K, Augustynski J. Spectral photoresponses of carbon-doped TiO2film electrodes[J]. Electrochemical and Solid-State Letters, 2004, 7(6): E31-E33.
[6]Sakthivel S, Kisch H. Daylight photocatalysis by carbon-modified titanium dioxide[J]. Angewandte Chemie International Edition, 2003, 42(40): 4908-4911.
[7]An G M, Ma W H, Sun Z Y, et al. Preparation of titania/carbon nanotube composites using supercritical ethanol and their photocatalytic activity for phenol degradation under visible light irradiation[J]. Carbon, 2007, 45(9): 1795-1801.
[8]Xiao Q, Ouyang L L. Photocatalytic activity and hydroxyl radical formation of carbon-doped TiO2nanocrystalline: Effect of calcination temperature[J]. Chem Eng J, 2009, 148(2-3): 248-253.
[9]Chin S F, Iyer K S, Raston C L, et al. Size selective synthesis of superparamagnetic nanoparticles in thin fluids under continuous flow conditions[J]. Adv Funct Mater, 2008, 18(6): 922-927.
[10]Li M, He J. Synthesis and room-temperature ferromagnetism of porous V-doped rutile TiO2microspheres[J]. Mater Lett, 2016, 174: 48-52.
[11] 吴玉程, 宋林云, 刘晓璐,等. 碳纳米管负载纳米TiO2复合材料的制备及组织结构表征[J]. 功能材料, 2008, 3(39): 497-499.
(WU Yu-cheng, SONG Lin-yun, LIU Xiao-lu, et al. Preparation and characterization of carbon nanotubes-TiO2nanocomposites[J]. Journal of Functional Materials, 2008, 3(39): 497-499.)
[12]Wang H, Wang H L, Jiang W F, et al. Photocatalytic degradation of 2,4-dinitrophenol (DNP) by multi-walled carbon nanotubes (MWCNTs)/ TiO2composite in aqueous solution under solar irradiation[J]. Water Res, 2009, 43(1): 204-210.
[13]Zhang F J, Chen M L, Oh W C. Photoelectrocatalytic properties of Ag-CNT/ TiO2composite electrodes for methylene blue degradation[J]. New Carbon Mater, 2010, 25(5): 348-356.
[14]Brownson J R S, Tejedor-Tejedor M I, Anderson M A. Photoreactive anatase consolidation characterized by FTIR spectroscopy[J]. Chem Mater, 2005, 17(25): 6304-6310.
[15]Burgos M, Langlet M. The sol-gel transformation of TIPT coatings: A FTIR study[J]. Thin Solid Films, 1999, 349(1-2): 19-23.
[16]Huang Y, Ho W, Lee S, et al. Effect of carbon doping on the mesoporous structure of nanocrystalline Titanium dioxide and its solar-light-driven photocatalytic degradation of NOx[J]. Langmuir, 2008, 24(7): 3510-3516.
[17]Yang J, Bai H, Tan X, et al. IR and XPS investigation of visible-light photocatalysis-Nitrogen-carbon-doped TiO2film[J]. Appl Surf Sci, 2006, 253(4): 1988-1994.
[18]Peiró A M, Peral J, Domingo C, et al. Low-temperature deposition of TiO2thin films with photocatalytic activity from colloidal anatase aqueous solutions[J]. Chem Mater, 2001, 13(8): 2567-2573.
[19]汪青, 尚静, 赵凤伟, 等. 多壁碳纳米管负载TiO2复合器件可见光光催化降解RhB[J]. 分子催化, 2010, 24(6): 537-541.
(WANG Qing, SHANG Jing, ZHAO Feng-we, et al. Visible-lightphoto catalytic degradation of Rhodamine Bover MWCNTs-TiO2composite device[J]. Journal of Molecular Catalysis(China), 2010, 24(6): 537-541.)
[20]Momeni M M, Ghayeb Y. Preparation of cobalt coated TiO2and WO3-TiO2nanotube films via photo-assisted deposition with enhanced photocatalytic activity under visible light illumination[J]. Ceram Int, 2016, 42(6): 7014-7022.
[21]Wu Y, Chen S, Zhao J, et al. Mesoporous graphitic carbon nitride and carbon-TiO2hybrid composite photocatalysts with enhanced photocatalytic activity under visible light irradiation[J]. Journal of Environmental Chemical Engineering, 2016, 4(1): 797-807.
[22]Momeni M M, Nazari Z. Preparation of TiO2and WO3-TiO2nanotubes decorated with PbO nanoparticles by chemical bath deposition process: A stable and efficient photo catalyst[J]. Ceram Int, 2016, 42(7): 8691-8697.
[23]Zhu S, Yang X, Wang G N, et al. Facile preparation of P-25 films dip-coated nickel foam and high photocatalytic activity for the degradation of quinoline and industrial wastewater[J]. In International Journal of Chemical Reactor Engineering, 2011, 9(1): 139-143.
[24]Jing J, Zhang Y, Li W, et al. Visible light driven photodegradation of quinoline over TiO2/graphene oxide nanocomposites[J]. J Catal, 2014, 316: 174-181.
[25]Haji Jumali, Mohamad Alosfur F K, Radiman S, et al. Rapid synthesis of TiO2/MWCNTs nanocatalyst with enhanced photocatalytic activity using modified microwave technique[J]. Mat Sci Semicon Proc, 2014, 25: 207-210.
[26]Nguyen V H, Ren Y, Lee Y R, et al. Microwave-assisted synthesis of carbon nanotube-TiO2nanocomposites in ionic liquid for the photocatalytic degradation of methylene blue[J]. Synthesis and Reactivity in Inorganic, Metal-Organic, and Nano-Metal Chemistry, 2012, 42(2): 296-301.
[27]Alosfur F K M, Jumali M H H, Radiman S, et al. Modified microwave method for the synthesis of visible light-responsive TiO2/MWCNTs nanocatalysts[J]. Nanoscale Res Lett, 2013, 8(1): 1-6.
[28]B Czech, W Buda, S Pasieczna-Patkowska, et al. MWCNT-TiO2-SiO2nanocomposites possessing the photocatalytic activity in UVA and UVC[J]. Applied Catalysis B: Environmental, 2014,162: 564-572.
[29]Wang W, Serp P, Kalck P, et al. Visible light photodegradation of phenol on MWNT-TiO2composite catalysts prepared by a modified sol-gel method[J]. Journal of Molecular Catalysis A: Chemical, 2005, 235(1-2): 194-199.
[30]Jung K H, Hong J S, Vittal R, et al. Enhanced photocurrent of dye-sensitized solar cells by modification of TiO2with carbon nanotubes[J]. Chem Lett, 2002, (8): 864-865.
[31]Banerjee S, Wong S S. Synthesis and characterization of carbon nanotube-nanocrystal heterostructures[J]. Nano Lett, 2002, 2(3): 195-200.
[32]Kamat P V, Bedja I, Hotchandani S. Photoinduced charge transfer between carbon and semiconductor clusters. One-electron reduction of C60 in colloidal TiO2semiconductor suspensions[J]. J Phys Chem-Us, 1994, 98(37): 9137-9142.
[33]Yu Y, Yu J C, Chan C Y, et al. Enhancement of adsorption and photocatalytic activity of TiO2by using carbon nanotubes for the treatment of azo dye[J]. Applied Catalysis B: Environmental, 2005, 61(1-2): 1-11.
Preparation of MWCNTs-TiO2photocatalysts in thin liquid films under continuous flow conditions and their photocatalytic activities for quinoline degradation
CUI Jia-li,GAO Yong-hua,GAO Li-zhen
(CollegeofEnvironmentalScienceandEngineering,TaiyuanUniversityofTechnology,Taiyuan030024,China)
MWCNTs-TiO2photocatalysts were formed within a very thin liquid film generated on a continuous flow spinning disc surface, in which two jets located in the center of the disc were fed with a suspension of HNO3-purified MWCNTs (0.5 g) in a mixture of tetra-n-butyl titanate (40 mL), ethanol (100 mL) and acetic acid (10 mL), and a solution of ethanol (30 mL), acetic acid (20 mL) and water (8 mL). The collected products were gelled at room temperature for 24 h, dried at 80 ℃ for 4 h and calcined at 350, 400 and 450 ℃ for 4 h. The samples were characterized by XRD, FT-IR, SEM, TEM and UV-vis DRS. The photocatalytic properties were evaluated by the degradation of quinoline under visible light irradiation. Results showed that TiO2nanoparticles of the photocatalyst were smaller (5-10 nm) than when there were no MWCNTs present (10-15 nm), and were well distributed between the MWCNTs. MWCNTs promoted the visible light absorption of the samples. The photocatalyst calcined at 450 ℃ showed the strongest visible light absorption and best catalytic activity, andproduced a quinoline degradation of 86.6% after 180 min.
SDP; Visible light; Photocatalyst; Quinoline
Natural Science Foundation of Shanxi of China(2014021034-1); National Natural Science Foundation of China (51408397).
introduction: CUI Jia-li, Ph. D, Lecturer. E-mail:cuijiali@tyut.edu.cn
1007-8827(2016)04-0399-08
TB333
A
2016-03-20;
2016-07-28
山西省青年科技研究基金(2014021034-1);国家青年科学基金(51408397).
崔佳丽,博士,讲师. E-mail:cuijiali@tyut.edu.cn

