替米考星明胶微囊含量测定方法研究
张李琦,郑明学,苏晓晴,吉明霞,史晨婕,白瑞,贡鑫,席柔,张黎,徐之勇
(山西农业大学动物科技学院,山西太谷030801)
替米考星明胶微囊含量测定方法研究
张李琦,郑明学,苏晓晴,吉明霞,史晨婕,白瑞,贡鑫,席柔,张黎,徐之勇
(山西农业大学动物科技学院,山西太谷030801)
为了建立起科学、准确的替米考星明胶微囊含量测定方法,试验分别建立了紫外分光光度法(UV)及高效液相色谱法(HPLC)2种方法,同时对2种分析方法的专属性、线性、准确度、精密度进行比较验证。结果表明,UV测得替米考星对照品与替米考星微囊均在(291±1)nm波长处有最大吸收峰,且HPLC测得二者的顺反异构体的保留时间基本一致,2种方法辅料均无干扰;线性关系试验中,替米考星对照品溶液在质量浓度为30.0~90.0 μg/mL范围内,2种方法均表现出良好的线性关系,且R2紫外=0.999 4<R2液相=0.999 5;准确度试验中,2种方法的平均回收率均在98.0%~102.0%,RSD均小于2%,但紫外法测得质量浓度45 μg/mL的供试品平均回收率为97.98%,没有达到规定要求;精密度试验中,2种方法的RSD均小于2%。因此,UV法与HPLC法都基本满足测定替米考星明胶微囊含量的要求,而采用HPLC法测定则更为准确,其可以用作对替米考星明胶微囊进行质量控制的测定方法。
替米考星明胶微囊;含量测定;高效液相色谱法;紫外分光光度法
替米考星是由英国Elanco公司于20世纪80年代开发研制的一种畜禽专用抗生素,其对革兰氏阴性菌和革兰氏阳性菌活性的抑制显著,同时对多种螺旋体和支原体的生长具有较强的抑制作用[1-2]。替米考星明胶微囊是山西农业大学兽医病理实验室以B型明胶为囊材、替米考星为芯材,通过单凝聚法制备而成。目前,测量替米考星含量最常用的分析方法有HPLC法和UV法;而用于替米考星明胶微囊含量测定的分析方法国内外尚未见报道。
本试验分别建立了UV法和HPLC法2种测定方法,且依据《兽用化学药物质量控制分析方法验证技术指导原则》[3]和《中华人民共和国兽药典》[4]中相关规定对2种方法的专属性、线性、准确度、精密度等进行方法学验证,并对所采用分析方法的科学性、准确性和可行性进行验证,以比较分析方法是否符合测试项目的目的和要求,从而建立替米考星明胶微囊的测定方法,以保证所用的分析方法确实能够用于替米考星明胶微囊的质量控制。
1 材料和方法
1.1 材料
1.1.1 主要试剂替米考星对照品(含量99.8%),北京索莱宝科技有限公司(ST9180);替米考星原料药(含量99%),宁夏泰瑞制药股份有限公司(G8141235);替米考星明胶微囊,山西农业大学兽医病理实验室自制(201512);胰酶,北京索莱宝科技有限公司(T8150);四氢呋喃(色谱纯),天津市光复精细化工研究所(20150405);二丁胺(色谱纯),天津市光复精细化工研究所(20150302);乙腈(色谱纯),飞世尔实验器材(上海)有限公司(A998-4)。1.1.2主要仪器UV-5200型紫外可见光分光光度计(上海元析仪器有限公司);ThermoU3000高效液相色谱仪(戴安中国有限公司)。
1.2 试剂的配制
1.2.1 胰酶液的配制[4]其参照《中华人民共和国兽药典》(2010版)进行。
1.2.2 UV法所需试剂的配制
1.2.2.1 替米考星对照品系列质量浓度的配制精密称取实际含量50 mg的替米考星对照品,用0.1 mol/L的盐酸溶液分别配制30.0,40.0,50.0,60.0,70.0,80.0,90.0 μg/mL系列浓度的替米考星对照品溶液[5]。
1.2.2.2 替米考星明胶微囊及空白明胶微囊溶液的配制[6-7]精密称取经研磨的替米考星明胶微囊0.1 g,置于100 mL烧杯中,加50 mL胰酶液,放于45℃超声波清洗器内超声6 h,期间每隔0.5 h超声(28 Hz,40 W)一次,每次15 min,于6 h后加入0.1 mol/L盐酸溶液定容至100 mL容量瓶内,摇匀,用0.5 μm滤膜过滤,即得1 mg/mL的替米考星明胶微囊母液。用同样方法配制空白明胶微囊溶液。
1.2.3HPLC法所需试剂的配制
1.2.3.1 磷酸稀释液、磷酸二丁胺缓冲溶液配制其参照《中华人民共和国兽药典》(2010版)进行[4]。
1.2.3.2 替米考星对照品系列浓度配制[15]其参照
1.2.2.1 替米考星对照品溶液的配制,注意改用磷酸稀释液稀释定容各浓度替米考星对照品溶液。
1.2.3.3 替米考星明胶微囊溶液的配制[9-10]参照
1.2.2.2 替米考星明胶微囊及空白明胶微囊溶液的配制,注意将0.1 mol/L盐酸改用磷酸稀释液稀释,定容替米考星明胶微囊母液。用同样方法配制空白明胶微囊溶液。
1.3 试验方法
1.3.1 UV法专属性测定取替米考星对照品溶液、替米考星明胶微囊溶液及空白明胶微囊溶液,利用紫外分光光度计在200~400 nm范围内扫描,根据紫外吸收图谱确定替米考星的最大吸收波长[11]。
1.3.2 UV法标准曲线的建立配制30.0,40.0,50.0,60.0,70.0,80.0,90.0 μg/mL的替米考星系列标准溶液,在确定的最大波长处测定对照品系列溶液的吸光度值(OD值),以对照品浓度(C)对OD值进行线性回归,建立替米考星微囊含量测定的标准曲线方程,得出回归方程、相关系数及线性图[12-13]。
1.3.3 UV法测定的准确度取3份30 μg/mL的空白明胶微囊溶液于3个烧杯中,每份10 mL,分别添加10 mL质量浓度为30,60,90 μg/mL的替米考星标准溶液,最终制备成15,30,45 μg/mL这3个质量浓度的供试液,在最大波长处测定吸光度,重复3次。以空白明胶微囊为参比,计算3个不同添加质量浓度的回收率、平均回收率、相对标准偏差(RSD),各浓度下的平均回收率均应在98.0%~102.0%,9个回收率数据的RSD应不大于2.0%(表1)[14]。
1.3.4 UV法测定的精密度
1.3.4.1 重复性取同一批号的替米考星明胶微囊制成140,160,180 μg/mL这3种不同质量浓度供试品溶液,以空白微囊为参比,在最大波长处测定吸光度,重复测定3次,进行精密度测定,计算RSD,其RSD应不大于2%[14]。
1.3.4.2 中间精密度按照重复性试验方法在另一时间换另一试验员再进行一次试验,计算出RSD,其RSD应不大于2%(表2)[14]。
1.3.5 HPLC法专属性的测定色谱条件参考《中华人民共和国兽药典》(2010版)[4]。精密量取10 μL替米考星对照品溶液和替米考星明胶微囊溶液、空白明胶微囊溶液进样,记录替米考星对照品溶液与替米考星明胶微囊溶液的保留时间是否相同,及空白明胶微囊溶液在此保留时间处有无吸收,并比较记录替米考星色谱峰分离度,替米考星顺反异构体分离度(R)不得小于2.0%[14-15],且理论板数按替米考星顺式峰计算,不低于3 000[4]。
1.3.6 HPLC法线性关系的测定配制同1.3.2替米考星对照品系列浓度溶液,进样记录色谱图,对每个浓度样品测定3次,以测得的峰面积(A)对被测样品浓度进行线性回归[16]。
1.3.7 HPLC法准确度的测定按照1.3.3方法制备15,30,45 μg/mL这3个质量浓度的供试液,各取10 μL进样,记录色谱图。重复3次[17-18],试验结果评定标准同1.3.3[9-10](表3)。
1.3.8 HPLC法测定的精密度[19]
1.3.8.1 重复性取同一批号的替米考星明胶微囊制成140,160,180 μg/mL这3种质量浓度供试品溶液,重复测定3次,每次取10 μL进样,记录色谱图,计算RSD,其RSD应不大于2%[14-15]。
1.3.8.2 中间精密度按照重复性试验方法在另一时间换另一试验员再进行一次试验,计算出RSD,其RSD应不大于2%(表4)[14-15]。
2 结果与分析
2.1 UV法专属性试验结果
由图1可知,替米考星对照品与替米考星微囊在200~400 nm处紫外扫描的最大吸收波长相同,均为(291±1)nm;干扰辅料空白明胶微囊在(291± 1)nm处几乎无吸收,可见,UV法测定的替米考星明胶微囊专属性良好。

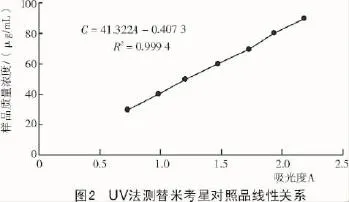
2.2 UV法建立标准曲线以对照品浓度(C)对OD(A)值进行线性回归,得标准曲线方程为C=41.322A-0.407 29(R2=0.999 4),线性关系如图2所示。由图2可知,替米考星对照品在浓度在30.0~90.0 μg/mL范围内线性关系良好。
2.3 UV法准确度测定结果
3种不同浓度的替米考星平均回收率为98.64%,其中,质量浓度为45 μg/mL的平均回收率不在98.0%~102.0%之内,RSD<2%,说明UV法准确度基本良好(表1)。
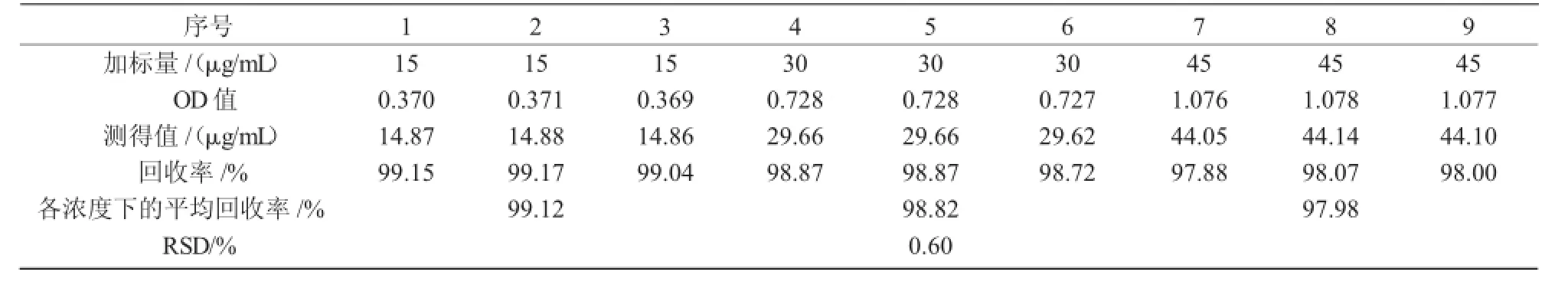
表1 UV法测定替米考星溶液准确度试验结果
2.4UV法精密度测定结果
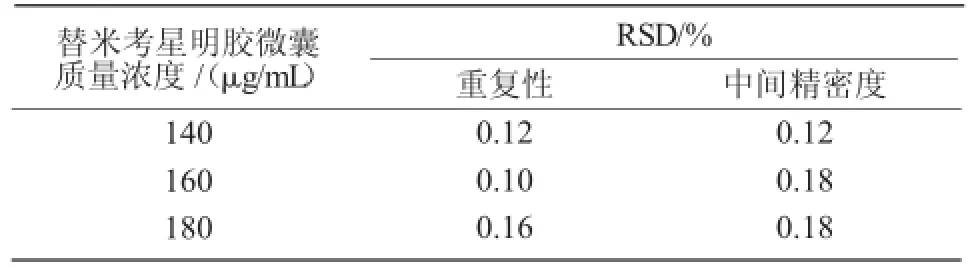
表2 UV法测不同浓度替米考星微囊溶液的精密度
UV法的重复性、中间精密度试验中,RSD值均小于2%,符合要求,说明UV测替米考星含量精密度良好(表2)。
2.5 HPLC法专属性试验结果
从图3可以看出,替米考星对照品与替米考星明胶微囊的顺反异构体保留时间基本一致,并且空白明胶微囊在此保留时间内没有色谱峰;替米考星样品的顺反异构体分离度及塔板数符合要求;替米考星对照品的顺反异构体分离度及其塔板数符合要求。表明HPLC法测替米考星明胶微囊专属性良好。

2.6 HPLC法建立标准曲线
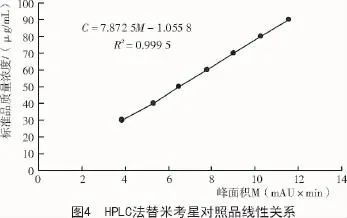
以测得的峰面积(M)作被测样品浓度(C)的函数作图进行线性回归,得出标准曲线方程为C=7.872 5M-1.055 8(R2=0.999 5),线性关系如图4所示。从图4可以看出,替米考星对照品在30.0~90.0 μg/mL范围内线性关系良好。
2.7 HPLC测准确度结果
3种不同浓度的替米考星平均回收率为99.49%,RSD<2%,说明HPLC法具有较高的准确度(表3)。
2.8 HPLC法精密度测定结果
HPLC法的重复性、中间精密度试验中,RSD值均小于2%,符合要求,说明HPLC法测替米考星含量精密度良好(表4)。
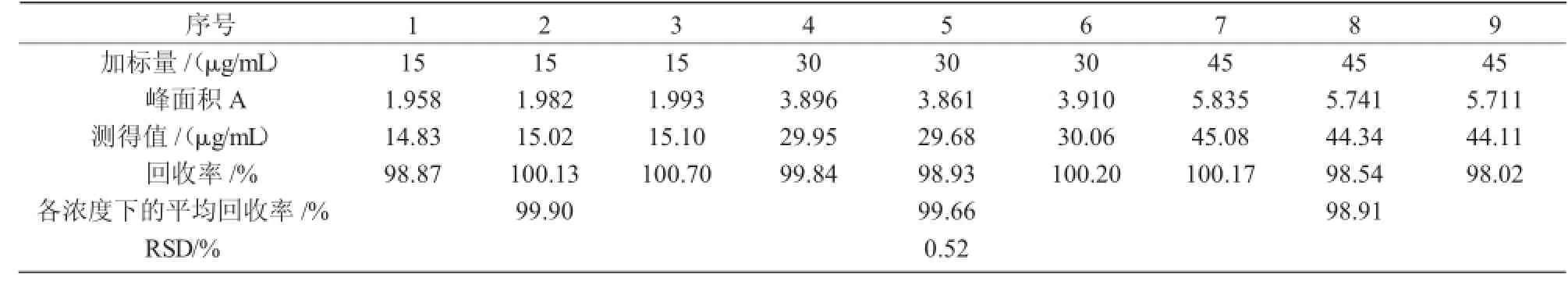
表3 HPLC法测定替米考星溶液准确度试验结果

表4 HPLC法测不同浓度替米考星微囊溶液的精密度
3 结论与讨论
本试验研究发现,UV法与HPLC法都基本满足测定替米考星明胶微囊含量的要求,在准确度测定试验中,HPLC法与UV法相比,HPLC法回收率更高,RSD较低,说明其准确度更高一些。宋艳红等[5]在利用UV法测量替米考星含量的准确度试验中得出,RSD为3.7%,不符合RSD值应不大于2%的要求;而闫春芝等[15]、张旭东等[8]在利用HPLC法测量替米考星含量的准确度试验中得出,其准确度的各项指标均满足要求。综上可以看出,UV法准确度较差,HPLC法的准确度更为精准。
本试验发现,在利用2种不同分析方法测量替米考星线性关系的试验中得出,利用HPLC法测定替米考星标准曲线的线性关系比UV法测定的线性关系结果更好(R2紫外=0.9994<R2液相=0.9995)。证明HPLC法的准确度要高于UV法。
有研究表明,UV法的专属性不高,其主要误差来源于共存物的谱线重叠而引起的光谱干扰;而HPLC法之所以有很高的准确度,是因为其常用的色谱柱具有很高的分离效能,可分离并分析高极性、高分子量和离子型等各种物质,柱效非常高,每米可达3万块以上,而且分析速度很快,具有高精度、高稳定性的特点[20]。
综上所述,UV法和HPLC法均可用于测定替米考星明胶微囊含量,但后者的准确度更高一些。
[1]农业部兽药评审中心.兽用化学药物质量控制分析方法验证技术指导原则(GPH5-1)[S].北京:中国兽药监察所,2009.
[2]Naccari F,Martino D.The rapeutic efficacy of tilmicosin in ovine mammaryinfections[J].Small Ruminant Research,2003,47:1-9.
[3]农业部兽药评审中心.兽用化学药物质量标准建立的规范化过程技术指导原则(GPH1-1)[S].北京:中国兽药监察所,2010.
[4]中华人民共和国兽药典委员会.中华人民共和国兽药典[M].北京:中国农业出版社,2010.
[5]宋艳红,白小红,李英.紫外分光光度法测定替米考星的含量[J].山西医科大学学报,2005(1):71-73.
[6]葛庆华,何雯.胰酶-超声法测定甲氨蝶呤明胶微球的药物含量[J].中国医药工业杂志,1990,21(12):553-557.
[7]张莎.缓释型药物载体明胶微球的制备及降解性能研究[D].西安:陕西科技大学,2010.
[8]张旭东,吕瑞娥,张宝国.替米考星的高效液相分析[J].郑州大学学报:理学版,2003(3):70-72.
[9]中华人民共和国农业部.兽药质量标准[S].北京:中华人民共和国农业部,2006:70-77.
[10]中国色谱网论坛.HPLC测定替米考星的含量[EB/OL]. [2009-04-03].http://www.sepu.net/dvbbs/dispbbs.asp?boardid=1 748id=174379.
[11]岳永波,李玉霞,魏占勇,等.替米考星溶液的紫外分光光度法测定[J].河北工业科技,2012(4):206-207.
[12]白东英,李引乾,黄勇旗,等.替米考星长效注射液的质量控制[J].西北农业学报,2008(3):64-67.
[13]陈懿.紫外分光光度法测定替米考星注射液含量[J].兽药与饲料添加剂,2008,13(1):29.
[14]黄晓龙.含量测定分析方法验证的可接受标准简介[EB/OL]. [2016-07-18].http://www.docin.com/p-1510323168.htmL.
[15]闫春芝,赵红彦,秦朝英.高效液相色谱法测定替米考星含量[J].中国兽药杂志,2006(8):26-27.
[16]冷晓红,李晓萍,张彤.HPLC法测定磷酸替米考星可溶性粉中磷酸替米考星的含量[J].中国兽药杂志,2014(7):34-36.
[17]闫小峰,孙志文.高效液相色谱法测定饲料中替米考星含量[J].中国饲料,2010(9):27.
[18]代园凤,陈雪,黄化刚,等.甲基硫菌灵悬浮剂的高效液相色谱分析[J].山西农业科学,2015,43(12):1652-1654.
[19]刘德金,刘爱玲,刘桂兰,等.检测替米考星含量的高效液相色谱法改良[J].南京农业大学学报,2011,34(3):135-139.
[20]章一.高效液相色谱法的优点与实际问题中的应用[J].化工管理,2014(24):127.
Study on the Methods for Determination of the Content
of Timicosin Gelatin Microcapsules
ZHANGLiqi,ZHENGMingxue,SUXiaoqing,JI Mingxia,SHI Chenjie,BAI Rui,GONGXin,XI Rou,ZHANGLi,XUZhiyong
(College ofAnimal Science and VeterinaryMedicine,Shanxi Agricultural University,Taigu 030801,China)
Toestablish a scientific and accurate methods for determination ofthe content oftimicosin gelatin microcapsules,this test compared UV and HPLC two kinds ofanalysis methods ofspecificity,linearity,accuracy and precision ofverification.The results showed that UVmeasured timicosin(reference substances)and timicosin gelatin microcapsules had the maximumabsorption peak at(291±1)nm, and the retention time of cis-trans-isomer measured by HPLC was basically the same,two methods of complementary makings were no interference.In linearitytests,the linear range oftimicosin solution was obtained within 30.0~90.0 μg/mL,and R2UV=0.999 4<R2HPLC=0.999 5.In accuracytests,the average recoveryofthe twomethods was all between 98.0%-102.0%,and RSDofthe twomethods was less than 2%,but UV was not consistent with the request in the recoveryrate ofarticle in the 45 μg/mL.In precision tests,the RSD ofthe two methods was all less than 2%.Therefore,the UV and HPLC methods can meet the requirement of determination of timicosin gelatin microcapsules,and HPLCis more accurate,which can be used todetermine the timicosin gelatin microcapsules.
timicosin gelatin microcapsules;content determination;HPLC;UV
S816.73
A
1002-2481(2016)12-1848-05
10.3969/j.issn.1002-2481.2016.12.27
2016-10-12
山西省现代农业鸡产业技术体系项目(2013-11-03)
张李琦(1991-),男,山西定襄人,在读硕士,研究方向:动物传染病诊断与防治。郑明学为通信作者。

