紫外分光光度法检测香椿中硝酸盐方法研究
朱 勇,应 杰,孙亚米,周丽绒
(1.农业部农产品质量安全风险评估实验室(宁波),浙江宁波 315040;2.宁波市鄞江中学,浙江宁波 315040)
紫外分光光度法检测香椿中硝酸盐方法研究
朱 勇1,应 杰2,孙亚米1,周丽绒1
(1.农业部农产品质量安全风险评估实验室(宁波),浙江宁波 315040;2.宁波市鄞江中学,浙江宁波 315040)
食品、农产品中检测硝酸盐含量采用的标准方法各有特点,基于香椿本身较高的亚硝酸盐含量会给采用NY/T 1279-2007检测硝酸盐带来影响,且硝酸根离子和亚硝酸根离子在紫外区219 nm处具有等吸收波长特性的原因,通过亚硝酸根对硝酸根标液干扰程度的研究,提出采用标准加入法或在硝酸根标液中加入一定量的亚硝酸根溶液模拟样品状态的方法来消除这一干扰,既达到简单便捷的目的,又确保了香椿数据的准确性。
香椿;硝酸盐;亚硝酸盐;紫外分光光度法
香椿(Toona sinensis)原产于中国,分布于长江南北的广泛地区,具有较高的营养价值。但随着深入研究发现,香椿中亚硝酸盐含量较高,从1.433~1 048 mg·kg-1[1-3]不等,远超GB 2762-2012《食品安全国家标准食品中污染物限量》对亚硝酸盐在蔬菜及其制品腌制蔬菜的限量规定(20 mg·kg-1以NaNO2计),香椿这一特性在新鲜蔬菜样品中属于较为特殊的情况,使得检测香椿中硝酸盐的含量需关注这一特殊现象。目前检测食品、蔬菜、水果中硝酸盐的标准方法主要有GB 5009.33-2010《食品安全国家标准食品中亚硝酸盐与硝酸盐的测定》和NY/T 1279-2007《蔬菜、水果中硝酸盐的测定紫外分光光度法》。GB 5009.33-2010采用离子色谱法能很好地分离硝酸盐与亚硝酸盐,使二者不受干扰,但仪器较为昂贵,不是所有实验室都有;第二种检测方法常用分光光度法,适合大部分实验室,缺点是硝酸盐的测定采用镉柱还原法,还原成亚硝酸盐后,测定亚硝酸盐值来计算硝酸盐的含量,试验过程烦琐,周期长,需要具备一定的经验;而NY/T 1279-2007利用紫外分光光度法测定新鲜蔬菜及水果中硝酸盐含量过程简单,操作方便。水果、蔬菜样品在去除色素、蛋白质及其他干扰物质的基础上,利用硝酸根离子和亚硝酸根离子在紫外区219 nm处具有等吸收波长的特性,测定其吸光度,其测得结果为硝酸盐和亚硝酸盐吸光度的总和。鉴于新鲜蔬菜、水果中亚硝酸盐含量甚微,可忽略不计,测定结果为硝酸盐的吸光度[4]。此法适用于大部分蔬菜水果,但香椿样品由于自身的亚硝酸盐含量的特殊性,采用NY/T 1279-2007方法,亚硝酸的含量对硝酸盐测定结果的影响程度还需进一步探讨。
1 材料与方法
1.1 仪器及试剂
BlueStar B紫外可见分光光度计(北京莱伯泰科仪器有限公司);ICS-2100离子色谱(美国赛默飞世尔科技公司);723N分光光度计(上海精密科学仪器有限公司);M illi-QADVA10超纯水仪(美国M illipore公司)。
水中亚硝酸盐氮成分分析标准物质为GBW(E)080223,以亚硝酸根计329 mg·L-1;水中硝酸根成分分析标准物质为GBW(E)080264,以硝酸根计1 000 mg·L-1,国家标准物质研究中心。
1.2 前处理方法
1.2.1 离子色谱法
5 g匀浆香椿样品,以80 m L水洗入100 m L容量瓶中,超声提取30 min,75℃水浴中放置5 m in,取出放置室温,加水稀释至刻度,摇匀后滤纸过滤,取部分溶液于10 000 r·min-1离心15 min,上清液过OnGuardⅡRP柱净化后待进样。
1.2.2 分光光度法
5 g匀浆香椿样品,置于50 m L烧杯中,加12.5 m L饱和硼砂溶液,以70℃左右的水约300 m L洗入500 m L容量瓶中,于沸水浴中加热15 min,取出置冷水浴中放置至室温,在振荡上述提取液时加入5 m L亚铁氰化钾溶液(106 g· L-1),摇匀,再加入5 mL乙酸锌溶液(220 g· L-1),加水定容,摇匀,放置30 min后,用滤纸过滤。吸取40.0 m L滤液,置于50 m L带塞比色管中,加入2 m L对氨基苯磺酸(4 g·L-1),静置5 m in,加入1 m L盐酸萘乙二胺(2 g·L-1),加水至刻度,混匀,静置15 min,上机比色。
硝酸盐测定采用镉柱还原。先以25 mL稀氨缓冲液冲洗镉柱,流速控制在3~5 m L·min-1,吸取20 m L滤液于50 m L烧杯中,加5 m L氨缓冲溶液混合,注入镉柱还原,以原烧杯收集流出液,当贮液漏斗中的样液流尽后,再加5 m L水置换柱内留存的样液,将全部收集液如前再经镉柱还原1次,第2次流出液收集于100 m L容量瓶中,继以水流经镉柱洗涤3次,每次20 mL,洗液一并收集于同一容量瓶中,加水至刻度,混匀取10 mL还原后的样液于50 m L比色管中,按亚硝酸盐比色法进行操作比色。
1.2.3 紫外分光光度法
取10 g匀浆香椿样品于100 m L烧杯中,用100 m L水分次将样品转移到250 m L容量瓶中,加入5 m L氨缓冲溶液,2 g粉末状活性炭,在可调式往返振荡器上(200次·min-1)振荡30 min,加入亚铁氰化钾溶液(150 g·L-1)和硫酸锌溶液(300 g·L-1)各2 m L,混合后加水定容至250 m L,摇匀放置5 min,过滤,取2 m L滤液于50 m L容量瓶内加水定容,比色。
1.3 仪器条件
离子色谱条件为Dionex IonPac AS11-HC离子色谱柱(4 mm×250 mm),流动相A为氢氧化钾溶液,梯度洗脱条件为6 mmol·L-130 min,70 mmol·L-15 min,6 mmol·L-15 m in,流速1.0 m L·m in-1,进样量25μL,柱温30℃,电导检测器检测池温度为35℃。分光光度计条件为1 cm比色杯,波长538 nm。紫外分光光度计条件为1 cm石英比色皿,波长219 nm。
1.4 标准曲线
1.4.1 离子色谱法
移取亚硝酸盐和硝酸盐标准溶液,加水稀释,制成系列标准溶液,含亚硝酸根离子浓度为0、0.5、1.0、1.5、2.0、2.5 mg·L-1;含硝酸根离子浓度为0、0.5、1.0、2.0、3.0、4.0 mg·L-1。用离子色谱仪分析,以浓度为横坐标、峰面积为纵坐标进行线性回归,制作标准曲线。
1.4.2 分光光度法
移取亚硝酸盐标准溶液,加水稀释,制成系列标准溶液,含亚硝酸根离子浓度为0、0.02、0.04、0.06、0.08、0.10、0.15、0.20、0.25 mg·L-1。用分光光度计分析,以浓度为横坐标、吸光度为纵坐标进行线性回归,制作标准曲线。
1.4.3 紫外分光光度法
移取硝酸盐标准溶液,加水稀释,制成系列标准溶液,含硝酸根离子浓度为0、2.0、4.0、6.0、8.0、10.0、12.0 mg·L-1。用紫外分光光度计分析,以浓度为横坐标、吸光度为纵坐标进行线性回归,制作标准曲线。
2 结果与分析
2.1 亚硝酸根对硝酸根标准溶液的影响
考虑到个别香椿中亚硝酸根的含量能高至1 048 mg·kg-1,参照NY/T 1279-2007的处理方式,无法消除亚硝酸根,在用紫外分光光度计检测硝酸根的同时,也有不同浓度的亚硝酸根干扰。模拟样品中各浓度亚硝酸盐(以亚硝酸钠计)经过前处理后残留在比色溶液中的浓度,模拟试剂采用标准溶液精准配制。随着亚硝酸根浓度的提高,吸光度均有不同的增加。
从表1可知,虽然亚硝酸根对硝酸根的吸光度有正向干扰,但从各自标线的相关系数线性关系来考量,相关系数符合试验要求。曲线整体抬升,硝酸根的吸光度收到干扰,斜率改变。虽然硝酸根、亚硝酸根是等吸收波长,但不完全是等浓度吸收。这同李祥的研究相符[6]。
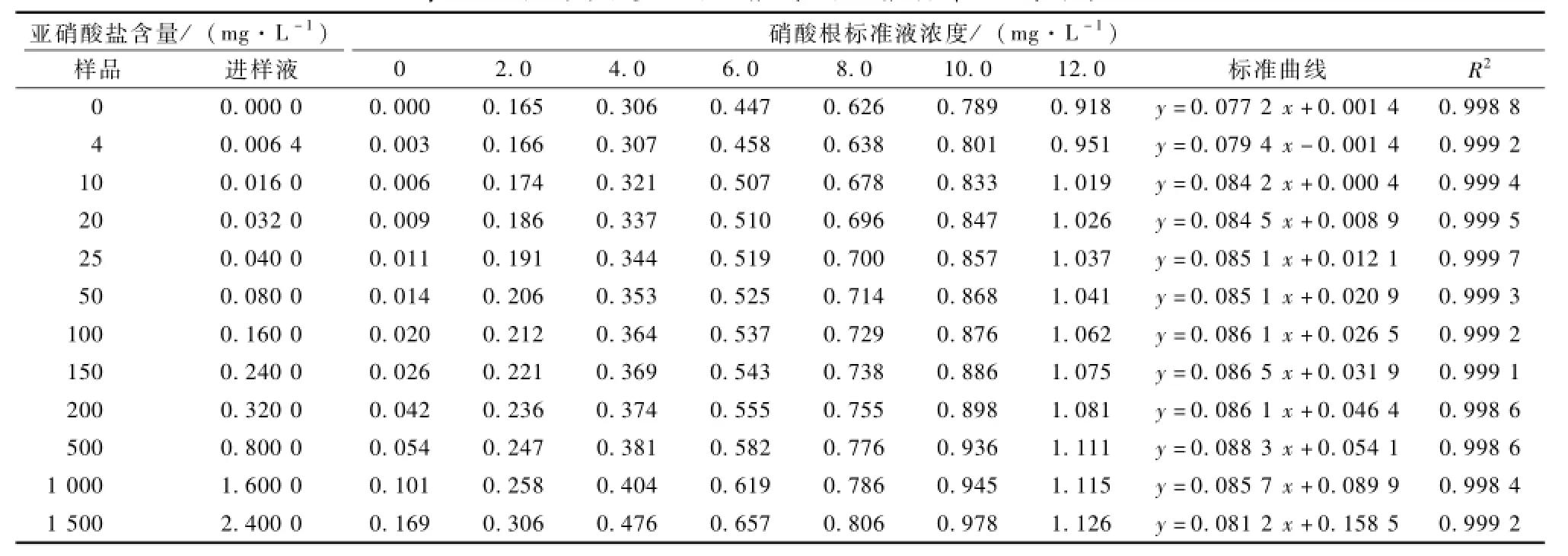
表1 不同浓度亚硝酸根对硝酸根标准曲线的干扰
将没有亚硝酸盐影响的标准曲线吸光度值分别代入受影响的标准曲线,计算出样品含亚硝酸盐4、10 mg·kg-1影响时的待进样溶液中硝酸根浓度,同没有影响时的值比较相对相差。
表2表明,当样品中含亚硝酸盐含量在4 mg· kg-1时,相对相差均小于5%,符合NY/T 1279-2007的精密度要求;而当样品中亚硝酸盐含量在10 mg· kg-1时,相对相差均大于5%,不符合标准要求。样品中亚硝酸盐含量越高,硝酸盐偏离正确值就越远。鉴于新鲜蔬菜、水果中亚硝酸盐含量甚微[4],目前新鲜蔬菜中的亚硝酸盐限量已取消,GB 2762-2005《食品中污染物限量》(已作废)将蔬菜中亚硝酸盐限量设定在4 mg·kg-1。所以除香椿以外的绝大部分新鲜蔬菜、水果样品中亚硝酸盐含量均会小于4 mg· kg-1,对硝酸盐测定带来的影响可以忽略,同时也验证了NY/T 1279-2007的原理部分。
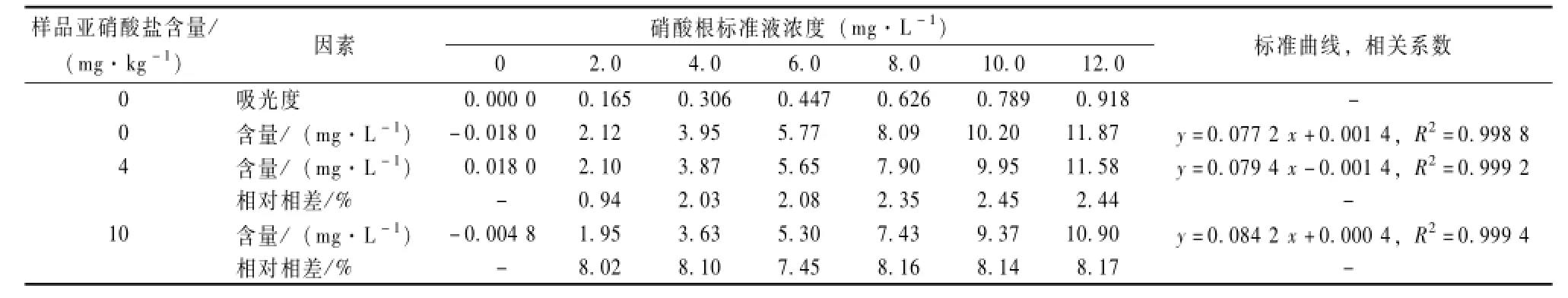
表2 不同浓度亚硝酸根对硝酸根干扰后含量的准确度
2.2 方法的前处理比较
GB 5009.33-2010的2个方法及NY/T 1279-2007均对样品的前处理做出各自规定,详见1.2部分。3个方法采用不同方式加入不同试剂,花费不同时间对样品进行硝酸根、亚硝酸根提取。以此为依据,将香椿样品采用这3个方法进行前处理,再分别用离子色谱、分光光度计、紫外分光光度计进行样液检测。由于紫外分光光度计法只是测试硝酸根的含量,故没有亚硝酸根的数据。
由表3可知,不同前处理方法所测得的亚硝酸根数据、硝酸根数据相对相差均小于5%,达到GB 5009.33-2010、NY/T 1279-2007所规定的精密度要求。由此完全可以选择适合本实验室的3个方法的前处理方式中任一个,以最便捷的方式、最适合本实验室人员操作习惯来完成试验,香椿样品的结果不受前处理方法的影响。

表3 采用不同标准试验结果mg·kg-1
2.3 香椿样品中亚硝酸根对硝酸根的影响
依据标准对香椿样品进行前处理及上机检测,离子色谱法、分光光度法分别测得亚硝酸根、硝酸根浓度。由表4可知,采用紫外分光光度计法考虑到亚硝酸盐对硝酸盐的干扰,将处理液分为3种方式进行上机检测。1)直接上机测定。2)采用标准加入法测定。将1 000 mg·L-1硝酸根标准溶液吸取一定量,用样液定容至50 m L,配成含标准溶液硝酸根离子浓度为0、2.0、4.0、6.0、8.0、10.0、12.0 mg·L-1系列,求得标准曲线后计算硝酸根含量。3)根据离子色谱法、分光光度法测得的香椿亚硝酸根均值含量156 mg·kg-1,经前处理,硝酸盐待测液中含亚硝酸根0.248 mg·L-1,配制硝酸根标准溶液时,所有标液中用移液枪均加入亚硝酸根标液0.037 7 m L,模拟样液的基体,配成的硝酸根系列标液均含0.248 mg·L-1的亚硝酸根。直接上机测定的结果受到亚硝酸根的干扰,明显偏高;采用标准加入法和标液中加亚硝酸根的方式可避免干扰,得到正确的检测结果。

表4 采用不同标准试验结果mg·kg-1
3 小结与讨论
食品、蔬菜、水果中硝酸根离子的测定一般采用3种方法。第一法涉及离子色谱仪,适合大批量样品,可以同时测定硝酸根和亚硝酸根;第二法为实验室常用方法,但硝酸根需要通过镉柱还原成亚硝酸根来测试,前处理烦琐,需要较强的动手能力,不适合大批量样品;第三法为紫外分光光度法,较为简便,试验过程中所用试剂较少,缺点是不能同时得到亚硝酸盐结果[6]。
硝酸根离子和亚硝酸根离子在紫外区219 nm处具有等吸收波长的特性,给采用紫外分光光度法测定香椿中硝酸根含量带来难度。通过标准加入法或在硝酸根标液中加入一定量的亚硝酸根溶液模拟样品状态这两种方法来消除这一基质干扰,既简单便捷,又确保了数据的准确性。
[1] 陈欣.香椿芽亚硝酸盐含量变化规律及亚硝酸盐降解技术研究[D].济南:山东大学,2010.
[2] 杨玉珍,彭方仁,曹一达.不同种源香椿芽硝酸盐、亚硝酸盐及Vc含量变化的研究[J].食品科学,2007,28(6):48-51.
[3] 乔海涛,时桂英,徐建余,等.不同采收期红香椿硝酸还原酶活性及亚硝酸盐含量的变化[J].山东农业科学,2016,48(1):51-53.
[4] 蔬菜、水果中硝酸盐的测定紫外分光光度法:NY/T 1279-2007[S].
[5] 食品安全国家标准食品中亚硝酸盐与硝酸盐的测定:GB 5009.33-2010[S].
[6] 李祥,陈宗姮,袁砚,等.亚硝酸盐对紫外分光光度法测定硝酸盐的影响[J].实验室研究与探索,2014,33(11):10-14.
[7] 吴大付,任秀娟,李东方.蔬菜硝酸盐含量测定方法研究[J].河南科技学院学报,2010,38(3):36-38.
(责任编辑:张瑞麟)
S-3
A
0528-9017(2017)01-0128-04
文献著录格式:朱勇,应杰,孙亚米,等.紫外分光光度法检测香椿中硝酸盐方法研究[J].浙江农业科学,2017,58(1):128-131.
10.16178/j.issn.0528-9017.20170141
2016-07-15
宁波市科技新苗培养计划(甬教基〔2015〕112号)
朱 勇(1978-),男,浙江普陀人,高级农艺师,从事农产品质量检测研究工作,E-mail:zjzszy@163.com。

