奶牛乳腺炎金黄色葡萄球菌FnBPA蛋白免疫研究
马保臣,董玉兰,柴同杰
(1.中国牧工商集团有限公司,北京丰台100070 ; 2.山东农业大学动物科技学院,山东泰安271018 ;3.中国农业大学动物医学院,北京海淀100193)
金黄色葡萄球菌是奶牛乳腺炎的重要病原。近些年来,抗生素的广泛应用,金黄色葡萄球菌的抗菌谱逐渐扩大,给临床治疗和预防金黄色葡萄球菌乳腺炎提出新的挑战。研究证实,金黄色葡萄球菌感染关键的一步为纤维连接蛋白结合蛋白(Fibronectin-Binding Protein,FnBP)和宿主蛋白(例如纤连蛋白(Fibronectin protein,Fn))之间形成的结合体,金黄色葡萄球菌FnBP与Fn形成吻合的结构,FnBP蛋白在金黄色葡萄球菌的感染中发挥重要作用[1]。Herman-Bausier P(2015)通过耐甲氧西林金黄色葡萄球菌感染人的内置设备证实,FnBPA(Fibronectin-Binding Protein A,FnBPA)在引起细菌粘附和形成细菌生物膜发挥重要作用[2]。本试验对奶牛乳腺炎金黄色葡萄球菌FnBPA基因进行调查,并对FnBPA基因进行了克隆与表达,用表达的蛋白制作蛋白疫苗进行了动物免疫,期望为研制奶牛金黄色葡萄球菌乳腺炎新型基因工程疫苗提供依据。
1 材料与方法
1.1 试验材料 337株金黄色葡萄球菌来自2002-2006年间本实验室从奶牛临床乳腺炎和隐性乳腺炎病例的乳样中分离鉴定。其中,临床型乳腺炎金黄色葡萄球菌124株,隐性乳腺炎金黄色葡萄球菌213株。载体均为本实验室保存,大肠杆菌DH5α,BL21(DE3)为本实验室保存;酶购自TaKaRa公司。核酸纯化和质粒提取试剂盒,购自U-gene公司。
1.2 试验方法
1.2.1 引物的设计与合成 根据GenBank发表的Fnbp和Cnap序列,利用 Primer 5.0软件分别设计了FnBPA基因引物,由上海生工生物工程技术服务有限公司合成。引物序列为:FnBPA-F 5′-CT GGATCC GGCCAAAATAGCGGTAAC-3′;FnBPA-R 5′-CT CTCGAG TAAGCTTACTTTTGGAAGTGT-3′,其中,GGATCC为BamHΙ酶切位点,CTCGAG为XhoΙ酶切位点。扩增的片段长度为350 bp左右。
1.2.2 PCR模板DNA的获取 参照文献[3]
1.2.3 PCR以及最适反应体系 DNA模板2 μL,Fnbp-F 1 μL,Fnbp-R(25 μmal/L/μL) 1 μL,dNTP 2 μL, MgCl24 μL, 10×PCR Buffer 5 μL,Taq酶 1 μL,ddH2O 34 μL。FnBPA基因扩增程序:94 ℃预变性3 min。94 ℃变性1 min, 47 ℃退火30 s,72 ℃延伸30 s,30个循环。72 ℃延伸7 min。Cnap基因扩增程序:94 ℃预变性3 min。94 ℃变性1 min,47 ℃退火1 min,72 ℃延伸1 min,30个循环。72 ℃延伸10 min。
1.2.4 克隆载体的构建与鉴定 选取分离株扩增出的350 bp DNA片段,纯化、连接,将重组质粒转化到感受态细胞DH5α中。将转化的受体菌均匀涂布到含50 μg/mL氨苄青霉素(AMP)、X-gal 和IPGT的LB琼脂平板中,从平板上挑取白色菌落,接种到含AMP的LB液体培养基中,37 ℃震荡培养过夜,提取质粒DNA。经PCR和酶切双重鉴定成功后,送上海博亚生物技术有限公司测序。
1.2.5 重组表达质粒的构建与鉴定 将菌株10A的FnBPA克隆载体质粒进行BamHΙ和XhoΙ双酶切,将回收后的DNA片段定向插入至表达载体pET-32a的多克隆区,相关的酶切、片段回收、连接反应以及转化等操作都按照说明书进行。将初选的阳性质粒分别进行PCR和双酶切鉴定,将表达载体阳性质粒命名为PET-FnBPA,送上海博亚生物技术有限公司测序。
1.2.6 重组菌的诱导表达、纯化、检测和定量 将重组菌落接种于5 mL LB培养基(含氨苄青霉素100 μg/mL)中,37 ℃摇床培养至对数生长前期(OD值约为0.6),加入1mol/L IPTG诱导4 h。取适量菌液离心集菌后进行SDS-PAGE分析表达情况。表达菌体经过反复冻融处理后,高速离心3 min,分别取上清和沉淀进行SDS-PAGE,对表达蛋白用镍离子亲和树脂进行纯化,然后进行SDS-PAGE电泳,纯化蛋白用计算机扫描分析其纯度。表达产物经SDS-PAGE后,进行电转移,然后进行免疫检测。将NC膜转移至50 mL脱脂牛乳中,轻摇封闭1 h,洗膜;然后加入一抗(鼠抗FnBPA血清),轻摇3 h,洗膜;加入二抗溶液(HRP标记的羊抗鼠抗体封闭液),轻摇3 h,洗膜;最后显色,至条带清晰后迅速用双蒸水终止显色。按照PIERCE公司的BCATM Protein Assay Kit操作,采用双波长法进行蛋白定量,纯化后的蛋白使用低温冻干机制成成品,动物试验备用。
1.2.7 FnBPA蛋白疫苗的制备 FnBPA蛋白为所纯化蛋白透析后的低温冻干制品,本试验共需要30 mg纯化蛋白,将其配制浓度为1 mg/1 mL。蛋白与完全弗氏佐剂和不完全弗氏佐剂按照1∶1比例充分混合乳化后用于动物免疫。
1.2.8 免疫奶牛 首先对5头试验奶牛(0314,0368,0288,0513,0445)进行系统检查,体温正常,无传染病,无外科疾病,年龄在3~6岁之间,无临床型乳腺炎,正常产奶。对试验牛用CMT检测各乳区乳样无隐性乳腺炎,排除金黄色葡萄球菌感染。本试验用0314,0368,0288号奶牛用于免疫注射,0513,0445号牛用于对照(注射生理盐水)。
1.2.9 免疫程序与方法 5头试验牛免疫2次,时间间隔11 d,第一次采用臀部皮下多位点注射(5 mg 蛋白/只。弗氏完全佐剂乳化);第二次采用臀部皮下注射(5 mg蛋白/只。弗氏不完全佐剂乳化)。对5头试验牛分别在免疫0 d,10 d,20 d,30 d和40 d采集血样。
1.2.10 间接ELISA法测定抗体效价 参照周宏(2005)[5]的方法。
2 结果
2.1 奶牛乳腺炎金黄色葡萄球菌的分子调查结果 对引起奶牛临床型和隐性乳腺炎的337株金黄色葡萄球菌分别进行FnBPA蛋白基因调查,51.04%(172/213)携带FnBPA蛋白基因,临床型乳腺炎金黄色葡萄球菌FnBPA蛋白的携带率为68.5%(85/124)。
2.2 基因测序、重组表达载体质粒的PCR与酶切鉴定 用于表达的菌株10A的FnBPA基因的序列被GenBank收录,收录编号为:DQ447162。选取分离株10A的FnBPA基因连接到pET-32a表达载体中,PCR与酶切结果见图1。
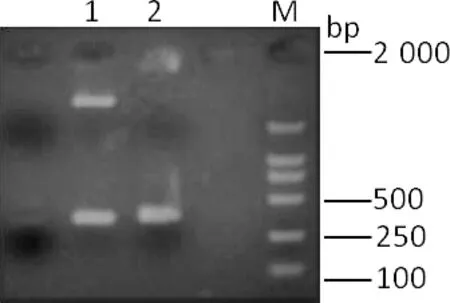
图1 重组质粒pET-Fnbp的PCR和双酶切鉴定
M: DL:2 000 DNA Marker ; 1: 重组质粒pET-FnBPA酶切;
2: 重组质粒PET-FnBPA PCR
2.3 FnBPA蛋白的SDS-PAGE,检测和定量 FnBPA蛋白SDS-PAGE显示,蛋白在上清和沉淀中都存在,以上清中较多,主要以可溶形式分泌表达,经镍离子亲和树脂纯化后的蛋白进行SDS-PAGE电泳,结果见图2。纯化蛋白经计算机扫描分析,显示其纯度在95%以上。本试验共获得FnBPA蛋白共计33 mg,定量结果为:2.8 mg/mL。

图2 纯化蛋白的SDS-PAGE
M: 蛋白分子量 ; 1,2: 纯化后的蛋白
2.4 试验牛临床体征以及免疫抗体测定 疫苗免疫注射后试验牛体温测量发现,只有0288号牛注射后有体温升高、采食量和产奶量减少,但3 d后恢复正常;其余试验牛体温没有明显变化。图3显示了试验牛注射FnBPA蛋白疫苗后的抗体滴度变化,每10 d测定1次抗体,最高抗体滴度达到7 log2,各注射牛FnBPA抗体消长规律基本一致,免疫30~40 d后抗体达到高峰。
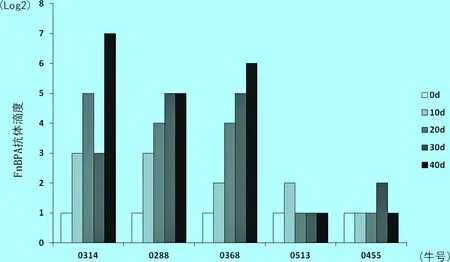
图3试验牛FnBPA抗体滴度
3 讨论
3.1FnBPA基因在奶牛乳腺炎金黄色葡萄球菌的存在情况 本试验对奶牛临床型和隐性乳腺炎金黄色葡萄球菌的FnBPA基因调查,结果显示,临床型乳腺炎金黄色葡萄球菌具有较高的FnBPA基因携带率。Shinji H等(2011)[5]调查认为,对于造成人严重感染的金黄色葡萄球菌,基本都有FnBPA蛋白参与作用,本试验中,分离的临床型乳腺炎金黄色葡萄球菌FnBPA基因携带率高,可能是FnBPA蛋白在感染中起到更重要的作用。
3.2FnBPA基因的克隆与原核表达 本试验应用PET融合表达系统对FnBPA基因进行了高效表达,该系统具有强的T7 Lac核启动子,能高效表达外源蛋白,并且融合伴随蛋白为短的融合型,对外源基因的影响较小。它在外源蛋白两翼各融合表达一个6×His的标签,有益于外源蛋白的纯化。本试验表达的融合蛋白以可溶性形式存在于胞浆中,有利于保持表达重组蛋白的天然结构。本试验对奶牛乳腺炎分离株10A进行了FnBPA蛋白的克隆与表达,经过SDS-PAGE和Western-Blotting特异性检测,证明获得了高纯度的FnBPA蛋白和该蛋白具有抗原性。
3.3 FnBPA蛋白疫苗免疫和前景 本试验充分证明了5 mg/头FnBPA蛋白疫苗免疫注射后,在奶牛体内能够产生抗体,并且在5~6周达到峰值,说明该蛋白疫苗具有很好的抗原性。疫苗注射后试验牛除0288号牛出现了体温升高和奶产量的变化外但很快康复,其他试验牛没有发现异常,说明该蛋白疫苗安全性在可控范围之内。周宏(2005)[4]也证实,FnBPA 蛋白疫苗在0,2周和3周3次免疫小鼠后(100 μg/只·次),抗体在2,4,6周的值分别为:2-4,2-7,2-10。宋战辉(2014)[6]用金黄色葡萄球菌粘附相关蛋白免疫小鼠,也证实了有很好的免疫原性。何焱等(2014)[7]进一步研究发现,乳腺炎金黄色葡萄球菌基因工程亚单位疫苗的可行性。总之,金黄色葡萄球菌表面蛋白疫苗是未来金黄色葡萄球菌疫苗研制的新方向,但还要很多的工作需要完成。本试验中蛋白疫苗能否对金黄色葡萄球菌产生保护还需要进一步试验,包括金黄色葡萄球菌乳腺炎模型,乳清中的抗体消长规律,攻毒试验等将成为今后重要的研究内容。

