HPLC手性流动相添加剂及其用于药物对映体拆分中的影响因素
徐雄,宁卫红,瞿志荣,杨瑞卿,谢永荣*
(1.赣南师范大学 化学化工学院,江西省高校功能材料化学重点实验室,江西赣州 341000;2.杭州师范大学有机硅化学及材料实验室,浙江杭州 311121)
手性是自然界及生命过程的基本特征之一[1]。自从反应停致畸事件以来,手性药物引起了人们的广泛关注,与此同时,手性药物对映体的拆分引起了人们的重视[2-14]。据统计,目前临床常用的药物中约有60%具有手性结构[15],而对于一些手性药物来说,能够产生药理作用的多为其中的一种对映体,而另外一种对映体无药理作用甚至产生显著的副作用。此外,手性药物所产生的药理活性与其手性特征密切相关,药物对映体在生物体内一般表现出不同的药理活性、代谢过程和毒理作用[16-17]。目前,临床上的手性药物要求使用光学纯的对映异构体,以确保药物的安全性。因此,研究药物对映体的拆分具有重要的实用价值。
现代仪器分析技术的发展,促进了药物对映体拆分技术的发展。高效液相色谱法、气相色谱法、毛细管电泳法以及超临界流体色谱法等是常用的仪器分析方法[18-26],其中高效液相色谱法以分离效率高、应用范围广、分析速度快和对各种分析物具有通用性等优点,备受研究人员喜爱,被认为是用于手性物质分析分离最有效的方法[27]。
高效液相色谱分离手性物质一般采用两种方法:直接法和间接法。间接法(即手性衍生化法)分离是利用手性衍生化试剂与样品反应形成非对映异构体,然后在非手性柱上进行分离。柱效高、价格便宜是该法的优点;但耗时且操作复杂,对手性试剂的纯度、反应过程中的稳定性等要求较高。直接法分离使用手性固定相或手性流动相添加剂分离手性物质,因其操作简便及分离优势而得到优先使用。然而,直接法分离中的手性固定相法因其条件的限制而不能被广泛使用,如需要昂贵的手性柱以及严格的立体定向性等。相比之下,使用手性流动相添加剂的方法分离物质具有更明显的优点,(1)常规的非手性柱和普通流动相即可实现分离,成本相对较低;(2)操作简便,拆分效果好;(3)可选择的手性添加剂种类多,范围宽,应用广;(4)可以用于制备光学纯药物。因此,HPLC手性流动相添加剂法为对映体分离提供了灵活的选择。手性流动相添加剂法是拆分药物对映体最便利有效的方法之一[28-30],其拆分原理是在流动相中添加某种手性试剂,该手性试剂与对映体溶质之间通过氢键、离子键、配位键或者空穴的包含作用等相互作用,形成非对映异构体,然后根据非对映异构体自身的稳定性及其在固定相和流动相之间的分配系数不同,从而实现对映体的拆分。
1 手性添加剂的种类及其拆分原理
1.1 环糊精类化合物
利用环糊精类化合物作为流动相手性添加剂是通过环糊精的内部空腔结构对药物对映体的包含作用,形成不同理化性质的手性包含物,使其在流动相和固定相中产生不同的分配系数,实现对映体的拆分。常用的环糊精化合物有β-环糊精、γ-环糊精、羟丙基-β-环糊精(HP-β-CD)、三甲基-β-环糊精(TM-β-CD)、羧甲基-β-环糊精(CM-β-CD)以及磺丁基醚-β-环糊精(SBE-β-CD)等,已应用于拆分肾上腺素的前药盐酸地匹福林[31]、盐酸替罗非班[32]、肌肉松弛药美索巴莫[33]、镇静催眠药佐匹克隆[34]、抗抑郁药西酞普兰[35]、非甾体抗炎药阿卓乳酸[36],β-肾上腺受体阻断剂美托洛尔和多巴胺再摄取抑制剂文拉法辛[37]、盐酸去甲苯福林[38]等。
1.2 手性金属配合物
手性试剂与金属离子形成的手性金属配合物,加入色谱流动相中,与拆分药物的对映体作用,形成两个非对映体配合物,它们与固定相发生立体选择性吸附和排斥作用不同,从而产生色谱的分离。常用的手性金属配合物中手性试剂通常是光学活性的氨基酸及其衍生物。它们适用于拆分氨基酸、羟基羧酸及其衍生物等。例如,L-脯氨酸、L-苯丙氨酸以及L-酒石酸及其衍生物,易于与过渡金属Cu2+、Zn2+、Ni2+、Cd2+等离子配位,形成手性金属配合物,已大量用于拆分盐酸莫西沙星[39]、氧氟沙星[40]、苯丙氨酸和色氨酸[41]、邻氯扁桃酸[42]、色氨酸[43]、扁桃酸衍生物[44]和甲状腺素[45]等。
1.3 手性离子对试剂
在色谱流动相中,加入能与药物对映体离子形成非对映体离子对的光学纯试剂,即手性离子对试剂。常用的手性离子对试剂有奎宁、奎尼丁、N-苄氧羰基-S-苯基-L-半胱氨酸甲酯、10-樟脑磺酸、N-苯甲酰氧基羰基-甘氨酸-L-脯氨酸和酒石酸衍生物等显碱性或酸性的试剂。手性离子对试剂的手性中心附近含有可离子化的官能团,在低极性的有机流动相中,与药物对映体分子产生静电作用或疏水性反应而生成非对映体离子对,非对映体离子对具有不同的稳定性,在流动相与固定相之间的分配行为有差异,进而差速迁移得以分离。手性离子对试剂已用于拆分普萘洛尔,苯丙醇胺、美托洛尔、肾上腺素和沙丁胺醇对映体[46-47]、胺类药物[48]等。
1.4 手性氢键试剂
手性氢键试剂是指能与药物对映体形成氢键,产生药物的非对映体,而得以分离物质。例如,N,N-二甲基-L-苯丙氨酸、N-乙酰基-L-缬氨酸-四丁酰胺等经过修饰的氨基酸和二肽类,它们已用于拆分左旋多巴[49]、巴比妥类、氨基酸及其衍生物、氨基醇等[50-51],它们通过在非极性或低极性的流动相中与药物对映体产生氢键作用来分离药物对映体。
2 流动相手性添加剂用于药物对映体拆分时的影响因素
不同的手性添加剂及浓度、流动相的pH与流速、柱温和有机改性剂等都对手性药物的拆分有影响,在具体应用中应不断试验与探索,才能获得最佳拆分效果。
2.1 不同的手性添加剂及浓度的影响
不同的手性添加剂具有不同的拆分原理,适用于不同结构的手性药物的拆分。通常一个有效的手性流动相添加剂,需要经过大量试验才能获得。翟明翚等[31]利用环糊精(β-CD)、羟丙基-β-环糊精(HP-β-CD)和羧甲基-β-环糊精(CM-β-CD)拆分盐酸地匹福林,获得较好的试验结果。上述三种手性流动相添加剂各自的拆分效果如图1所示,可见羧甲基-β-环糊精才能获得基线分离盐酸地匹福林对映体的目的(图1c)。
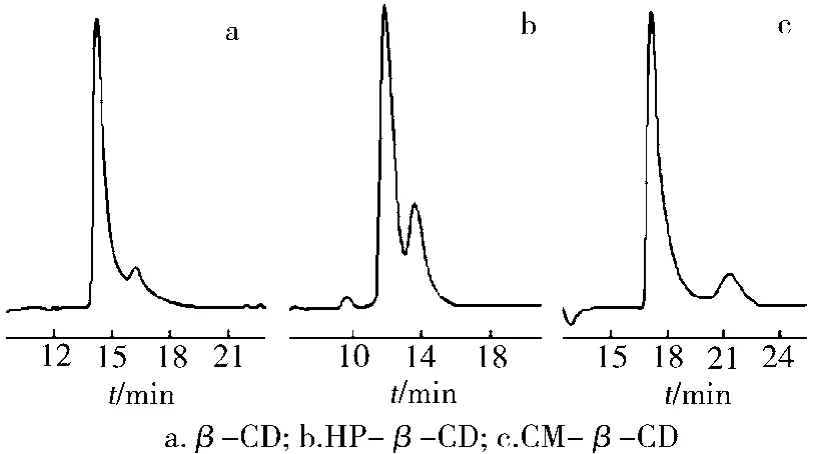
图1 不同的手性添加剂拆分盐酸地匹福林谱图[31]
CM-β-CD不同浓度拆分盐酸地匹福林的效果如图2所示。可见,随着CM-β-CD浓度的增加,分离度R于增大后减小,说明手性添加剂的浓度对药物对映体的拆分有影响,不同的浓度可能会改变分子间的作用力。然而整体上不同浓度范围内的CM-β-CD对盐酸地匹福林均有拆分效果,说明选取合适的手性添加剂对化合物的手性拆分的重要性。
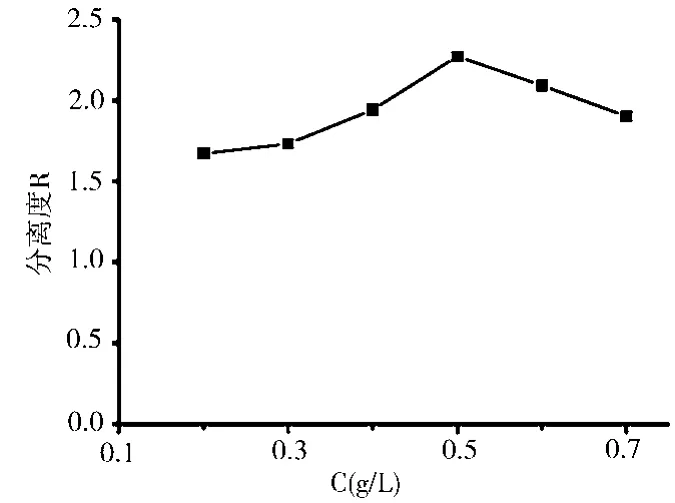
图2 手性添加剂浓度对分离度的影响
2.2 流动相不同的pH值及流速的影响
对带有酸性或碱性基团的药物分子,流动相的pH对其对映体的拆分有较大的影响,在不同酸碱条件下,对化合物对映体的分离具有非常显著的影响。翟明翚等[33]报道了用CM-β-CD手性流动相添加剂拆分美索巴莫对映体的试验结果,图3展示了不同流动相pH值对美索巴莫左右旋体拆分的影响。可见,随着流动相pH值的增大,对映体拆分的分离度呈现抛物线变化,这是因为美索巴莫分子在不同的pH值下具有不同的电离状态(图4所示),美索巴莫呈现出不同的分子结构,与CM-β-CD产生出不同的作用力,使非对映体包合物得到速差迁移,实现拆分目的。
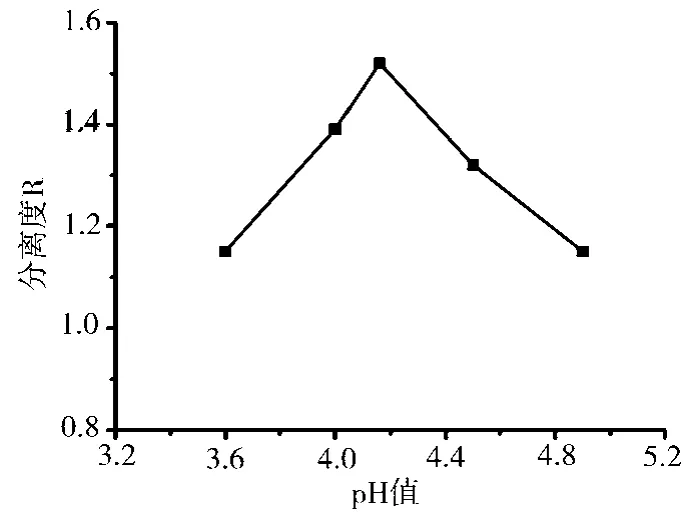
图3 流动相pH值对美索巴莫左右旋体拆分的影响
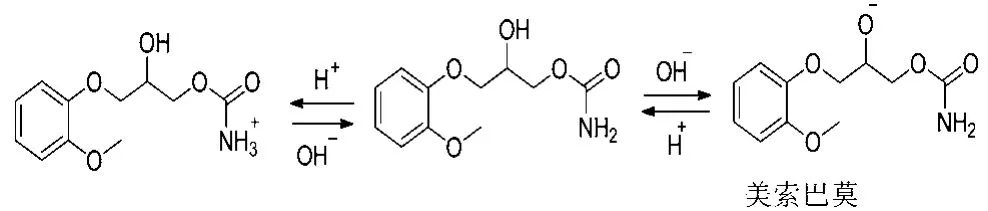
图4 美索巴莫的电离平衡反应
流速对美索巴莫左右旋体拆分的影响如图5所示。可见,当流速较快时,CM-β-CD与药物对映体分子形成的二个非对映体包合物在固定相上吸附的时间较短,迁移差异小,分离效果降低。但流速慢,出峰时间长,峰形变宽,色谱峰拖尾严重,拆分效果也变差。因此不同的流速对其拆分呈现不同的分离效果和分离度,选取合适的中等流速能够实现化合物的有效拆分。
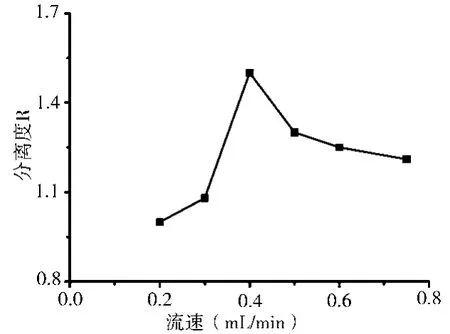
图5 流速对美索巴莫左右旋体的拆分的影响
2.3 柱温的影响
色谱柱温的改变会影响流动相中各分子的运动速率和解离状态,从而影响药物对映体与手性流动相添加剂的作用原理,产生拆分效果的差异。张虎等[36]报道了用手性流动相添加剂磺丁基醚-β-环糊精(SBE-β-CD)拆分阿卓乳酸对映体的研究。图6展示了柱温对拆分效果的影响。可见,随着柱温的升高,阿卓乳酸对映体的分离度逐渐减小,拆分效果变差。这可能是随着柱温的升高,阿卓乳酸对映体与手性流动相添加剂SBE-β-CD的作用发生了改变,非对映体复合物稳定性降低,色谱行为差异缩小,使拆分效果降低。
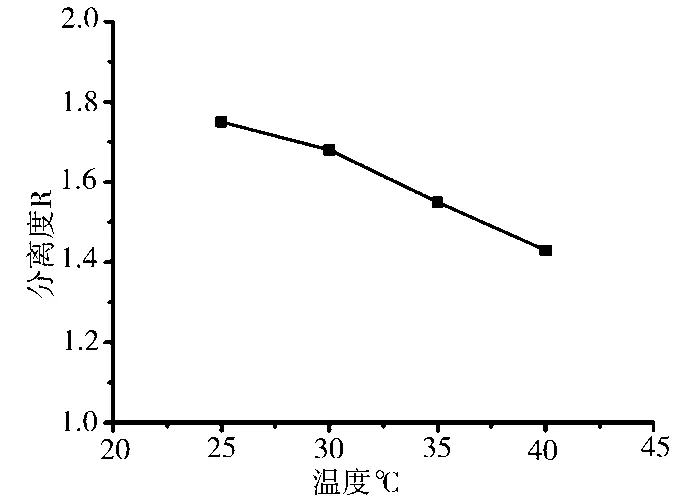
图6 柱温对阿卓乳酸对映体拆分效果的影响
通常柱温越高,色谱保留时间越短,拆分效果越差;柱温越低,保留时间越长,色谱峰变宽,分离度也下降,拆分效果越差,且柱温过低会导致柱压升高,损害色谱柱。所以,选择合适的柱温在药物对映体拆分应用中也很重要。
2.4 有机改性剂的影响
二元或多元溶剂系统组成的流动相,通常用有机溶剂作为改性剂,调节流动相的极性,改善色谱的峰形和平滑度,提高药物对映体的分离效能。翟明翚等[38]选用了甲醇或乙腈作为有机改性剂,研究了用CM-β-CD手性流动相添加剂拆分盐酸去甲苯福林对映体的效果,图7展示结果表明:甲醇-水、乙腈-水、以及甲醇-乙腈-水三种不同组成的溶剂系统组成的流动相,拆分盐酸去甲苯福林对映体的效果不同,其中甲醇-水系统组成的流动相未达到拆分药物对映体的效果,乙腈-水系统只实现部分对映体的拆分,而甲醇-乙腈-水系统,能实现对映体的基线分离。可见,不同有机改性剂组成的流动相对药物对映体的拆分效果也影响很大。
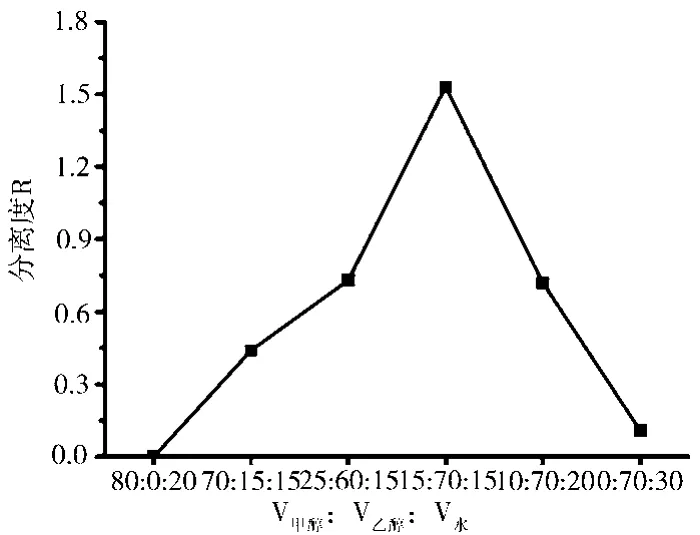
图7 有机改性剂的选择及比例对分离度的影响
有机改性剂的作用大小与其本身的溶解性、pH值、极性以及黏度有关。通常拆分酸性药物对映体选择酸性有机改性剂,拆分碱性药物对映体选择碱性有机改性剂。常用的有机改性剂有甲醇、乙腈、三乙胺以及缓冲盐溶液等。
3 结语
手性流动相添加剂法是重要的对映体拆分方法之一,具有操作简便、效率高、消旋化少、添加剂的选择范围宽等特点。能够应用于各种类型的手性药物的拆分试验。随着分析技术的不断进步,相信会有越来越多的手性药物拆分技术开发,手性流动相添加剂法拆分药物对映体技术也可以得到较大的发展。

