UPLC-QE/MS 法分析丹参酒炙前后5 种质变化合物
崔伟亮, 李慧芬, 张学兰, 宋梦晗, 刁家葳, 张丹捷, 王晓宁
(山东中医药大学, 山东 济南 250355)
丹参为唇形科植物丹参Salvia miltiorrhiza Bge.的干燥根及根茎[1], 始载于《神农本草经》, 列为草部上品[2], 生品性偏寒凉, 而酒制后寒凉之性缓和, 活血祛瘀、 调经止痛之功增强[3-5]。 中药炮制是药物中化学成分量变和质变的过程, 关乎药性变化、 功能主治改变、 临床应用调整[6]。现代研究发现, 丹参中主要含水溶性成分和脂溶性成分, 水溶性成分主要为多聚酚酸类, 有丹参素、 原儿茶醛、 丹酚酸A ~G、 紫草酸、 咖啡酸、迷迭香酸等, 具有抗缺血、 抗氧化、 改善微循环等作用[7-9]; 脂溶性成分大多为丹参酮类, 包括隐丹参酮、 丹参酮ⅡA、 丹参酮ⅡB、 二氢丹参酮Ⅰ、 二氢异丹参酮Ⅰ、 异丹参酮Ⅰ、 异丹参酮Ⅱ、 异隐丹参酮等, 具有改善血流循环、 抑制血小板聚集、 改善冠状动脉供血、 提高耐缺氧能力等作用[10]。
课题组前期对丹参酒炙前后质变特征化合物进行了含有量测定, 发现酚酸类主要成分中丹参素钠、 原儿茶醛、 迷迭香酸、 咖啡酸含有量升高, 丹酚酸B、 紫草酸含有量降低, 丹参酮类主要成分中丹参酮ⅡA、 丹参酮Ⅰ、 二氢丹参酮Ⅰ含有量升高,隐丹参酮含有量降低。 在前期工作的基础上, 本实验采用UPLC-QE/MS 法分析丹参酒炙前后5 种质变化合物模拟炮制品的化学成分, 探讨丹参酒炙前后质变特征化合物的转化机制, 为揭示其增效机理提供实验依据。
1 仪器与试药
1.1 仪器 UltiMate 3000 超高效液相色谱仪(美国Thermo 公司); Q ExactiveTMhybrid quadrupole-Orbitrap mass spectrometer (美国Thermo 公司);FA1604N 型电子天平(上海精密科学仪器有限公司); NewClassic MF 型天平(十万分之一, 瑞士Mettler-Toledo 公司); LDZ4-0.8 型离心机(北京医用离心机厂); KQ-250E 型医用超声波清洗器(昆山市超声仪器有限公司)。
1.2 试药 迷迭香酸对照品(天津士兰科技有限公司, 批号20283-92-5), 原儿茶醛、 丹酚酸B、咖啡酸、 隐丹参酮、 丹参酮Ⅰ、 丹参酮ⅡA对照品(中国食品药品检定研究院, 批号分别为200102、111562-200403、 0810-9803、 0852-9601、 0867-200205、 110766-200416); 丹参素、 阿魏酸、 紫草酸、 丹酚酸C、 二氢丹参酮Ⅰ(上海源叶生物科技有限公司, 批号分别为B20155、 B20007、 B21683、B20263、 B20256)。 甲醇为色谱纯; 其余试剂均为分析纯; 水为娃哈哈纯净水。
2 方法与结果
2.1 质变化合物模拟炮制品制备[11-12]称取迷迭香酸、 丹酚酸B、 隐丹参酮、 二氢丹参酮Ⅰ、 丹参酮ⅡA对照品适量, 分别加80%甲醇超声溶解, 即得。 取适量置于扁形称量瓶中, 于200 ℃烘箱内烘20 min, 取出, 放凉, 备用。
2.2 供试品溶液制备 取“2.1” 项下烘干的各质变化合物模拟炮制品, 分别加1 mL 80%甲醇超声溶解, 即得。
2.3 对照品溶液制备 精密称取丹参素、 原儿茶醛、 咖啡酸、 阿魏酸、 迷迭香酸、 紫草酸、 丹酚酸B、 丹酚酸C、 二氢丹参酮Ⅰ、 隐丹参酮、 丹参酮Ⅰ、 丹参酮ⅡA对照品各约0.5 mg, 分别置于1 mL量瓶中, 加80% 甲醇溶解并定容至刻度, 即得贮备液, 精密移取适量置于5 mL 量瓶中, 加80%甲醇稀释并定容至刻度, 即得。
2.4 液质条件
2.4.1 正离子模式 Halo C18柱(100 mm×2.1 mm,2.7 μm); 流动相乙腈(A) -水(B), 梯度洗脱(0~7 min, 70%→55%B; 7 ~12 min, 55%→40%B; 12~17 min, 40% →0B); 柱温45 ℃; 检测波长280 nm; 进样量3 μL; 体积流量0.25 mL/min。离子源为大气压离子源; 鞘气体积流量310 kPa;辅助气体积流量69 kPa; 裂解电压3.5 kV; 源内温度320 ℃; 辅助气温度350 ℃; S-lenS RF 水平55%; 分辨率70 000; 质谱扫描范围m/z 100 ~1 000。
2.4.2 负离子模式 Halo C18柱(100 mm×2.1 mm,2.7 μm); 流动相乙腈(B) -水(A), 梯度洗脱(0~5 min, 95%→60%A; 5 ~12 min, 60%→65%A; 12~15 min, 65%→0A); 柱温45 ℃; 检测波长280 nm; 进样量3 μL; 体积流量0.25 mL/min。离子源为大气压离子源; 鞘气体积流量310 kPa;辅助气体积流量69 kPa; 裂解电压3.0 kV; 源内温度320 ℃; 辅助气温度350 ℃; S-lenS RF 水平55%; 分辨率70 000; 质谱扫描范围m/z 100 ~1 500。
2.5 丹参酒炙前后质变化合物模拟炮制品成分分析 化合物通过质谱数据解析、 已知对照品定位并参考文献进行鉴别, UPLC-QE/MS 综合分析, 发现了迷迭香酸、 丹酚酸B、 隐丹参酮、 二氢丹参酮Ⅰ、 丹参酮ⅡA。 混合对照品UPLC 色谱图见图1,5 种质变化合物模拟炮制品总离子流图见图2~6,数据分析见表1, 模拟炮制后分解产物见表2。
根据5 种化合物模拟炮制品的质谱数据, 由文献及相应化合物在反相柱上的保留值可知, 在图2~3 中, tR为1.12 min 得到m/z 197.04 [M-H]-的准分子离子峰, 其保留时间与丹参素对照品一致, 确定其相对分子质量为198.17, 与丹参素相符, 故鉴定为丹参素; tR为2.68 min 获得分子离子峰m/z 179.03 [M-H]-, 其保留时间与咖啡酸对照品一致, 确定其相对分子质量为180.15, 与咖啡酸相符, 故鉴定为咖啡酸; tR为3.71 min 得到m/z 359.08 [M-H]-的准分子离子峰, 其保留时间与迷迭香酸对照品一致, 确定其相对分子质量为360.31, 与迷迭香酸相符, 故鉴定为迷迭香酸。
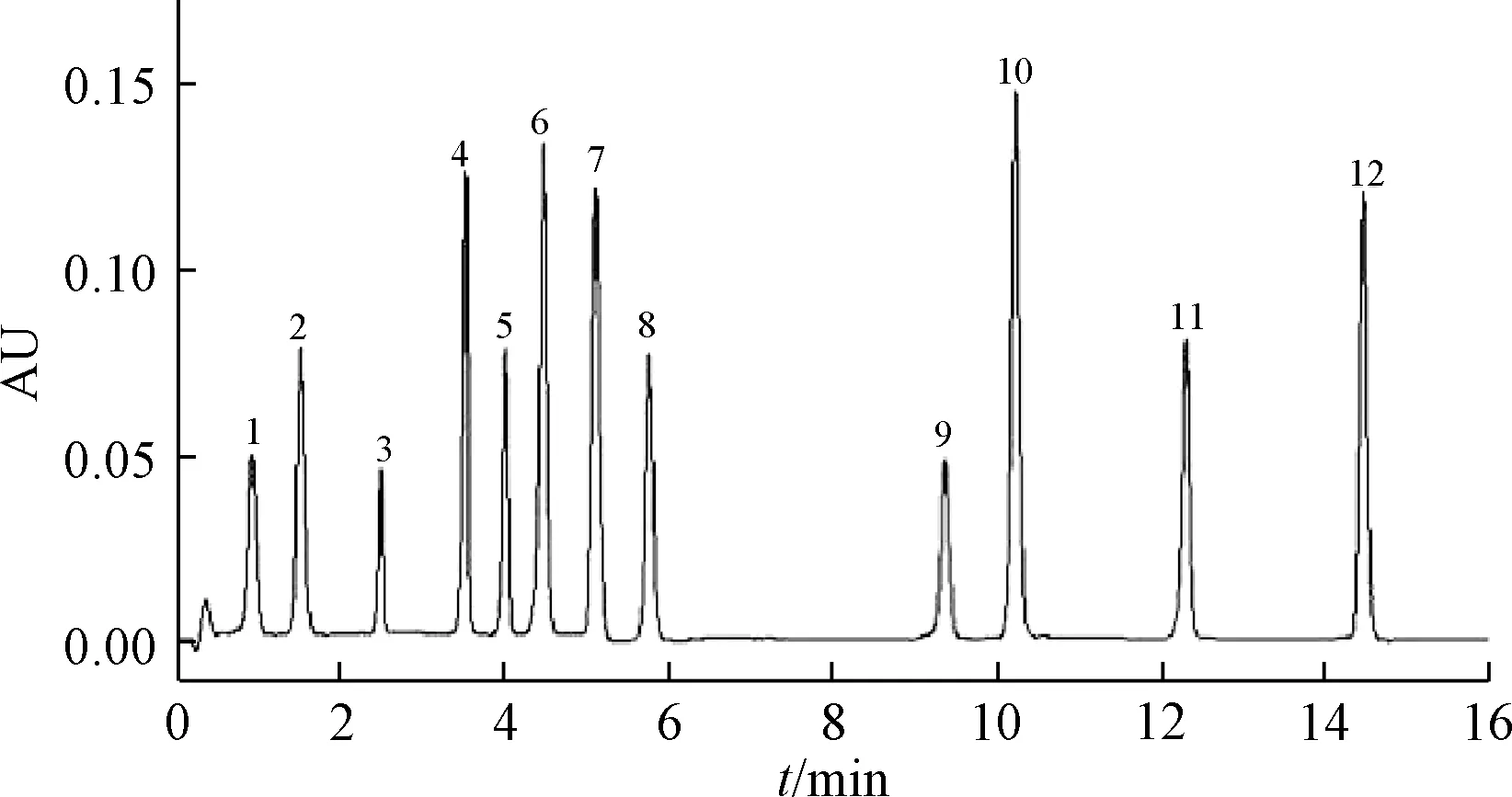
图1 混合对照品UPLC 色谱图Fig.1 UPLC chromatogram of mixed reference substance

图2 迷迭香酸总离子流图Fig.2 Total ion current chromatogram of rosemary acid
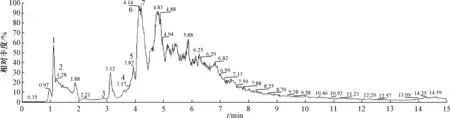
图3 丹酚酸B 总离子流图Fig.3 Total ion current chromatogram of salvianolic acid B

图4 隐丹参酮总离子流图Fig.4 Total ion current chromatogram of cryptotanshinone

图5 二氢丹参酮Ⅰ总离子流图Fig.5 Total ion current chromatogram of dihydrotanshinoneⅠ

图6 丹参酮ⅡA 总离子流图Fig.6 Total ion current chromatogram of tanshinoneⅡA

表1 丹参酒炙前后5 种质变化合物模拟炮制品UPLC-MS 鉴定结果Tab.1 UPLC-MS identification results of five kinds of qualitative change compounds in wine processing of S. miltiorrhiza

表2 丹参酒炙前后5 种质变化合物模拟炮制品成分分析结果Tab.2 Analysis results of five kinds of qualitative change compounds in wine processing of S. miltiorrhiza
图3 中, tR为5.08 min 得到m/z 193.04 [MH]-的准分子离子峰, 其保留时间与阿魏酸对照品一致, 确定其相对分子质量为194.19, 与阿魏酸相符, 故鉴定为阿魏酸。 tR为1.28 min 得到m/z 193.04 [M-H]-的准分子离子峰, 其保留时间与原儿茶醛对照品一致, 确定其相对分子质量为194.19, 与原儿茶醛相符, 故鉴定为原儿茶醛; tR为3.87 min 得到m/z 537.10 [M-H]-的准分子离子峰, 其保留时间与紫草酸对照品一致, 确定其相对分子质量为538.46, 与紫草酸相符, 故鉴定为紫草酸。
图4 中, tR为10.48 min 得到m/z 297.11[M+H]+的准分子离子峰, 其保留时间与隐丹参酮对照品一致, 确定其相对分子质量为296.35, 与隐丹参酮相符, 故鉴定为隐丹参酮。 图5~6 中, tR为9.82 min 得到m/z 279.10 [M+H]+的准分子离子峰, 其保留时间与二氢丹参酮Ⅰ对照品一致, 确定其相对分子质量为278.30, 与二氢丹参酮Ⅰ相符, 故鉴定为二氢丹参酮Ⅰ; tR为12.46 min 得到m/z 277.08 [M+H]+的准分子离子峰, 其保留时间与丹参酮Ⅰ对照品一致, 确定其相对分子质量为276.29, 与丹参酮Ⅰ相符, 故鉴定为丹参酮Ⅰ; tR为12.46 min 得到m/z 295.13 [M+H]+的准分子离子峰, 其保留时间与丹参酮ⅡA对照品一致, 确定其相对分子质量为294.34, 与丹参酮ⅡA相符, 故鉴定为丹参酮ⅡA。
3 讨论与结论
根据对照品定位并参照文献, 采用UPLC-QE/MS 对丹参中5 种质变化合物模拟炮制品进行分析和成分鉴别, 结果表明该方法快速、 灵敏、 准确度高, 可较全面、 准确地分析各化合物在炮制过程中的变化规律, 为揭示丹参成分转化机制提供科学依据。 实验中曾采用100 ℃水浴加热20、 50 min 模拟炮制, 但加热前后各成分无明显变化, 又采用烘箱200 ℃干烘10、 20、 50 min 对对照品进行模拟炮制, 模拟炮制前后成分变化也不大, 最后采用80%甲醇超声溶解后于200 ℃烘20 min, 各成分发生较明显变化。 本研究表明, 丹参酒炙前后质变的5 种主要成分在模拟炮制条件下均发生了质变。
国内外研究发现, 丹酚酸B 在体内首先代谢为丹参素及咖啡酸, 咖啡酸进一步代谢为阿魏酸和异阿魏酸, 两者继续代谢为甲基化阿魏酸[13-15]。同时, 有学者研究表明丹酚酸B 口服生物利用度低, 丹参素的生物利用度、 最大血药浓度明显高于丹酚酸B, 平均驻留时间、 半衰期明显长于后者,故丹参素在体内作用持久[16]; 迷迭香酸在体内可代谢为咖啡酸、 阿魏酸、 甲基化迷迭香酸和香豆酸[17]; 隐丹参酮在体内可转化为丹参酮ⅡA[18-19]。由此可知, 丹参酒炙后主要成分的体外模拟炮制产物与其体内代谢转化基本一致, 推测丹参酒炙后活血化瘀药效增强可能与丹酚酸B、 迷迭香酸、 隐丹参酮等分子量较大的主要成分炮制后转化成更利于吸收、 活性更强的成分关系密切。

