HPLC-DAD法同时测定柴黄片中6种成分的含量Δ
丁长玲,崔俊凤,石效荣,徐洋洋,成文娜,张金杰,赵丽(.滨州医学院附属医院药学部,山东滨州5660;.滨州市食品药品检验检测中心,山东滨州 5668;.滨州医学院附属医院疼痛科,山东滨州5660)
柴黄片质量标准收载于2015年版《中国药典》(一部)[1],是由柴胡和黄芩经现代工艺加工制备而成的中药制剂,具有清热解表之功效,临床上用于治疗风热感冒引起的发热、周身不适、咽喉肿痛、头痛目眩等病症[2]。现行标准中只规定了黄芩中黄芩苷的含量测定,没有规定柴胡中活性成分的含量控制,黄芩中主要活性成分黄芩苷、汉黄芩苷、黄芩素、汉黄芩素的含量以及柴胡中的主要活性成分柴胡皂苷a和柴胡皂苷d含量高低均会影响制剂的功效。为了更好地控制药品质量,确保柴黄片的临床疗效,笔者采用高效液相色谱-二极管阵列检测器(HPLC-DAD)法同时测定柴黄片中的黄芩(黄芩苷、汉黄芩苷、黄芩素、汉黄芩素)和柴胡(柴胡皂苷a和柴胡皂苷d)中6种有效成分的含量,为全面评价该药物的质量提供一种简便快速、准确可靠的检验方法,并为临床应用该制剂提供确切的质量保障。
1 材料
1.1 仪器
Agilent Technologies 1260 HPLC仪、Agilent Technologies G1315D DADVL检测器(美国安捷伦科技有限公司);XSE205DU电子天平(瑞士梅特勒-托利多公司);KQ-700 DV超声波清洗器(昆山超声仪器有限公司)。
1.2 药品与试剂
柴黄片(陕西盘龙制药集团有限公司,批号20170812、20171216、20180623,规格:0.5 g);6种对照品黄芩苷(批号:110715-201720,纯度:93.5%)、汉黄芩苷(批号:110753-200411,纯度:95.5%)、黄芩素(批号:111595-201306,纯度:97.6%)、汉黄芩素(批号:111514-201605,纯度:96.5%)、柴胡皂苷 a(批号:110777-201510,纯度:93.2%)和柴胡皂苷 d(批号:110778-201205,纯度:94.6%)均来源于中国食品药品检定研究院;柴胡、黄芩药材均购自安徽井泉集团中药饮片有限公司(批号:分别为20170611、20180226),均经山东中医药大学中药鉴定室周凤琴主任中药师检定为正品;乙腈为色谱纯、磷酸为优级纯、乙醇为分析纯、试验用水为超纯水。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品贮备溶液 精密称取6种对照品适量,分别置于25 mL量瓶中,加入适量的50%乙醇,振摇,溶解后定容至刻度,摇匀,即得黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d的质量浓度分别为0.948 8、0.414 8、0.393 9、0.407 2、0.404 5、0.386 3 mg/mL的对照品贮备溶液。
2.1.2 混合对照品溶液 分别精密量取黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d对照品贮备溶液各4.0、2.0、1.0、1.0、1.0、1.0 mL,置于10 mL量瓶中,摇匀,得混合对照品溶液,每1 mL溶液中含黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d分别为379.52、82.96、39.39、40.72、40.45、38.63 μg。
2.1.3 供试品溶液 取本品10片,用手术刀片轻轻刮除包衣,精密称定,研细;取约0.5 g,精密称定,置于100 mL量瓶中,加入50%乙醇适量,30℃水温超声处理(功率:500 W,频率:40 kHz)45 min,放冷;加50%乙醇至刻度,摇匀,滤过,精密量取续滤液5 mL,置于50 mL量瓶中,加50%乙醇至刻度,摇匀,用0.45µm微孔滤膜滤过,取续滤液即得。
2.1.4 缺柴胡阴性对照溶液 取黄芩100 g,按照柴黄片相应工艺制法制成100片,按“2.1.3”项下方法制成缺柴胡阴性对照溶液。
2.1.5 缺黄芩阴性对照溶液 取柴胡100 g,按照柴黄片相应工艺制法制成100片,按“2.1.3”项下方法制成缺黄芩的阴性对照溶液。
2.2 色谱条件及系统适用性、专属性试验
色谱柱:Agilent Eclipse XDB-C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-磷酸三乙胺水溶液(B,取三乙胺5 mL用水稀释至1 000 mL,用磷酸调节pH至7.0)为流动相进行梯度洗脱(0~50 min,25%A→70%A;50~60 min,70%A);流速:1.0 mL/min;检测波长:210 nm(柴胡皂苷a和柴胡皂苷d)、277 nm(黄芩苷、汉黄芩苷、黄芩素和汉黄芩素);柱温:30℃;进样量:5 μL。精密吸取混合对照品溶液、供试品溶液(批号:20170812)和阴性对照溶液各5 μL进样分析,结果各检测成分色谱峰与相邻色谱峰的分离度均大于1.5,对称因子在0.90~1.10,理论板数以黄芩苷峰计均大于6 000;在供试品溶液的色谱图上,在与对照品溶液黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d相应的位置上,均有相同保留时间的色谱峰,阴性对照溶液在对应保留时间处未见色谱峰,不干扰测定,表明系统的适用性良好及方法的专属性良好。色谱见图1、图2、图3。
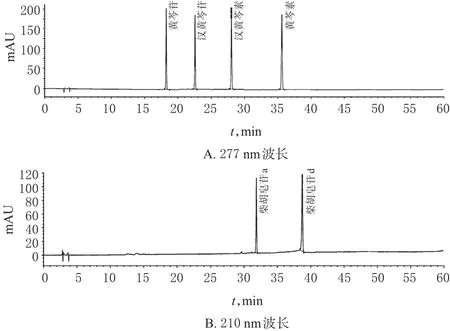
图1 混合对照品溶液高效液相色谱图Fig 1 HPLC chromatogram of mixed control solution
2.3 线性关系、检测限、定量限考察
取混合对照品溶液1、5、10、15、20 μL,注入HPLC仪中,在“2.2”项色谱条件下进样测定,以对照品进样量(μg)为横坐标(x),对各成分的峰面积(纵坐标,y)进行线性回归,计算出线性回归方程。另将混合对照品溶液逐级稀释,当信噪比3∶1时得检测限,当信噪比为10∶1时得定量限,结果见表1。
2.4 精密度试验
精密吸取混合对照品溶液,在“2.2”项色谱条件下连续进样6次,记录黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d的色谱峰面积,计算其RSD分别为0.62%、0.71%、0.55%、0.67%、0.83%、0.79%(n=6),表明该仪器的精密度良好。
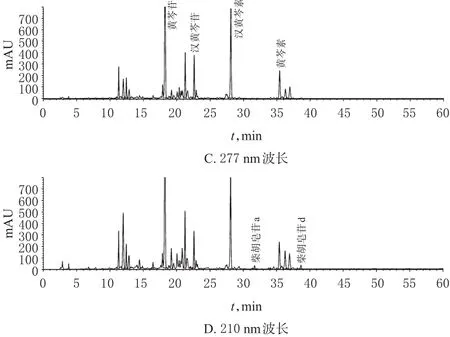
图2 供试品溶液高效液相色谱图Fig 2 HPLC chromatogram of test sample
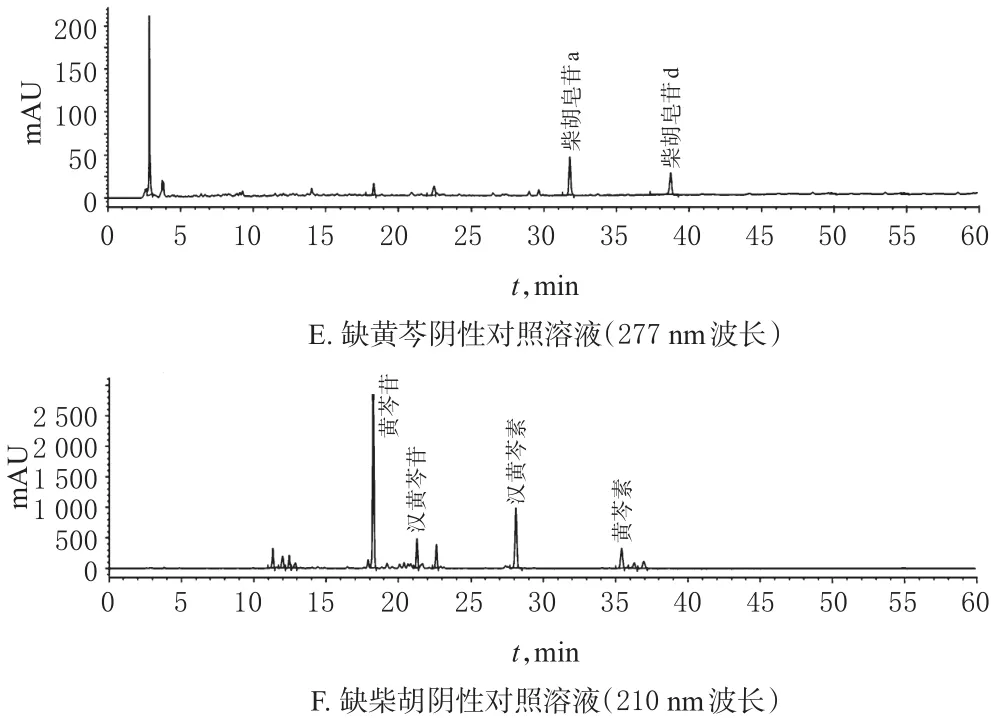
图3 阴性溶液高效液相色谱图Fig 3 HPLC chromatogram of negative solution

表1 6种成分的线性关系Tab 1 Linear relationship of 6 components
2.5 稳定性试验
精密吸取同一批供试品溶液(批号:20170812)5 μL,在“2.2”项色谱条件下,在配制后0、4、8、16、32、48 h进样测定,记录黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d的色谱峰面积,计算其RSD分别为0.51%、0.57%、0.72%、0.64%、0.85%、0.93%(n=6),表明供试品溶液在48 h内稳定性良好。
2.6 重复性试验
取批号为20170812的药品,按“2.1.3”项下方法制备供试品溶液6份,在“2.2”项色谱条件下进样测定,记录黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d的峰面积,计算其含量的RSD分别为0.83%、0.80%、0.75%、0.69%、0.98%、1.02%(n=6)。
2.7 加样回收率试验
精密称取含量已知的柴黄片(批号:20170812)6份,分别置于100 mL量瓶中,分别精密加入0.948 8 mg/mL黄芩苷对照品溶液20.0 mL、0.414 8 mg/mL汉黄芩苷对照品溶液10.0 mL、0.393 9 mg/mL黄芩素对照品溶液5.0 mL、0.407 2 mg/mL汉黄芩素对照品溶液2.0 mL、0.404 5 mg/mL柴胡皂苷a 1.5 mL、0.386 3 mg/mL柴胡皂苷d 1.0 mL,加入50%乙醇适量,30℃水温超声处理(功率:500 W,频率:40 kHz)45 min,放冷,加50%乙醇至刻度,摇匀;滤过,精密量取续滤液5 mL,置于25 mL量瓶中,加50%乙醇至刻度,摇匀,用0.45µm微孔滤膜滤过,取续滤液在“2.2”项色谱条件下进样5 μL,测定,计算回收率,结果见表2。
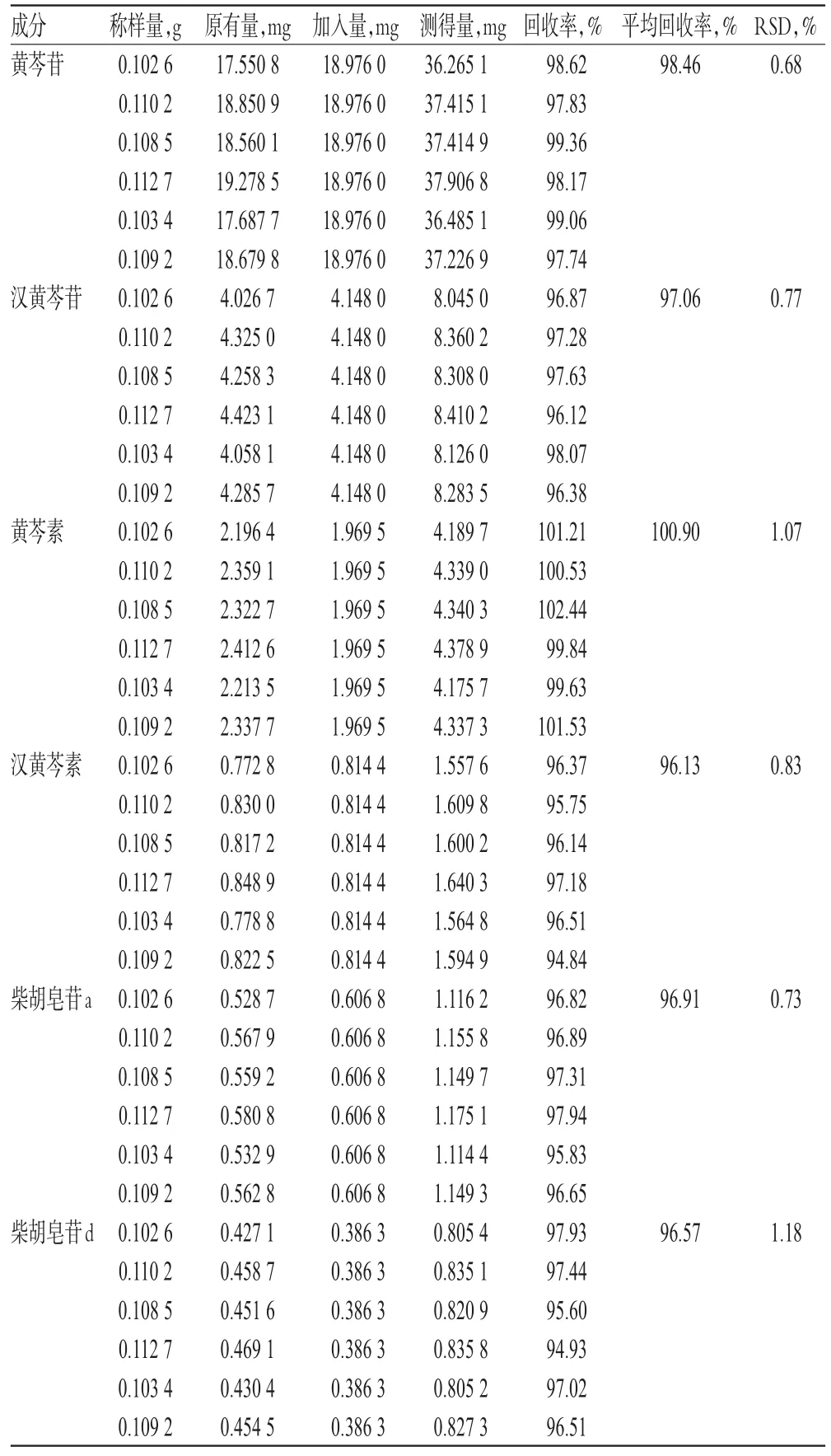
表2 回收率试验结果(n=6)Tab 2Results of recovery tests(n=6)
2.8 样品含量测定
取3批样品(批号分别为20170812、20171216、20180623),按“2.1.3”项下方法制备供试品溶液,精密吸取供试品溶液和对照品溶液各5 μL,在“2.2”项色谱条件下进样测定,结果见表3。
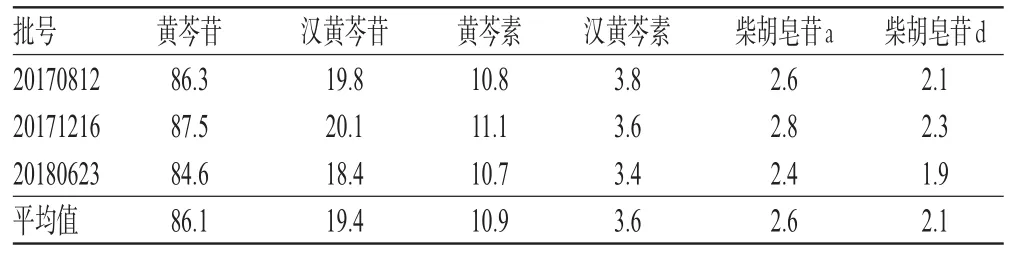
表3 样品含量测定结果(mg/片,n=3)Tab 3 Results of content determination of samples(mg/tablet,n=3)
3 讨论
3.1 检测波长的选择
笔者参考文献[2-4] 和对照品溶液的紫外扫描图谱(190~400 nm),发现黄芩苷在278 nm、汉黄芩苷在276 nm、黄芩素在272 nm、汉黄芩素在276 nm波长处有最大吸收,柴胡皂苷a、柴胡皂苷d在210 nm波长处有最大吸收,故本文在满足含量测定要求的前提下,综合考虑到峰形、分离度等因素,确定采用HPLC-DAD法,以277、210 nm分别为柴黄片中6种成分含量测定的波长,不但可避免杂质干扰且灵敏度高。
3.2 流动相的选择
笔者在预试验过程中并参考文献[5-9] 方法,分别考察了甲醇-0.05%磷酸水溶液、乙腈-0.05%磷酸水溶液、乙腈-水、甲醇-水、乙腈-磷酸三乙胺水溶液为流动相时进行等度和梯度洗脱对结果的影响。结果显示,在前4种流动相下各成分峰形和分离度均达不到要求,而以乙腈-磷酸三乙胺水溶液为流动相进行等度和梯度洗脱时,供试品溶液中的各检测成分色谱峰与相邻色谱峰的分离度均大于1.5,对称因子在0.90~1.10,理论板数均大于6 000,故本研究选择乙腈-磷酸三乙胺水溶液作为流动相进行梯度洗脱。
3.3 提取方法的考察
笔者在进行样品处理时首先参考了2015年版《中国药典》(一部)中相应的处理方法[1],参考相关文献[10-13] 及该处方的制备工艺,选用30%乙醇、50%乙醇、70%乙醇、30%甲醇和50%甲醇作为提取溶剂,分别超声30、45 min,结果发现,以50%乙醇作为溶剂,超声处理45 min,黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d提取效率更高,因此本研究选用50%乙醇超声45 min作为提取方法。
3.4 含量测定6种指标性成分的选择
柴黄片具有清热解表功效,临床上用于风热感冒引起的发热等病症,其主要活性成分为黄酮类和皂苷化学成分,其中黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d 6种成分含量较高[14]。现代药理学研究表明,黄芩的有效成分均具有广谱抗菌、抗病毒及良好的抗炎作用,且该作用与黄芩提取物浓度呈正相关,呈现出清热镇痛功效[15]。柴胡中的有效成分柴胡皂苷a和柴胡皂苷d也具有解热、镇痛、抗炎、抗菌作用[16]。黄芩和柴胡活性明确,其中有效成分含量的高低是衡量柴黄片质量的重要指标,也是影响药效的主要因素。为了更好地保证柴黄片在临床使用上的有效性和安全性,故笔者以黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d为指标评价柴黄片的质量更为全面和合理。
3.5 含量结果分析
本试验对3批柴黄片中的黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d进行了含量测定,结果发现,同一厂家不同批号之间含量测定结果有一定的差异,进一步说明了开展多种成分质量控制的中成药整体控制比以单一指标成分控制中成药质量更可靠[17]。如果对该药品进行6种成分的质量控制,就可以从源头控制药材质量和制备过程,进而控制柴黄片的质量,保证临床疗效。
综上,本研究建立了HPLC-DAD法同时测定柴黄片中6种成分含量的方法;按照有效成分不低于3批制剂平均含量80%的要求,建议在柴黄片质量控制标准中,每片含黄芩苷、汉黄芩苷、黄芩素、汉黄芩素、柴胡皂苷a和柴胡皂苷d应分别不低于69.0、15.0、8.0、3.0、2.0、1.5 mg。

