新生儿持续肺动脉高压最新治疗进展
朱玲


【摘要】 新生儿持续肺动脉高压(PPHN)是新生儿重症监护区最常见的疾病之一。可因先天性发育异常、围生期缺氧、感染等因素使肺血管压力增高,导致出生后右心血液不能有效进入肺内氧合,产生严重低氧血症。因发病机制的不同,新生儿持续肺动脉高压有别于儿童或者成人肺动脉高压的治疗。目前治疗PPHN的方法主要有高频机械通气、吸入NO、磷酸二酯酶抑制剂等方法。本综述旨在针对继发性PPHN寻求最新且全面的治疗方法。
【关键词】 新生儿; 肺动脉高压; 持续胎儿循环
doi:10.14033/j.cnki.cfmr.2019.20.082 文献标识码 A 文章编号 1674-6805(2019)20-0-03
Recent Advances in the Treatment of Neonatal Persistent Pulmonary Hypertension/ZHU Ling.//Chinese and Foreign Medical Research,2019,17(20):-186
【Abstract】 Persistent pulmonary hypertension of the newborn(PPHN) is one of the most common diseases in the neonatal intensive care unit.Because of congenital developmental abnormalities,perinatal hypoxia,infection and other factors,pulmonary vascular pressure increases,resulting in the right heart blood after birth can not effectively enter the pulmonary oxygenation,resulting in severe hypoxemia eventually.Due to different pathogenesis,the treatment persistent pulmonary hypertension of newborn is different from that in children or adults.At present,the main methods of PPHN treatment are high frequency mechanical ventilation,inhalation of NO,phosphodiesterase inhibitors and so on.This review aim to seek the latest and comprehensive treatment for secondary PPHN.
【Key words】 Newborn; Pulmonary hypertension; Persistent fetal circulation
First-authors address:Chengdu Women and Children Central Hospital,Chengdu 611130,China
新生兒持续肺动脉高压(persistent pulmonary hypertension of the new born,PPHN)是NICU常见的危重症疾病。PPHN发病率与地域及经济水平相关,在西方发达国家发病率为(1.8~1.9)/1 000,亚洲国家发病率(1.2~4.6)/1 000[1-2]。死亡率高达20.6%[3]。该病对新生儿循环系统、呼吸系统均会造成严重威胁,死亡风险高。因此对PPHN的病因、诊断、治疗方法进行研究意义重大。
1 发病机制及原因
PPHN发病机制多由肺组织发育不全、肺血管发育不良、肺血管适应不良三大因素造成,最终导致肺血管阻力增加,血液不能进入肺内氧合,导致低氧血症[4]。肺组织发育不全及发育不良等肺组织原发的结构异常多致原发性PPHN,临床治疗效果差,死亡率高。但临床更多PPHN为围生期低氧、低温、酸中毒、胎粪吸入、肺部感染、RDS等原因导致肺血管适应不良造成继发性PPHN,治疗效果较理想[5]。
PPHN多发生于足月儿及过期产儿,发病机制不尽相同。早产儿发生PPHN因发病早晚发病机制不尽相同。早产儿早发型PPHN是由于肺血管不成熟所致发育不全;而晚发型PPHN则因严重BPD所致肺血管适应不良所致。
2 诊断方法
危重患儿中,若吸入纯氧亦无法纠正严重的低氧血症(PaO2<50 mm Hg),且排除先天性心脏病,临床表现与肺部病变不符的低氧血症后可首先考虑PPHN。临床常用的方法是测量动脉导管前后(右上肢与下肢)血氧饱和度,若上下肢血氧饱和度(SpO2)相差大于20%则可诊断PPHN。临床中亦可出现上下肢SpO2差异不显著,可通过心脏彩超测量肺血管阻力、肺血流、肺毛细血管楔压、右心压力、三尖瓣反流程度等参数间接测量出肺动脉压力,从而诊断PPHN。心导管检查虽作为诊断PPHN的“金标准”,但其为有创操作,且PPHN多为危重患儿,现临床很少使用。目前根据上下肢SpO2差异联合心脏彩超得以确诊PPHN[6-7]。
3 治疗方法
临床以继发性PPHN多见,首先需寻找出导致PPHN的高危因素,针对病因治疗。其次常规需要改善肺通气,纠正酸中毒,改善外周循环,强化心功能,维持正常血压等治疗。
3.1 机械通气
PPHN均需有创机械通气治疗。通气模式常选择具有小潮气量的高频振荡通气(high frequency oscillation ventilation,HFOV),HFOV能够募集更多肺泡,增加肺血管总表面积,改善通气/血流比值,促进二氧化碳排出,改善肺部氧合,降低肺动脉阻力,更能及时改善心、脑、肾等重要脏器的氧合,防止多脏器功能损伤。但应用HFOV时Paw较高,使用前需纠正低血容量、低血压,改善心功能,保证回心血量。目前有条件进行HFOV治疗的医院,多联合iNO治疗PPHN,能够取得理想效果[8-9]。
3.2 药物治疗
3.2.1 吸入一氧化氮(Inhaled Nitric Oxide,iNO) 鸟苷酸环化酶(GC)能够使GTP与5GMP 合成环磷酸鸟苷(cGMP),NO能够激活GC,促进cGMP合成,cGMP使细胞内游离钙减少,使血管平滑肌舒张,从而扩张肺血管,见图1。
NO能够高选择性扩张肺血管,直接降低肺动脉阻力,改善肺部氧合,国外有很多的动物研究肯定了iNO的安全性及有效性[10];iNO对早产儿中PPHN,即使在早期预防性应用,并不能改善其预后,可能与早产儿本身合并肺发育不良有关[11]。
早目前很多大型医院已将iNO作为治疗PPHN最常用的方法。常规使用方法为开启NO设备后,初始参数设定为NO流速20 ppm;治疗过程中逐渐下调,每4~6小时可下调5 ppm,降至5 ppm维持治疗,一般治疗时长为72 h。若临床上下肢SPO2差异不大,但呼吸机参数要求高,当氧指数(OI=FiO2×MAP÷PaO2),OI>20即可使用iNO。
iNO的使用,抑制PPHN的進展,可快速缓解低氧血症,改善病情,更降低ECMO的风险,缩短了住院时间。临床多数PPHN患儿对iNO起效迅速,效果良好。但iNO治疗PPHN还有很多局限性:(1)NO气源价格昂贵,很多基层医院无法开展。即使能够转诊至有条件的上级医院,转诊过程花费时间长,组织缺氧不能及时纠正,可致多脏器功能损伤,预后差。近年来发现国外已研究出利用空气募集NO的设备[10],期待以后更多基层医院能够具备iNO治疗条件;(2)iNO能够快速纠正低氧血症,但没有文献支持iNO能够降低患儿死亡率;(3)iNO增加肺出血、脑出血风险;(4)iNO半衰期短,治疗完成后可有反跳现象[11]。
3.2.2 西地那非(Sildenafil) 磷酸二酯酶-5(phosphodiesterase,PDE)能够使环磷酸鸟苷(cGMP)分解为GTP与5GMP,西地那非系PDE5抑制剂,抑制cGMP的分解,从而间接扩张肺血管,见图1。在无iNO的医院,可首选西地那非联合机械通气等其他治疗方法治疗PPHN。西地那非用法:2 mg/(kg·次),口服,3次/d,直至患儿撤机[12-15]。
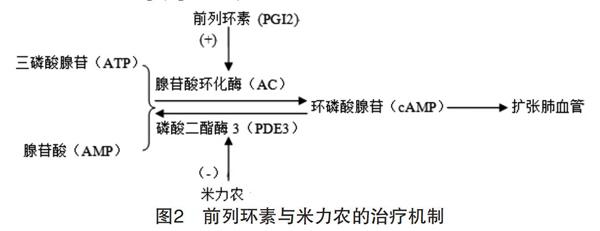
3.2.3 米力农(Milrinone) 磷酸二酯酶-3(PDE3)能够使环磷酸腺苷(cAMP)分解为ATP与AMP,米力农系PDE3抑制剂,从而抑制cAMP的分解,间接扩张肺血管见图2。同时米力农可增加心肌收缩力,改善心功能[15-16]。米力农用法:负荷量
50 μg/kg,>1 h静脉输注;维持量0.33~0.99 μg/(kg·min),维持24~72 h。米力农扩血管为非选择性,需注意监测血压,同时警惕心律失常等不良反应。
西地那非及米力农均为磷酸二酯酶抑制剂均在降低肺动脉高压具有一定作用,但由于其安全性尚未完全确定,只能作为辅助iNO或在其他常规治疗方法无效时使用。
3.2.4 前列环素(prostacyclin PGI 2) 腺苷酸环化酶(AC)能够使ATP与AMP合成环磷酸腺苷(cAMP),PGI2激活AC,促进cAMP合成,同cGMP一样也能使细胞内游离钙减少,扩张肺血管,见图2。前列环素用法:10~50 ng/(kg·min),SaO2>90%后逐渐减量至5 ng/(kg·min)维持至72 h[17]。
PGI2在基层医院可得,在没有其他药物选择的情况下,可联合呼吸机治疗PPHN。但PGI2有强大的扩血管作用,有浓度依赖性,需密切监测动脉血压,及时调整用量。
3.2.5 波生坦(Bosentan) 内皮素(endothelin,ET)由血管内皮细胞产生,其中ET-1为其异构体之一,但ET-1与ETa受体结合后可出现强烈且持久的缩血管作用,见图3。国内外均有研究表明ET-1与PPHN有着紧密联系,Mei等[18-19]的一项研究中,PPHN组患儿血清ET-1显著高于非PPHN组。波生坦为非选择性ET-1受体阻滞剂,波生坦与ETa受体结合,抑制ET-1的血管平滑肌收缩作用,抑制肺血管收缩,降低肺血管阻力。
波生坦已成熟应用于成人的肺动脉高压,现已有研究证明可用于新生儿PPHN中,希望有更多的临床研究能够支持波生坦在新生儿PPHN作用[20-21]。
3.2.6 其他 硫酸镁、酚妥拉明均能使血管扩张,但特异性均差,会影响全身血管收缩,需要加强血压、血钙的监测,预防不良反应发生,临床应用少。
体外膜肺(extracorporeal membrane oxygenation,ECMO)是救治严重呼吸衰竭患儿的终末手段。所有机械通气不能改善的低氧性呼吸衰竭均可考虑。目前使用ECMO指征:(1)OI>40超过4 h;(2)OI>20超过24 h或呼吸困难持续恶化;(3)严重低氧血症(PaO2<40 mm Hg);(4)持续PPHN伴右心衰竭。ECMO治疗时是将患儿血液通过外部膜肺使血液体外氧合,为肺功能恢复提供时间。但国内只有少数几家新生儿ECMO中心,治疗费用昂贵。ECMO禁忌证:致死性染色体疾病(13/18三体);严重脑损伤或颅内出血;<34周早产儿;不能逆肺外器官损伤等均不能入组ECMO治疗[22-23]。
4 总结
随着危重新生儿的增多,导致PPHN发生率增高,且病因多种多样。在针对治疗原发病的同时,尽快纠正PPHN,使循环改善,组织及脏器得到有效供氧。目前治疗PPHN的治疗方法国内外都大致相同,iNO都是治疗PPHN首选方法,但其费用高,NO获取困难,基层医院难以开展[24]。希望随着医疗技术的进步,NO小型制备机器得以发展,能有效推广iNO的使用。若无iNO,西地那非可做替代治疗[25],其他药物治疗安全性及有效性尚存在争议,但对于基层医院,能够因地制宜,根据自身医疗条件,选择适当的治疗方法。更期待有简单、疗效明确治疗PPHN的方法,为PPHN提供及时有效的治疗。
参考文献
[1] Walshsukys M C,Tyson J E,Wright L L,et al.Persistent Pulmonary Hypertension of the Newborn in the Era Before Nitric Oxide:Practice Variation and Outcomes[J].Pediatrics,2000,105(1Pt1):14.
[2] Steurer M A,Jelliffe-Pawlowski L L,Baer R J,et al.Persistent Pulmonary Hypertension of the Newborn in Late Preterm and Term Infants in California[J].Pediatrics,2017,139(1):e20161165.
[3] Nakwan N,Jain S,Kumar K,et al.An Asian multicenter retrospective study on persistent pulmonary hypertension of the newborn:incidence,etiology,diagnosis,treatment and outcome[J].Journal of Maternal-Fetal and Neonatal Medicine,2018:1-11.
[4]杜立中.新生儿持续肺动脉高压诊治的若干进展[A].全国儿科学新进展、急重症诊治新技术学术会议[C].广州:中国小儿急救医学,2007.
[5] Dani C,Corsini I,Cangemi J,et al.Nitric oxide for the treatment of preterm infants with severe RDS and pulmonary hypertension[J].Pediatric Pulmonology,2017,52(11):1461-1468.
[6] De B W P,Yogen S,Zoltan M,et al.Application of Neonatologist Performed Echocardiography in the assessment and management of persistent pulmonary hypertension of the newborn[J].Pediatric Research,2018,84(S1):68-77.
[7] Bhattacharya S,Sen S,Levy P T,et al.Comprehensive Evaluation of Right Heart Performance and Pulmonary Hemodynamics in Neonatal Pulmonary Hypertension[J].Current Treatment Options in Cardiovascular Medicine,2019,21(2):10.
[8]周偉,荣箫.高频振荡通气在新生儿的应用[J].中国新生儿科杂志,2012,9(4):135-137.
[9]董世霄,刘红,钱素云.高频振荡通气治疗新生儿持续肺动脉高压疗效评价[J].山西医科大学学报,2012,43(9):700-703.
[10] Fernanda B,Lucía V,Fernando S,et al,Efficacy and safety of a novel nitric oxide generator for the treatment of neonatal pulmonary hypertension:Experimental and clinical studies[J].Pulmonary Pharmacology & Therapeutics,2019(54):68-76.
[11] Ellsworth K R,Ellsworth M A,Weaver A L,et al.Association of Early Inhaled Nitric Oxide With the Survival of Preterm Neonates With Pulmonary Hypoplasia[J].Jama Pediatr,2018,172(7):e180761.
[12] Hussain A S ,Ali R,Ahmed S,et al.Oral sildenafil use in Neonates with persistent pulmonary hypertension of Newborn [J].J Ayub Med Coll Abbottabad,2017,29(4):677-680.
[13]刘九月,李同川,张慧娟,等.高频振荡通气联合西地那非治疗新生儿持续性肺动脉高压[J].新乡医学院学报,2014,31(1):51-53.
[14] Shah P S,Ohlsson A.Sildenafil for pulmonary hypertension in neonates[J].Cochrane Database Syst Rev,2017,39(8):CD005494.
[15]寇晨,张巍.磷酸二酯酶抑制剂在新生儿持续肺动脉高压治疗中的研究进展[J].儿科药学杂志,2013,19(6):57-59.
[16] Giaccone A,Zuppa A F,Sood B,et al.Milrinone Pharmacokinetics and Pharmacodynamics in Neonates with Persistent Pulmonary Hypertension of the Newborn[J].American Journal of Perinatology,2017,34(8):749-758.

