30 μm高比表面积TiO2纳米管的制备工艺
(上海民航职业技术学院,上海 200232)
GRIMES 等[1]于2001年首次提出TiO2纳米管阵列薄膜的制备方法, 采用阳极氧化法在纯钛片表面制备了一层高度有序的纳米管阵列结构。通过控制阳极氧化电压、氧化时间、电解质组成和pH等,有效控制了TiO2纳米管的微观结构参数(如纳米管的管径、管长和管壁厚度等),实现了对制备工艺的控制。
TiO2纳米管是整齐垂直排列在导电基底上的,这种结构会大大降低光生载流子的复合, 有利于光生载流子的快速迁移, 从而产生很强的光电性能。此外,与纳米TiO2薄膜相比,TiO2纳米管阵列薄膜具有更大的比表面积和更强的吸附能力,因此,阳极氧化法制备TiO2纳米管阵列薄膜成为研究的热点[2-13]。
课题组的前期工作[14-20]表明:阳极氧化法制备TiO2纳米管的长度与电化学生成TiO2纳米管的速度和溶液中F-溶解TiO2纳米管的速度有关。当电化学生成TiO2纳米管的速度大于溶液中F-溶解TiO2纳米管的速度时,TiO2纳米管不断生长。TiO2纳米管的不断生长与电解质体系在反应过程中电流密度变化和pH变化有关,一定范围内,电流密度的增加会提高电化学形成TiO2纳米管的速度;pH的增加会降低F-溶解TiO2纳米管的速度。
为了得到更长的TiO2纳米管阵列,本工作在甘油+0.5%(质量分数,下同)NaF体系中,采用阳极氧化法制备了TiO2纳米管阵列。
1 试验
1.1 试样的前期处理
将工业纯钛箔(厚100 μm;wN≤0.012%,wC≤ 0.02%,wSi<0.04%,wFe≤0.06%)裁剪成尺寸为3 cm×6 cm的试样,用砂纸(350~1 000号)逐级打磨纯Ti表面致表面看不到划痕,试样依次用去离子水冲洗,丙酮超声清洗除油,去离子水清洗后,吹干备用。
1.2 阳极氧化法制备TiO2纳米管
阳极氧化试验包括一台提供阳极氧化电压的直流稳压电源、一台电磁搅拌器和一个恒温水浴槽。
室温下,在容器(由聚四氟乙烯制成)中加入一定体积的甘油+0.5% NaF溶液,采用两电极体系进行阳极氧化。其中,钛片为阳极,纯铂片为阴极,直流电压为20 V,温度为0,20,40 ℃,反应时间为7 h,制得TiO2纳米管。采用去离子水清洗、干燥TiO2纳米管后,采用日本生产的JSM-6700F型场发射扫描电子显微镜(FE-SEM)进行观察,确定较好的反应温度后,20 V直流电压下,改变反应时间制备TiO2纳米管,然后用去离子水清洗、干燥备用。
试验过程中施加搅拌,主要目的是减少Ti/电解液界面间双电层的厚度,保证Ti电极表面各处的电流密度和温度是一致的。
1.3 pH对TiO2纳米管生长的影响
为进一步研究pH的影响,在阳极氧化的过程中,采用美国Extech公司生产的笔式pH计pH100测量溶液及试样附近的pH变化情况。
2 结果与讨论
2.1 反应温度对TiO2纳米管长度的影响
由图1可见,0 ℃时TiO2纳米管长度为1 034 nm,20 ℃时TiO2纳米管长度为2 601 nm,40 ℃时TiO2纳米管长度为5 152 nm。随着反应温度的升高,制得TiO2纳米管的长度不断增加。这是因为:温度升高,电解液的导电性增强,纳米管的形成电压降低,电流密度增大,纳米管增长速率增大,这和文献[21]的结果相吻合。

(a) 0 ℃ (b) 20 ℃ (c) 40 ℃
2.2 反应温度对该体系反应电流密度的影响
为进一步研究温度对电流密度的影响,分别测量了20 ℃和40 ℃时该体系反应1 h内的电流密度变化曲线,见图2。
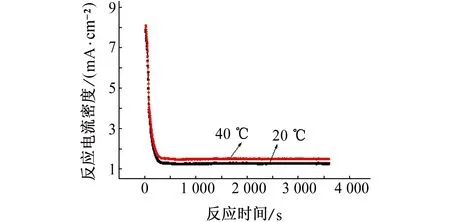
图2 不同温度下电流密度随反应时间的变化曲线Fig. 2 Variation curves of current density with reaction time under different temperatures
由图2可见,在反应初期,20 ℃时的电流密度为7.87 mA/cm2,40 ℃时的电流密度为8.10 mA/cm2;随着反应的进行,两种温度下电流密度均直线下降,反应至290 s后,电流密度趋于稳定,20 ℃时的约为1.27 mA/cm2,40 ℃时的约为1.50 mA/cm2。该结果进一步证明温度升高会增加溶液的反应电流密度,故高温条件下生成的TiO2纳米管的长度比低温条件下的长。故建议在40 ℃下制备TiO2纳米管。
2.3 反应时间对纳米管形貌的影响
反应温度为40 ℃,在0.5% NaF+甘油溶液中对纯Ti片进行阳极氧化反应,反应时间为24 h和36 h,制得TiO2纳米管的形貌见图3。由图3可见,反应24 h后纳米管长度为20.29 μm,反应36 h后纳米管长度为29.50 μm。

(a) 24 h
图4是在不同溶液体系中,纯钛经阳极氧化后制得TiO2纳米管的长度与反应时间的关系。
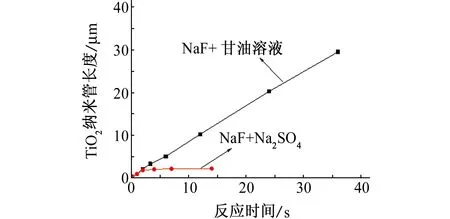
图4 不同体系中纳米管长度与反应时间的关系Fig. 4 The relationship between nanotube length and reaction time in different systems
由图4可见:在0.5% NaF+甘油溶液中,TiO2纳米管的长度随反应时间的延长而不断增加;而在0.5% NaF+1 mol/L Na2SO4溶液中,反应3 h后,TiO2纳米管的长度增加不明显,最后稳定在2.3 μm左右,不会再随着反应时间的延长而增加。这是因为:TiO2纳米管的形成是电场作用下的TiO2形成、TiO2溶解和TiO2纳米管与F-反应引起的化学溶解共同作用的结果。电解液的性质决定了电化学生长过程,在不同的溶液体系中,纳米管的生长速度不一样,F-反应引起的化学溶解速度也不一样,TiO2纳米管的增长速度(nm/s)和TiO2纳米管的增长常数(nm/V)也不同,所以纳米管生长与化学溶解达到平衡的时间也不一样。
0.5% NaF+甘油溶液比较黏稠,溶液中F-的扩散能力较弱,所以对纳米管的化学溶解作用没有0.5% NaF+1 mol/L Na2SO4溶液的强,所以在0.5% NaF+甘油溶液中,纳米管长度可以随反应时间的延长而不断增加。
3 结论
在0,20,40 ℃的0.5% NaF+甘油溶液中对Ti片进行阳极氧化7 h,得到的TiO2纳米管长度分别为1 034,2 601,5 152 nm。溶液温度升高使得溶液的电流密度增大,反应至约290 s,电流密度趋于稳定,20 ℃时的电流密度约为1.27 mA/cm2,40 ℃时的约为1.50 mA/cm2,所以高温促进了TiO2纳米管的生长,40 ℃是较好的反应温度。
在40 ℃的0.5% NaF+甘油溶液中对Ti片进行阳极氧化36 h,TiO2纳米管长度达到30 μm左右,即纳米管长度可以随反应时间的延长而增加。
致谢:感谢上海大学分析测试中心褚玉良老师在纳米管SEM检测过程中提供的帮助!

