PGⅠ、PGR检测联合ME-NBI在胃癌及癌前病变诊断中的应用
张霁雯 吴永梅 罗酩 李文娟
(上海市宝山区罗店医院内科,上海 201908)
消化道恶性肿瘤是我国最常见的恶性肿瘤之一,其发病率居在全国各类肿瘤的前列。1993年至1997年,全国几大城市肿瘤流行病学调查结果显示,消化系统肿瘤的发病率占恶性肿瘤总数的一半以上,胃癌、结直肠癌位居第一和第四位[1-6]。临床Ⅰ期胃癌患者的5年生存率约为91%,而Ⅳ期的胃癌患者的5年生存率低于10%[7]。胃癌手术后的5年生存率约为30%~50%,进展期约40%,早癌手术后约为90%。早癌及癌前病变缺乏特异性的临床症状,大多数患者一般消化道症状出现后,通过对症支持治疗后症状都有相应的缓解,而这种现象是人群中胃癌及癌前病变错失早期诊断或漏诊的重要原因之一。晚期消化道肿瘤预后不佳,不仅对健康造成严重威胁,而且会带来巨大的社会和经济损失。早期诊断和早期干预,对提高五年生存率乃至治愈率都具有重要意义。目前,临床上对于胃部疾病的检查主要依据于胃镜和胃镜下的活检,检测“血清PG法”(胃蛋白酶原,pepsinogen,PG),以及放大内镜—窄带成像技术(magnifying endoscopy-narrow band imaging,ME-NBI)等检查方法,本研究收集2017年7月至2019年6月来我院消化内科就诊的患者245例患者,探讨胃蛋白酶原Ⅰ(pepsinogenⅠ,PGⅠ)、胃蛋白酶原Ⅰ/胃蛋白酶原Ⅱ(pepsinogenⅠ/pepsinogenⅡ,PGⅠ/PGⅡ, PGR)与ME-NBI联合检测在胃癌及癌前病变中的价值,现报告如下。
1 资料与方法
1.1一般资料 收集2017年7月至2019年6月来我院消化内科就诊的患者246例为疾病组,其中男117例,女129例,年龄20~70岁,平均年龄(51.5±4.9)岁。排除标准:严重高血压、心脏病及肺部疾病患者,严重智力障碍、交流障碍或有严重焦虑抑郁等心理疾病者,精神病和依从性差,不能配合随访者等影响实验结果的药物者,严重心肺、肝肾功能不全者,正在接受食管、胃及十二指肠疾病治疗者,患有其他能影响PG分泌的疾病(如前列腺癌、胰腺癌)者,孕妇、哺乳期妇女,胃肠道狭窄、畸形、穿孔、梗阻,胃癌术后或有胃、十二指肠部手术史者。根据病理及胃镜检查结果,将受试者分为5组:慢性浅表性胃炎组79例,慢性萎缩性胃炎组78例;早期胃癌组(包括重度不典型增生组及胃恶性溃疡组)47例和进展期胃癌组41例。所有患者均接受血清PG检查,普通胃镜下发现可疑病变者(如溃疡、胃癌、息肉等),通过活检明确病变。另选取于我院进行常规健康体检,且经体检后未发现患有胃肠道、心脏、肝脏和肾脏方面等疾病的100人为健康组。男51人,女49人,年龄25~76岁,平均年龄(50.1±7.9)岁。排除标准:高血压、心脏病、肺部疾病患者、严重智力障碍、精神病、交流障碍或有严重焦虑抑郁等心理疾病,依从性差不能配合随访,孕妇、哺乳期妇女。
1.2检测方法 主要仪器:BECKMAN AU-5800全自动生化分析仪;试剂:宁波瑞源生物科技有限公司生产的胃蛋白酶原Ⅰ、Ⅱ检测试剂盒及标准品。采用乳胶增强免疫比浊法测定血清胃蛋白酶原PGⅠ、PGⅡ。内镜使用奥林巴斯260Z电子放大胃镜,主机采用具有窄带成像技术(endoscopy-narrow band imaging,ME-NBI)功能的奥林巴斯EVIS-260系统,可以同时通过窄带成像按键进行转换。病理标本处理:10%福尔马林固定液、常规石蜡包埋,苏木精及伊红染色。病理诊断标准参照《新编常见恶性肿瘤诊治规范胃癌分册》(1998年)[8]以及《中国慢性胃炎共识意见》(2017年,上海)[9]。
1.3样品采集 通过双盲法抽取受试者空腹静脉血3 mL,以3 000 r/min离心5 min后分离血清,进行检测,并将未检的样本在-80 ℃的条件下进行储存。
1.4胃镜检查 医师在术前向患者及其家属解释说明胃镜检查及活检可能的结果及存在的风险,并签署了知情同意书。告知患者在检查前10~12 h禁止饮食,术前1d及术前10~20 min前口服二甲硅油和盐酸利多卡因胶浆用作咽部麻醉。首先常规电子内镜对胃进行全面观察,进镜通过贲门后立即由电子胃镜活检孔注入10 mL二甲基硅油散悬混液。进行全貌胃腔观察,进镜至十二指肠降部后退镜仔细观察,其中胃腔部分观察顺序为:幽门管—幽门—胃窦前壁—胃窦后壁—胃窦小弯侧—胃窦大弯侧—胃角—胃角前壁(倒镜)—胃角后壁(倒镜)—胃底正面(倒镜)—胃底前壁(倒镜)—胃底后壁(倒镜)—胃底小弯侧(倒镜)—中部胃小弯前壁(倒镜)—中部胃小弯后壁(倒镜)—下部胃小弯前(倒镜)壁—下部胃小弯后壁(倒镜)—胃体大弯侧下部—胃体大弯侧中部—胃体大弯侧上部部—胃底大弯侧正面。如在检查后发现胃黏膜充血、糜烂和粗糙不平等病变后,用0.9%氯化钠溶液清洗位于胃黏膜表面的粘液及附着物,吸净胃内残留黏液,用NBI进一步观察病变,结束观察后,在病变区域取6~8块组织进行活组织检查,用10%甲醛溶液固定,送至病理科进行常规病理检查。若病理检查结果诊断为早期胃癌或高级别上皮内瘤变,再进行内镜下黏膜剥离术或普外科一般手术治疗,术后,由同一病理医师对标本进行常规病理检查。
1.5阳性判断标准 PGⅠ<70 ng/mL为阳性,PGR<3.0判断为阳性,PGⅠ联合PGR(PGⅠ<70 ng/mL或PGR<3.0),ME-NBI对早期胃癌的诊断标准。
1.6观察指标检测 健康组与不同胃病组血清胃蛋白酶原PGⅠ、PGⅡ、PGⅠ/PGⅡ (PGR)数值。以病检及胃检结果为金标准,衡量PGⅠ、PGR以及PGⅠ联合PGR三种检查方法的准确度、灵敏度、特异度、阳性预测以及阴性预测值。
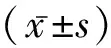
2 结 果
2.1健康组与不同胃病组血清PGⅠ、PGⅡ、PGⅠ/PGⅡ (PGR) 检测结果比较 与健康组相比,慢性萎缩性胃炎组和早期胃癌组的PGⅠ水平和PGⅠ/PGⅡ比值均显著性下降(P<0.05)。与慢性浅表性胃炎组相比,早期胃癌组和慢性萎缩性胃炎组PGⅠ水平和PGⅠ/PGⅡ比值均显著性下降(P<0.05)。慢性萎缩性胃炎组血清PGⅠ/PGⅡ比值明显低于早期胃癌组(P<0.05)。早期胃癌组与进展期胃癌组和慢性萎缩性胃炎的PGⅠ水平无统计学差异(P>0.05)。见表1。
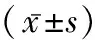
表1 健康组与不同胃病组血清PGⅠ、PGⅡ、PGⅠ/PGⅡ (PGR) 检测结果
注:与健康组比较,*P<0.05;与慢性浅表性胃炎组比较,#P<0.05;与早期胃癌组比较,△P<0.05。
2.2病检及胃检结果、PGⅠ、PGR以及PGⅠ联合PGR对胃癌的诊断结果 246例患者经过病检及胃检后,确诊为胃癌者88例(35.77%),非胃癌患者158例(64.23%);经过检查血清PGⅠ后,诊断为早期胃癌者102例(41.16%),非胃癌患者144例(58.54%);经过检查血清PGR后,诊断为早期胃癌者28例(11.38%),非胃癌患者218例(88.62%);经过检查血清PGⅠ联合PGR后,诊断为胃癌者116例(47.15%),非胃癌患者130例(52.85%)。以病检及胃检结果作为金标准,PGⅠ联合PGR检查对胃癌的诊断特异度和阳性预测值高于PGⅠ和PGR单独检查,PGⅠ联合PGR检查、PGⅠ检查与PGR检查特异度和阳性预测值比较差异具有统计学意义(P<0.05)。同时检查的三种检查方法准确度、灵敏度和阴性预测值方面差异均无统计学意义(P>0.05)。见表2。

表2 病检及胃检结果、PGⅠ、PGR以及PGⅠ联合PGR对胃癌的诊断价值及阳性预测值和阴性预测值(%)
注:与PGR检查比较,*P<0.05。
2.3健康组与不同胃病组放大内镜—窄带成像技术检查结果 图1 A显示健康者胃黏膜皱襞正常且光滑,形态规律,红白相间,黏膜浆液清亮,呈中等量,未见新生物及静脉曲张,未见溃疡及占位,未见明显异常。图1 B显示慢性浅表性胃炎患者胃黏膜完整,但充血、水肿,红白相间,多发点片状糜烂,可见少量黄绿色胆汁滞留,未见赘生物。图1 C显示慢性萎缩性胃炎患者胃黏膜颜色红白相间,以红为主,黏膜下血管透见,黏膜表面粗糙不平,呈颗粒状,萎缩黏膜脆性增加,反光增强,同时伴有慢性浅表性胃炎的表现,如充血红斑、附着粘液等。图1 D显示早期胃癌患者胃粘膜表面不平且呈结节状,有灰白色物覆盖,失去色泽,基底不平整。图1 E显示进展期胃癌患者肿瘤形成突起和溃疡,边界不清,周围黏膜有结节、有出血、糜烂等表现。

注:A健康组(男,42岁);B慢性浅表性胃炎组(男,45岁);C慢性萎缩性胃炎组(女,47岁);D早期胃癌组(男,56岁);E进展期胃癌(女,58岁)图1 放大内镜—窄带成像技术检查
3 讨 论
胃癌是最常见的恶性肿瘤之一,而提高肿瘤患者的生活质量和降低其死亡率等问题则主要是依靠早期诊断和治疗。目前,胃镜和胃镜下的活检是确诊癌症的“金标准”,但普通胃镜有一定局限性,如,早癌表现不典型,活检阳性率不高,不能及早发现,不典型增生患者不能作为筛查手段。“血清PG法”在早期癌症筛查中具有准确性高、安全性高、简便等特点,得到了越来越多的关注、认可和推广。对胃蛋白酶原Ⅰ、胃蛋白酶原Ⅱ和PGR水平的联合检测对胃癌及早癌的筛查具有重要的价值。在胃癌的发病过程中,由于胃粘膜细胞质量和数量上的改变,必然会引起PG分泌的变化。这是通过检测血清PG含量来判断胃粘膜病变的主要理论依据[10-11]。血清PG可根据各亚型的含量和比值,间接反映胃底腺粘膜和全胃胃粘膜的变化,尤其对萎缩性胃炎具有重要的诊断意义[12-13]。NBI被称为“数字化色素内镜”,操作方便,通过小按钮可以使NBI图像与普通的内镜图像进行自由转换,使操作者可以轻松完成内镜检查。放大内镜—窄带成像技术(ME-NBI)可以达到“光学活检”的目的。ME-NBI技术不仅可以判断病变的良性、恶性以及恶性病变的范围,还可以初步判断恶性病变的组织学分化程度。
本研究结果表明,乳胶增强免疫比浊法测定血清PGⅠ、PGⅡ,慢性萎缩性胃炎、早期胃癌、进展期胃癌患者的PGⅠ、PGR水平低于对照组,在早期胃癌及进展期胃癌中尤为明显,对胃粘膜病变具有早期诊断价值和指导意义。研究结果显示,246例患者经过病检及胃检后,确诊为胃癌者88例(35.77%),非胃癌患者158例(64.23%)。以病检及胃检结果作为金标准,PGⅠ联合PGR检查对胃癌的诊断特异度和阳性预测值高于PGⅠ或PGR单独检查,PGⅠ联合PGR检查、PGⅠ检查与PGR单独检查特异度和阳性预测值比较具有统计学意义(P<0.05)。说明PGⅠ联合PGR检查可以发现较多的高危可疑患者,减少漏检和漏诊,提高胃癌的检出率。
综上所述,采用PGⅠ联合PGR检查有一定的参考价值,联合病理检查和胃镜检查结果可提高胃癌的早期诊断率,值得临床推广应用。

